HPLC法测定复元胶囊中五味子醇甲的含量*
2022-03-14周凤盈王殿奎耿春辉王夏青
周凤盈,王殿奎,耿春辉,孙 琛,王夏青
(衡水市综合检验检测中心,河北 衡水 053000)
复元胶囊是由五味子、人参、黄芪、熟地黄、山茱萸等二十一味中药制成,该药具有健脾补肾,益气活血,祛湿醒脑等功效。临床上主要治疗脑供血不足、脑转耳鸣,痴呆等症。痴呆又称阿尔茨海默病(Alzheimer Disease,AD),目前,美国已将AD纳入无法预防、无法治愈的十大死亡病种之一[1]。该药经多年应用于临床,疗效确切[2-3]。五味子为木兰科植物五味子的干燥成熟果实,具有补肾养心、益气生津、收敛固涩等功效。五味子醇甲(C24H32O7)是从五味子的干燥成熟果实中提取出的一类木脂素类,据现代药物学分析研究发现五味子中所含的化学成分主要有木脂素类,也是发挥五味子多种功效的有效成分[4],五味子醇甲作为中药五味子的主要活性成分之一,在各个系统具有广泛的药理作用,尤其在中枢神经系统的作用最为显著,对神经退行性疾病AD 具有潜在的预防和治疗作用[5],《中国药典2020年版一部》[6]将五味子醇甲(C24H32O7)作为五味子的定量指标。复元胶囊目前的标准仅对何首乌、丹参、冰片进行定性鉴别,而无定量方法,不能有效地控制药品质量。为了更好地控制产品质量,经过反复实验确定采用高效液相色谱(HPLC)法对复元胶囊中五味子活性成分五味子醇甲(C24H32O7)的含量进行分析。此方法灵敏度高,专属性强,重复性好,操作简便,可作为复元胶囊的质量标准提升的依据。
1 仪器与试药
1.1 仪 器
Waters e2695高效液相色谱仪(检测器:2489紫外检测器);XS205DU电子天平 梅特勒-托利多科技(中国)有限公司 精度:0.01 mg;KQ-300VDE超声波清洗器(昆山市超声仪器有限公司)。
1.2 试 药
甲醇(色谱纯),默克股份两合公司;其他试剂均为分析纯;水为纯化水;五味子醇甲对照品(批号:110857-201815 纯度:99.7%),中国食品药品检定研究院;复元胶囊,由河北省衡水市中医院制剂室(批号分别为20220309、20220507、20220802,规格:0.3 g)。
2 方法与结果
2.1 色谱条件
色谱柱:Waters SunFire C18柱(250 mm×4.6 mm,5 μm);检测器型号:Waters 2489;流动相:甲醇-水(65∶35),检测波长为250 nm;流速: 1.0 mL/min;柱温:30 ℃;进样量:10 μL,按上述色谱条件照《中国药典2020年版四部》[7](通则0512)高效液相色谱法进行测定,理论板数按五味子醇甲峰计均高于3000;五味子醇甲峰与其前后相邻峰的分离度均大于1.5。
2.2 对照品贮备液的制备
精密称取五味子醇甲对照品适量,置50 mL容量瓶中,用甲醇溶解并稀释至刻度,制成每1 mL含0.4096 mg的对照品贮备液。
2.3 对照品溶液的制备
精密量取2.2项下对照品贮备液5 mL,置100 mL量瓶中,加甲醇稀释至刻度,摇匀备用。
2.4 供试品溶液的制备
取供试品内容物约5 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,密塞,称定重量,超声处理(功率250 W,频率33 kHz)30 min,放冷,再次称定,用甲醇补足减失重量,摇匀,滤过,取续滤液作为供试品溶液。
2.5 阴性对照溶液制备
按复元胶囊的处方比例和工艺手法制成不含五味子的阴性样品,按2.4项下的方法制成阴性对照溶液。
2.6 检测限与定量限
精密量取2.3项下对照品溶液,用甲醇稀释至浓度依次由高到低的溶液,将对照品各色谱峰测出的信号与空白样品测出的信号比较,以测得五味子醇甲(C24H32O7)的检测限(S/N=3)和定量限(S/N=10),结果见表1。
2.7 线性关系的考查
精密量取2.2项下对照品贮备液各1,2.5,5,7.5,10 mL,分别置100 mL量瓶中,用甲醇稀释至刻度,摇匀;按2.1项下的色谱条件测定,进样量10 μL;对照品溶液浓度(X,μg/mL)为横坐标,以峰面积(Y)为纵坐标,绘制标准曲线并进行回归计算,得回归方程。结果表明:五味子醇甲(C24H32O7)在4.096~40.96 μg/mL线性范围内,所测对照品溶液的浓度与被测组分峰面积均存在良好的线性关系。结果见表1。

表1 线性关系、检测限及定量限测定结果Table 1 Linear relationship, detection limit and quantitative limit determination results
2.8 精密度试验
精密吸取2.3项下对照品溶液10 μL,按2.1项下的色谱条件连续进样测定6次,记录峰面积值分别为2119341、2127342、2116523、2116971、2119798、2115639,平均值为 2119269,RSD为0.2%(n=6)。结果表明仪器具有良好的精密度。
2.9 重复性试验
取供试品(批号:20220309),照2.4项下供试品溶液制备方法配制6份供试品溶液,按2.1项下的色谱条件测定,以外标法计算五味子醇甲(C24H32O7)的含量分别为0.2049 mg/g、0.2037 mg/g、0.2057 mg/g、0.2043 mg/g、0.2061 mg/g、0.2044 mg/g,平均含量为0.2048 mg/g,RSD为0.4%(n=6)。结果表明方法重复性良好。
2.10 稳定性试验
精密吸取2.4项下供试品溶液(批号:20220309)10 μL,分别在0、3、6、9、12、24 h测定峰面积值的变化,结果峰面积值分别为2118254、2117623、2118598、2117835、2118046、2118919,平均值为2119879,RSD为0.2%(n=6)。结果表明供试品在24 h内稳定性良好。
2.11 加样回收率试验
精密称取已知五味子醇甲(C24H32O7)含量的供试品(批号:20220309)内容物6份,每份称重约为2.5 g,分别精密加入2.2项下的对照品贮备液1250 μL,照 2.4项下的方法制备供试品溶液,按2.1项下的色谱条件测定,计算平均回收率,结果见表2。
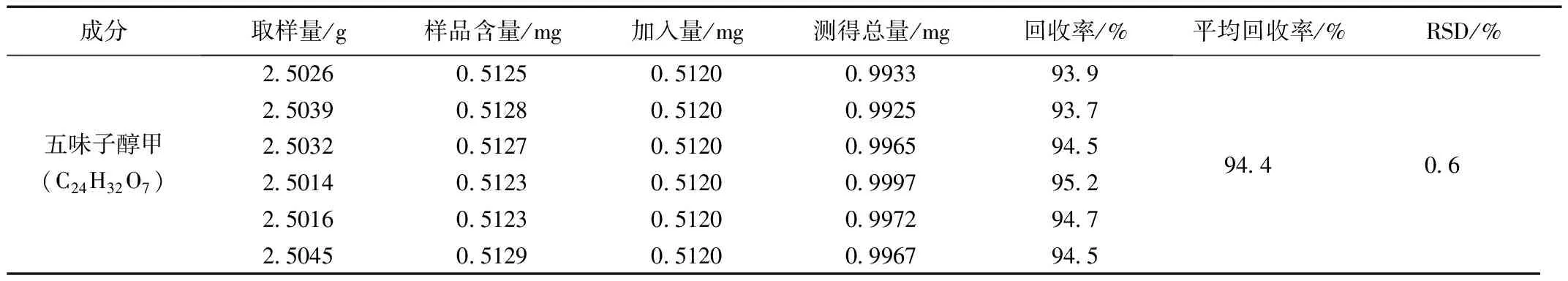
表2 加样回收试验结果Table 2 Results of sample recovery test
2.12 样品的测定
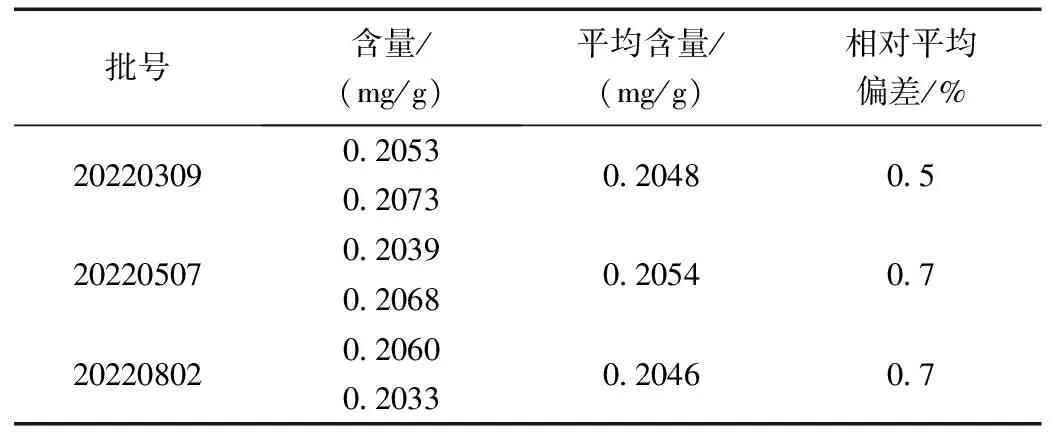
表3 五味子醇甲(C24H32O7)的含量测定结果Table 3 Determination results of Schizandrin A(C24H32O7)
取1.2项下三批样品按2.4项下的方法制成供试品溶液,按2.1项下色谱条件测定,精密量取供试品溶液、对照品溶液各10 μL,注入液相色谱仪中记录峰面积,按外标法计算五味子醇甲(C24H32O7)的含量,测定结果见表3。
3 讨 论
3.1 专属性
分别取2.3、2.4、2.5项下的溶液,照2.1项下的色谱条件测定,对照品主峰与供试品相应位置峰的保留时间分别为22.257 min、22.479 min,阴性对照溶液在相应位置无杂质峰干扰,供试品主峰能达到很好的分离,结果见图1。

图1 高效液相色谱图Fig.1 HPLC chromatogram
3.2 系统适用性
色谱系统的适用性试验通常包括理论板数、分离度、灵敏度、拖尾因子和重复性五个参数[7],要使上述参数均达到规定的要求,色谱条件的选择尤为重要。在色谱条件中合适的流动相组成及比例是色谱条件的重要因素,在实验中参照《中国药典 2020 版一部》[6]及参考文献测定方法[8-11],采用下列不同流动相进行洗脱:甲醇-水(78∶22)、甲醇-水(55∶45)、甲醇-水(65∶35)、乙腈:水(34∶66)及乙腈:0.1%磷酸(34∶66),对比了使用上述流动相进行洗脱的分离情况,以理论板数、分离度、灵敏度、拖尾因子和重复性等参数进行考察,优化选择以甲醇-水(65∶35)进行洗脱,能达到有效分离,被测成分峰形好,分离效果最佳。
3.3 供试品溶液制备方法选择
参照《中国药典 2020 版一部》[6]及参考文献测定方法[9-12],供试品制备时取同一供试品分别以50%甲醇、70%甲醇、甲醇、70%乙醇、乙酸乙酯作为提取溶剂,超声提取30 min后,照2.1项下的色谱条件进行测定,测得复元胶囊中的五味子醇甲(C24H32O7)的含量分别为0.1439 mg/g、0.1832 mg/g、0.2048 mg/g、0.1647 mg/g、0.1739 mg/g,供试品中五味子醇甲(C24H32O7)含量测定结果最高的提取溶剂是甲醇,由此确定甲醇为提取溶剂;同时考察了不同的超声时间对提取效率的影响,分别对同一供试品超声提取20 min、30 min、40 min及50 min,照2.1项下的色谱条件进行测定,测得复元胶囊中的五味子醇甲(C24H32O7)的含量分别为0.1559 mg/g、0.2048 mg/g、0.2046 mg/g和0.2049 mg/g,结果表明,供试品超声提取30 min,五味子醇甲(C24H32O7)可被提取完全。
3.4 耐用性试验
耐用性系指在测定条件有小的变动时,测定结果不受影响的承受程度[7]。根据《中国药典》2020年版四部[7](通则9101)的要求,本试验主要考察不同品牌色谱柱、柱温、流动相的组成等变动因素对测定结果的影响。
3.4.1 色谱柱的考察
取同一供试品溶液,按照2.1项下色谱条件,采用不同品牌的色谱柱Zafex JXC-18柱(250 mm×4.6 mm,5 μm)、Waters SunFire C18柱(250 mm×4.6 mm,5 μm)、Agilent ZORBAX SB-C18柱(250 mm×4.6 mm,5 μm)测定供试品中五味子醇甲(C24H32O7)的含量,结果见表4。

表4 不同色谱柱测得五味子醇甲(C24H32O7)的含量测定结果Table 4 Determination results of Schisandrin A (C24H32O7) content measured by different chromatographic columns
实验结果表明,不同品牌的色谱柱对测定五味子醇甲(C24H32O7)的含量没有影响。
3.4.2 柱温的考察

表5 不同色谱柱温度测得五味子醇甲(C24H32O7)的含量测定结果Table 5 Determination results of Schizandrin A (C24H32O7) at different chromatographic column temperatures
取同一供试品溶液,采用Waters SunFire C18柱(250 mm×4.6 mm,5 μm),按照2.1项下的色谱条件,分别在25 ℃、30 ℃、35 ℃、40 ℃条件下测定供试品中五味子醇甲(C24H32O7)的含量,结果见表5。
实验结果表明在25~40 ℃范围内可准确测定五味子醇甲(C24H32O7)的含量。
3.4.3 流动相比例的考察
取同一供试品溶液,分别选择甲醇-水(65∶35)、甲醇-水(64∶36)、甲醇-水(67∶33)三种比例流动相,按2.1项下的色谱条件测得五味子醇甲(C24H32O7)的含量分别为0.2048 mg/g、0.2039 mg/g 、0.2050 mg/g,平均含量为0.2046 mg/g,RSD为0.3%(n=3)。
本实验通过对不同品牌色谱柱、柱温、流动相的组成比例的考察,表明在色谱条件有微小变化时,供试品中五味子醇甲(C24H32O7)的含量测定结果无明显变化,测定结果表明本实验方法耐用性良好。
4 结 论
本文通过大量的试验,采用高效液相色谱(HPLC)法定量测定五味子主要成分五味子醇甲(C24H32O7)的含量,通过方法学验证实验表明此检验方法专属性强,准确度高,重现性好、耐受性良好,建立复元胶囊中五味子醇甲的含量测定方法,可以有效控制复元胶囊的质量,为质量标准的提升提供依据。
