人凝血因子Ⅷ浓缩制剂治疗血友病甲的临床观察研究
2022-03-13包久铭
包久铭
(福建中医药大学附属南平市人民医院,福建 南平 353000)
血友病甲又称为“血友病A”、“甲型血友病”、“抗血友病球蛋白缺乏症”、“第Ⅷ因子缺乏症”等[1]。该病由凝血因子Ⅷ编码基因异常引起,属于凝血功障碍性遗传病,在男性中发病,常见皮肤、黏膜、肌肉、关节等自发性出血,创伤出血,肌肉血肿等临床表现,随疾病发展可使患者产生肌肉萎缩、呼吸困难、局部血管坏死、慢性关节病变等问题,增加患者残疾率、死亡率[2]。根据血友病甲患者凝血因子Ⅷ活性水平,可见患者分为轻、中、重三种类型,中型与重型最为常见[3]。目前,该病尚无特异性疗法,临床多根据患者实际情况结合已有的成功经验,进行出血防控治疗、药物治疗、替代治疗等[4]。文献资料表示,替代治疗应用效果较高,能够有效改善患者症状,减少患者关节病变发生率,提升患者日常生活质量[5]。在替代治疗中人凝血因子Ⅷ浓缩制剂属于常用药物之一,可通过活化凝血Ⅷ因子,纠正凝血功能障碍,维持患者体内血流动态平衡。本研究通过回顾性分析收治中、重型60例血友病甲患者临床资料,探究人凝血因子Ⅷ浓缩制剂治疗效果,希望能够为临床用药与研究提供指导。
1 资料及方法
1.1 资料
回顾性分析60例研究对象临床资料。本组研究对象选自本院2018年1月至2022年6月收治血友病甲患者,均为男性,年龄最小2岁,最大16岁。根据人凝血因子Ⅷ浓缩制剂使用剂量将60例患者分为两组:(1)甲组30例,年龄2~15(7.15±2.25)岁;体重12~58(30.54±8.94)kg;有家族史15例,无家族史15例;治疗前30天出血次数≤2次12例,>2次18例;中型15例,重型14例。(2)乙组30例,年龄2~16(7.22±2.84)岁;体重11~59(30.62±9.44)kg;有家族史16例,无家族史14例;治疗前30天13例出血次数≤3次,17例出血次数>2次;中型13例,重型17例。两组一般资料差异无统计学意义(P>0.05)。
1.2 方法
入组患者均采用注射用重组人凝血因子Ⅷ(生产企业:BaxterBioScienceManufacturingSàrl;进口药品注册标准:S20120028;商品名称:百因止)治疗。具体操作:医务人员按照使用说明利用药品所附冻干粉及5mL灭菌注射用水配置药物,采用带有鲁尔接头塑料注射器静脉给药。静脉滴注速度控制在10mL/min以内。按照本院合理用药监测系统要求,严重血友病甲患者预防性治疗时,常规剂量20~40IU/kg,每次给药间隔时间为2~3d,6岁以下儿童推荐剂量20~50IU/kg,3~4/周。为深入了解注射用重组人凝血因子Ⅷ临床应用效果,明确不同剂量对中重度血友病甲患者的影响,给予甲组患者小剂量治疗,即每次10IU/kg,每3天1次;给予乙组患者中剂量治疗,即15~30IU/kg,每7天3次,具体根据患儿实际情况确定。所有患者连续用药28d。
1.3 观察指标
观察比较研究对象临床治疗有效性与安全性。
临床治疗有效性涉及内容:(1)临床疗效:患者用药后12h疼痛症状缓解,关节活动能力改善,用药后48h后血肿消失,用药28d后症状体征完全消失,相关检查结果恢复正常,机体功能恢复正常,视为显效;患者用药48h后疼痛缓解或血肿消失,用药28d症状大幅度改善,多数检查结果恢复正常,关节活动能力显著提高,视为有效;为满足上述要求视为无效,总有效率=显效率+有效率。(2)人凝血因子Ⅷ活性水平:测定并记录治疗前、第1次输注24h后人凝血因子Ⅷ活性水平。(3)生活质量评分:采用中文版血友病患儿生活质量评估量表(CHO-KLAT)进行评价,量表包含35个条目,涉及8方面内容,总分0~175分,得分越高表示患者生活质量水平越高,健康状况越好。
临床治疗安全性涉及内容:(1)生命体征指标:测定输注前、输注后6h研究对象脉搏、体温、呼吸、血压等水平,并对两组患者进行比较。(2)抑制物:统计研究对象抑制物(破坏凝血因子Ⅷ的抗体)产生情况。(3)病毒学监测结果:测定与记录输注28d时研究对象乙肝表面抗原(HBs-Ag)、人类免疫缺陷病毒抗体(HIV-Ab)、丙肝表面抗体(HCV-Ab)等阳性率。(4)不良反应:统计用药期间研究对象恶心、头晕、皮肤瘙痒、低血压等发生率。
1.4 统计学方法

2 结果
2.1 临床治疗有效性评价
2.1.1 临床疗效分析
乙组患者显效率高于甲组(P<0.05),详见表1。

表1 甲乙两组临床疗效比较[n(%)]
2.1.2 人凝血因子Ⅷ活性水平
甲组与乙组患者治疗前人凝血因子Ⅷ活性水平相当,P>0.05;第1次输注24h后乙组水平高于甲组(P<0.05)。详见表2。
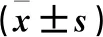
表2 甲乙两组人凝血因子Ⅷ活性水平比较
2.1.3 生活质量评分
60例患者治疗后CHO-KLAT评分显著高于治疗前(P<0.05);治疗后甲组评分比乙组更高(P<0.05)。见表3。
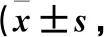
表3 甲乙两组CHO-KLAT评分比较份)
2.2 临床治疗安全性评价
2.2.1 生命体征指标水平
60例患者输注后脉搏、体温、呼吸、收缩压、舒张压与输注前差异无统计学意义(P>0.05);甲组于乙组患者输注后上述指标差异无统计学意义(P>0.05)。见表4。
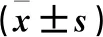
表4 生命体征指标水平比较
2.2.2 抑制物产生情况
60例患者报告抑制物产生阳性2例,阳性率为3.33%(2/60),均为既往没有接受过治疗的患者,甲组与乙组各分布1例。见表5。

表5 抑制物产生情况
2.2.3 病毒学监测情况
表6显示,甲组与乙组患者治疗28d时HBs-Ag、HIV-Ab、HCV-Ab等检测结果均为阴性,说明血友病甲患者应用人凝血因子Ⅷ浓缩制剂治疗病毒感染风险较低。
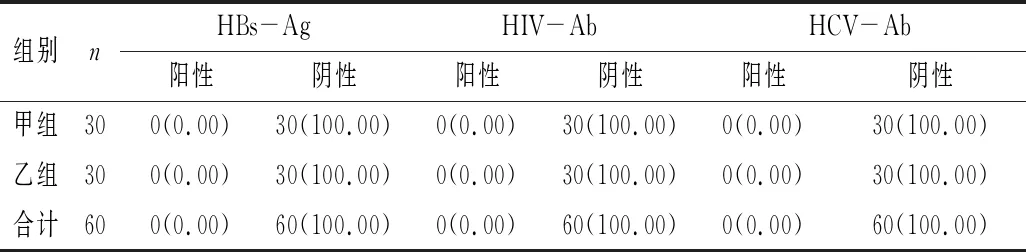
表6 治疗28d时HBs-Ag、HIV-Ab、HCV-Ab检测结果[n(%)]
2.2.4 不良反应发生情况
甲组不良反应总发生率低于乙组(P<0.05)。
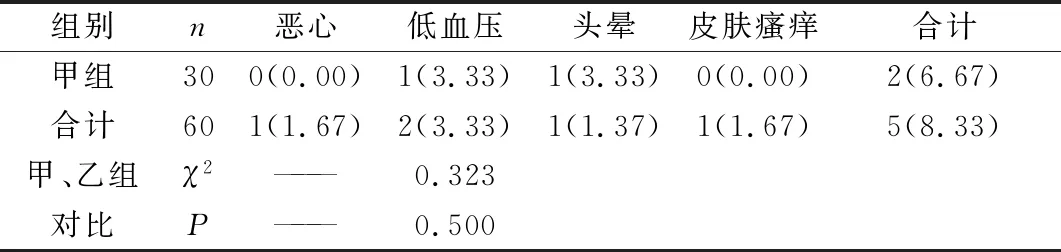
表7 不良反应发生情况[n(%)]
3 讨论
3.1 人凝血因子Ⅷ浓缩制剂及其对血友病甲的治疗效果
凝血因子替代治疗是目前血友病甲治疗主流方法,其有效性与安全性已经得到广泛认可。血友病甲因血液中缺乏凝血因子Ⅷ,导致机体出现凝血功能障碍,血液动力状态无法维持稳定,产生各种症状,损害患者健康。凝血因子替代治疗可通过向患者体内输注凝血因子Ⅷ,激活患者凝血机制,促进FXa活化提高凝血因子a水平,与此同时在钙离子、磷脂、活化凝血因子X等作用下,生成因子X酶复合物,有效改善患者凝血功能障碍。本研究与之研究结论较为相符。本研究中应用的百因止,为第3代重组人凝血因子Ⅷ,以重组人凝血因子Ⅷ为主要成分,此外加入了0.9~1.3%蔗糖、21~25mg/mL甘氨酸、18~23mM组氨酸、2~3mM氯化钙、27~36mEq/L钠、32~40mEq/L氯、≤64~96μg/mL聚山梨酯80、≤20μg/1000IU咪唑、≤5μg/1000IU磷酸三丁酯、≤0.6μg/1000IU铜,药品稳定性、安全性更强,适用于血友病甲以及人凝血因子Ⅷ缺乏引起的出血症状治疗。本组60例患者输注药物后,人凝血因子Ⅷ活性水平得到改善,治疗28d总有效率达到100.00%,CHO-KLAT评分得到提高,说明本组所用药物能够纠正凝血功能障碍,产生较为满意的临床治疗效果,促进患者生活质量提高。与此同时,60例患者用药后生命体征稳定,抑制物产生阳性率与不良反应发生率较低,无病毒感染病例,说明人凝血因子Ⅷ浓缩制剂应用安全水平较高。
3.2 不同剂量人凝血因子Ⅷ浓缩制剂的临床治疗效果
研究发现,凝血因子替代治疗过程中,预防治疗可有效减少出血、关节病变等不良事件发生率[1]。但预防治疗需求定期使用人凝血因子Ⅷ,这在一定程度上将提高治疗成本,加重医疗负担。对此,临床提出不同用药方案,并对其临床效果、经济成本进行了探究,发现小剂量方案成本优势明显,中剂量方案临床疗效优于小剂量[2]。本研究主要采用了小剂量(每次10IU/kg,每3天1次)与中剂量(15~30IU/kg,每7天3次)治疗方案,并对二者应用效果进行探究,发现中剂量用药临床治疗有效性更高,且安全水平和小剂量相当,从临床治疗有效性与安全性方面来看,中剂量更适用。
综上所述,替代治疗是血友病甲治疗重要方法之一,在替代治疗中人凝血因子Ⅷ浓缩制剂能够满足中、重型血友病甲临床治疗需求,在保证治疗安全性的同时,获取满意临床疗效。但在人凝血因子Ⅷ浓缩制剂治疗过程中,不同剂量可产生不同临床疗效,中剂量治疗有效性明显高于小剂量,且治疗安全有保障。临床可根据患者实际情况尝试采用中剂量治疗方案,促进患者治疗效果提升,实现患者生活质量有效改善。
