安儿宁颗粒在幼年大鼠临床前安全性评价研究
2022-03-11徐聪杨正标王海苹李怀平郑高利宣尧仙陈颖
徐聪杨正标王海苹李怀平郑高利宣尧仙陈颖*
(1. 杭州医学院安全性评价研究中心,杭州 310053;2. 浙江省药物安全性评价技术研究重点实验室,杭州医学院,杭州 310053;3. 金诃藏药(山东)健康产业有限公司,济南 250104)
安儿宁颗粒为经典藏医儿科用药“久协更卓”的现代剂型,处方由天竺黄、红花、人工牛黄、岩白菜、甘草、高山辣根菜、洪连、檀香、唐古特乌头九味藏药组成[1]。安儿宁颗粒具有清热祛风、化痰止咳功效,临床上主要用于治疗小儿风热感冒、咳嗽有痰、发热咽痛等上呼吸道感染[2-3]。处方中青藏高原特有药材唐古特乌头,为毛茛科乌头属,含有内酯型二帖生物碱,文献报道对小鼠具有一定的急性毒性[4-5];另红花,为活血化瘀药材,可显著延长凝血酶原和凝血酶时间,可能具有潜在的安全风险[6]。安儿宁颗粒上市近20年,据2018 ~ 2020年国家药品不良反应数据库数据反馈显示[7],安儿宁颗粒使用患儿约为1480万,其中有122例报告发生腹泻或皮疹等不良反应。虽然其不良反应报告率 < 0.01%,但鉴于安儿宁颗粒正逐渐被联合用药用于其他小儿适应症[8-13],且目前缺少安儿宁颗粒对幼龄动物的相关毒理学数据,本文特开展大剂量安儿宁颗粒在幼年大鼠的单次给药以及3个月重复给药的毒性研究,进一步评价其儿科用药安全性。
1 材料与方法
1.1 材料
1.1.1 实验动物
240只3 ~ 4周龄健康SPF级SD大鼠,雌雄各半,体重为40 ~ 60 g,购自上海市西普尔-必凯实验动物有限公司【SCXK(沪)2018-0016】。饲养期间各组大鼠自由饮水(经LAWS-2000实验动物反渗透纯水机处理纯水和摄食(钴60辐照的全价营养颗粒饲料),给药前大鼠禁食不禁水,温度20.5 ~ 25.5℃,相对湿度50% ~ 68%,每小时通风次数≥15次,12 h光照明暗交替,饲养于杭州医学院安全性评价研究中心屏障系统【SYXK(浙)2017-0010】。实验机构通过国家GLP认证和AAALAC认证,实验遵循GLP原则。本研究方案获得本机构实验动物伦理委员会的批准(GLP-A-003)。
1.1.2 主要试剂与仪器
安儿宁颗粒(清膏),黄棕色胶状物,3.1 g生药/g清膏,批号:20160201,金诃藏药股份有限公司提供;人工牛黄,批号:150731,青海九康中药饮片有限公司生产;临用前,按处方量比例1 g安儿宁颗粒清膏加34.2 mg人工牛黄,配制成“安儿宁颗粒”原液,用于高剂量组给药,中、低剂量组受试物取“原液”按比例用纯水配制成相应的给药浓度。唐古特乌头提取清膏(3.57 g生药/g,金诃藏药股份有限公司,批号:20160201),棕褐色粘稠液体,用纯水配制成给药浓度。
CA-1500全自动血凝分析仪(Sysmex,日本);7100全自动生化分析仪(Hitachi,日本);N-600尿液分析仪(长春迪瑞);ADVIA2120全自动血细胞分析仪(Bayer,德国);IMS-972电解质分析仪(深圳希莱恒);YZ6EI检眼镜(苏州医疗器械厂)。
1.2 方法
1.2.1 单次给药毒性实验
幼年大鼠按体重随机分为给药组和溶媒对照组,每组20只,雌雄各半。给药组大鼠灌胃给予安儿宁颗粒240 g生药/kg体重,分2次(间隔4 h)给予最大适用浓度(每毫升4 g生药)、最大给药体积(30 mL/kg);溶媒对照组灌胃等体积纯水。
观察给药后大鼠的一般反应(外观、行为活动、精神状态、食欲、大小便及其颜色、皮毛、鼻、眼、口有无异常分泌物等)及死亡情况,死亡动物及时尸检,若肉眼观察有病变脏器则进行病理组织学检查。给药后第1、2、3、4、7、9、11、15天称体重;第15天所有大鼠剖检,观察主要脏器的大小、形态、颜色和质地等。
1.2.2 重复给药毒性实验
幼年大鼠按体重随机分为溶媒对照组、唐古特乌头组、安儿宁颗粒低、中、高剂量组,每组40只,雌雄各半,分别灌胃给予纯水、唐古特乌头5.5 g生药/kg体重、安儿宁颗粒3 g/kg体重、11 g/kg体重和40 g/kg体重(按生药计),给药体积10 mL/kg,每天给药1次,连续91 d,停药后恢复观察4周。
实验期间每天观察大鼠的一般反应:外观、行为活动、精神状态、食欲、大小便及其颜色、皮毛、鼻、眼、口有无异常分泌物等,每周称体重和摄食量1次;给药前、给药中期、停药后1 d和恢复期结束检测大鼠眼科和尿液指标。在给药中期(给药45 d)、停药次日和恢复期结束,每组分别随机取10、20、10只大鼠(雌雄各半),进行血液学(RBC、WBC、HGB、PLT、HCT、MCV、MCH、MCHC、MPV、RDW、#NEUT、%NEUT、#LYMPH、%LYMPH、#MONO、%MONO、#EOS、%EOS、#BASO、%BASO、#LUC、%LUC、#RETIC、%RETIC、MCVr、CHr、CHCMr)、血清生化学(含电解质)(AST、ALT、ALP、CK、LDH、BUN、Crea、T.P、ALB、GLU、T.BIL、T.CHO、TG、γ-GT、K+、Na+、Cl-、TCa)、凝血功能(PT、TT、Fbg、APTT)检测,心脏、肝、脾、肺、肾、肾上腺、胸腺、脑、生殖器官(雄性为睾丸和附睾,雌性为卵巢和子宫)等主要脏器的称重、大体观剖检和组织病理学检查。综合评估“安儿宁颗粒”对幼年大鼠的毒性情况。
1.3 统计学分析
选用SPSS统计分析软件进行数据统计分析。计量资料采用平均值 ± 标准差(±s)表示,选用单因素方差(One-way ANOVA)进行显著性分析;计数资料采用卡方检验(χ2)进行显著性分析。显著性水平为0.05。
2 结果
2.1 单次给药毒性实验
溶媒对照组幼龄大鼠未见明显异常反应;给药组幼龄大鼠在给药后约30 min陆续出现流涎、活动减少、闭眼,至给药后约3 h消失,同时出现着色尿、软便、稀便、肛周污浊,给药后48 h所有反应基本消失,未出现死亡或濒死。给药组大鼠体重随实验时间延长而增加,但增长速度低于溶媒对照组(P< 0.01或P< 0.05),见图1。实验结束后剖检显示,给药组和溶媒对照组大鼠各脏器组织的外观形态均未见明显异常。以上反应主要为短时间内空腹给予高浓度、大体积中药混悬液后的常见反应,不排除对大鼠体重增长率有减缓影响。

图1 单次经口给予安儿宁颗粒对幼年大鼠体重的影响Note. Compared with the control group, *P < 0.05,**P < 0.01.Figure 1 Effects of single oral administrated AEN on body weight of juvenile SD rats
2.2 重复给药毒性实验
2.2.1 一般反应、体重和摄食量
实验期间,各组大鼠外观、行为和活动等一般反应均未见明显异常,无死亡或濒死。安儿宁颗粒高剂量组大鼠给药后第2周(♀)、第1 ~ 7周(♂)和13周(♂)体重均显著低于溶媒对照组(P< 0.01或P< 0.05),其余各组大鼠的体重和溶媒对照组无明显差异(见图2)。安儿宁颗粒低剂量组大鼠给药后第8、11、12周(♂)和第13周(♀)、中剂量组大鼠给药后第8、11周(♂)和第2、11、12周(♀)、高剂量组大鼠给药后第1 ~ 5、7、9、11 ~ 13周(♂)和第1 ~ 3、9、12 ~ 13周(♀)摄食量显著低于溶媒对照组(P< 0.01或P< 0.05),其余各组大鼠的摄食量和溶媒对照组无明显差异(见图2)。唐古特乌头组大鼠的摄食量和体重未见明显影响。
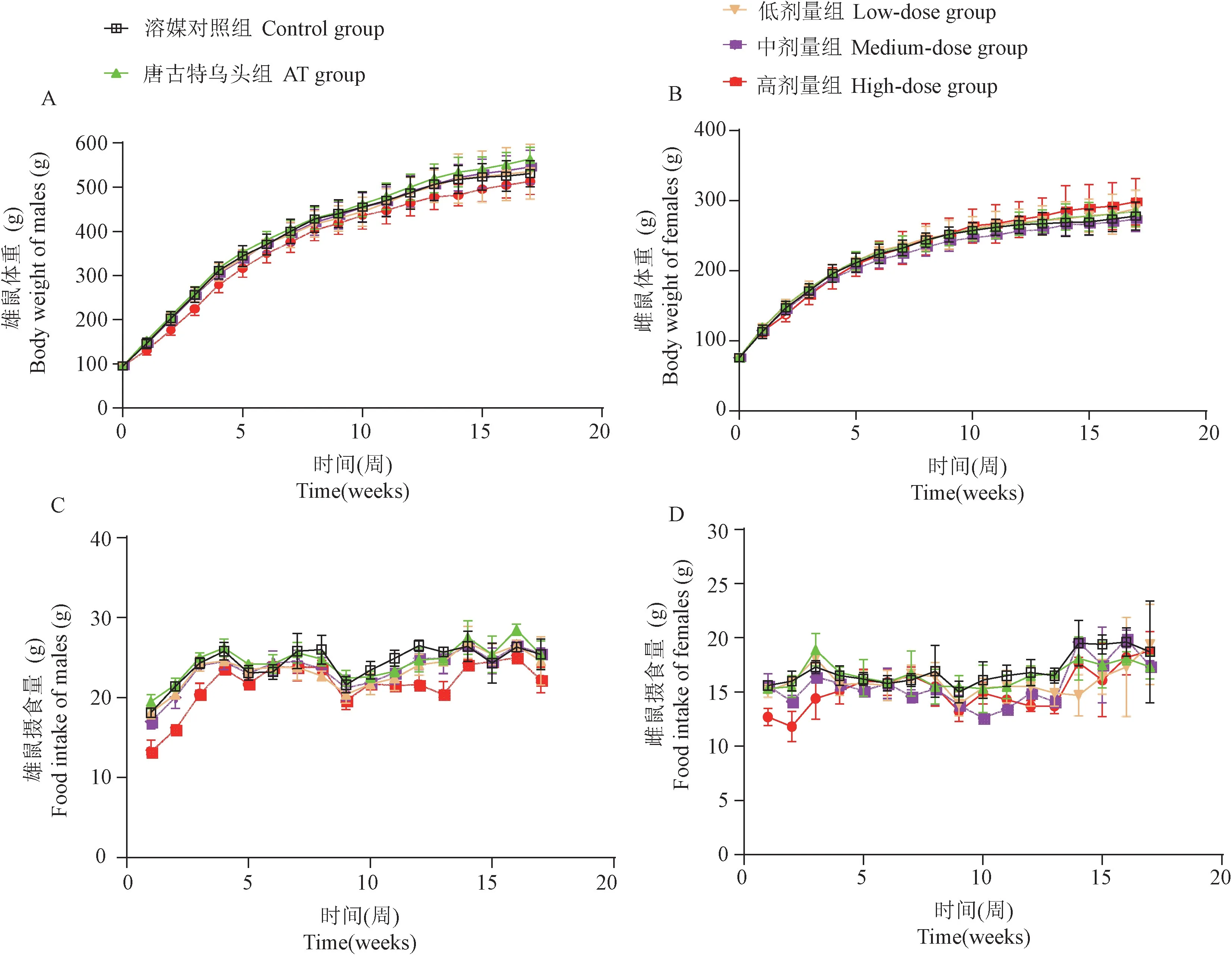
图2 重复经口给予安儿宁颗粒对幼年大鼠体重和摄食量的影响Figure 2 Effects of repeated oral administrated AEN on body weight and food intake of juvenile SD rats
2.2.2 血液学
停药次日,和对照组比,唐古特乌头组、安儿宁颗粒低、中、高剂量组雄鼠的中性粒细胞数显著升高(P< 0.01或P< 0.05),唐古特乌头组、安儿宁颗粒低、高剂量组雄鼠的单核细胞数显著升高(P< 0.01或P< 0.05),上述指标至恢复期结束后均回归正常,说明是可逆的。另出现个别指标波动,停药次日:唐古特乌头组雄鼠和安儿宁颗粒中剂量雌鼠的嗜酸性粒细胞数、高剂量组雌鼠的淋巴细胞数(P< 0.01)有效幅度的降低,且无剂量相关性,结合实验室背景数据,判断其无毒理学意义(表1)。
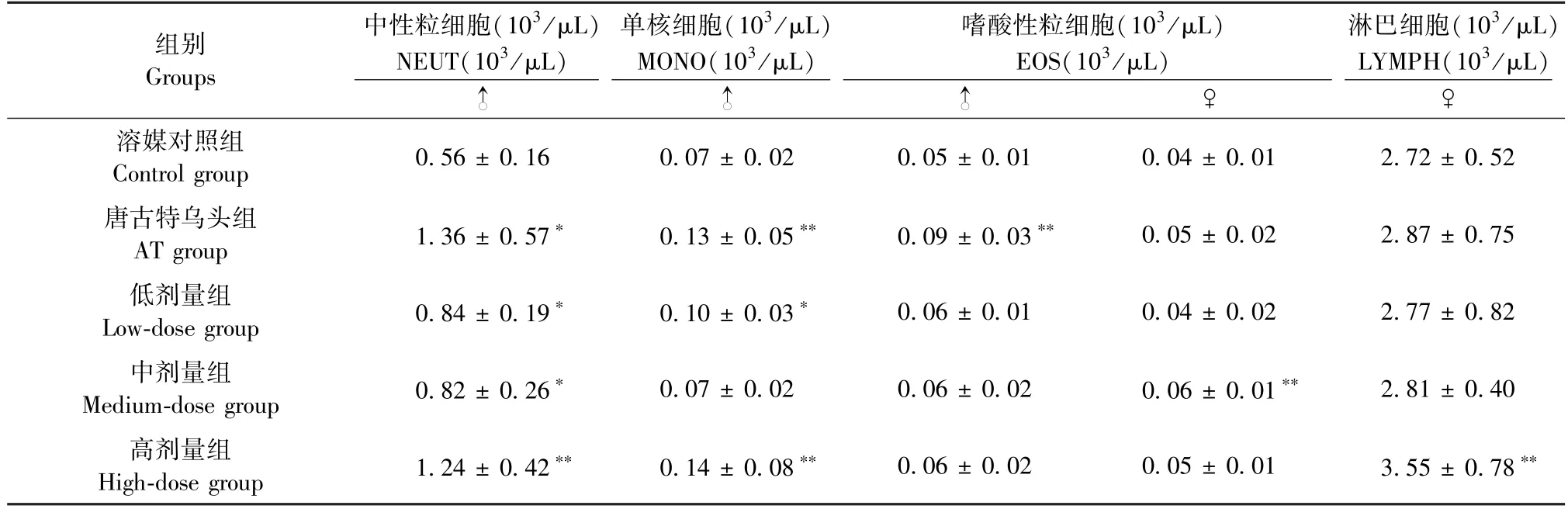
表1 安儿宁颗粒对幼年大鼠血液学指标的影响(停药检查阶段)(x- ± s,n = 10)Table 1 Effects of AEN on hematology in juvenile SD rats(Drug withdrawal)(x- ± s,n = 10)
2.2.3 血清生化学
停药检查,唐古特乌头组和安儿宁颗粒高剂量组雄鼠的血清白蛋白显著高于溶媒对照组(P< 0.01或P< 0.05),停药4周恢复正常,提示可能与唐古特乌头给药剂量有关;停药时,安儿宁颗粒低、中、高剂量组雄鼠的AST、Na+、Cl-显著低于溶媒对照组(P< 0.01或P< 0.05),呈一定的剂量反应关系,停药4周后均恢复正常,可能与给药有关;另停药时高剂量雄鼠ALT和唐古特乌头组雌鼠GLU小幅降低(P< 0.01),考虑为无毒理学意义(见表2)。
表2 安儿宁颗粒对幼年大鼠血清生化学指标的影响(停药检查阶段)( ± s,n = 10)Table 2 Effects of AEN on serum biochemistry in juvenile SD rats(Drug withdrawal)( ± s,n = 10)

表2 安儿宁颗粒对幼年大鼠血清生化学指标的影响(停药检查阶段)( ± s,n = 10)Table 2 Effects of AEN on serum biochemistry in juvenile SD rats(Drug withdrawal)( ± s,n = 10)
2.2.4 凝血功能
停药时高剂量组雄鼠和安儿宁颗粒中、高剂量组雌鼠的APTT和TT均较溶媒对照组有小幅降低(P< 0.01或P< 0.05),但均在实验室背景数据范围内,未表现明显的剂量-反应关系,综合考虑其无毒理学意义。具体见表3。
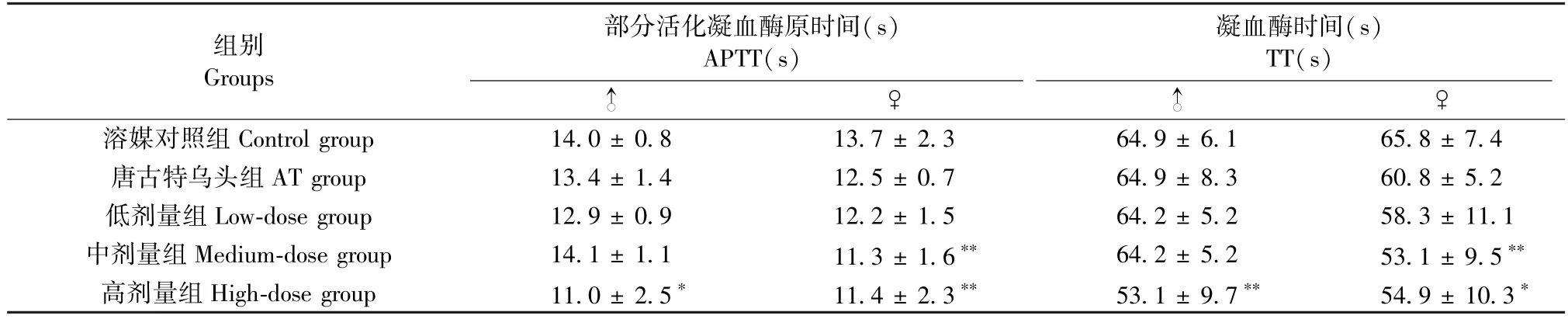
表3 安儿宁颗粒对幼年大鼠凝血指标的影响(停药检查阶段)(x- ± s,n = 10)Table 3 Effects of AEN on coagulation index in juvenile SD rats(Drug withdrawal)(x- ± s,n = 10)
2.2.5 眼科和尿液检查
各检查阶段中,唐古特乌头和安儿宁颗粒各剂量组的眼科检查和尿液检查指标均与对照组大鼠相似(P> 0.05),无统计学差异。
2.2.6 脏器重量和系数以及组织病理学检查
停药检查时高剂量组雄鼠的肝、肾系数及雌鼠的肝、肾重量和系数均高于溶媒对照组(P< 0.01),但病理组织学检查未见明显病变,判断为无毒理学意义的无规律个体差异。各组其他脏器的重量和系数均与相应时间的对照组相似(P> 0.05)(见表4)。
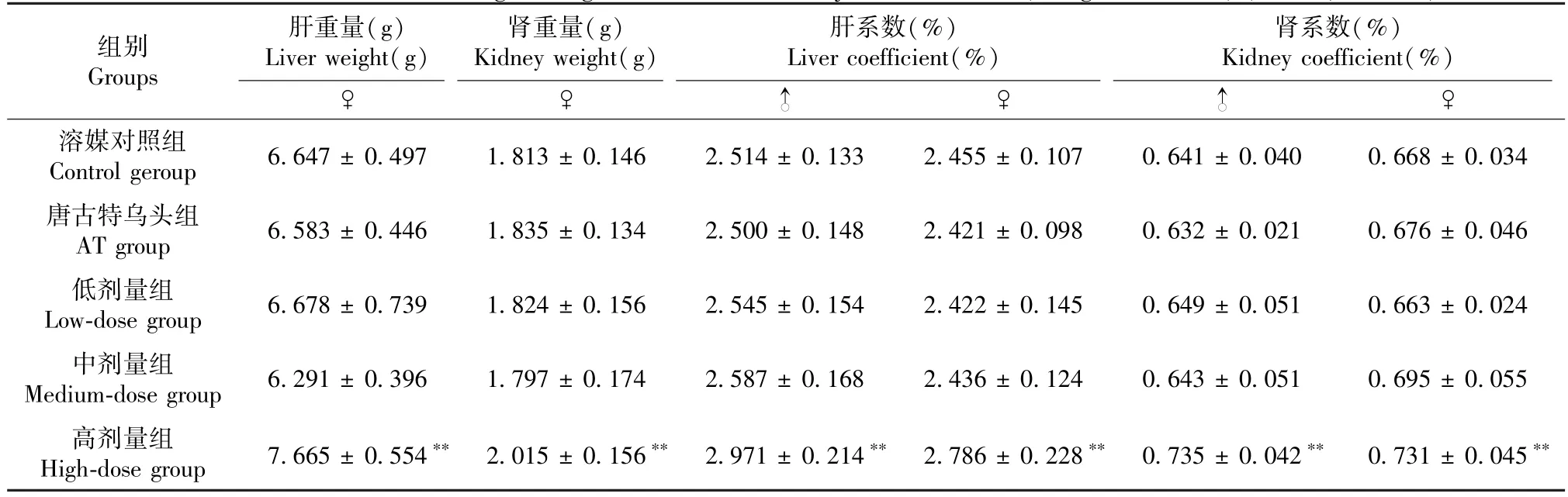
表4 安儿宁颗粒对幼年大鼠脏器重量和脏器系数的影响(停药检查阶段)(x- ± s,n = 10)Table 4 Effects of AEN on organ weight and coefficient in juvenile SD rats(Drug withdrawal)(x- ± s,n = 10)
各组大鼠各脏器的组织病理学检查,均未出现与药物有关的明显的实质性病变(见图3)。
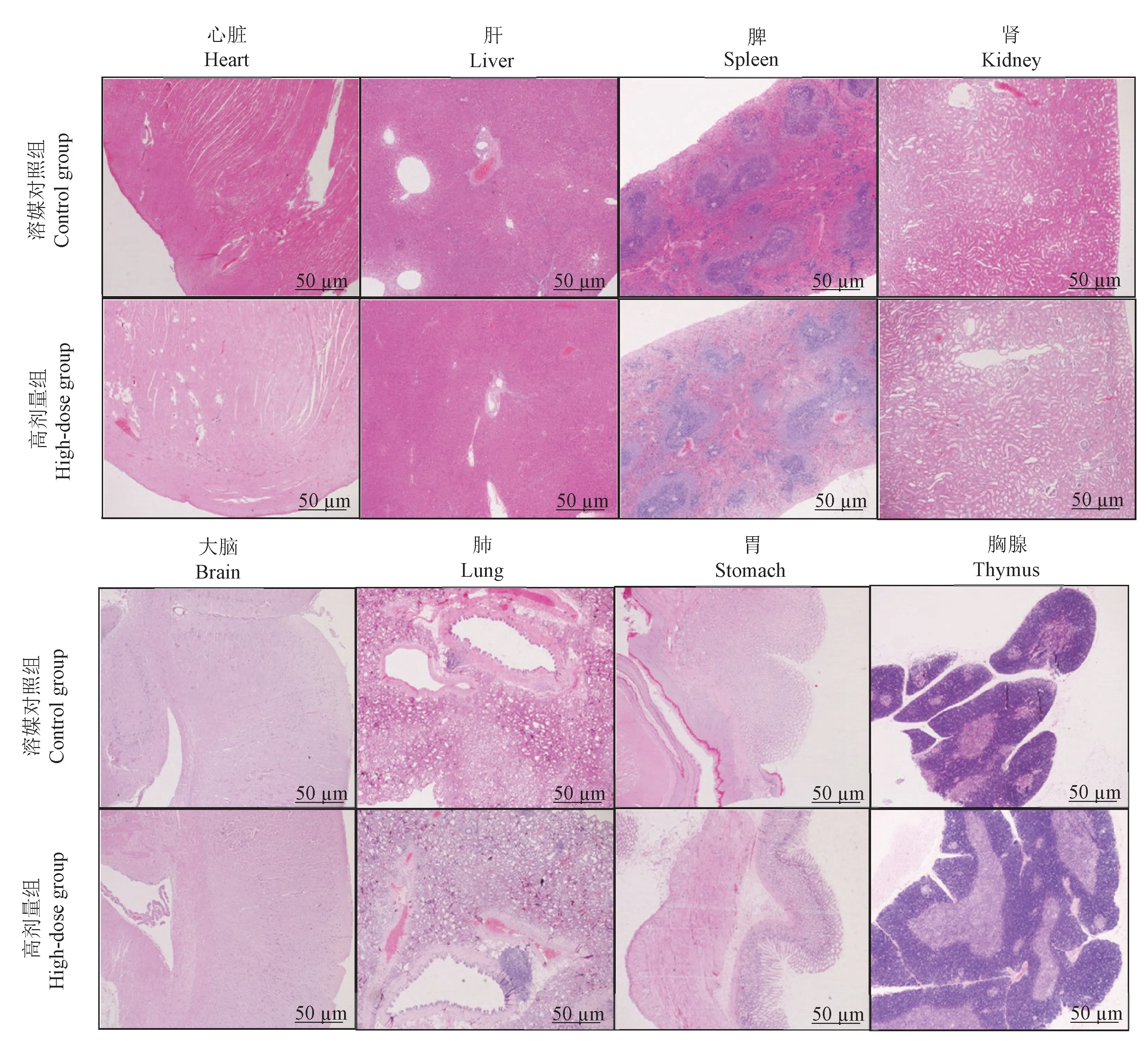
图3 重复经口给予安儿宁颗粒后幼年大鼠主要脏器的病理学图片(停药检查阶段)Figure 3 Histopathological images of main organs of juvenile SD rats after repeated oral administrated AEN (Drug withdrawal)
3 讨论
儿童的各器官和系统处于发育过程中,其脏器结构、生理功能与成人存在差别,可能会对药物毒性或对毒性的耐受程度产生不同的影响[14-16]。因此,需要采用幼年动物的非临床试验安全性数据,以充分评估儿科药物的临床长期使用安全性[17]。安儿宁颗粒作为藏医经典儿科用药,方中多含藏医特有药材,其中唐古特乌头为青藏高原特有毛茛科植物唐古特乌头和船盔乌头的干燥全草。传统藏医认为唐古特乌头无毒且具有清热解毒功效,但现代有研究发现唐古特乌头中的总生物碱对小鼠具有一定的心脏毒性[5],且由于唐古特乌头不是内地常用药材,易被认为属于有大毒的乌头类中药(川乌、草乌等)。为明确安儿宁颗粒中唐古特乌头的毒性,并充分评估安儿宁颗粒在临床使用中对儿童患者的安全性,有必要开展安儿宁颗粒对幼年动物的单次给药毒性和重复给药毒性实验。
据《儿科用药非临床安全性研究技术指导原则》,幼龄动物毒理学实验首选啮齿类动物[18],本研究采用传统动物品系SD大鼠。重复给药毒性实验中设计SD大鼠的起始给药年龄为3 ~ 4周,相当于人类的儿童期(2 ~ 12岁),给药结束年龄为16 ~ 17周,相当于已成年,用以支持2岁儿童至成年的发育阶段中药物的毒性评价[19-20]。
据2020版《中华人民共和国药典》记载,每1 g安儿宁颗粒含生药材0.485 g,临床用量为每次1.5 g(< 1岁),3 g/次(1 ~ 5岁),6 g/次(> 5岁),每日3次,儿童(按标准体重30 kg计)临床日用量为0.144 g生药/ kg体重,按体表面积折算成幼年大鼠(按100 g体重计)日用量为0.864 g生药/ kg体重。本研究单次给药毒性实验的剂量为临床日用量的277.8倍,重复给药毒性实验低、中、高剂量分别为临床日剂量的3.5、12.7、46.3倍;唐古特乌头组剂量与安儿宁颗粒高剂量所含唐古特乌头的剂量相同(临床日剂量的46.3倍),以充分暴露安儿宁颗粒及唐古特乌头的毒性。
本研究考虑成药颗粒剂含有较多辅料成分,无法提高动物实验给药剂量,为了加大毒性暴露和保证给药剂量的准确性,故采用特制高浓度安儿宁颗粒(清膏)和人工牛黄临用前按比例配制。研究结果显示,幼年大鼠单次给予最大给药量的安儿宁颗粒,体重随实验时间延长而增加,但增长速率低于溶媒对照组;重复3个月给予安儿宁颗粒,一般观察及凝血、尿液、眼科、组织病理学检查等均未见明显毒性反应,可见高剂量雄鼠摄食量小幅减少和体重增长略有减缓,嗜中性粒细胞(%NEUT、# NEUT)和单核细胞数(%MONO、# MONO)、血清白蛋白(ALB)可逆性升高,天门冬氨酸转氨酶(AST)、Na+、Cl-可逆性下降,上述变化偏离本实验室背景数据幅度较小,且停药后基本恢复正常,组织病理学检查也未见毒性靶器官。因此,安儿宁颗粒在幼年大鼠的单次给药毒性和重复给药毒性实验中,基本无显著毒理学意义的反应,但由于均可见体重速率的减缓,提示临床上患儿大剂量使用安儿宁颗粒可能会有降低摄食和体重减轻的风险。综合评价,安儿宁颗粒的相对安全剂量为40.0 g生药/kg体重,未观察到有害作用(NOAEL)剂量为11.0 g生药/kg体重。临床上,儿童按每日最大服用量(18 g成品药),3 ~ 5 d的临床用药疗效安全。
值得注意的是,本研究中单次给药毒性和重复给药毒性实验古特乌头生药材的剂量分别为33 g/kg体重和5.5 g/kg体重,相当于标准体重儿童日服用唐古特乌头生药材156 g和26 g,是法定标准日服用量(0.6 ~ 1.2 g)[7]上限的120和20多倍。仅表现为重复给药毒性实验中唐古特乌头组嗜中性粒细胞和单核细胞数、血清白蛋白可逆性升高,未出现文献中的毒性反应[5]。考虑文献中总生物碱采用乙醇提取得到,而安儿宁颗粒采用水提取工艺,经加热煎煮,有毒成分可能被降解,毒性显著降低[7]。且有文献指出虽然唐古特乌头与有毒中药乌头均属毛茛科乌头属植物,但其主要活性成分为内酯型生物碱,基本无毒且具有清热解毒功效,其药效物质基础、药理作用、安全性,与传统中药乌头(川乌、草乌、雪上一枝蒿等)完全不同[7]。结合本研究结果,安儿宁颗粒中藏药唐古特乌头的临床使用具有安全性。
本研究充分评估了安儿宁颗粒对幼年动物的毒性反应,更进一步论证其长期使用的安全性,同时也为安儿宁颗粒用于儿童手足口病和哮喘等适应症提供一定的理论基础。
