恩替卡韦治疗乙型肝炎的疗效分析及评价
2022-03-09刘同博
刘同博



[摘要] 目的 分析恩替卡韋治疗乙型肝炎的疗效。 方法 选取2019年1月至2020年1月黑龙江省佳木斯市传染病院108例乙型肝炎患者,采用随机数字表法分为观察组和对照组,观察组(n=54)患者服用恩替卡韦,对照组(n=54)采用干扰素 α-2a 注射液治疗,比较两组患者临床疗效、ATL复常率、HBV-DNA转阴率、凝血酶原活动度、HBV-DNA应答率、谷丙转氨酶(ALT)、天门冬氨酸氨基转移酶(AST)、总胆红素(TBIL)水平。 结果 观察组与对照组临床治疗总有效率(96.30% vs. 75.93%)比较,差异有统计学意义(P<0.05);观察组ATL复常率(96.30%)、HBV-DNA转阴率(92.59%)均明显高于对照组的77.78%、75.93%,差异有统计学意义(P<0.05);观察组治疗后凝血酶原活动度均明显高于对照组,差异有统计学意义(P<0.001);观察组治疗后HBV-DNA应答率为94.44%,明显高于对照组的79.63%,差异有统计学意义(P<0.05);观察组治疗后谷丙转氨酶(ALT)、天门冬氨酸氨基转移酶(AST)、总胆红素(TBIL)水平明显低于对照组,差异有统计学意义(P<0.001)。 结论 给予乙型肝炎患者恩替卡韦抗病毒治疗,临床效果明显,可显著提高ATL复常率和HBV-DNA转阴率,并且改善肝功能,对稳定患者病情,避免病情进展具有重要帮助。
[关键词] 恩替卡韦;乙型肝炎;肝功能;凝血酶原活动度;HBV-DNA应答;乙型肝炎病毒感染
[中图分类号] R512.6 [文献标识码] B [文章编号] 1673-9701(2022)02-0116-04
Analysis and evaluation of the therapeutic efficacy of adopting entecavir in the treatment of hepatitis B
LIU Tongbo
Department of Pharmacy, Jiamusi Infectious Disease Hospital in Heilongjiang Province, Jiamusi 154007, China
[Abstract] Objective To analyze the therapeutic efficacy of adopting entecavir in the treatment of hepatitis B. Methods A total of 108 patients with hepatitis B admitted from January 2019 to January 2020 were selected and divided into the observation group (n=54) and the control group (n=54) according to the random number table method in Jiamusi Infectious Disease Hospital in Heilongjiang Province. The observation group was treated with entecavir, while the control group was treated with interferon α-2a injection. The clinical efficacy, ATL normalization rate, HBV-DNA negative conversion rate, prothrombin activity, the response rate of HBV-DNA, the levels of alanine aminotransferase (ALT), aspartate aminotransferase (AST) and total bilirubin (TBIL) of patients in the two groups were compared. Results The overall response rate of clinical treatment between the observation group and the control group was (96.30% vs. 75.93%), with statistically significant difference (P<0.05). The ATL normalization rate (96.30%) and HBV-DNA negative conversion rate (92.59%) in the observation group were all significantly higher than those of 77.78% and 75.93% in the control group, with statistically significant differences(P<0.05). After treatment, the prothrombin activity in the observation group was significantly higher than that in the control group, with statistically significant difference (P<0.001). After treatment, the response rate of HBV-DNA in the observation group was 94.44%, which was significantly higher than that of 79.63% in the control group, with statistically significant difference between the two groups (P<0.05). After treatment, the levels of alanine aminotransferase (ALT), aspartate aminotransferase (AST) and total bilirubin (TBIL) in the observation group were lower than those in the control group,with statistically significant differences (P<0.001). Conclusion Antiviral treatment with entecavir in patients with hepatitis B has obvious clinical efficacy, which can significantly improve ATL normalization rate and HBV-DNA negative conversion rate, and improve hepatic function, which is of great help to stabilize patients′ condition and avoid disease progression.
[Key words] Entecavir; Hepatitis B; Hepatic function; Prothrombin activity; HBV-DNA response; Hepatitis B virus infection
乙型肝炎属于常见肝脏系统传染性疾病,主要由乙型肝炎病毒(hepatitis B virus,HBV)持续感染引起,此病在全球范围内均属于高发疾病。据不完全统计,全球无症状HBV携带者高达2.8亿,仅我国就有1.3亿携带者[1]。慢性乙型肝炎持续进展,可引发肝硬化、肝衰竭、肝癌疾病,不仅对患者身心健康造成严重影响,同时也会显著威胁到生命安全。目前,针对乙型肝炎,临床主要采用抗病毒类药物进行干预和治疗,为了保证患者治疗效果,减少耐药菌株,需要为患者选择正确的治疗药物,从而保证用药安全性和有效性。恩替卡韦属于常见抗病毒治疗药物,本研究从所在医院乙型肝炎患者中选取服用该药的患者进行分析,并与采用干扰素α-2a注射液治疗患者进行对比,现报道如下。
1 资料与方法
1.1 一般资料
从2019年1月至2020年1月黑龙江省佳木斯市传染病院收治的所有乙型肝炎患者中抽取满足研究条件的108例患者,将其作为研究样本,纳入病例均符合用药规范,且对临床治疗情况知情,纳入病例均无药敏史,且依从性良好。采用随机数字表法分为观察组和对照组,每组各54例。观察组男女比例为29∶25,年龄21~83岁,平均(55.65±5.74)岁,病程1~15年,平均(6.92±1.87)年;对照组男女比例为30∶24,年龄20~82岁,平均(55.87±5.57)岁,病程1~16年,平均(6.95±1.90)年。两组患者资料准确无误,且经数据统计分析,两组不受年龄、性别、病程及其他因素影响(P>0.05),具有可比性。本研究经医院医学伦理委员会批准。纳入标准[2]:①所选患者符合慢性乙型肝炎诊断标准,病历资料完善;②患者对本研究知情同意,且支持后续随访工作;③患者符合用药标准;④实验室检查无严重异常指标者;⑤能够正常交流沟通者;⑥西医诊断明确者。排除标准[2]:①合并严重精神类疾病及其他器质性病变者;②拒绝复查及随访者;③合并其他严重疾病者;④合并认知功能、行为功能异常者;⑤存在用药禁忌或具有可预见性用药风险者;⑥心肺功能严重异常者;⑦合并肝硬化及肝癌者;⑧中途放弃药物治疗者。诊断标准:参照《慢性乙型肝炎诊断标准(2015年版)》[3]:血清HBsAg和(或)HBV DNA阳性,既往有乙型肝炎病史或HBsAg阳性超过6个月。
1.2 方法
1.2.1 观察组 本组患者采用恩替卡韦(中美上海施贵宝制药有限公司,国药准字H20080798,规格:0.5 mg/片)进行治疗,给药方式为口服,服药剂量为每天0.5 mg,每天1次。本组患者连续用药6个月,用药期间定期回院观察。
1.2.2 对照组 本组患者采用干扰素α-2a注射液(厦门特宝生物工程股份有限公司,国药准字S20160001, 180 μg(66万U)/0.5 ml)治疗,给药方法为皮下注射,每次剂量为0.5 ml,每周1次。本组患者连续用药6个月,用药期间定期回院观察。
1.3 观察指标及评价标准
1.3.1 临床疗效判断标准[4] ①显效:检查结果正常,症状及其他体征消失;②好转:临床症状和体征明显改善,相关检查结果正常;③无效:未达到上述疗效,或病情加重。总有效率=(显效+好转)例数/总例数×100%。
1.3.2 转阴及应答 比较两组患者治疗后ATL复常率、HBV-DNA转阴率及治疗后HBV-DNA应答率。HBV-DNA应答率分为完全应答、部分应答和无应答,应答率[5]=(完全应答+部分应答)例数/总例数×100%。
1.3.3 临床检验结果 比较两组患者治疗前后凝血酶原活动度、谷丙转氨酶(alanine aminotransferase,ALT)、天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)、总胆红素(total bilirubin,TBIL)水平,做好详细记录。
1.4 统计学方法
采用SPSS 25.0统计学软件进行数据分析,计量资料以(x±s)表示,采用t检验。计数资料以[n(%)]表示,采用χ2检验,P<0.05为差异有统计学意义。P<0.001为差异有极其显著的统计学意义。
2 结果
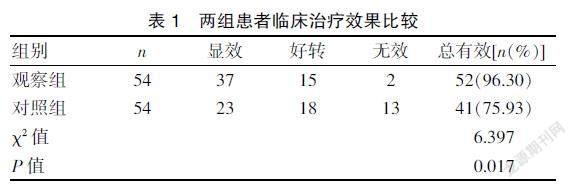
2.1 两组患者临床治疗效果比较
观察组与对照组临床治疗总有效率(96.30% vs.75.93%)比较,差异有统计学意义(P<0.05)。见表1。
2.2 两组患者相关指标转阴率比较
观察组ATL复常率为96.30%、HBV-DNA转阴率为92.59%,均明显高于对照组的77.78%、75.93%,差异有统计学意义(P<0.05)。见表2。
2.3 两组患者治疗前后凝血酶原活动度比较
两组患者治疗前凝血酶原活动度比较,差异无统计学意义(P>0.05);经过用药治疗后,观察组凝血酶原活动度明显高于对照组,差异有统计学意义(P<0.001)。见表3。
2.4 两组患者治疗后HBV-DNA应答情况比较
观察组治疗后HBV-DNA应答率为94.44%,明显高于对照组的79.63%,差异有统计学意义(P<0.05)。見表4。
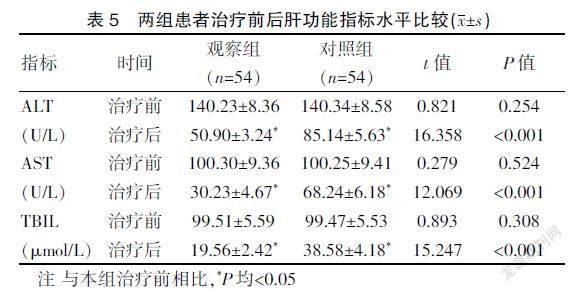
2.5 两组患者治疗前后肝功能指标水平比较
两组患者治疗前谷丙转氨酶(ALT)、天门冬氨酸氨基转移酶(AST)、总胆红素(TBIL)水平比较,差异无统计学意义(P>0.05);经过用药治疗后,观察组与对照组上述指标均有一定降低,与本组治疗前相比,差异有统计学意义(P<0.05)。但是,观察组治疗后ALT、AST、TBIL水平明显低于对照组,差异有统计学意义(P<0.001)。见表5。
3 讨论
我国乙型肝炎疾病发病率较高,一般发病超过6个月时间可称为慢性乙型肝炎,此时HBV病毒已经大量存在于患者体内,并且复制速度极快,形成免疫应答反应。慢性乙型肝炎病毒具有传染性,传播途径比较广泛,包括母婴传播、血液传播、性传播等,对患者生活质量造成严重影响。有学者[6-7]提出,对发病因素的研究至关重要,对临床治疗具有一定指导意义。目前针对乙型肝炎的发病机制,学界及临床均无统一定论,但普遍认同家族遗传、饮酒、HIV感染等因素是其主要发病原因,并且往往是上述因素共同影响和作用的结果。
大量研究证实[8-9],慢性炎症反应所产生的刺激长期存在乙型肝炎患者机体内,加之HBV病毒持续复制,可导致患者肝脏细胞出现免疫性损伤,并产生病理性变化,进而造成患者机体免疫功能缺损。有学者[10]指出,HBV病毒持续感染是慢性乙型肝炎患者出现肝硬化、肝细胞严重损伤的主要诱因,而HBV病毒复制的过程是具有连续性,并呈现高活跃性,进入到肝细胞内后,会与细胞核孔中相关复合物进行结合,从而使肝细胞结构发生整体变化,对肝细胞正常的生理功能造成严重损害,使其无法发挥正常代谢作用。
目前,临床治疗乙型肝炎主要通过抗病毒类药物,对乙型肝炎病毒复制进行有效抑制,并且改善患者肝功能,为患者病情恢复提供必要支持[11]。恩替卡韦属于乙型肝炎抗病毒治疗的一线药物,其发挥药效的主要途径是对乙型肝炎病毒聚合物自身的生物活性进行有效抑制,从而发挥抗病毒效果。有研究[12]证实,乙型肝炎患者通过口服恩替卡韦,能够在体内迅速产生磷酸化活性成分,此种成分能够与乙型肝炎病毒多聚酶形成竞争关系,抑制乙型肝炎病毒的复制,从而延缓患者病情进展。也就是说,恩替卡韦进入到患者体内后,经过磷酸化处理后,可轉变为一定化合物,活性强,与病毒多聚酶形成竞争关系后,能够对病毒DNA合成过程进行相应阻碍,同时避免病毒多聚酶转录,从而发挥明显抗病毒功效。
本研究分析恩替卡韦的临床疗效,并与干扰素进行对比,结果证实,服用恩替卡韦的患者,其临床治疗总有效率(96.30%)、ATL复常率(96.30%)、HBV-DNA转阴率(92.59%)均明显高于服用干扰素者,与文献[13-14]报道结果基本一致,充分说明恩替卡韦的临床应用优势。与此同时,服用恩替卡韦后,患者凝血酶原活动度及肝功能指标(ALT、AST、TBIL)水平改善更为明显,提示临床恩替卡韦在乙型肝炎抗病毒治疗中所发挥的关键作用。有研究[15]证实,长期服用恩替卡韦,不会增加临床耐药性,并且能够延缓患者肝硬化、肝纤维化进程,降低死亡风险。
综上所述,给予乙型肝炎患者恩替卡韦抗病毒治疗,临床效果显著,能够在提高ATL复常率和HBV-DNA转阴率的同时,明显改善患者肝功能,对稳定患者病情,避免病情进展具有重要帮助。但是,本研究未对两组用药期间不良反应发生情况进行相应统计,这是因为患者普遍耐受性良好,轻微不良反应未经处理自行改善。
[参考文献]
[1] 陈潇潇.恩替卡韦和替比夫定治疗高病毒载量慢性乙型肝炎患者的远期疗效分析[J].当代医学,2020,26(30):184-186.
[2] 田琰,武胜,邓双双.扶正化瘀胶囊结合抗病毒药物对乙型肝炎肝硬化的治疗效果及谷草转氨酶-血小板比值指数的影响[J/OL].中华中医药学刊:1-12[2020-11-08].http://kns-cnki-net.wvpn.ncu.edu.cn/kcms/detail/21. 1546.R.20201020.0957.062.html.
[3] 中华医学会肝病学分会.慢性乙型肝炎诊断标准(2015年版)[J].中西医结合肝病杂志,2015,25(6):384-386.
[4] 林文武,余雪平,郑怡娟,等.恩替卡韦与替诺福韦对HBeAg阳性初治慢性乙型肝炎患者的疗效及安全性分析[J].中外医学研究,2020,18(28):55-57.
[5] 韩思源,全冰.替诺福韦酯与恩替卡韦单药序贯治疗在阿德福韦酯治疗失败慢性乙型肝炎中的应用比较[J].中国医学创新,2020,17(27):11-14.
[6] 詹爱琴,陈春丽,安轶,等.恩替卡韦对慢性乙型肝炎患者Treg/Th17细胞平衡及相关细胞因子水平的影响分析[J].新疆医学,2020,50(9):906-909.
[7] 夏小芳,吴建,施维群,等.扶正化瘀胶囊联合恩替卡韦治疗慢性乙型肝炎肝纤维化的疗效及对血液流变学和血清IL-17表达的影响[J].中国临床药学杂志,2020, 29(5):334-338.
[8] 史娜,宋娟丽,王静,等.红外肝病治疗仪联合恩替卡韦及乙肝抗纤汤治疗老年慢性乙型肝炎的疗效[J].国际老年医学杂志,2020,41(5):322-325.
[9] 周秀芬,刘英果,孙容花,等.恩替卡韦联合奥沙利铂、卡培他滨治疗对乙型肝炎病毒相关晚期肝细胞癌患者外周血淋巴细胞亚群的影响[J].中国肝脏病杂志(电子版),2020,12(3):79-84.
[10] 司永.茵陈贞芪六君子汤加减联合恩替卡韦治疗慢性乙型肝炎肝硬化的疗效及对肝功能、病毒复制能力的影响[J].四川中医,2020,38(9):105-109.
[11] 孙静,朱琳,池欣,等.恩替卡韦单药与联合干扰素抗病毒治疗对慢性乙型肝炎患者肝细胞癌发生风险的影响[J].临床肝胆病杂志,2020,36(9):1975-1979.
[12] 方奕,陈毅雄,裴冬萍,等.恩替卡韦联合复方嗜酸乳杆菌治疗CHB合并NAFLD患者疗效及其对血清相关酶系的影响[J].实用肝脏病杂志,2020,23(5):634-637.
[13] 吴雄飞,方利娟,陈艳.替诺福韦联合干扰素-α治疗HBeAg阳性慢性乙型肝炎患者疗效及其血清细胞因子水平变化[J].实用肝脏病杂志,2020,23(5):638-641.
[14] 陈海燕,林万宝,闵胜利.胸腺五肽联合恩替卡韦抗病毒治疗慢性乙肝血清ALT水平与肝细胞肝癌发生风险相关性[J].黑龙江医学,2020,44(8):1074-1076.
[15] 白洁.逍遥散联合恩替卡韦对慢性乙型病毒性肝炎患者乙肝病毒的脱氧核糖核酸阴转率、乙型肝炎e抗原阴转率的影响[J].中国药物经济学,2020,15(8):113-115.
(收稿日期:2021-01-15)
3624501908264
