电化学氧化处理焚烧厂渗滤液膜浓缩液混凝出水的研究
2022-03-08何雪连
肖 玉,何雪连,彭 月,刘 建
(西南交通大学地球科学与环境工程学院,成都 611756)
引 言
2019年,生活垃圾焚烧处理量约占我国生活垃圾无害化处理量的51%[1],焚烧已成为我国生活垃圾最主要的处理方式。垃圾焚烧前需堆放发酵以提高垃圾热值,此过程不可避免会产生大量垃圾渗滤液。现阶段国内一般采用“预处理+生物处理+膜深度处理”组合工艺处理垃圾渗滤液,但膜深度处理环节会产生约占渗滤液处理量15%~30%的膜浓缩液。膜浓缩液是一种含大量盐分的高浓度有机废水,可生化性差,处理难度大[2]。回喷焚烧是处理膜浓缩液最简单、快捷的方法,但回喷焚烧会加剧焚烧及烟气处理设备腐蚀[3]。因此,亟需寻找一种更为高效、经济的膜浓缩液处理方法。
目前,研究膜浓缩液处理的主要技术有蒸发、混凝、膜蒸馏及高级氧化技术。课题组Ren等[4]研究表明,混凝过程能够去除膜浓缩液中大量有机物,但混凝出水仍存在未降解的有机物,需进一步去除。高级氧化通常作为混凝预处理后的深度处理技术,主要包括臭氧氧化、Fenton氧化和电化学氧化技术[5-6]。其中,电化学氧化主要通过阳极直接降解或阳极反应产生·OH等氧化性物质间接降解废水中的有机物,具有环境兼容性好、不易产生二次污染、处理效率高、操作简便、易于实现自动化等特点。膜浓缩液的高盐分使其具有良好的电导率,采用电化学氧化处理无需额外添加电解质。膜浓缩液混凝出水中的大量Cl-可在阳极氧化产生强氧化性的游离氯(Cl2、HClO和ClO-),从而促进有机物的间接氧化[7]。近年来,已有不少利用电化学氧化技术处理膜浓缩液的报道[8-9],但针对膜浓缩液中有机物的去除特性和降解机理的研究报道较少。
鉴于此,本文采用电化学氧化技术处理焚烧厂渗滤液膜浓缩液混凝出水,探究不同阳极材料、电流密度、初始pH值和电解时间对有机物的去除影响。在此基础上,采用三维荧光光谱分析膜浓缩液中有机物的去除特性;并通过对氯离子的转化分析,探讨电解过程中有机物的降解机理,以期为电化学氧化处理渗滤液膜浓缩液或高盐有机废水提供实验依据和理论支撑。
1 材料与方法
1.1 实验样品
本次实验所使用的渗滤液膜浓缩液取自西南地区某城市生活垃圾焚烧发电厂渗滤液纳滤膜处理系统。膜浓缩液混凝预处理的操作条件为调整初始pH值为6,然后投入2.0 g/L聚合硫酸铁(PFS)和20 mg/L聚丙烯酰胺(PAM)。混凝前后膜浓缩液的水质如表1所示。

表1 混凝前后膜浓缩液水质特征Tab.1 Water quality characteristics of leachate membrane concentrate before and after treated by coagulation process
1.2 试剂和仪器
聚合硫酸铁(PFS,分析纯),购于天津鼎盛鑫化工有限公司。聚丙烯酰胺(PAM,阳离子型),购于天津市致远化学试剂有限公司。氢氧化钠(NaOH,分析纯)、硫酸(H2SO4, 分析纯),购于成都科龙化工有限公司。硝酸银(AgNO3,分析纯),购于国药集团化学试剂有限公司。N,N-二乙基-对苯二胺硫酸盐(C6H16N2·H2SO4,分析纯),购于天津市科密欧化学试剂有限公司。钌铱(Ru-Ir/Ti)、铱钽(Ta-Ir/Ti)、不锈钢和石墨电极(50 mm×60 mm×1.5 mm),购于清河县云轩金属材料有限公司。
实验装置如图1所示,主要包括恒压恒流电源、石英反应器、磁力搅拌器和尾气吸收瓶(15% NaOH溶液)。TPR-1520D恒压恒流电源购于香港龙威仪器仪表公司,HJ-6B数显恒温磁力搅拌器购于常州市金坛友联仪器研究所。

1—石英反应器;2—聚四氟乙烯盖;3—阳极;4—阴极;5—导线;6—搅拌子;7—磁力搅拌器;8—恒压恒流电源;9—尾气吸收瓶 图1 电化学氧化实验装置Fig.1 Electrochemical oxidation experimental device
1.3 实验方法
取250 mL废水于石英反应器中,以Ru-Ir/Ti、Ta-Ir/Ti、不锈钢和石墨电极为阳极,不锈钢电极为阴极,调整电极间距为1.0 cm,接通电源并设定恒定电流后开始电化学反应。待反应至预设时间,用45μm混合纤维滤膜对电解出水进行过滤处理后取样分析。
1.4 分析方法
TOC采用岛津TOC-L CPH CN200型TOC分析仪测定;游离氯采用N,N-二乙基-1,4-苯二胺分光光度法测定;氯离子采用硝酸银滴定法测定;色度采用分光光度法测定,以CN值表示:
(1)
式中:A436、A525、A620分别表示膜浓缩液在436、525、620 nm波长时的吸光度值。
三维荧光(3D-EEM)光谱分析采用日立F-7000型荧光分光光度计,扫描激发波长220~450 nm、发射波长250~500 nm、间隔5 nm、速度2400 nm/min。图谱绘制使用Origin 8.5软件进行。
2 结果与讨论
2.1 影响因素分析
2.1.1 阳极材料对有机物的去除影响
设置电流密度40 mA/cm2,在初始pH值为4.02的条件下,分别采用Ru-Ir/Ti、Ta-Ir/Ti、石墨和不锈钢电极作为电化学氧化的阳极电解60 min,考察不同阳极对有机物的去除影响。由表2可知,Ta-Ir/Ti、石墨和不锈钢阳极对TOC的去除效果相差不大,Ru-Ir/Ti阳极对TOC去除效果最佳,去除率为39.55%。结合图2可知,不同阳极对电化学处理出水的色度有显著影响,Ru-Ir/Ti和Ta-Ir/Ti阳极对色度的去除效果显著,均达95%以上,处理出水几乎无色。原因是Ru-Ir/Ti和Ta-Ir/Ti阳极均为DSA稳定电极,在电化学过程中自身不会溶解,电解过程中产生的?OH和游离氯等氧化物能够作用于含发色基团的有机物从而使其高效降解[10]。相比之下,不锈钢阳极对CN的去除效果最差,去除率仅为16.43%。这是因为电化学反应过程中,不锈钢阳极中的Fe会不断失电子产生Fe2+,继而被次氯酸等物质氧化成Fe3+,使溶液成黄绿色,影响出水色度。综上所述,实验选取Ru-Ir/Ti阳极作为电化学氧化处理的最佳阳极。
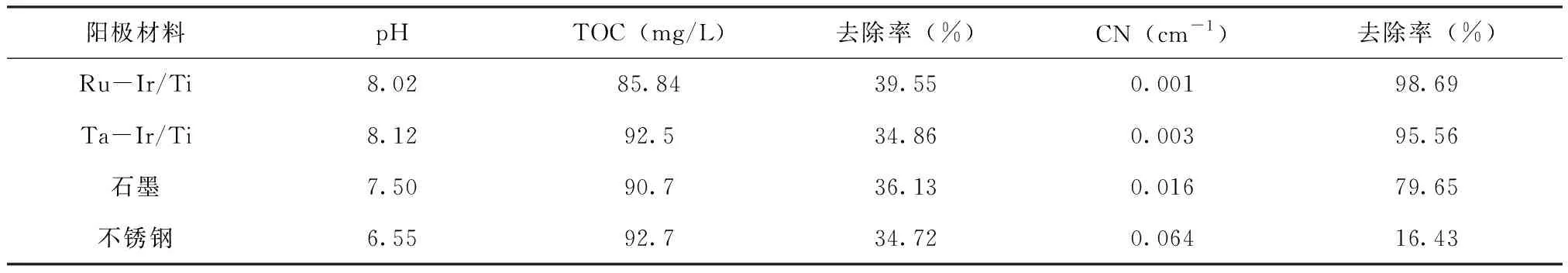
表2 不同阳极对TOC和CN的去除影响

图2 不同阳极电解后的出水色度 Fig.2 the effluent color of different anode electrolysis
2.1.2 电流密度对有机物的去除影响
以Ru-Ir/Ti为阳极,在初始pH值为4.02的条件下电解60 min,考察不同电流密度对有机物的去除影响。由图3可知,随着电流密度增加,TOC去除率也不断增加。当电流密度从10 mA/cm2增加至40 mA/cm2时,去除率从24.96%增加至39.55%,增幅明显。原因是电流密度增加,阴阳电极之间产生的电子数量也随之增加,从而产生更多的强氧化剂,强化直接和间接氧化作用[11]。但继续增加电流密度至50 mA/cm2时,TOC去除率增幅不大,仅增加了0.89%。由此可见,增加电流密度虽会增加单位面积电极上的过电量、加强有机物的降解,但过高的电流密度会不仅对TOC去除率的提高有限,还会增加反应能耗。此外,不同电流密度下,电解出水基本无色,可见低电流密度条件下,含发色基团有机物也能得到有效去除。因此,实验选取40 mA/cm2为最佳电流密度。

图3 电流密度对TOC的去除影响Fig.3 Effect of current density on TOC removal
2.1.3 初始pH值对有机物的去除影响
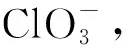
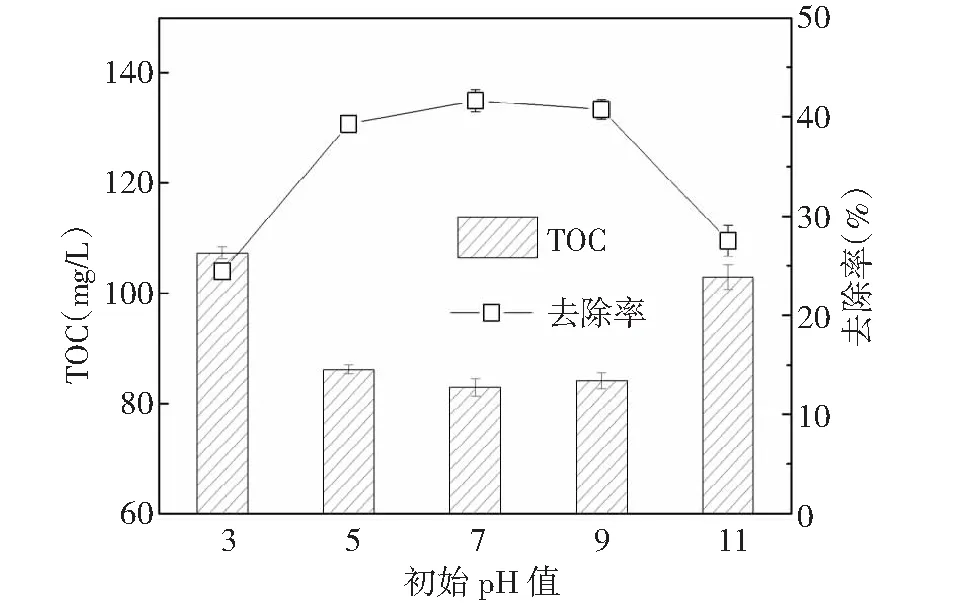
图4 初始pH值对TOC的去除影响Fig.4 Effect of initial pH on TOC removal
2.1.4 电解时间对有机物的去除影响
以Ru-Ir/Ti为阳极,在电流密度为40 mA/cm2、初始pH值为7的条件下电解,考察不同电解时间对有机物的去除影响。由图5可知,随着电解时间增加,TOC浓度不断降低,去除率不断增加。前60 min TOC去除率的增幅最为明显,去除率增加至41.63%。分析原因,在电解初始阶段,废水中存在较多易被电化学氧化的有机物,伴随氧化性游离氯的不断产生,TOC的去除效率迅速增加[14]。继续增加电解时间至180 min,TOC去除率为48.89%,仅增加了7.26%。原因是易被氧化的物质已在电解初期被去除,难降解大分子物质转化为小分子物质,但小分子物质在电化学氧化过程不易被彻底矿化;同时,还观察到随着电解时间增加,阴极不锈钢板的结垢现象越明显,这也会导致电流效率下降。因此,综合考虑经济效率,实验选取60 min为最佳电解时间。

图5 电解时间对TOC的去除影响Fig.5 Effect of electrolysis time on TOC removal
CN的去除率及出水pH值的变化情况如图6所示,研究表明电解对CN的去除效果显著,仅电解10 min,CN的去除效果就达到了91.84%,电解至30 min 时,CN去除率接近100%,这说明废水中的含发色基团物质最先被氧化去除[15]。电解反应过程中溶液pH先增加然后趋于平缓,原因是电解过程中阴极会发生析氢反应,使得溶液中OH-浓度增加,pH值升高。
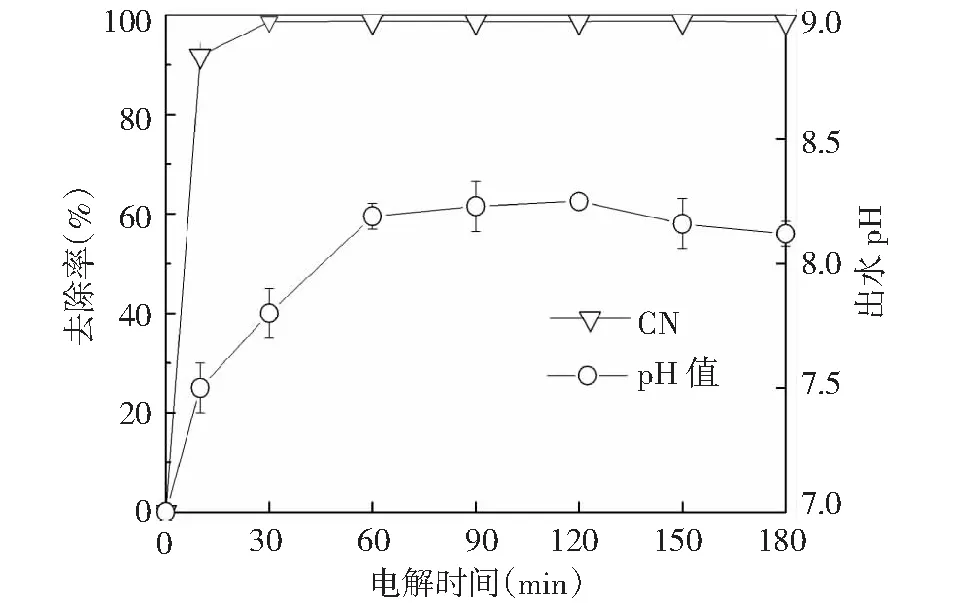
图6 电解时间对CN的去除影响及出水pH值Fig.6 Effect of electrolysis time on TOC removal and effluent pH
2.2 有机物去除特性
膜浓缩液中的主要有机物为大分子腐殖质,采用3D-EEM荧光光谱对电解出水中的腐殖质进行了表征和转化分析[16]。如图7所示,膜浓缩液在激发波长/发射波长为250/460处存在紫外区富里酸荧光峰F1,主要表征低分子量、高荧光效率的类富里酸物质;在激发波长/发射波长为365/455处存在可见光区富里酸荧光峰F2,主要表征相对稳定、分子量较大的类腐殖酸物质[17]。
由表3可知,膜浓缩液混凝出水荧光峰F1和F2的峰强分别为2665和2960,电化学氧化处理后,F1和F2峰强均明显降低且峰位蓝移。电解10 min后,F1和F2的峰强分别降至190.1和262.8,分别降低了92.87%和91.12%;电解60 min后,荧光峰F1消失,F2峰强继续降低至52.85。这说明电化学氧化过程能有效去除膜浓缩中的类富里酸及类腐殖酸物质,并且类富里酸物质优先被去除。电化学氧化处理后,膜浓缩液中的有机物分子量及分子聚合度明显降低[18]。
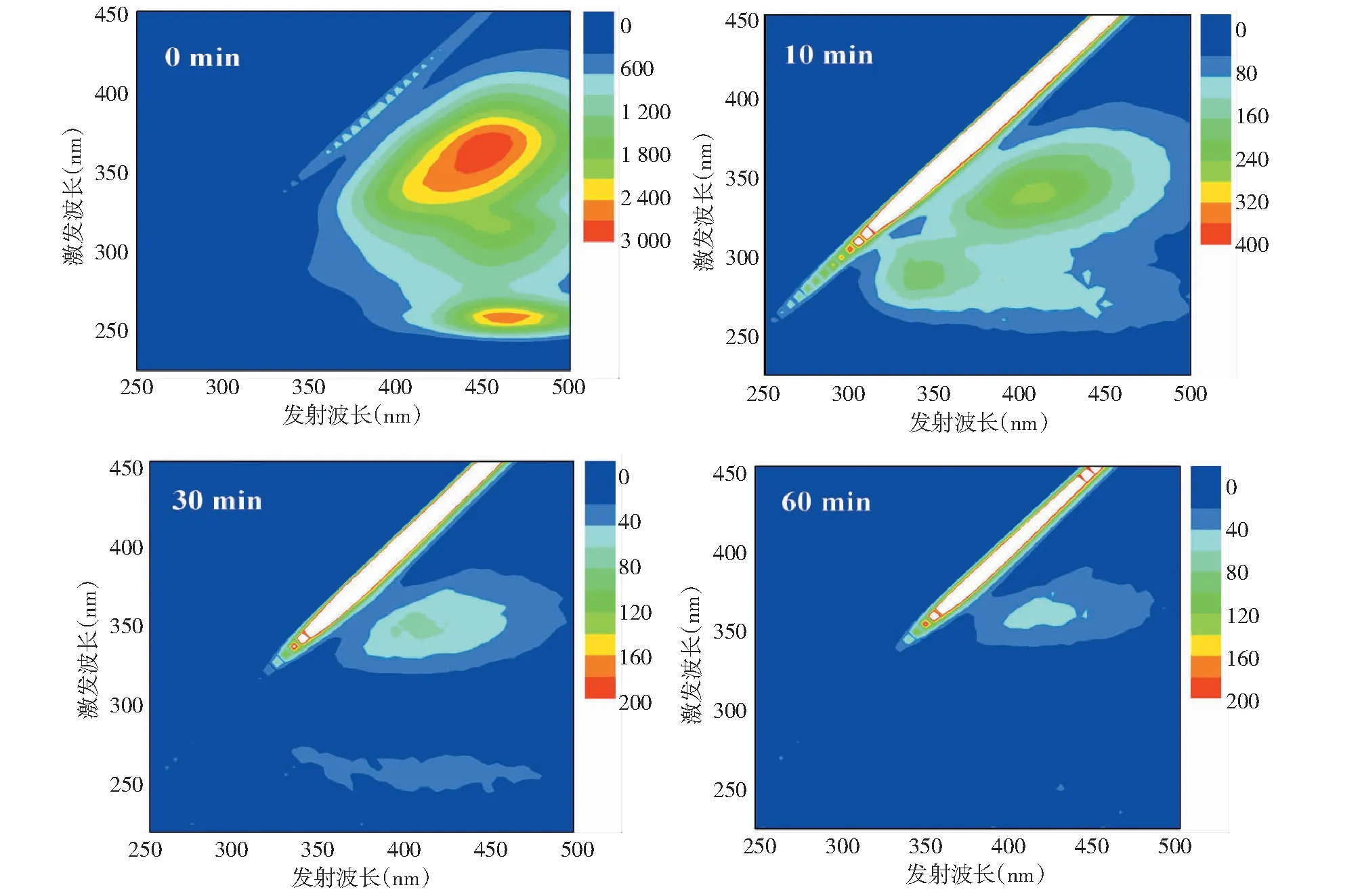
图7 电化学氧化处理前后三维荧光光谱Fig.7 3D-EEM spectrum before and after electrochemical oxidation treatment

表3 电化学氧化处理前后三维荧光峰位及峰值Tab.3 Position and values of fluorescence peak before and after electrochemical oxidation treatment
2.3 有机物去除机理
电化学氧化技术主要通过阳极直接氧化和阳极产生强氧化剂间接氧化废水中的有机物。大量文献表明[19~22],高氯废水电解处理过程主要通过阳极氧化氯离子生成强氧化剂(Cl2、HClO、ClO-)间接氧化水中的有机物,反应如下:
阳极反应
2Cl-→Cl2+2e-
(2)

(3)
2H2O→O2+4H++4e-
(4)
阴极反应
2H2O+2e-→2OH-+H2
(5)
ClO-+H2O+2e-→Cl-+2OH-
(6)
溶液反应
Cl2+H2O→HClO+H++Cl-
(7)
HClO→H++ClO-
(8)
电解过程中,产生的游离氯(Cl2、HClO和ClO-)一方面会与污染物反应而被消耗,另一方面,以Cl2形式存在的部分游离氯会从溶液中逸出被碱液吸收。因此,实验过程测得的游离氯浓度为实际产生的游离氯与上述被消耗的游离氯浓度之差。电解过程溶液中游离氯和Cl-浓度的情况如图8所示。结果表明,随着电解时间增加,溶液中氯离子浓度逐渐降低,游离氯浓度不断增加。电解过程中,Cl-在Ru-Ir/Ti阳极表面被直接氧化形成Cl2、HClO和ClO-(反应7和8),这类氧化物质进而释放到溶液中与有机物发生化学反应,破坏其分子结构,使其降解为小分子物质或直接矿化为CO2和水。结合不同电解时间TOC去除率的变化可知,游离氯浓度的增加有利于有机物的去除。但当游离氯增加到一定浓度,其对TOC去除率的提高作用有限。

图8 电解过程Cl-的转化Fig.8 Conversion of Cl- in the electrolytic process
3 结 论
3.1 选用Ru-Ir/Ti为电解阳极,在初始pH值为7、电流密度为40 mA/cm2的优化条件下电解60 min,TOC和CN的去除率分别可达41.33%和98.69%。
3.2 电化学氧化能有效去除膜浓缩中的类富里酸及类腐殖酸物质,并且类富里酸物质优先被去除。电化学氧化处理后,膜浓缩液中的有机物分子量及分子聚合度明显降低。
3.3 膜浓缩液中的氯离子在电解过程中可转化为游离氯(Cl2、HClO和ClO-),并利用其强氧化性对有机物进行高效降解,但过多的游离氯对TOC去除率的提高作用有限。
3.4 电化学氧化能够降低渗滤液膜浓缩液混凝出水中的有机物浓度,是一种处理渗滤液膜浓缩液的有效方法,研究成果可为渗滤液膜浓缩液或高盐有机废水的处理提供依据。
