中药醇沉前浓缩液质控指标的完善及标准建立——以党参醇沉为例
2022-10-14潘晶晶任丹丹瞿海斌龚行楚
潘晶晶,任丹丹#,瞿海斌, 3,龚行楚, 3*
中药醇沉前浓缩液质控指标的完善及标准建立——以党参醇沉为例
潘晶晶1, 2,任丹丹1, 2#,瞿海斌1, 2, 3,龚行楚1, 2, 3*
1. 浙江大学药学院,药物信息学研究所,浙江 杭州 310058 2. 组分中药国家重点实验室浙江大学交叉创新中心,浙江 杭州 310058 3. 浙江大学金华研究院,浙江 金华 321016
完善中药醇沉前浓缩液质控指标,并建立浓缩液质量标准。制备多批次党参浓缩液,研究密度与浓缩液其他性质间的关系。将党参炔苷保留率、与乙醇充分混合的浓缩液质量百分比以及单位质量浓缩液产生沉淀质量作为醇沉工艺评价指标,开展膜分散醇沉实验研究,筛选浓缩液关键性质并建立其与上述评价指标的定量模型。基于所建模型,采用预测误差传播的方法建立党参浓缩液的质量标准,并进行实验验证。浓缩液密度与固含量之间具有良好的线性关系。相比密度,浓缩液黏度能更灵敏地体现出不同批次浓缩液的性质差异。筛选出浓缩液的黏度和固含量为浓缩液关键性质。建立的二阶多项式模型2大于0.97。建立了不等式组作为浓缩液质量控制标准,实验验证结果表明,模型预测性能较好,建立的党参浓缩液的质量标准较为可靠。建议增加黏度作为浓缩液品质的控制指标,并建立综合考虑密度和黏度的浓缩液质量标准,通过放行控制提高醇沉工艺效果及批次间一致性。
中药醇沉;浓缩液质量控制;党参;黏度;党参炔苷;葡萄糖;果糖;蔗糖;总黄酮
《中国药典》2020年版一部通过规定药材和饮片质量标准,规定“制法”项,规定部分中间体质量标准,以及规定制剂质量标准[1],体现了对中成药质量的全流程控制。该质量控制思路与国际公认的药品“质量源于设计”理念不谋而合[2],即通过加强原料、中间体和制药过程控制,提高药品质量的控制水平。但是,《中国药典》2020年版一部中对中间体标准的规定明显少于对药材和制剂质量标准规定。目前,学术界和产业界对制药中间体的质量标准研究较少。
浓缩液是中药生产中常见的中间体,后续经常是干燥、沉淀或者与其他物料混合等工艺[3-5]。工业生产中大多以密度作为指标控制浓缩终点。但工业生产中也观察到密度相同的浓缩液,后续处理所得产液性质相差较大的情况。这提示仅以密度作为浓缩液质量指标可能是不够的。
醇沉是中药浓缩液的下游工艺之一,能部分除去糖、蛋白质和盐类等强极性成分[6-8],具有成本低、易操作、安全性高、除杂能力强等优点[9-10]。为减少醇沉中活性成分包裹损失,工业中常用“慢加快搅”或长时间静置的方法[11]。课题组前期提出以“与乙醇充分混合的浓缩液质量比例”(well-mixing ratio,WMR)作为定量描述包裹现象的指标[12];WMR值越接近于100%,说明包裹现象越少。本课题组采用微混合器加醇,能有效减少包裹损失现象[13]。张寒等[14]和闫安忆等[15]采用了偏最小二乘和逐步回归等方法建立浓缩液和醇沉工艺评价指标的定量关系,进而发现浓缩液中其他理化性质也可能是影响醇沉工艺评价指标的关键物料属性。如果增加其他指标控制浓缩液品质,会要求新指标能够快速低成本地测量,以确保工业应用的可行性。党参醇沉是参芪扶正注射液的重要纯化工艺[16]。本实验以党参醇沉前的浓缩液为研究对象,测定多批次浓缩液的理化性质,研究密度与其他性质的关系。进一步根据浓缩液理化性质和醇沉工艺评价指标的关系,确定浓缩液的关键性质。最后采用预测误差传播的方法建立党参浓缩液的质量标准,并根据所得标准进行浓缩液质量控制。
1 仪器与材料
1.1 仪器
Rotavapor R-200型旋转蒸发仪,瑞士Buchi公司;2 PB-20005II型平流泵,北京兴达科技发展有限公司;CT3001F型齿轮泵,保定瑞福流体科技有限公司;03-1型磁力搅拌机,杭州仪表电机有限公司;DHG-9146A型烘箱,上海精宏实验设备有限公司;DDBJ-350型便携式电导率仪,杭州启威仪器有限公司;Cary60型紫外可见分光光度计,美国Agilent公司;DMA5000M型密度测量仪、AMVn型黏度测量仪,奥地利Anton Paar GmbH公司;Milli-Q型超纯水系统,美国Millipore公司;Agilent 1100型高效液相色谱仪,配备G1314C型VWD检测器、Agilent 1260型高效液相色谱仪,配备G4260B型ELSD检测器,美国Agilent公司。
1.2 试剂与材料
对照品-果糖(批号200519,质量分数>99.5%)、柠檬黄(批号201206,质量分数>95.0%)均购自上海阿拉丁试剂有限公司;对照品-葡萄糖(批号200917)购自上海生工生物工程有限公司,质量分数>99.8%;对照品蔗糖(批号200620)购自上海Sigma-Aldrich公司,质量分数>99%;对照品党参炔苷(批号200311)、芦丁(批号190623)购自上海融禾医药科技有限公司,质量分数均>98%。三乙胺购自上海阿拉丁试剂有限公司;乙腈购自德国默克股份有限公司;95%乙醇购自浙江常青化工有限公司;超纯水由Milli-Q型超纯水系统制备。党参药材来源和批号见表1。
2 方法
2.1 膜分散微混合器
课题组前期设计制作了膜分散微混合器[13],能够实现乙醇和浓缩液的连续高效混合。膜分散微混合器材质为聚四氟乙烯,其结构和具体尺寸见之前的工作[13],采用了平均孔径为18 μm的不锈钢膜。
2.2 党参浓缩液的制备
党参药材和水分别按1∶8、1∶6的比例加热回流提取2次,每次提取0.5 h,滤过后合并滤液,通过旋转蒸发仪进行浓缩制得密度约为1.2 g/mL的浓缩液。所得浓缩液的编号见表1。
表1 党参药材来源、批号及所得浓缩液的编号
Table 1 Source and batch number of CodonopsisRadix and number of concentrates
批号药材来源浓缩液编号批号药材来源浓缩液编号 191022亳州元丰堂农副产品经销有限公司N6190816甘肃岷县易盛德中药材有限责任公司N3 191025亳州元丰堂农副产品经销有限公司N14190825甘肃岷县易盛德中药材有限责任公司N7 190929亳州元丰堂农副产品经销有限公司N9190908甘肃岷县易盛德中药材有限责任公司N10 191006亳州元丰堂农副产品经销有限公司N2190827甘肃岷县易盛德中药材有限责任公司N12 200423亳州永刚饮片厂有限公司N1191018山西潞州参源堂党参销售店N15 200331亳州永刚饮片厂有限公司N5191025山西潞州参源堂党参销售店N4 191221亳州永刚饮片厂有限公司N8191007山西潞州参源堂党参销售店N13 190805甘肃岷县易盛德中药材有限责任公司N11
2.3 实验设计
选择N1、N2、N8、N9、N12、N14共6批党参浓缩液,只改变浓缩液固含量,进行膜分散微混合器醇沉实验,实验装置图如图1所示。
使用平流泵、齿轮泵分别将乙醇溶液及党参浓缩液泵入微混合器中。收集出口混合物于锥形瓶中并置于搅拌机上搅拌5 min后滤过,收集上清液。实验后,依次用0.05% Na2CO3溶液和乙醇洗涤该装置。其中,各批次浓缩液固含量分别为50%、55%、60%。
固定工艺条件如下:醇料比为1.5∶1.0,浓缩液体积流量为60 mL/min,乙醇体积分数为95%,搅拌时间为5 min。具体实验条件如表2所示。
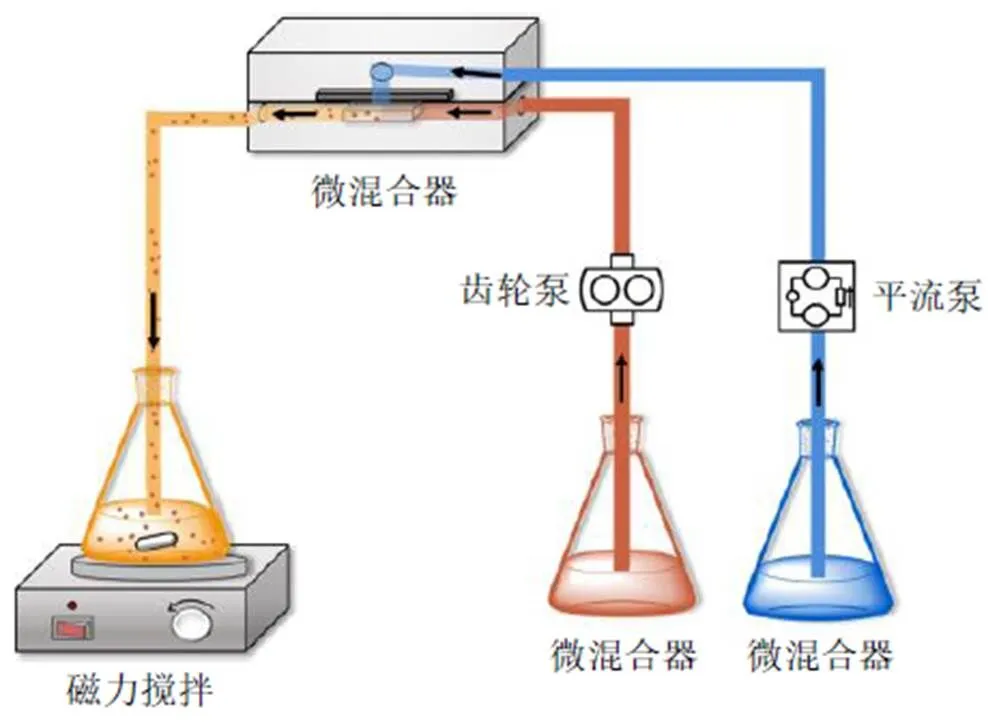
图1 实验装置图
2.4 党参浓缩液中指标成分及相关物理参数的定量测定
2.4.1 党参炔苷含量测定
(1)对照品溶液的制备:精密称取党参炔苷对照品适量,加20%乙腈溶解并定容至量瓶中,制成0.465 mg/mL党参炔苷对照品储备液。
表2 不同性质浓缩液醇沉实验条件及结果
Table 2 Experimental conditions and results of ethanol precipitation of concentrates with different properties
编号实验条件实验结果编号实验条件实验结果 浓缩液浓缩液固含量/%WMR/%党参炔苷保留率/%单位质量浓缩液产生沉淀质量/(g∙g−1)浓缩液浓缩液固含量/%WMR/%党参炔苷保留率/%单位质量浓缩液产生沉淀质量/(g∙g−1) 1N95099.9895.580.24211N125599.9593.570.461 2N1250100.0094.900.33712N25599.1593.080.499 3N25099.9694.910.36913N145598.4590.570.519 4N145099.9094.510.37414N15598.2890.390.562 5N145099.7492.920.40815N85598.1689.100.614 6N1450100.0093.570.40616N96085.6784.090.366 7N145099.0992.810.40117N126084.0278.240.605 8N15099.9994.030.46918N26081.8176.040.666 9N85099.9194.150.47419N16080.0773.450.716 10N95599.9793.940.335
(2)供试品溶液的制备:精密量取适量党参醇沉上清液,加20%乙腈溶解并定容至2mL,摇匀,静置。经0.22 μm微孔滤膜滤过后,取续滤液作为供试品溶液。
(3)色谱条件:党参炔苷含量测定采用HPLC法[15]。色谱柱为Zorbax SB-C18柱(250 mm×4.6 mm,5 μm);柱温30 ℃;进样量10 μL;检测波长269 nm;流动相为乙腈-水(20∶80),等度洗脱;体积流量为1.0 mL/min。典型色谱图如图2所示。
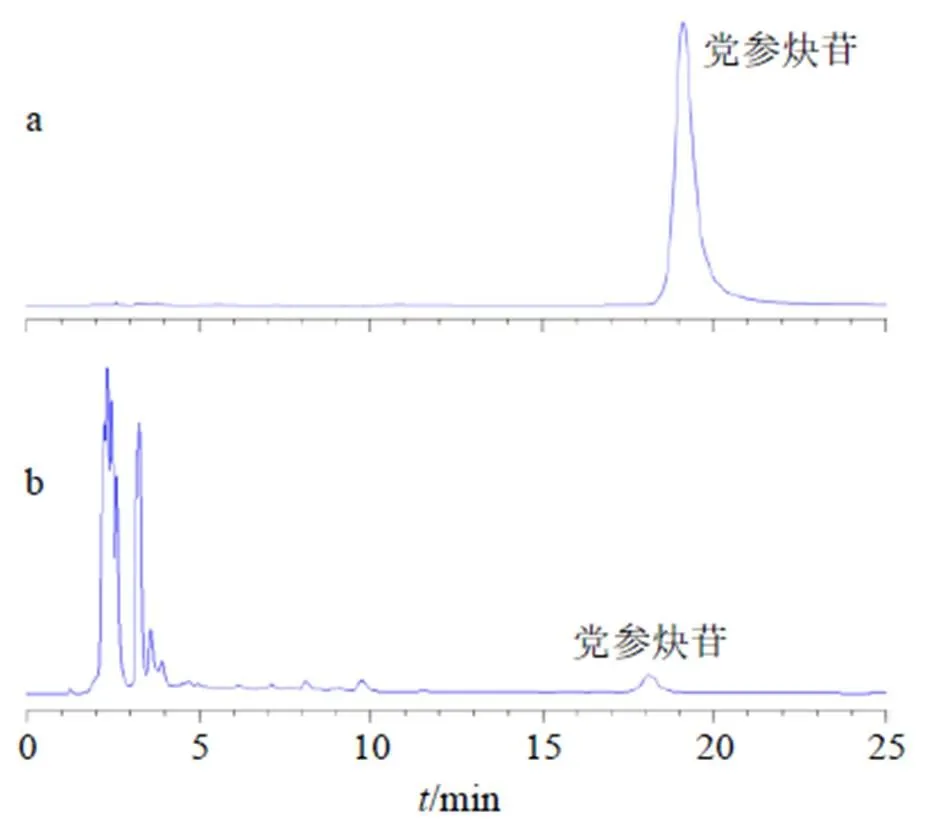
图2 党参炔苷对照品(a)、党参醇沉上清液(b)的典型HPLC-UV图
(4)线性关系考察:精密量取党参炔苷对照品储备液,分别加入20%乙腈稀释至93.00、46.50、27.90、18.60、9.40 μg/mL的系列对照溶液,以上系列对照溶液进样检测后,以峰面积为纵坐标(),对照溶液质量浓度为横坐标()制作标准曲线,测得党参炔苷的线性回归方程为=17.81-9.102,=0.999 7,线性范围为9.40~93.00 μg/mL。在此范围内,党参炔苷质量浓度与峰面积线性关系良好。
(5)精密度试验:取由党参醇沉上清液[17]制备得到的供试品溶液,按“2.4.1(3)”项下色谱条件重复进样6次,以党参炔苷峰面积计算精密度RSD为1.3%,表明仪器的精密度良好。
(6)重复性试验:用党参醇沉上清液[17]分别制备6份供试品溶液,按“2.4.1(3)”项下色谱条件进样检测,以党参炔苷质量浓度计算重复性RSD为1.7%,表明该方法具有较好的重复性。
(7)稳定性试验:取党参醇沉上清液[17]制备得到的供试品溶液,分别于0、3、6、9、12、15 h按“2.4.1(3)”项下色谱条件进样检测,党参炔苷峰面积的RSD为0.7%,表明供试品溶液在15 h内稳定。
(8)加样回收率试验:分别取已测定党参炔苷含量的由党参醇沉上清液[17]制备得到的供试品9份,分为3组,每组3份。分别按照样品中质量与加入量之比为1.0∶0.8、1.0∶1.0、1.0∶1.2,精密加入党参炔苷对照品适量,加20%乙腈定容至2 mL,摇匀,静置,经0.22 μm微孔滤膜滤过,取续滤液按“2.4.1(3)”项下色谱条件进样检测,结果党参炔苷的平均加样回收率为103.8%,RSD为1.56%,说明建立的分析方法准确,可用于党参炔苷含量的测定。
(9)样品测定:将样品按“2.4.1(2)”项中方法配制成供试品溶液,再按“2.4.1(3)”项下色谱条件对样品进样检测,测定其中的党参炔苷含量。
2.4.2 葡萄糖、果糖和蔗糖含量测定
采用HPLC-ELSD法测定样品中葡萄糖、果糖和蔗糖的含量[18]。
(1)对照品溶液的制备:分别精密称取果糖、葡萄糖、蔗糖对照品适量,置25 mL量瓶中,用85%乙腈超声溶解并定容,制成对照品贮备液。将贮备液定量稀释,制成系列不同质量浓度的混合对照品溶液。
(2)供试品溶液的制备:分别取适量党参浓缩液以适量85%乙腈为溶剂进行稀释定容。溶液经离心后,用0.22 μm滤膜滤过,取续滤液作为供试品溶液。
(3)色谱条件:色谱柱为XBridge BEH Amide柱(250 mm×4.6 mm,5 μm);柱温为34 ℃;体积流量为0.9 mL/min,进样量为5 μL。流动相A为0.3%三乙胺水溶液,流动相B是0.3%三乙胺-乙腈溶液,梯度洗脱:0~37 min,85%~76% B;37~38 min,76%~60% B;38~48 min,60%~100% B;后运行时间为10 min。ELSD操作参数如下:雾化器温度为65 ℃,蒸发器温度为60 ℃,气体体积流量为1.8 L/min。典型色谱图如图3所示。
2.4.3 总黄酮含量测定 采用紫外分光光度法测定浓缩液中的总黄酮含量[19]。定量移取浓缩液于10mL容量瓶中,依次加入5.0% NaNO2溶液、10% Al(NO3)3溶液、1.0 mol/mL NaOH溶液[17]。用50%乙醇定容至10 mL,摇匀,于510 nm处测定其吸光度()值[17]。以芦丁作为对照品,定量稀释后测定值,以芦丁含量计算得样品中总黄酮含量。
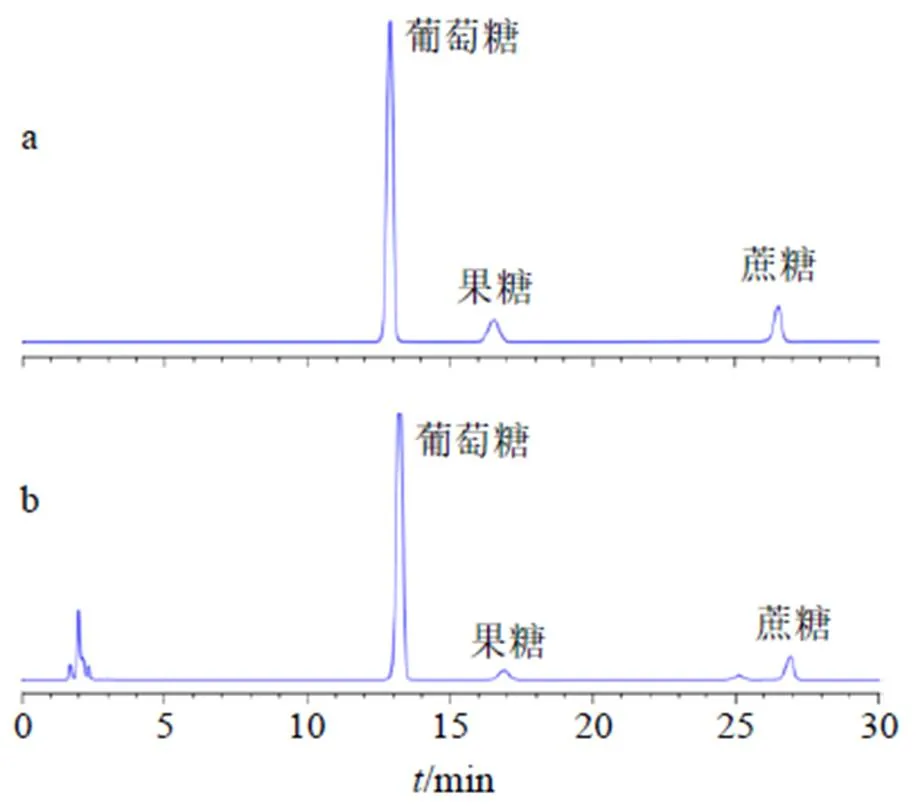
图3 混合对照品(a)、党参浓缩液(b) 的典型HPLC-ELSD图
2.4.4 密度和黏度测定 浓缩液密度通过密度测量仪测定,不同固含量、不同温度下的浓缩液密度用表示。浓缩液黏度通过黏度测量仪测定,使用落球黏度计,根据落球时间计算样品黏度。不同固含量、不同温度下的浓缩液黏度用表示。
2.4.5 其他指标的测定
(1)总固体含量测定:采用重量法[13]。准确称取适量样品,置于恒定质量的称量瓶中,置于烘箱中,在105 ℃下干燥至恒定质量后称定。重复3次。
(2)电导率:将浓缩液用水稀释至总固含量为2%,在25 ℃下通过便携式电导率仪测量其电导率。
(3)色素:以柠檬黄作为对照品,采用紫外可见分光光度计测定浓缩液中色素的含量[20]。波长设置为430 nm。浓缩液稀释后测定值。以柠檬黄含量计算样品中色素含量。
2.5 数据处理
用课题组前期提出的WMR法表征醇沉过程中混合情况的好坏[12]。WMR值和党参炔苷保留率的计算方法分别见公式(1)、(2)。
WMR=(1/0+22/0)/(0+0/2-1) (1)
党参炔苷保留率=22/00(2)
0为总固体质量浓度,0为党参炔苷的质量浓度,0为醇沉中浓缩液用量,1为乙醇溶液用量,2为所得上清液的总质量,2为上清液中总固体质量浓度,2为上清液中党参炔苷质量浓度,浓缩液与乙醇混合越充分,WMR值越接近1
选择党参炔苷保留率、WMR以及单位质量浓缩液产生沉淀质量作为醇沉工艺评价指标。采用多元线性回归法,用公式(3)建立工艺评价指标和浓缩液性质的定量模型,筛选出浓缩液关键性质。
(3)
为平方根反正弦变化后的党参炔苷保留率、平方根反正弦变化后的WMR值、单位质量浓缩液产生沉淀质量,0为常数项,a为各项的偏回归系数X为浓缩液各性质
采用逐步回归法对模型进行简化,添加及删除模型中各项的显著性水平设为0.1,模型中剩余的项认为是浓缩液关键性质。数据分析由V 11.0.0 Design Expert(美国Stat-Ease公司)软件完成。
用2阶多项式模型拟合工艺评价指标与关键浓缩液性质的定量模型,如公式(4)所示。通过向后逐步回归法简化方程,值设置为0.10。
(4)
3 结果
3.1 不同批次浓缩液的理化性质
不同来源、不同批号的党参药材制备所得15批党参浓缩液的理化性质见表3。其中包括电导率(1,固含量45%)、党参炔苷含量(2)、果糖含量(3)、葡萄糖含量(4)、蔗糖含量(5)、色素含量(6)、总黄酮含量(7)、密度(固含量45%,25 ℃,,8)、黏度(固含量45%,25 ℃,,9)。各批浓缩液中所测得的党参炔苷、葡萄糖、果糖、蔗糖、色素和总黄酮含量的总和为浓缩液总固体的25.64%~73.00%,提示不同批次党参浓缩液化学组成相差较大。在相同温度和固含量下,15批浓缩液密度的RSD为1.078%,是所有指标中变化最小的,提示密度指标不适合用于体现不同批次药材所得浓缩液的差异。党参炔苷含量、蔗糖含量、色素含量和黏度的RSD均超过了40%。
3.2 密度与浓缩液其他性质之间的关系
3.2.1 密度与浓缩液其他性质的相关性 计算了表3中浓缩液密度与浓缩液其他性质的Pearson相关系数,结果如表4所示。在检验水准α=0.05的情况下,认为浓缩液密度(8)与电导率(1)、总黄酮含量(7)均有正相关关系,与党参炔苷含量(2)存在负相关关系。因为相关系数检验值大于0.05,所以认为浓缩液密度(8)与果糖含量、葡萄糖含量、蔗糖含量、色素含量、黏度之间的线性相关关系不显著。
3.2.2 密度与浓缩液温度的关系 测定了15批浓缩液密度与温度的关系,结果如图4所示。浓缩液的密度与温度是线性关系,且随温度的上升而下降。用线性公式=0+1拟合,结果如表5所示,各方程2均大于0.99,拟合效果较好。
表3 浓缩液理化性质
Table 3 Physicochemical properties of concentrates
浓缩液Z1/(mS∙cm−1)Z2/(μg∙g−1)Z3/(mg∙g−1)Z4/(mg∙g−1)Z5/(mg∙g−1)Z6/(mg∙g−1)Z7/(mg∙g−1)Z8/(g∙mL−1)Z9/(mPa∙s) N120.08341.8306.979.5056.274.1383.7091.216101.88 N222.20453.0343.089.4331.184.0115.1071.20359.41 N319.91313.8324.896.8649.391.6353.6321.20546.43 N423.00405.5284.070.12117.621.3704.2041.21341.82 N521.10431.5174.156.6419.491.9623.8031.210101.45 N621.60434.9308.375.01103.801.5864.2961.21450.74 N718.61684.0379.661.14147.601.5845.2761.20978.30 N818.09351.3373.490.8175.402.4032.7941.187111.66 N924.0018.5585.9136.720.001.5265.8751.22619.36 N1020.10542.2409.466.75138.511.4803.6721.21356.55 N1119.44391.3336.7102.2149.213.8764.4441.18759.80 N1216.58589.0438.861.96154.140.8292.8591.19031.06 N1321.40144.2504.1106.9456.362.9166.0291.23238.41 N1418.98294.8450.796.1468.652.5884.2381.21287.60 N1520.40137.2444.592.9760.172.3804.1121.21741.32 平均值20.37368.9377.685.5475.182.2864.2701.20961.72 标准差1.93175.699.921.4147.141.0400.9600.01328.17 RSD/%9.5047.5926.4525.0262.7045.5122.491.07845.64
表4 密度(Z8)与浓缩液的部分其他性质的Pearson相关系数及其检验的P值
Table 4 Pearson correlation coefficient and P value between density (Z8) and some other properties of concentrates
理化性质Pearson相关系数P值理化性质Pearson相关系数P值 Z10.6490.009Z5−0.2370.395 Z2−0.5220.046Z6−0.0640.821 Z30.3380.218Z70.6420.010 Z40.2790.315Z9−0.3060.267
3.2.3 密度与浓缩液固含量的关系 选择理化性质相差较大的2批浓缩液N1和N12,改变固含量测定其密度,结果见图5。可以看到,浓缩液的密度随固含量的提高而增大,相同固含量的不同批次浓缩液在相同温度下的密度差别较小。尝试用线性方程=0+1拟合浓缩液密度与固含量,得0=0.517±0.009,1=0.973±0.005,2=0.995。从结果来看,浓缩液固含量和密度之间的线性关系相当好,提示浓缩液固含量和密度指标在很大程度上可以相互替代。黄慧敏等[21]研究浓缩液固含量和密度之间的关系时,也得到类似结论。考虑到浓缩液密度大小受实验室温度影响,所以后续实验中以固含量代替密度。
3.3 浓缩液关键性质筛选
不同性质浓缩液的醇沉实验结果如表2所示。由于WMR值、党参炔苷保留率均为百分率数据,所以建模前将WMR值、党参炔苷保留率进行平方根反正弦变换。采用公式(3)对实验结果进行处理,建立浓缩液性质与平方根反正弦变化后的WMR值(1)、平方根反正弦变化后的党参炔苷保留率(2)和单位质量浓缩液产生沉淀质量(3)的定量模型,进而识别出浓缩液关键性质。
公式(3)是一个多元线性回归模型,为了避免自变量之间的多重共线性现象,与密度具有较高相关性的电导率、总黄酮和党参炔苷含量不参与建模。逐步回归后所得偏回归系数及方差分析结果如表6所示。各模型的显著水平<0.000 1,说明模型显著。模型2均大于0.75,说明可以解释大部分变异。根据模型结果可知,浓缩液的关键性质为固含量和黏度。
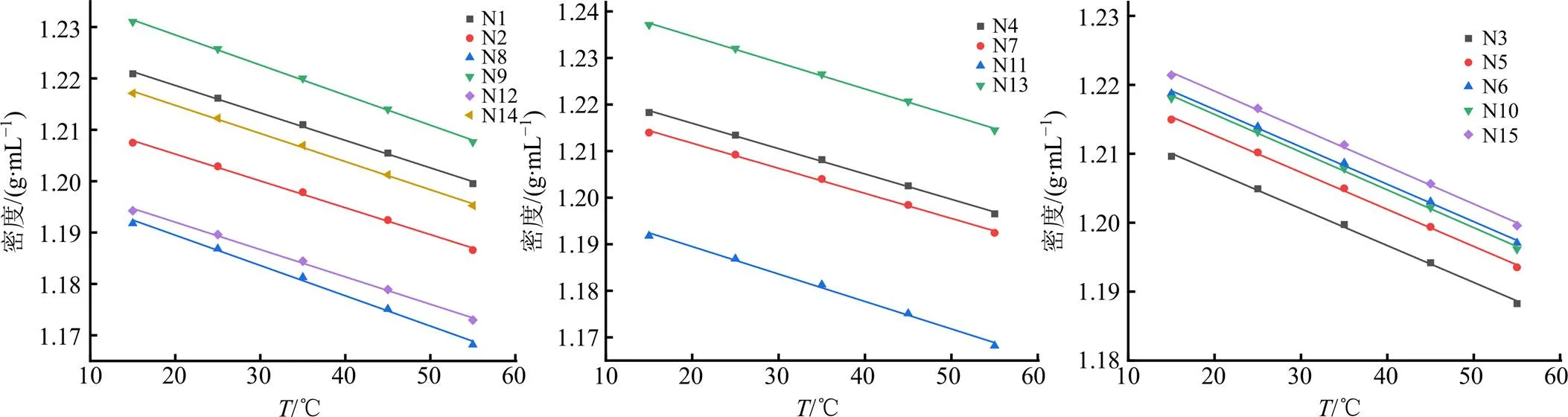
图4 浓缩液密度随温度变化
表5 密度随温度变化的拟合结果
Table 5 Fitting results of density and temperature
浓缩液c0/(×10−4 g·mL−1·℃−1)c1/(g·mL−1)R2浓缩液c0/(×10−4 g·mL−1·℃−1)c1/(g·mL−1)R2 N1−5.347±0.1361.229±0.0010.998 1N9−5.855±0.1211.241±0.0010.998 7 N2−5.225±0.1401.216±0.0010.997 8N10−5.475±0.1341.226±0.0010.997 6 N3−5.346±0.1371.218±0.0010.998 0N11−5.896±0.2271.201±0.0010.995 6 N4−5.442±0.1301.227±0.0010.998 2N12−5.323±0.1451.203±0.0010.997 8 N5−5.369±0.1251.223±0.0010.997 8N13−5.661±0.2541.246±0.0010.998 5 N6−5.422±0.1381.227±0.0010.997 6N14−5.475±0.1331.226±0.0010.997 6 N7−5.386±0.1401.222±0.0010.997 9N15−5.456±0.1391.230±0.0010.997 4 N8−5.900±0.2271.202±0.0010.995 6
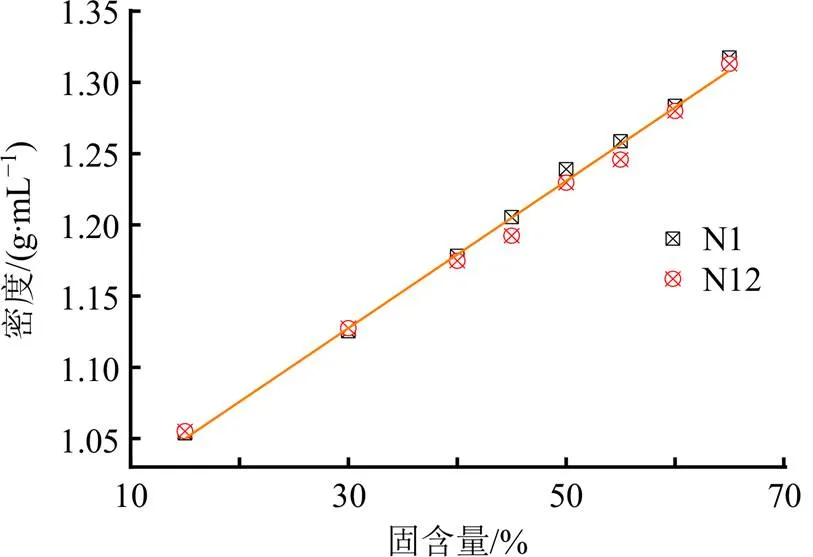
图5 浓缩液密度随固含量变化
密度变化能够较准确地体现出浓缩液中水含量变化,所以工业生产中以密度作为指标来控制浓缩终点是很合理的。考虑到密度与固含量的高相关性,表6中自然地筛选出固含量作为关键性质。但是从表6结果来看,仅以密度作为浓缩液质量指标是不够的。黏度同样是与醇沉效果相关的重要指标。考虑到黏度也可以采用在线黏度计测定,在实际工业生产中能够实现快速低成本的检测,所以建议工业生产中同时将密度和黏度作为浓缩液关键指标进行控制。
表6 多元线性回归模型的偏回归系数及方差分析
Table 6 Partial regression coefficient and variance analysis of multiple linear regression model
模型项Y1Y2Y3 偏回归系数P值偏回归系数P值偏回归系数P值 常量3.372 8−2.592 2−−1.073 4− 固含量−−−0.000 70.032 00.002 5<0.000 1 黏度−0.036 0<0.000 1−0.023 8<0.000 10.025 5<0.000 1 R20.789 30.833 60.853 1 Radj20.776 90.812 80.833 6 P值<0.000 1<0.000 1<0.000 1
3.4 浓缩液关键性质对膜分散党参醇沉工艺效果的影响
将浓缩液的黏度取自然对数,WMR值、党参炔苷保留率进行平方根反正弦变换,采用公式(4)研究浓缩液固含量(1)、浓缩液黏度的自然对数(2)与平方根反正弦变化后的WMR值(1)、平方根反正弦变化后的党参炔苷保留率(2)、单位质量浓缩液产生沉淀质量(3)的定量关系,建模结果如表7所示。模型的值均小于0.05,说明模型显著;模型2均大于0.90,说明可以解释大部分变异。各指标的等高线图如图6所示。WMR值和党参炔苷保留率随浓缩液固含量、浓缩液黏度的增加而降低,说明较大的浓缩液黏度及固含量都不利于浓缩液和乙醇的充分混合。单位质量浓缩液产生沉淀的质量随浓缩液固含量、浓缩液黏度的增加而增加,说明浓缩液黏度越大,其所含的不溶于乙醇的可沉淀物质越多。
3.5 浓缩液质量标准的建立
浓缩液是中药生产中重要的中间体,其质量影响后续的醇沉等精制过程,因此,建立浓缩液的质量标准非常重要。本研究采用WMR值、党参炔苷保留率以及单位质量浓缩液产生沉淀质量为指标建立党参浓缩液的质量标准。以固含量和浓缩液黏度对平方根反正弦变化后的WMR(1)、平方根反正弦变化后的党参炔苷保留率(2)、单位质量浓缩液产生沉淀质量(3)建模,所建立的模型如公式(5)所示。
表7 二阶多项式回归模型的偏回归系数及方差分析
Table 7 Partial regression coefficients and variance analysis of second-order polynomial regression models
模型项Y1Y2Y3 偏回归系数P值偏回归系数P值偏回归系数P值 常量−13.240−−8.330−0.209− X158.345<0.000 136.389<0.000 1−0.499<0.000 1 X2−0.0440.000 80.215<0.000 1−0.286<0.000 1 X1X2−−−0.4790.005 80.7750.054 3 X12−56.826<0.000 1−33.744<0.000 1−− R20.975 40.982 50.916 6 Radj20.970 40.977 50.900 0 P值<0.000 1<0.000 1<0.000 1
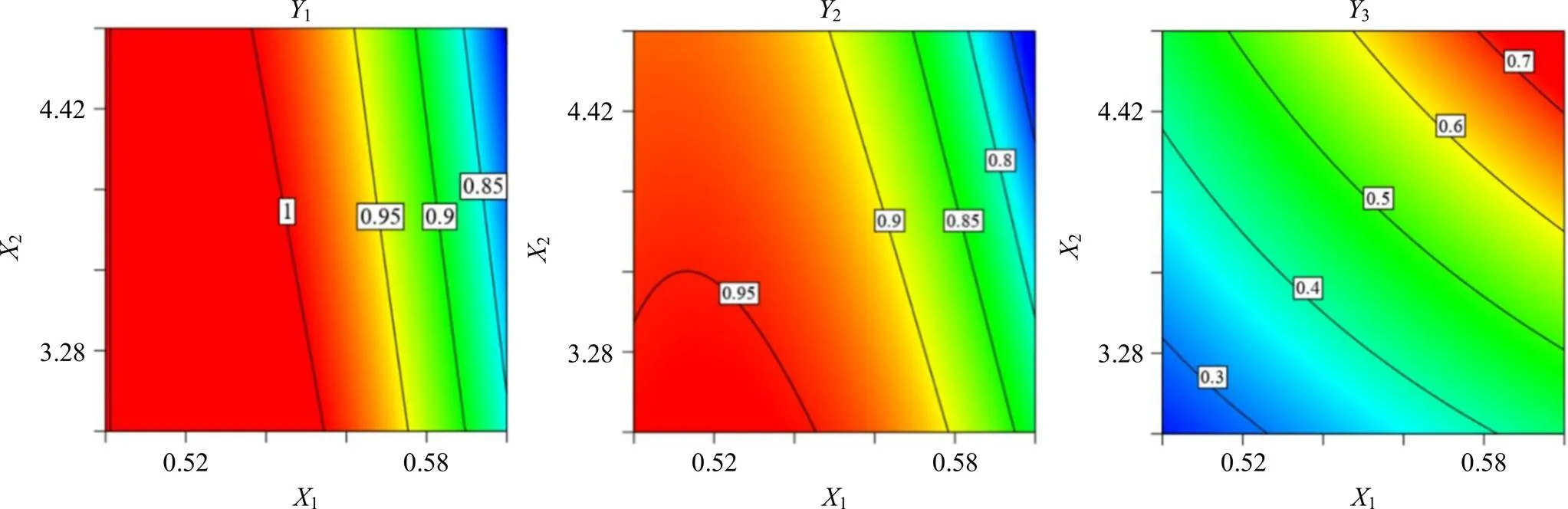
图6 WMR值(Y1)、党参炔苷保留率(Y2)和单位质量浓缩液产生沉淀质量(Y3)的等高线图
1=−13.240+58.3451-0.0442-56.82612
2=−8.330+36.3891+0.2152-0.47912-33.74412
3=0.209-0.4991-0.2862+0.77512(5)
采用预测误差传播的方法对浓缩液质量标准进行计算[22]。假设残差服从均值为零的正态分布,正态分布的标准差与残差相同,即分别为0.024 9、0.013 1、0.039 4。若要求WMR值大于95%的概率为90%,党参炔苷保留率大于90%的概率为90%,单位质量浓缩液产生沉淀质量大于0.300 g/g的概率为90%,则根据公式(5)建立不等式组(6)。
1=−13.240+58.3451-0.0442-56.82612-0.1×SDresidual1≥1.345
2=−8.330+36.3891+0.2152-0.47912-33.74412-0.1×SDresidual2≥1.249
3=0.209-0.4991-0.2862+0.77512-0.1×SDresidual3≥0.300 (6)
其中0.1为标准正态分布的临界值,即1.282。将不等式组(6)化简得不等式组(7)。
58.3451-0.0442-56.82612-14.616 9≥0
36.3891+0.2152-0.47912-33.74412-9.595 8≥0
−0.4991-0.2862+0.77512-0.141 5≥0 (7)
符合不等式组(7)的为合格浓缩液,应予以放行直接投入醇沉工艺,不符合不等式(7)的为不合格浓缩液,可在合规的情况下稀释后再投入醇沉工艺生产。使用MATLAB(R2016a,美国The Math Works公司)依据不等式(7)做图,浓缩液性质的具体可行范围如图7所示。
3.6 浓缩液质量控制的验证实验
选择编号为N5、N11、N15的浓缩液进行验证实验,将N5浓缩液的固含量稀释至55%,N15浓缩液固含量稀释至53%,N11的浓缩液分别稀释至52%和56%。进行4组验证实验(V1~V4)。将浓缩液性质代入不等式组(7),固含量为53%的N15、固含量为52%的N11满足不等式组(7),是合格浓缩液。固含量为55%的N5、固含量为56%的N11不满足不等式组(7),为不合格浓缩液。验证实验条件及结果分别见表8及图7所示。从验证实验结果可知,预测值和实验值接近,说明所建模型有较好的预测性能。V1和V3实验所得的党参炔苷保留率低于90%,未达到预设标准。V2和V4的实验所得结果符合预设标准。说明采用不等式组(7)能够较好地控制浓缩液品质。

图7 浓缩液性质的可行范围及验证点
3.7 浓缩液黏度和浓缩液部分其他性质之间的相关性
表9列出了浓缩液黏度与浓缩液部分其他性质之间Pearson相关系数及值。发现黏度(9)与其他测得的性质相关性不强(>0.1)。表3中不同批次浓缩液黏度相差较大(RSD=45.64%),说明影响浓缩液黏度的可能是某些本实验中未检测的物质,比如一些相对分子质量较大的成分。这也意味着浓缩液黏度提供了一些其他检测指标未能反映出来的信息,检测黏度会有利于全面表征出不同批次浓缩液中固体成分的差异。
表8 验证实验点条件及工艺指标考察结果
Table 8 Verification experimental points conditions and process index investigation results
试验点是否满足不等式浓缩液浓缩液固含量/%固含量45%、25 ℃下黏度/(mPa∙s)党参炔苷保留率/%WMR/%单位质量浓缩液产生沉淀质量/(g·g−1) 实测值预测值实测值预测值实测值预测值 V1否N555101.4587.5189.1998.1197.880.5700.582 V2是N115259.8093.7793.84100.2199.760.4300.428 V3否N115659.8087.4888.9097.4997.130.5310.535 V4是N155341.3293.8293.65100.3599.790.4190.409
表9 浓缩液黏度(Z9)与浓缩液部分其他性质之间Pearson相关系数及P值
Table 9 Pearson correlation coefficient and P value between viscosity and some other properties of concentrates
理化性质Pearson相关系数P值理化性质Pearson相关系数P值 Z1−0.3720.172Z5−0.0730.769 Z20.2910.293Z60.3820.160 Z3−0.5280.043Z7−0.3960.144 Z4−0.3610.186Z8−0.3060.267
3.8 浓缩液固含量与黏度的关系
选择2批浓缩液N1和N12,改变固含量测定其黏度,并尝试用指数型关系式=0×e1x(0、1为常数项)进行拟合,拟合结果如图8和表10所示。浓缩液的黏度随固含量的增加而增大。在固含量较大时,黏度随固含量的增加上升明显。与浓缩液N12相比,浓缩液N1的黏度随固含量的增加上升较快。
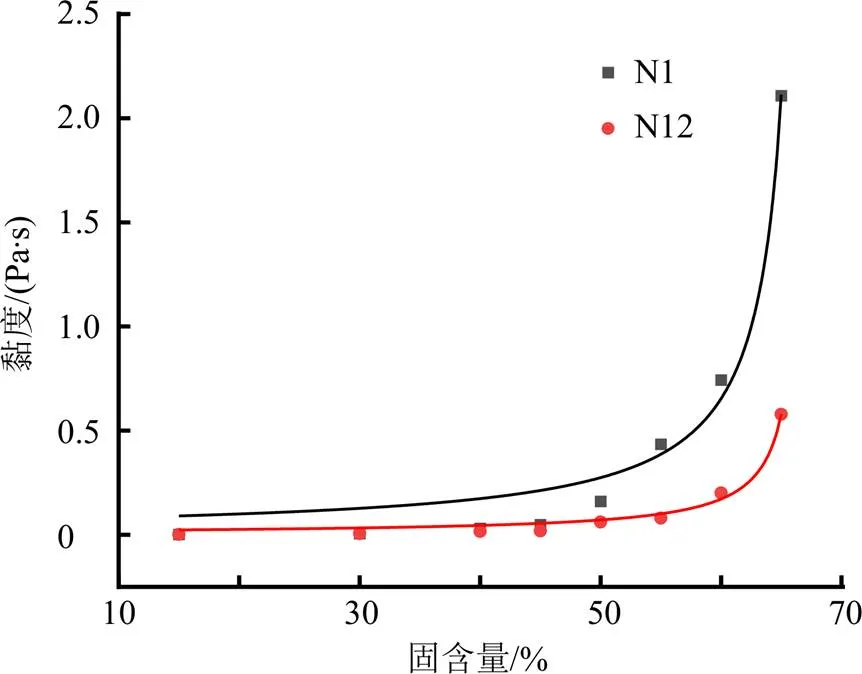
图8 浓缩液黏度随固含量变化
表10 黏度随固含量变化的拟合结果
Table 10 Fitting results of viscosity and solid content
浓缩液批号f0/(mPa∙s)f1R2 N10.014 0±0.009 018.319±1.0070.994 5 N120.001 7±0.001 019.594±1.0720.994 7
3.9 浓缩液黏度与温度的关系
测定了15批浓缩液黏度与温度的关系,结果如图9所示。浓缩液黏度随温度的上升而下降。用指数公式=0×e1x(0、1为常数项)拟合,结果如表11所示,各方程2均大于0.99,拟合效果较好。根据图9,当温度较低时,不同批次的浓缩液黏度相差较大;随着温度的升高,不同批次浓缩液黏度的差距变小。
4 讨论
本研究首先制备了不同批次的党参浓缩液,并测定了浓缩液的理化性质。发现相同温度和固含量下,密度的RSD是所有指标中变化最小的,提示密度不适合用于体现不同批次浓缩液的差异。研究了浓缩液各性质与密度的关系,用线性方程拟合获得了浓缩液密度与温度、固含量的定量关系。发现浓缩液固含量和密度间的线性关系很好。
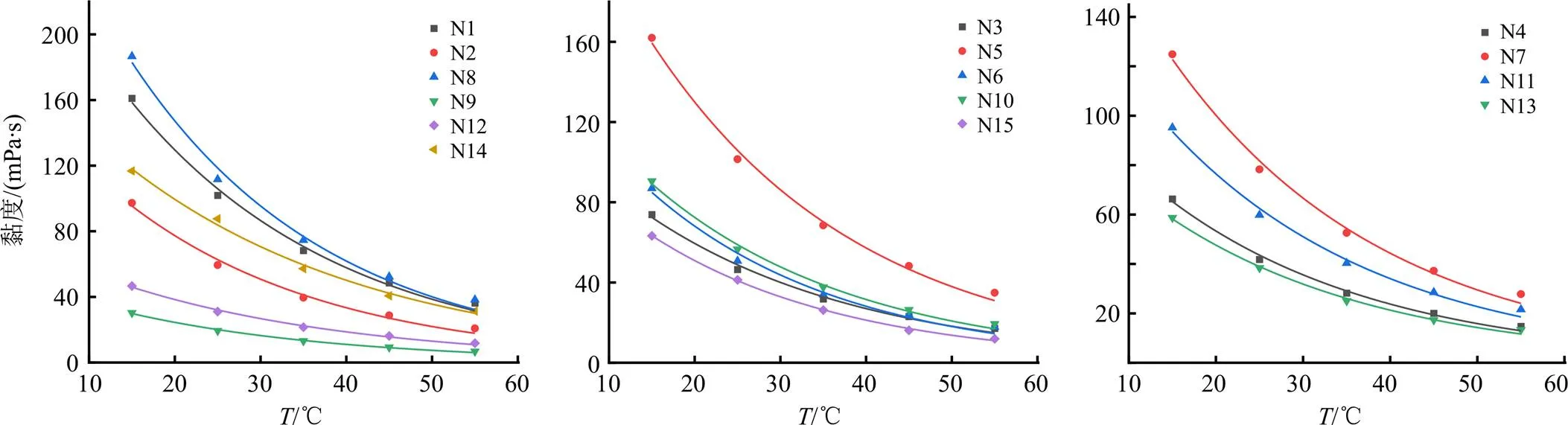
图9 浓缩液黏度随温度变化
表11 黏度随温度变化的拟合结果
Table 11 Fitting results of viscosity and temperature
浓缩液g0/(mPa∙s)g1/℃−1R2浓缩液g0/(mPa∙s)g1/℃−1R2 N1290.6±14.0−0.040 4±0.002 00.994 8N954.3±2.2−0.039 8±0.001 70.996 2 N2179.1±10.8−0.042 0±0.002 50.992 3N10166.5±7.8−0.041 6±0.001 90.995 3 N3131.0±7.2−0.039 5±0.002 20.993 0N11171.7±8.8−0.040 4±0.002 10.994 0 N4119.7±5.6−0.040 4±0.001 90.995 1N1278.9±3.1−0.036 0±0.001 60.995 8 N5295.0±13.4−0.040 9±0.001 80.995 6N13106.4±4.1−0.040 2±0.001 60.996 7 N6164.9±12.3−0.044 2±0.003 20.989 2N14197.3±8.3−0.034 2±0.001 60.994 9 N7226.4±11.4−0.040 8±0.002 10.994 4N15122.1±2.8−0.043 7±0.001 00.999 0 N8350.7±21.8−0.043 4±0.002 60.992 2
改变浓缩液的固含量进行膜分散醇沉实验,将党参炔苷保留率、WMR值、单位质量浓缩液产生沉淀质量作为工艺评价指标,筛选确定浓缩液固含量及黏度为浓缩液关键性质。随后建立了浓缩液固含量及黏度与工艺评价指标的定量模型,模型2均大于0.90。基于所建模型,采用预测误差传播的方法建立了浓缩液的质量标准,符合不等式组的为合格浓缩液,可予以放行投入醇沉工艺;不符合不等式组的为不合格浓缩液。浓缩液质量控制的验证实验结果表明,模型有较好预测性能,所制定的浓缩液质量标准较为可靠。浓缩液黏度随着固含量的增加而增加,随温度的提高而降低,与本研究所检测的其他浓缩液理化性质相关性较小。目前工业生产中大多仅控制醇沉前浓缩液密度或体积,本研究建议增加黏度作为浓缩液品质的控制指标,从而能在药材批次变化时更好地表征出浓缩液质量差异。
本研究的不足之处包括:第一,在测定党参浓缩液时并未检测所有可能的指标,包括多糖含量和蛋白质含量等。如果获得更多指标进行分析,有可能使筛选得到的浓缩液关键性质改变。第二,中药种类多且成分复杂,不同中药水煎浓缩液的性质指标可能差异较大,黏度能否用于完善其他中药浓缩液的质量标准仍有待进一步考察。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典 [S]. 一部. 2020: 3-1902.
[2] Pramod K, Tahir M A, Charoo N A,. Pharmaceutical product development: A quality by design approach [J]., 2016, 6(3): 129-138.
[3] Sun L Q, Wang S Y, Li Y J,. Impact of parameter fluctuations on the performance of ethanol precipitation in production of Re Du Ning Injections, based on HPLC fingerprints and principal component analysis [J]., 2016, 14(1): 73-80.
[4] 念波, 石兴云, 刘静, 等. 应用响应面设计优化黄精速溶茶加工工艺 [J]. 云南农业大学学报: 自然科学, 2019, 34(2): 297-302.
[5] 李星, 王雪慧, 蒋鹏娜, 等. 平喘颗粒提取工艺的研究[J]. 中华中医药杂志, 2017, 32(7): 3150-3153.
[6] 蒋美林, 张学瑜, 邵峰, 等. 醇料比对双黄连制剂醇沉效果及沉淀物形态影响 [J]. 中草药, 2020, 51(19): 4954-4959.
[7] Ku Y, Jansen O, Oles C J,. Precipitation of inulins and oligoglucoses by ethanol and other solvents [J]., 2003, 81(1): 125-132.
[8] Boulet M, Britten M, Lamarche F. Dispersion of food proteins in water-alcohol mixed dispersants [J]., 2001, 74(1): 69-74.
[9] Tai Y N, Shen J C, Luo Y,. Research progress on the ethanol precipitation process of traditional Chinese medicine [J]., 2020, 15: 84.
[10] 丁鸿, 徐芳芳, 杜慧, 等. 基于决策树算法的热毒宁注射液金银花青蒿醇沉过程质量控制研究 [J]. 中草药, 2021, 52(19): 5836-5844.
[11] 刘苗, 于筛成, 张虹, 等. 中药醇沉工艺及设备浅析 [J]. 中成药, 2007, 29(8): 1202-1204.
[12] Tai Y N, Pan J J, Qu H B,. An index for quantitative evaluation of the mixing in ethanol precipitation of traditional Chinese medicine [J]., 2021, 8(10): 181.
[13] Pan J J, Shao J Y, Qu H B,. Ethanol precipitation ofconcentrate with a membrane dispersion micromixer [J]., 2020, 251: 119633.
[14] 张寒, 闫安忆, 龚行楚, 等. 丹参注射液生产中一次醇沉上清液浓缩工艺质控指标研究 [J]. 中国中药杂志, 2011, 36(11): 1436-1440.
[15] 闫安忆, 龚行楚, 瞿海斌. 一种中药醇沉前浓缩液关键质量控制指标的辨析方法 [J]. 中国中药杂志, 2012, 37(11): 1558-1563.
[16] 罗雨. 近红外光谱法在参芪扶正注射液醇沉工艺质控中的应用研究 [D]. 杭州: 浙江大学, 2017.
[17] 许之麟. 基于QbD理念的党参水提醇沉工艺研究 [D]. 杭州: 浙江大学, 2016.
[18] Shao J Y, Cao W, Qu H B,. A novel quality by design approach for developing an HPLC method to analyze herbal extracts: A case study of sugar content analysis [J]., 2018, 13(6): e0198515.
[19] Chen Y J, Wang J, Wan D R. Determination of total flavonoids in threecrude drugs by UV-Vis spectrophotometry [J]., 2010, 6(24): 259-263.
[20] 许之麟, 黄文华, 龚行楚, 等. 设计空间法优化党参一次醇沉工艺 [J]. 中国中药杂志, 2015, 40(22): 4411-4416.
[21] 黄慧敏, 张爱玲, 温伍玖, 等. 基于近红外光谱技术的复方大黄汤浓缩液同步快速检测 [J]. 中国实验方剂学杂志, 2020, 26(4): 126-132.
[22] Gong X C, Guo J L, Pan J J,. The development ofquality standard considering the effects of processing [J]., 2021, 29(1): 77-84.
Improvement and establishment of concentrate quality standard of concentrate quality control index for ethanol precipitation process of traditional Chinese medicine: A case study of
PAN Jing-jing1, 2, REN Dan-dan1, 2, QU Hai-bin1, 2, 3, GONG Xing-chu1, 2, 3
1. Pharmaceutical Informatics Institute, College of Pharmaceutical Sciences, Zhejiang University, Hangzhou 310058, China 2. State Key Laboratory of Component-Based Chinese Medicine, Innovation Center in Zhejiang University, Hangzhou 310058, China 3. Jinhua Institute of Zhejiang University, Jinhua 321016, China
To improve the quality control index of concentrate before ethanol precipitation of traditional Chinese medicine and establish the quality standard of concentrate.Multiple batches of Dangshen () concentrates were prepared to study the relationship between density and other properties of the concentrates. The lobetyolin recovery, mass percentage of concentrate fully mixed with ethanol solution and precipitate mass generated per gram concentrate were used as indicators of ethanol precipitation process. The membrane dispersion ethanol precipitation experiments were carried out to screen the critical properties of concentrates. The quantitative models between the above evaluation indicators and critical properties of concentrates were established. Based on the established models, the quality standard ofconcentrates was established by using a prediction error propagation method and verified by experiments.There was a good linear relationship between density and solid content of concentrate. Compared with density, viscosity of concentrate could more sensitively reflect the property differences of different batches of concentrates. The viscosity and solid content were selected as the critical properties of the concentrates.2values of the established second-order polynomial models were greater than 0.97. The verification experimental results showed that the prediction performance of the models was good, and the established quality standard ofconcentrates was reliable.It was recommended to increase the viscosity as a quality control index of concentrates. By establishing the quality standard of concentrates that comprehensively consider density and viscosity, batch-to-batch consistency of ethanol precipitation process is expected to be improved.
ethanol precipitation of traditional Chinese medicine; concentrate quality control;; viscosity; lobetyolin; glucose; fructose; sucrose; total flavone
R283.6
A
0253 - 2670(2022)19 - 6012 - 11
10.7501/j.issn.0253-2670.2022.19.008
2022-04-14
国家中医药管理局创新团队与人才支持计划项目(ZYYCXTD-D-202002)
潘晶晶,硕士研究生,研究方向为中药制药工程。E-mail: 21819006@zju.edu.cn
龚行楚,副教授,研究方向为中药质量控制。E-mail: gongxingchu@zju.edu.cn
#共同第一作者:任丹丹,硕士研究生,研究方向为中药制药工程。E-mail: 22019007@zju.edu.cn
[责任编辑 郑礼胜]
