辛酰水杨酸纳米胶束制剂的制备及其含量测定
2022-03-08潘继飞渠广民陈建英
潘继飞,薛 松,王 鑫,渠广民,封 静,陈建英*
(1.山东省药学科学院 山东省皮肤与黏膜给药工程技术研究中心,山东 济南 250101;2.山东福瑞达医药集团有限公司 山东省黏膜与皮肤给药技术重点实验室,山东 济南 250101;3.山东省食品药品审评查验中心,山东 济南 250014)
辛酰水杨酸(capryloyl salicylic acid,简称CSA),化学名为2-羟基-5-(1-氧代辛基)苯甲酸,是近年来由国外开发,在化妆品和皮肤外用制剂中应用的活性化合物[1]。CSA既保持了水杨酸剥除老化角质的功效,又增强了与皮肤细胞的亲和力,更容易渗透入角质层,可作为美白淡斑、延缓衰老、治疗黑头粉刺的外用成分[2]。CSA具有较强的疏水性,在制剂中通常溶于油相中,经乳化后配制为膏霜或乳液,痤疮的产生多与皮脂分泌旺盛和毛孔堵塞有关,含油脂的产品无疑加剧这一诱因。
胶束属于胶体分散体系,粒径较脂质体和微粒更小,一般在5~100 nm,聚合物胶束疏水内核和亲水外壳的载药体系具有增溶难溶药物、提高生物利用度、靶向和缓释等优点,目前广泛应用于抗肿瘤药物的研究开发[3-5]。在日化领域,聚合物胶束可包载疏水性成分用于在驻留型护肤品中,避免油脂成分的使用,赋予产品清爽、滋润的肤感[6-8]。
目前,CSA纳米胶束制剂尚未见研究报道,CSA的含量测定方法国内仅见报道采用反相色谱测定法[9-10],但该方法成本高,耗时长,不利于推广应用。本研究采用直接溶解法制备了CSA纳米胶束,同时建立了一种更简捷的测定含量的高效液相色谱法(HPLC),用于检测纳米胶束型制剂中辛酰水杨酸的含量,以期为拓展CSA的应用及CSA纳米胶束制剂产品的质量控制奠定基础。
1 仪器与材料
1.1 仪器
高效液相色谱仪(LC-20AT型泵、SPD-M20A型检测器、Lab Solution液相色谱数据工作站,日本岛津公司);XA105DU分析天平(Mettler Toledo);PB-10 pH计(赛多利斯);Nano-ZS90马尔文动态激光光散射粒度仪(马尔文帕纳科);ZEISS EVO 钨灯丝扫描电子显微镜(卡尔蔡司)。
1.2 材料
辛酰水杨酸(上海麦克林C860254,纯度≥98 %);乙腈、甲醇为色谱纯试剂;其余为分析纯试剂。
2 方法与结果
2.1 CSA纳米胶束制剂的制备
取CSA原料2.5~5.0 g,溶于20 ml丙二醇和40 ml PEG30蓖麻油,加入适量防腐剂,缓慢加入纯化水至1000 ml,0.45 μm微孔滤膜过滤,获得自组装纳米胶束溶液。
2.2 CSA纳米胶束的粒径测定
按照2.1项中CSA胶束的制备方法,制备0.25 %和0.5 %的CSA胶束溶液及空白胶束溶液,采用激光粒度分布仪测定胶束的粒径分布及Zeta电位。空白胶束、0.25 %和0.50 %的CSA胶束平均粒径(Di)值分别为11.30,8.86和7.96 nm,多分散系数(PDI)值分别为0.112,0.164和0.157,粒径分布2~12 nm,不同CSA浓度的胶束Zeta电位均呈现负值,且随着CSA浓度的增加胶束的粒径减小(图1和表1)。

图1 不同浓度CSA纳米胶束及空白胶束的粒径分布图
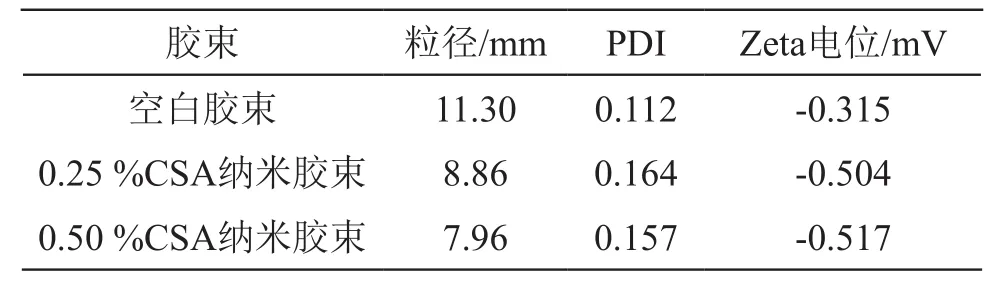
表1 不同浓度CSA纳米胶束及空白胶束的表征
2.3 CSA纳米胶束的SEM
将制备得到的CSA胶束稀释5倍后滴在铜网上,静置10 min,用滤纸从铜网的底部将溶液吸走。待铜网干燥后,喷金,置扫描电镜下观察胶束的形态。图2中A、B、C图分别是空白胶束、CSA浓度为0.25 %和0.5 %胶束的SEM照片。

图2 自组装CSA纳米胶束的SEM照片(A:空白胶束;B:0.25 %CSA胶束;C:0.5 %CSA胶束)
2.4 纳米胶束中CSA的含量测定
2.4.1 溶液制备 空白溶液:照CSA溶液剂处方配制不含CSA的空白供试品溶液。精密量取0.2 ml置入50 ml量瓶,加入甲醇流动相稀释至刻度,摇匀。
对照品溶液制备:精密称取CSA约20 mg置入100 ml量瓶,加入适量甲醇溶解,并稀释至刻度,摇匀,精密量取1 ml置入10 ml量瓶,加入甲醇稀释至刻度,摇匀。制成每1 ml中含有CSA约0.02 mg的对照品溶液。供试品溶液制备:精密量取CSA纳米胶束溶液0.4 ml置入100 ml量瓶,加入甲醇并稀释至刻度,摇匀。
2.4.2 色谱条件 色谱柱:Waters XBridge C18(4.6 mm×150 mm,5 μm)。流动相:甲醇-乙腈-0.1 mol/L磷酸溶液(48:30:22),检测波长225 nm,柱温40 ℃,流速1.0 ml/min,进样体积10 μl。理论板数按CSA峰计算应不低于3000,拖尾因子不高于1.5。
2.4.3 波长选择 取CSA对照品溶液,DAD检测器在190~400 nm波长范围内进行紫外扫描,见图2,结果表明,CSA有两个紫外吸收峰,波长分别为225 nm和269 nm,225 nm的吸收值高于269 nm,因此选择225 nm为检测波长。
2.4.4 专属性试验 分别取空白溶液、对照品溶液及供试品溶液各10 μl,注入液相色谱仪,记录色谱图。结果表明,CSA保留时间约4.8 min,空白溶液在CSA出峰位置无干扰,表明本色谱条件专属性良好。见图3~5。
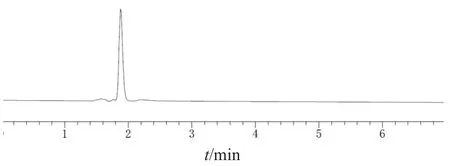
图3 空白溶液HPLC图谱
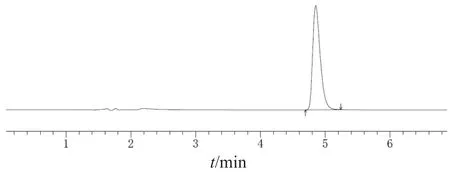
图4 辛酰水杨酸对照品溶液HPLC图谱
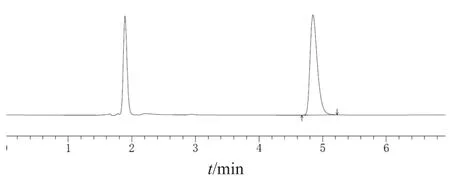
图5 供试品溶液HPLC图谱
2.4.5 线性试验 精密称取CSA对照品约20 mg,置入100 ml量瓶,加入适量甲醇使完全溶解,并稀释至刻度,摇匀;精密量取0.5,1,2,3,4,5 ml分别置入10 ml量瓶,加入甲醇稀释至刻度,摇匀,精密量取上述溶液各10 μl注入液相色谱仪,记录色谱图及峰面积,以浓度C为横坐标,峰面积A为纵坐标做线性回归,求得CSA的线性回归方程为A=50483C+10595,相关系数r=0.9997,结果表明,CSA浓度在4.10~41.14 μg/ml浓度范围内线性关系良好。
2.4.6 精密度试验 精密量取CSA对照品溶液10 μl注入液相色谱仪,连续进样6次,记录色谱图及峰面积,计算RSD为0.15 %,表明仪器精密度良好。取同一批样品,连续配制6份供试品溶液,记录色谱图及峰面积,计算含量RSD为0.56 %,表明方法精密度良好。
2.4.7 回收率试验 精密称取CSA对照品适量(约相当于CSA处方量的80 %,100 %,120 %),按处方加入其它辅料,分别平行配制3份,照2.1项下配制成供试品溶液。依法测定,计算回收率。结果见表2。

表2 回收率试验结果
2.4.8 样品含量测定 按照2.1项下制备本品3批样品,按照2.2.1项下制备供试品及对照品溶液,按照2.2.2项下色谱条件,分别取10 μl注入色谱仪,记录色谱图及峰面积,按外标法计算含量,含量结果分别为102.90 %,99.60 %,104.85 %。
3 讨论
本研究首次制备了自组装CSA纳米胶束制剂,获得了粒径小于20 nm、粒径分布均匀的纳米胶束溶液。CSA的加入使胶束粒径减小,高浓度CSA纳米胶束粒径小于低浓度CSA纳米胶束。目前国内已报道的CSA含量测定方法流动相为乙腈-5 mmol/L癸烷磺酸钠(含质量分数0.1 %磷酸),其中的离子对试剂癸烷磺酸钠和色谱柱的固定相结合产生不可逆吸附,进而影响固定相活性位点,从而达到分析样品的作用,该方法中离子对试剂较难从色谱柱上冲洗干净而造成色谱柱使用寿命的缩短,大大提高了该分析方法的耗材成本;此外,该方法需要较长的平衡时间使流动相中的离子对和硅羟基发生作用,色谱柱需要较长的清洗时间也提高了该分析方法的时间成本。本研究建立了纳米胶束制剂中CSA的HPLC含量测定方法,采用甲醇-乙腈-0.1 mol/L磷酸溶液(48:30:22)为流动相,经方法学验证,该方法专属性好、准确度和精密度高,具有方便、快捷、适用性强等优点,填补了现行检测方法的空白,为CSA制剂产品的质量控制提供依据。CSA纳米胶束制剂的长期稳定性和安全性有待进一步试验研究。
