石墨消解-电感耦合等离子体质谱法测定烟用香精中的重金属
2022-03-07杨振东严莉红白若石马雁军周骏
杨振东,严莉红,白若石,马雁军,周骏
烟草与烟气化学
石墨消解-电感耦合等离子体质谱法测定烟用香精中的重金属
杨振东,严莉红,白若石,马雁军,周骏*
上海烟草集团有限责任公司技术中心北京工作站,北京 101121
【目的】优化和建立石墨消解-电感耦合等离子体质谱联用的方法测定烟用香精中的重金属。【方法】选择自主设计的新型消解罐,研究不同消化温度、不同消解液用量对样品消化的影响,将优化结果与微波消解-电感耦合等离子体质谱联用法对比检出限、定量限、加标回收率、RSD。并依据GB/T 27417—2017《合格评定化学分析方法确认和验证指南》对建立的方法进行方法学验证。【结果】一次性加入10 mL HNO3与2 mL H2O2作为消解液,在170℃的最高消解温度下,烟用香精4.0 h内完成石墨消解,过程中无需补加消解液。对于烟用香精中不同重金属元素Cr、Cd、Ni、Pb、As的测定,本方法与微波消解-电感耦合等离子体质谱法相比,检出限、定量限无显著差异,RSD值更低。方法的测量范围、线性范围、检出限、定量限、精密度、正确度6个参数符合GB/T 27417—2017的指标要求。【结论】本实验构建的方法步骤简单、检出限低、回收率高、重复性好,满足烟用香精检验的要求,具有普遍适用性,适合大批量烟用香精样品的快速检测。
石墨消解;电感耦合等离子体质谱;烟用香精;重金属
烟用香精是用两种或两种以上香料、适量溶剂和其他成分调和制成的,在烟草制品加工过程中施加于烟草中能突出或修饰烟草制品风格并能改善刺激性、杂气等烟草制品品质的具有一定香气、香味的混合 物[1-2]。烟用香精生产过程如果控制不当,可能带入重金属Cr、Cd、Ni、Pb、As等重金属元素,这些重金属进入人体后对人体神经系统、内脏器官会造成潜在的危害[3-4]。因此,烟用香精中的重金属含量是卷烟生产企业使用前的必检项目。检测过程分为烟用香精的消解和上机测定两部分,现有烟草行业标准(YC/T 294—2009)采用电加热器消解、石墨炉原子吸收法测定,上海烟草集团企业标准(QJ/SYJF35—2020)选择微波消解、电感耦合等离子体质谱法测定。
传统的电加热器消解耗酸量大,且消解过程中需要不断补加酸液,存在控温能力差、终点不易确定等缺点[5];微波消解时间短,用酸少,能有效地防止污染和元素的挥发损失,但是需要人工加消解液、转移、定容,不适合大批量样品的检测[6]。石墨消解具有智能化的控制程序,自动加酸、消解、赶酸、定容、处理批量大等优点,包裹式加热使样品受热更均匀,使后续重金属测定结果的重复性和准确性更高,近年来在重金属检测中的应用不断见诸报道[7]。石墨炉原子吸收法1次只能测定1种元素,而电感耦合等离子体质谱法能够同时测定多种元素。因此,石墨消解香精-电感耦合等离子体质谱法测定烟用香精中的重金属是方法改进的方向,但是目前尚未有相关文献报道。
本项目组改良了一种用于石墨消解的新型聚四氟乙烯消解罐[8],并建立了石墨消解-电感耦合等离子体质谱法测定烟用香精中的重金属元素Cr、Cd、Ni、Pb、As的方法,旨在为烟用香精中的重金属检测提供一种简单、准确、适合大批量样品的检测方法。
1 材料与方法
1.1 仪器、试剂与材料
1.1.1 仪器
电感耦合等离子体质谱仪(德国耶拿公司,型号:PQ-MS);全自动石墨消解仪(美国托马斯公司,型号:DEENA),微波消解仪(美国培安公司,型号:MARS6)。
新型消解罐与厂家消解罐结构图如图1所示,厂家消解罐为一端开口的圆柱体结构;新型消解罐包括底部罐体(1)、消解罐套(2)和消解罐盖(3);消解罐盖(3)的上端设置有封板(31),封板(31)上设置有通孔(32),消解罐套(2)的下端与底部罐体(1)的上端可拆卸密封连接,消解罐套(2)的上端与消解罐盖(3)的下端可拆卸密封连接;消解罐套(2)内设置有回流盖(21),回流盖(21)位于消解罐套(2)的上部;消解罐套(2)内壁上设置有回流槽(22),回流槽(22)连通位于回流盖(21)上、下两侧的消解罐套(2)的内部空腔,回流槽(22)能够平衡回流盖(21)上、下两侧的气压,使用更安全,并且回流槽(22)可方便消解罐盖(3)内凝结的液体回流至消解罐套(2)内,回流盖(21)和封板(31)起到两次凝结回流的作用。与厂家消解罐相比,新型消解罐能够更加有效的降低酸液和易挥发金属的损失。
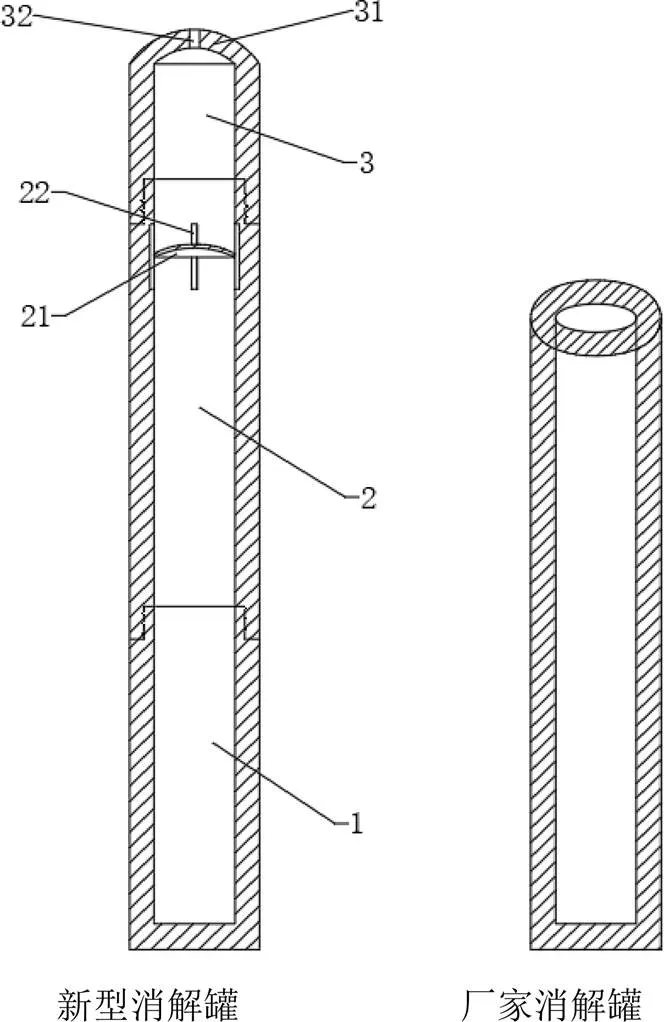
注:1.底部罐体;2.消解罐套;3.消解罐盖;21. 回流盖;22. 回流槽;31. 封板;32. 通孔
1.1.2 试剂
硝酸(德国默克,超级纯);双氧水(北京化工厂,优级纯);重金属元素(Cr、Cd、Ni、Pb、As)混标(北京有色金属研究院)储备液(100 mg·L-1),用5%硝酸分级稀释到0.10、0.20、0.50、1.00、2.00、5.00 µg·L-1作为混合标准工作溶液;超纯水(18.2 M Ω·cm-1)。
1.1.3 供试材料
烟用香精样品共计11个,每个样品充分混合均匀后从中取不低于100 mL构成实验室样品。涉及样品的物理性质见表1,共有5个香精、5个料液、1个浸膏,其中4个样品粘稠、7个样品不粘稠。依据YC/T 145.4—1998《烟用香精乙醇中溶混度的评估》测定25℃时,1体积样品在20体积一定浓度乙醇水溶液中的混溶度,其中4个样品与水混溶、4个样品与50%的乙醇水溶液混溶、2个样品与70%的乙醇水溶液混溶、1个样品与95%乙醇混溶。
表1 香精样品物理性质
Tab.1 Physical properties of flavor samples
样品编号样品名称是否粘稠混溶度/%(乙醇水溶液浓度V/V) 1香精粘稠50 2香精不粘稠50 3香精不粘稠70 4香精不粘稠70 5香精不粘稠95 6料液粘稠50 7料液粘稠0 8料液不粘稠0 9料液不粘稠0 10料液不粘稠0 11浸膏粘稠50
1.2 实验方法和条件
1.2.1 石墨消解方法
分析天平准确称取某烟用香精0.200 g,精确至0.001 g,置于自制石墨消解罐中。加入硝酸和双氧水,升温程序设置见表2,每次升温结束震荡消解罐,震荡的时间均控制在20~40 s。升温到最高消解温度后保持至消解液残余约1 mL、消解液澄清无色或淡黄色时停止加热后冷却;滴加超纯水定容到50 mL或100 mL。
表2 石墨消解升温程序
Tab.2 Heating process of graphite digestion
起始温度/℃升温时间/min终点温度/℃ 室温3050 503080 8030100 10030130 13030150 15030最高设置温度
1.2.2 微波消解方法
分析天平准确称取烟用香精0.200 g,精确至0.001 g,置于微波消解罐中。加入6 mL硝酸和1 mL双氧水,5 min升温到100℃并保持5 min;5 min升温到130℃并保持5 min;5 min升温到160℃并保持5 min;10 min升温到190℃并保持20 min;冷却后用超纯水定容到50 mL或100 mL。
1.2.3 电感耦合等离子体质谱仪仪器条件
射频功率1200 W,载气流速1.2 L·min-1,进样速率0.1 mL·min-1,重复次数5次,碰撞气He气流速0.1 L·min-1,获取模式为全定量分析。Cr元素测量同位素52,Cd元素测量同位素111,Ni元素测量同位素60,Pb元素测量同位素208,As元素测量同位素75,各个元素积分时间均为6 s。以5 μg·L-1In元素为内标。
2 结果与讨论
2.1 消解液体系的确定
烟用香精的主要致香成分为糖苷类潜香化合物以及糖胺类潜香化合物、酮类、酸类、杂环类化合物[9-10]等有机物,溶剂包括水、酒精、丙二醇等。因此烟用香精的消解主要是对有机物的消解。有机物的消解需要强氧化剂,常用的消解液包括HNO3/HClO4、HNO3/HCl、HNO3/H2O2三种体系[11-14]。
HNO3/HClO4和HNO3/HCl消解液体系中引入的Cl元素导致(1)ICP-MS检测需要H2碰撞模式或校正方程以消除ArCl对As元素的质谱干扰[15];(2)Cl元素与Cr、As形成易挥发的Cl化物导致检测结果偏低[16]。对于重金属元素含量为痕量的烟用香精:(1)H2碰撞模式下质谱灵敏度降低、噪音升高会导致检出限与定量限升高;(2)当干扰元素的强度大于被分析元素的强度时,校正方程带来的误差较大,甚至无法使用[17]。因此,HNO3/HClO4和HNO3/HCl消解液体系不适用于重金属元素含量为痕量的烟用香精的消解。H2O2在消解后不会引入非金属元素质谱干扰和产生易挥发金属络合物,故本试验中选择HNO3/H2O2体系。
2.2 石墨消解罐的设计
石墨消解仪厂家配备的消解罐为敞口的中空圆柱体管子(高度10 cm),在消解过程中有大量的消解液损失,特别是易于挥发的HNO3/H2O2消解液体系,因此在消解过程中需要不断补充消解液以免消解液烧干。本项目组改良的消解罐通过增加罐体高度和设置回流盖有效减少消解液挥发损失,过程中无需补加消解液,同时通过小孔保持罐体内外压平衡。
2.3 石墨消解消解液用量的优化
选取某烟用香精,称取多份0.200 g(精确到0.001 g)样品,消解液HNO3与H2O2在不同加入体积条件下对比消解结果,最高消解温度为170℃,升温程序与1.2.1中一致。如表3所示:10 mL HNO3与1 mL H2O2、8 mL HNO3与2 mL H2O2条件下无法消解完全,存在少量不溶物。10 mL HNO3与2 mL H2O2、10 mL HNO3与3 mL H2O2、12 mL HNO3与2 mL H2O2条件下消解完全,消解时间总时间分别为4.0 h、4.3 h、4.5 h,综合试剂与时间成本,优化结果为选择10 mL HNO3与2 mL H2O2消解液体系。
表3 不同消解液所需消化时间
Tab.3 Digestion time required by different digestion liquids
消解液体积/mL消解总时长/h消解结果 硝酸双氧水 1013.7少量不溶物 1024.0澄清 1034.3澄清 823.5少量不溶物 1224.5澄清
2.4 石墨消解消化温度的优化
选取某烟用香精,称取多份0.200 g(精确到0.001 g)样品,设计了160℃、170℃、180℃、190℃等4个最高消化温度对比实验,选择10 mL HNO3与2 mL H2O2消解液体系,消解程序与1.2.1中一致。升至最高温度后,待消解液残余约1 mL、消解液澄清无色或淡黄色时停止加热,记录消化时间。如表4所示,要达到消解终点,最高消解温度为160℃时需要6.0 h,170℃时需要4.0 h,180℃时需要3.7 h,190℃时需要3.5 h。
表4 不同消化温度处理所需消化时间
Tab.4 Digestion time of treatments under different digestive temperatures
最高消化温度/℃最高温度消解时间/h总时长/h 160 3.06.0 170 1.04.0 180 0.73.7 190 0.53.5
上述烟用香精称取多份0.200 g(精确到0.001 g)样品,每一样品加入一定体积的重金属元素(Cr、Cd、Ni、Pb、As)的混标溶液,制备成加标量为1.0 mg·kg-1的烟用香精。每个加标浓度样品分别做10次平行样品,按照上述石墨消解方法进行消解计算加标回收率。结果如表5所示:元素Cr、Cd、Ni、Pb在不同最高消解温度条件下加标回收率、RSD值无显著变化;元素As在最高消解温度为180℃、190℃与最高消解温度为160℃、170℃条件下相比,加标回收率由92.8%~93.1%显著降低到85.6%~90.6%、RSD值由2.59%~2.81%显著升高到3.69%~8.71%。综合考虑消解时长、加标回收率、RSD值,170℃为最优最高消化温度。
表5 不同消解温度下烟用香精加标回收率(n=10)
Tab.5 Recoveries of tobacco flavor under different digestive temperatures(n=10)
最高消化温度CrCdNiPbAs 回收率/%RSD/%回收率/%RSD/%回收率/%RSD/%回收率/%RSD/%回收率/%RSD/% 160℃98.32.8899.11.9896.12.2796.72.4192.82.59 170℃99.82.5198.51.6694.52.5596.12.5193.12.81 180℃97.33.3398.51.7194.92.4997.22.8290.63.69 190℃97.23.0697.11.9395.73.8796.62.7185.68.71
2.5 测量范围和线性范围
依据GB/T 27417—2017《合格评定化学分析方法确认和验证指南》中5.2测量范围的验证方法,通过标准溶液的精密度、正确度对本方法的测量范围进行验证,对重金属元素(Cr、Cd、Ni、Pb、As)混标工作溶液0.10、0.50、2.00µg·L-1等3个不同浓度进行10次检测分析,以10次检测结果的室内变异系数(CVI)表征精密度、回收率表征正确度。结果如表6所示,符合GB/T27417—2017关于元素含量为0.1 µg·L-1时CVI小于43%,元素含量为0.5、2.0 µg·L-1时CVI小于21%;元素含量小于0.1 mg·L-1时回收率为60%~120%的要求。
表6 标准溶液的正确度及精密度(n=10)
Tab.6 Precision and accuracy of standard solutions(n=10)
元素0.1 µg·L-10.5 µg·L-12.0 µg·L-1 回收率/%RSD/%CVI/%回收率/%RSD/%CVI/%回收率/%RSD/%CVI/% Cr96.13.132.398.12.63.899.71.30.7 Cd95.92.829.299.22.14.299.91.10.6 Ni95.82.728.298.22.34.7102.11.20.6 Pb97.43.333.998.72.44.999.51.30.7 As98.72.525.399.11.93.899.81.10.6
依据GB/T 27417—2017中5.3线性范围的验证方法,对本方法的线性范围进行验证,重金属元素Cr、Cd、Ni、Pb、As的线性回归方程的相关性系数均大于0.999,符合依据GB/T 27417—2017中线性回归方程相关系数不低于0.99的要求。
2.6 检出限和定量限
依据GB/T 27417—2017,采用空白标准偏差法验证检出限和定量限。本实验优化的石墨消解方法和1.2.2中的微波消解,分别重复11次空白实验,将各测定结果换算为样品中元素的含量,计算11次平行测定的标准偏差,以3倍标准偏差计算检出限,10倍标准偏差计算定量限。由表7可以看出,石墨消解与微波消解处理烟用香精得到的重金属元素Cr、Cd、Ni、Pb、As的检出限、定量限不存在显著差异。
表7 2种消解方法检出限与定量限对比
Tab.7 Comparison of LOD and LOQ between two methods
金属元素石墨消解法微波消解法 检出限/(mg·kg-1)定量限/(mg·kg-1)检出限/(mg·kg-1)定量限/(mg·kg-1) Cr0.0150.0500.0140.047 Cd0.0140.0470.0140.043 Ni0.0110.0370.0120.040 Pb0.0160.0530.0150.049 As0.0140.0470.0120.040
2.7 石墨消解与微波消解加标回收率对比实验
选取某烟用香精,称取多份0.200 g(精确到0.001g)样品,分别添加不同体积的重金属元素(Cr、Cd、Ni、Pb、As)的混标溶液,加标量分别为0.106 mg·kg-1、0.208 mg·kg-1、0.510 mg·kg-1、1.020 mg·kg-1,按照本实验优化的石墨消解方法和1.2.2中的微波消解处理样品,所有样品均消解完全后按照1.2.3所述条件下进行重金属含量测定。每个加标浓度样品分别做10次平行样品,平行样品求平均值后计算加标回收率。结果如表8所示:石墨消解法不同元素加标回收率为90.6%~104.9%,微波消解法不同元素加标回收率为90.4%~103.1%,两种方法均能满足实验要求。但是对于As元素,石墨消解法与微波消解法加标回收率分别为:90.6%~97.6%、94.3%~98.1%。石墨消解法对于As元素的加标回收率低于微波消解,特别是在低加标浓度条件下,这是因石墨消解法消解过程时长4.0 h,微波消解法时长仅为1.0 h,而As元素易于挥发。石墨消解法不同元素RSD为1.38%~5.14%,微波消解法不同元素RSD为2.09%~5.91%,石墨消解的RSD整体上低于微波消解法,这是由于石墨消解包裹式加热使样品受热更均匀、智能化的控制程序使后续重金属测定结果的重复性更好。
表8 2种消解方法加标回收率对比(n=10)
Tab.8 Recoveries of two digestion methods(n=10)
元素原始值/(mg·kg-1)加标量/(mg·kg-1)测定值/(mg·kg-1)回收率/%RSD/% 石墨消解微波消解石墨消解微波消解石墨消解微波消解 Cr0.4160.1060.5150.52193.499.14.324.08 0.2080.6230.61999.597.61.983.21 0.5100.9130.91997.598.62.062.21 1.0201.4241.42698.899.01.732.09 Cd0.1030.1060.2050.21196.2101.93.515.08 0.2080.3050.31397.1101.02.583.66 0.5100.6380.629104.9103.12.312.75 1.0201.1701.090104.696.81.592.81 Ni0.1070.1060.2080.20995.396.24.563.98 0.2080.3040.30294.793.83.573.67 0.5100.6410.623104.7101.22.332.85 1.0201.0661.09994.097.32.562.43 Pb0.2040.1060.3090.30299.192.55.145.88 0.2080.3980.39293.390.44.995.09 0.5100.6740.68092.293.31.382.51 1.0201.1901.18396.796.02.372.39 As0.4570.1060.5530.55790.694.34.995.91 0.2080.6520.65893.896.64.714.31 0.5100.9410.95294.997.12.563.25 1.0201.4531.45897.698.12.612.33
2.8 石墨消解-电感耦合等离子体质谱法的正确度及精密度
依据GB/T 27417—2017中5.5正确度的验证方法,采用加标回收率的方法对正确度进行验证;依据GB/T 27417—2017中5.6精密度的验证方法,以10次检测结果数值的CVI表示精密度。选取10种不同的烟用香精分别命名为样品1~10,重金属元素(Cr、Cd、Ni、Pb、As)本底值均为未检出。分别称取多份0.200 g(精确到0.001g)样品,每一样品加入一定体积的重金属元素(Cr、Cd、Ni、Pb、As)的混标溶液,制备成加标量为1.0 mg·kg-1的烟用香精。每个加标浓度样品分别做10次平行样品,按照上述优化的石墨消解方法进行消解,所有样品消解结束后均澄清无不溶物,然后在上述相同条件下进行重金属含量测定,之后计算加标回收率、RSD、CVI。结果如表9所示:不同金属元素的加标回收率为92.1%~103.1%,符合GB/T 27417—2017中被测组分含量1~100 mg·kg-1时回收率为90%~110%的要求。不同金属元素的CVI为1.1%~3.2%,符合GB/T 27417—2017中被测组分含量为1 mg·kg-1时CVI小于30%的要求。
表9不同烟用香精正确度和精密度(n=10)
Tab.9 Accuracy and precision of different tobacco flavors(n=10)
样品编号CrCdNiPbAs 回收率/%RSD/%CVI/%回收率/%RSD/%CVI/%回收率/%RSD/%CVI/%回收率/%RSD/%CVI/%回收率/%RSD/%CVI/% 197.31.881.999.71.381.499.61.972.095.82.312.492.11.992.2 299.82.512.598.51.661.794.52.552.796.12.512.693.12.813.0 396.32.332.4101.51.791.893.92.392.597.51.821.995.62.692.8 497.21.061.1103.12.032.096.72.873.093.61.711.897.82.712.8 595.62.312.498.32.352.495.21.932.094.51.831.997.92.612.7 698.11.761.897.51.211.294.62.212.394.81.651.796.81.401.4 794.11.912.0101.91.071.193.81.972.195.11.351.497.81.912.0 895.92.993.1102.82.132.198.72.852.996.81.491.598.11.351.4 997.11.821.998.71.551.696.52.993.197.11.591.697.51.631.7 1095.82.712.899.01.721.797.93.123.294.81.992.194.91.551.6
3 结论
(1)使用本实验设计的新型消解罐,在10 mL HNO3与2 mL H2O2消解液体系、最高消解温度为170℃条件下,烟用香精4.0 h消解完全,与电加热器、石墨消解仪厂家配备的消解罐相比消解过程中无需补加消解液。与微波消解相比,更适合大批量样品的检测。
(2)本实验建立的方法与微波消解-电感耦合等离子体质谱法相比:检出限、定量限无显著差异;元素Cr、Cd、Ni、Pb加标回收率无显著差异、元素As加标回收率略低;RSD值低,重复性更好。
(3)依据GB/T 27417—2017对本实验建立的石墨消解-电感耦合等离子体质谱联用方法测定不同烟用香精中元素Cr、Cd、Ni、Pb、As进行方法学验证,检测过程中所涉及的测量范围、线性范围、检出限、定量限、精密度、正确度6个参数均符合要求,表明本方法满足烟用香精检验的要求,准确可靠,且具有普遍适用性,易于推广。
[1] 刘欣,向海英,张涛,等. 水蒸气蒸馏分离-气相色谱/质谱法测定烟用香精和料液中的防腐剂[J]. 云南大学学报(自然科学版),2018, 40(3): 551-560.
LIU Xin, XIANG Haiying, ZHANG Tao, et al. Steam distillation pretreatment coupled with GC-MS for determination of preservatives in flavouring and casing for tobacco[J]. Journal of Yunnan University, 2018, 40(3): 551-560.
[2] 米其利,张建平,楼牧梦,等. 我国典型湿热地区变质烟用香精中腐败微生物的多样性分析[J]. 微生物学通报,2019, 46(9): 2121-2133.
MI Qili, ZHANG Jianping, LOU Mumeng, et al. Diversity of spoilage microorganisms in tobacco flavor in the typical hot-humid areas in China[J]. Microbiology China, 2019, 46(9): 2121-2133.
[3] 田娟娟,杜慧娟,潘秋红,等. 电热板消解与密闭罐消解对土壤中49种矿质元素ICP-MS法检测的影响[J]. 分析测试学报,2009, 28(3): 319-325.
TIAN Juanjuan,DU Huijuan, PAN Qiuhong, et al. Digestionon Determination of 49 Mineral Elements in Soil by Inductively Coupled Plasma Mass Spectrometry[J]. Journal of Instrumental Analysis, 2009, 28(3): 319-325.
[4] 高会艳. ICP-MS和ICP-AES测定地球化学勘查样品及稀土矿石中铌钽方法体系的建立[J]. 岩矿测试,2014, 33(3): 312-320.
GAO Huiyan. Determination Systems of Nb and Ta in Geochemical Samples and Rare Earth ores by ICP-MS and ICP-AES[J]. Rock and Mineral Analysis, 2014, 33(3): 312-320.
[5] 廖惠云,张映,庄亚东,等. 烟用香精中重金属铅和砷的分析研究[J]. 中国烟草学报,2008, 14(4): 8-12.
LIAO Huiyun, ZHANG Ying, ZHUANG Yadong, et al. Analysis of Pb and As in cigarette flavors[J]. Acta Tabacaria Sinica, 2008, 14(4): 8-12.
[6] 刘秀彩. 石墨炉原子吸收法测定烟用香精中的镉[J]. 烟草科技,2010, 271(2): 35-38.
LIU Xiucai. Determination of Cadmium in Tobacco Flavorby Graphite Furnace Atomic Absorption Spectrometry[J]. Tobacco Science & Technology, 2010, 271(2): 35-38.
[7] 钱薇,蒋倩,王如海,等. 程序控温石墨消解-氢化物原子荧光光谱法测定植物中痕量硒[J]. 光谱学与光谱分析,2014, 34(1): 235-240.QIAN Wei,JIANG Qian, WANG Ruhai, et al. Determination of Trace Selenium in Plants by Hydride Generation Atomic Fluorescence Spectrometry with Program Temperature-Controlled Graphite Digestion[J]. Spectroscopy and Spectral Analysis, 2014, 34(1): 235-240.
[8] 杨振东,郑晓曼,陈莉莎,等. 重金属消解罐:中国,CN212432756U[P]. 2021-01-29.
YANG Zhendong, ZHENG Xiaoman, CHEN Lisha, et al. Digestion tank of heavy metal[P]. CN 212432756U.
[9] 高海有,刘秀明,高莉, 等. 烟用香精香料研究现状与发展趋势[J]. 香料香精化妆品, 2019, 4(2): 69-73.
GAO Haiyou, LIU Xiuming, GAO Li, et al. The Current Situation and Trends of Tobacco Flavor Research [J]. Flavour Fragrance Cosmetics, 2019, 4(2): 69-73.
[10] 谢剑平. 形势与未来:烟草科技发展展望[J]. 中国烟草学报,2017, 23(3): 1-7.
XIE Jianping. On the development prospects of tobacco science and technology in China[J]. Acta Tabacaria Sinica, 2017, 23(3): 1-7.
[11] 王艳艳,时志强,张彪. 氢化物发生-原子荧光法测定污泥中的痕量汞[J]. 光谱学与光谱分析,2013, 33(3): 826-828.
WANG Yanyan, SHI Zhiqiang, ZHANG Biao. Determination of Trace Mercury in Sludge Samples by Hydride Genetration-Atomic Fluorescence Spectrometry[J]. Spcetroscopy and Spectral Angalysis, 2013, 33(3): 826-828.
[12] 耿頔,韦朝阳,季宏兵.湖泊水体悬浮物中痕量砷的测定方法[J]. 环境科学学报,2015, 35(6): 1728-1734.
GENG Di, WEI Chaoyang, JI Hongbing. Determination of Trace arsenic on suspended solids of lake water[J]. Spcetroscopy and Spectral Angalysis, 2015, 35(6): 1728-1734.
[13] 孙德忠,安子怡,许春雪,等. 四种前处理方法对电感耦合等离子体质谱测定植物样品中27种微量元素的影响[J]. 岩矿测试, 2012,31(6): 961-996.
SUN Dezhong, AN Ziyi, XU Chunxue, et al. Comparison of Different Digestion Procedures for Elemental Determination in Plant Samples by Inductively Coupled Plasma-Mass Spectrometry[J]. Rock and Mineral Analysis, 2012, 31(6): 961-996.
[14] 张霖琳,梁宵,加那尔别克·西里甫汗,等. 在土壤及底泥重金属测定中不同前处理和分析方法的比较[J]. 环境化学,2013, 32(2): 302-306.
ZHANG Linlin, LIANG Xiao, JANARBEK Xiriphan, et al. Comparison of different pretreatment and analytical method of heavy metals in soil and sediment samples[J]. Environmental Chemistry, 2013, 32(2): 302-306.
[15] 刘锋,石志芳,姜霞,等.HPLC-ICP-MS法分析太湖沉积物中砷的形态及分布特征[J]. 质谱学报,2011, 32(3): 170-175.
LIU Feng, SHI Zhifang, JIANG Xia, et al. Speciation Analysis of Arsenic and Their Distribution Characteristic in Sediments of Taihu Lake by HPLC-ICP-MS[J]. Journal of Chinese Mass Spectrome try Society, 2011, 32(3): 170-175.
[16] 袁小雪,周定友,李杰,等. ICP-MS在PM2.5元素分析中的应用进展[J]. 光谱学与光谱分析,2020, 40(8): 2373-2381.
YUAN Xiaoyue, ZHOU Dingyou, LI Jie, et al. Progress in the Analysis of Elements in PM2.5by ICP-MS[J]. Spcetroscopy and Spectral Angalysis, 2020, 40(8): 2373-2381.
[17] 赵小学,张霖琳,张建平,等. ICP- MS 在环境分析中的质谱干扰及其消除[J]. 中国环境监测,2014, 30(3): 101-106.
ZHAO Xiaoxue, ZHANG Linlin, ZHANG Jianping, et al. Spectral Interference and Elimination of Environmental Analysis with ICP-MS [J]. Environmental Monitoring in China, 2014, 30(3): 101-106.
Determination of heavy metals in tobacco flavors by graphite digestion-ICP-MS
YANG Zhendong, YAN Lihong, BAI Ruoshi, MA Yanjun, ZHOU Jun*
Beijing Branch, Technology Center, Shanghai Tobacco Group Co., Ltd., Beijing 101121, China
[Background] The graphite digestion-ICP-MS method for the determination of heavy metals in tobacco flavor was optimized and established. [Methods] The influence of digestion temperature and digestion solution dosage on sample digestion was studied by using a new self-designed digestion tank. The established method was compared with microwave digestion-ICP-MS method in terms of LOD, LOQ, standard recovery rate, RSD. Moreover, the established method was validated according to national standard GB/T 27417 ― 2017 for conformity assessment. [Results] The results showed that under the maximum digestion temperature of 170 ℃ and by using 10 mL HNO3/2 mL H2O2as the digestion solution, the digestion was completed within 4.0 h. For the determination of different heavy metal elements Cr, Cd, Ni, Pb and As in tobacco flavor, the proposed method had no obvious difference in the LOD and LOQ compared with the microwave digestion-ICP-MS method and the RSD value was lower. The six parameters of the method, including measurement range, linear range, LOD, LOQ, precision and accuracy, were in accordance with the requirements of national standard GB/T 27417-2017. [Conclusion]The proposed method has the advantages of simple operation, low LOD, high recovery rate and good repeatability, which meets the requirement of tobacco flavor testing and is suitable for the rapid detection of large quantities of tobacco flavor samples.
graphite digestion; ICP-MS; tobacco flavors; heavy metal
Corresponding author. Email:zhoujun100@sohu.com
上海烟草集团北京卷烟厂有限公司项目(No. TP2018-C5)
杨振东(1985—),博士,工程师,主要从事烟草化学研究,Tel:010-59028261,Email:jnssds@126.com
周骏(1966—),Tel:010-59028201,Email:zhoujun100@sohu.com
2021-02-23;
2021-12-24
杨振东,严莉红,白若石,等. 石墨消解-电感耦合等离子体质谱法测定烟用香精中的重金属[J]. 中国烟草学报,2022,28(1). YANG Zhendong, YAN Lihong, BAI Ruoshi, et al. Determination of heavy metals in tobacco flavors by graphite digestion-ICP-MS[J]. Acta Tabacaria Sinica, 2022, 28(1). doi: 10.16472/j.chinatobacco.2021.T0028
