钴锰氧化物的表征分析及其催化氧化甲苯的性能对比研究
2022-03-04王文祥刘泗东吴平霄
黎 雯, 王文祥, 刘泗东, 吴平霄
(1.广东环境保护工程职业学院, 广东 佛山 528216;2.佛山科的气体化工有限公司, 广东 佛山 528000;3.华南理工大学环境与能源学院, 广东 广州 510006)
0 引言
挥发性有机物(VOCs)是臭氧和二次有机颗粒物的重要前驱体, 其在大气化学反应过程中扮演着极其重要的角色, 对生态环境和人类健康造成巨大伤害[1-2]。催化燃烧法是处理VOCs 的常用方法,具有适应范围广、起燃温度低、污染小等优点。 在催化燃烧过程中,催化剂可显著降低有机物分解反应的活化能,同时富集反应物提高反应速率。因此,催化剂是影响催化燃烧法处理效果的关键因素之一。催化剂在化学反应里可改变反应物化学反应速率而不改变化学平衡, 且本身的质量和化学性质在化学反应前后均没有发生改变的物质。 过渡金属(Mn,Co,Ni 等)氧化物作为催化剂因含有多种价态的金属离子、 高浓度的亲电子氧化物物种和一定浓度的氧空位及廉价易得的优势被广泛用于催化氧化去除VOCs[1,3,4]。
除过渡金属种类外, 催化剂的结构和活性位点分散度也是影响催化燃烧法的关键因素。 水滑石(LDH)是一种具有层状结构的阴离子型多金属化合物, 其二维层状结构被认为是设计吸附剂和催化剂的优选模板[5]。MO 等[6]和CASTAO 等[7]以水滑石为前驱体制备出CoMnAl 基混合金属氧化物(CoMnAl-MMO),发现其可有效催化分解有机物,并详细分析了CoMnAl-MMO 的催化氧化机理[8]。
有关CoMnAl-MMO 的研究以往大多集中在金属比例及合成方法对材料催化活性的影响上, 但其与单金属氧化物的催化活性在统一系统中并未有过对比评价,CoMnAl-MMO 以水滑石为前驱体合成的层状混合金属氧化物的结构优势与催化活性的关系也尚未明确。 对此, 通过制备单金属氧化物Co3O4,Mn3O4及CoAl-MMO,CoMnAl-MMO 等催化剂,以探索分析其活性与结构的关系。
1 材料与方法
1.1 试剂
实验所用试剂:甲苯,Co(NO3)2·6H2O,Mn(NO3)2·6H2O,Al(NO3)2·9H2O,KMnO4,CO(NH2)2及乙醇均为分析纯。
1.2 实验过程
1.2.1 样品的制备
采用静态尿素法制备出CoMnAl-LDH[7], 其中n(Co)∶n(Mn)∶n(Al)为4 ∶1 ∶1。再将制备的CoMnAl-LDH 在温度为500 ℃条件下煅烧5 h, 得到CoMnAl-MMO。
将质量为2.91 g Co(NO3)2·6H2O,质量为1.876 g Al(NO3)2·9H2O,质量为3.754 g CO(NH2)2溶于150 mL 水中,超声10 min 后将其倒入300 mL 高压反应釜中,在温度为105 ℃条件下反应48 h 后,再经离心、清洗、干燥、研磨、过筛后得到CoAl-LDH 备用,再将其在温度为500 ℃条件下煅烧5 h 后得到CoAl-MMO。
称取质量为2.91 g 的Co(NO3)2·6H2O 和质量为3.76 g 的CO(NH2)2将其溶于150 mL 水中后倒入高压反应釜中,在温度为105℃条件下水解产生Co(OH)2,经离心、清洗、干燥、研磨、过筛后于马弗炉中,在温度为500 ℃条件下煅烧5 h 得到Co3O4。
Mn 的氧化物包括Mn3O4,Mn2O3,MnO23 种 类型,根据文献[9]研究,选取催化性能较强的Mn3O4作为代表。称取质量为2.0 g 的KMnO4倒入烧杯中,加入120 mL 质量分数为60%乙醇溶液, 经超声后得到均相溶液于高压反应釜中,在温度为120 ℃条件下反应8 h,清洗后干燥、研磨、过筛,即得到Mn3O4[10]。
1.2.2 材料表征
(1)材料形貌(SEM):采用Car Zeis 公司EVO LS10 型扫面电镜(工作电压为20 kV)观察;
(2)材料晶型结构:采用PANalytical B.V.公司X射线衍射仪(Axios Pw440 仪器,功率为4 kV,铑靶端X 光管)进行分析;
(3)材料活性物质价态:采用ULVAC-PHI 公司PHI X-tool 的X 射线光电子能谱(XPS)测定分析,以C 1S 的结合能为284.6 eV 作为校准;
(4)程序升温还原(H2-TPR)、程序升温脱附(O2-TPD):采用美国麦可莫瑞提公司的全自动程序升温化学吸附仪(AutoChemII 2920)检测分析。
1.2.3 催化活性实验
采用固定床反应装置对材料进行催化活性评价[11]。 先将100 mg 的催化材料与100 mg 的石英砂混合后,填充在反应器的等温区,再将甲苯蒸汽和空气在混气罐中混合均匀, 保持甲苯质量浓度为3.76 g/m3,气体流速为100 mL/min,空速为20 000 mL/gh;采用气相色谱(GC)检测甲苯浓度。
2 结果与分析
2.1 材料的表征
2.1.1 微观形貌
CoMnAl-LDH,CoMnAl-MMO,CoAl-LDH,CoAl-MMO,Co3O4,Mn3O4的SEM 图像见图1。 由图1 可以看出, 实验制备的CoMnAl-LDH,CoMnAl-MMO 表面呈明显的片状结构,片层较大较薄,且为有规则的堆积成花的样式。 CoAl-LDH,CoAl-MMO 表面则呈较小的片状结构,部分呈规则的六边形。 Co3O4的片状结构表面具有较多的孔隙和细小颗粒。 Mn3O4表面则呈粒状,颗粒较为蓬松且分布较多的孔隙。

图1 CoMnAl-LDH,CoMnAl-MMO,CoAl-LDH,CoAl-MMO,Co3O4,Mn3O4 的SEM 图像
2.1.2 物相
CoMnAl-LDH 和CoMnAl-MMO,CoAl-LDH 和CoAl-MMO,Co3O4和Mn3O4的XRD 谱图像,见图2。由图2(a)可以看出,CoMnAl-LDH 和CoAl-LDH 衍射峰均呈明显的层状结构特征,且衍射峰较强、基线较平稳,说明品相单一、结晶度较好。 煅烧后得到尖晶石结构,但基线高且不平稳、峰宽。 推断原因是由于金属离子的取代作用,形成晶格缺陷,破坏了原子平衡,使晶格发生扭曲。钴氧化物的尖晶石结构缺陷有利于表面氧空穴的产生, 而氧空穴有利于加速氧分子的吸附和分离,形成活性亲电氧物种,使材料表现出低温还原性[6,12]。由图2(c)中可以看出,Co3O4和Mn3O4表现出良好的结晶度,其衍射特征峰强度强、基线平稳。
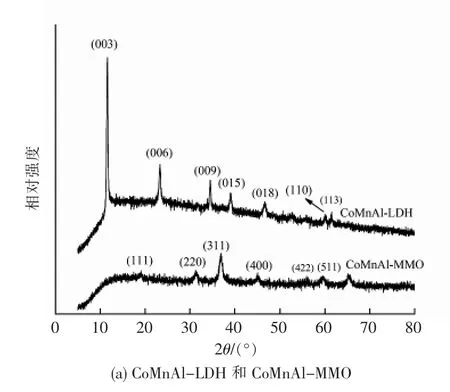
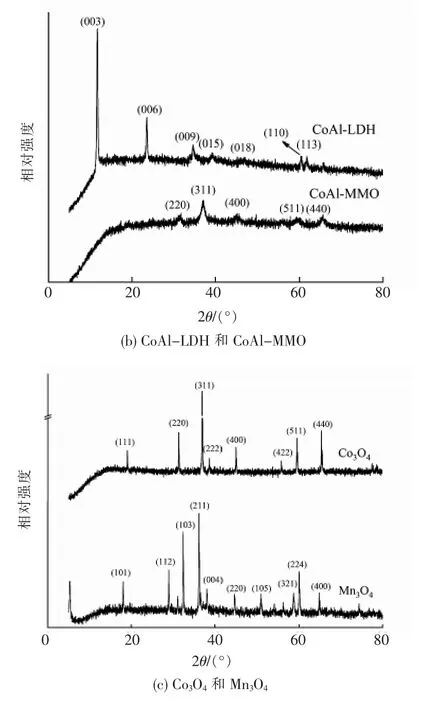
图2 CoMnAl-LDH 和CoMnAl-MMO,CoAl-LDH 和CoAl-MMO,Co3O4 和Mn3O4 的XRD 谱图像

2.1.3 表面元素金属氧化物中Co(a),Mn(b)的XPS 图像,见图3。由图3 可以看出, 通过对Co 2p1/2进行分峰, 发现CoMnAl-MMO,CoAl-MMO,Co3O4中均含有Co2+和Co3+。 但是相比较Co3O4,CoMnAl-MMO 和CoAl-MMO 中Co 2p3/2和Co 2p1/2的结合能较高,推断原因是由于多金属氧化物中Co 与Mn/Al 形成了固溶体。此外,相比较CoAl-MMO,CoMnAl-MMO 中的Co 峰更宽化。推断原因是由于受到锰的影响,其晶格发生扭曲,影响了钴的电子分布。 另有研究表明,在含钴材料催化氧化反应中, 活性点位主要为Co3+,Co2+几乎不活跃[15]。 通过分析发现,3 种氧化物材料中Co3+含量排序为:CoAl-MMO > CoMnAl-MMO > Co3O4。由此推测,CoAl-MMO 和CoMnAl-MMO 的Co3+含量较高是由于其催化活性明显优于Co3O4。
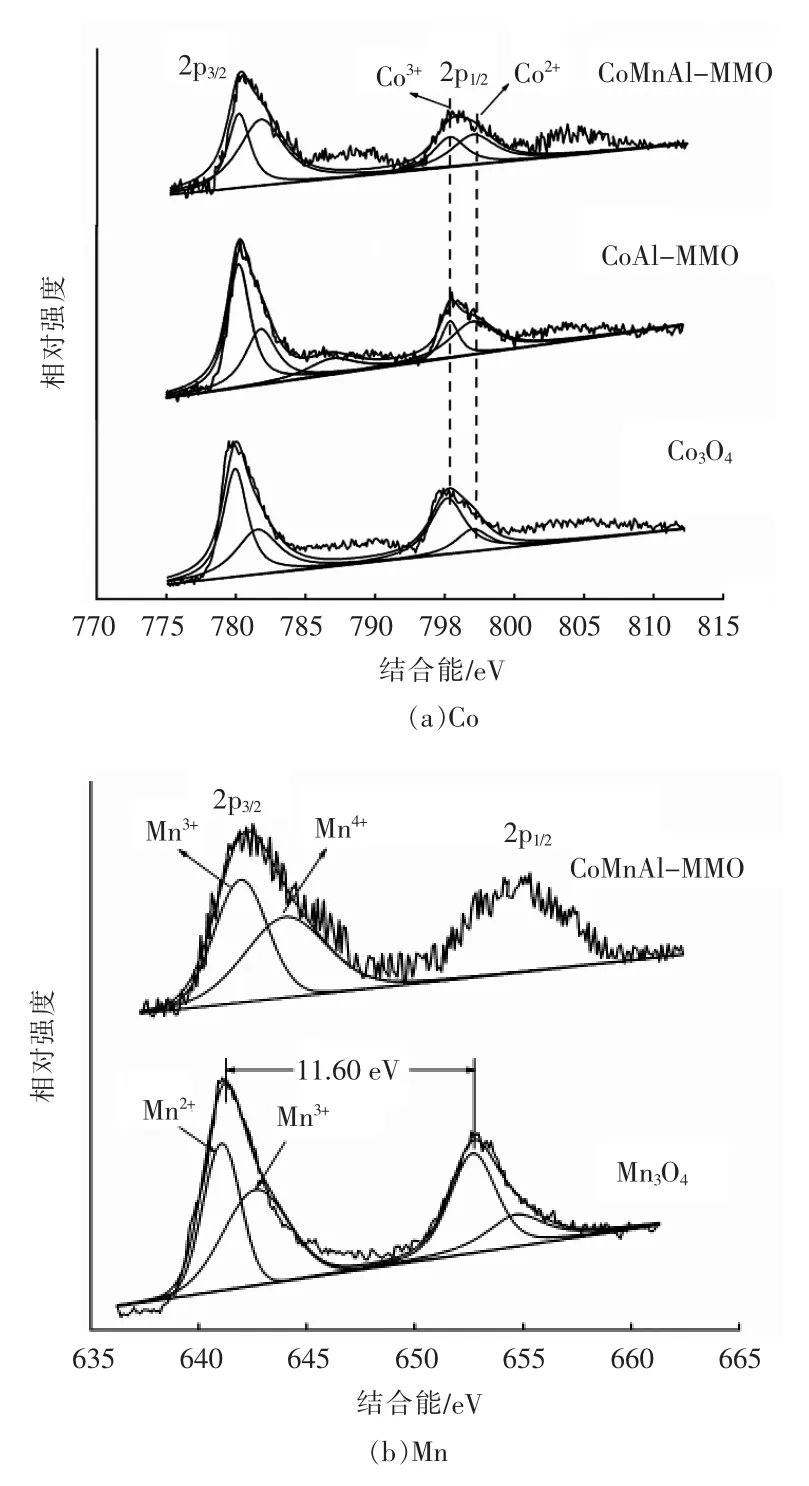
图3 金属氧化物中Co,Mn 的XPS 图像
因高自旋的Mn3+受Jahn-Teller 效应影响,材料中则同时存在Mn3+和Mn4+[16]。 通过对Mn 2p3/2进行分峰,发现CoMnAl-MMO 中含有Mn3+(642.0 eV)和Mn4+(643.9 eV),Mn3O4中则同时存在Mn2+(641.0 eV)和Mn3+(642.7 eV)。研究表明,高价态的锰在低温条件下更易被还原, 更有利于晶格氧与有机物发生反应[17]。 因此,Mn3+和Mn4+在催化氧化甲苯过程中发挥着重要作用。
综上分析,CoAl-MMO 的催化活性明显优于Co3O4的主要原因是由于Co3+含量的增加。 CoMnAl-MMO 的催化活性优于CoAl-MMO 的主要原因是由于Mn3+和Mn4+。 此外,不同元素掺杂形成的固溶体结构使尖晶石晶格扭曲产生更多的表面氧空穴,也在一定程度上增强了CoAl-MMO 和CoMnAl-MMO的催化活性。
2.1.3 还原性能
钴锰氧化物的H2-TPR 谱图像, 见图4。CoMnAl-MMO 在温度为310 ℃处的还原峰应为Co3O4和Mn4+的还原峰[18-20];在温度为459 ℃处为固溶体中锰的还原峰, 包括Mn4+还原成Mn3+-Mn2+,Mn3+-Mn2+还原成Mn2+[17]。 在温度约700 ℃左右为CoAl2O4固溶体中CoO 的还原峰。 该峰也出现在CoAl-MMO 的H2-TPR 谱图中[18-19]。CoAl-MMO 在温度分别为320 ℃,347 ℃的峰应为Co3O4→CoO→Co的2 步还原峰[18-19]。Co3O4在温度为300 ~410 ℃范围内也出现了该还原反应H2消耗峰。 对比CoMnAl-MMO 和CoAl-MMO,Co3O4的H2-TPR 图谱, 发现由于固溶体结构出现和锰的加入, 使还原峰向低温区移动,峰强度增强,说明CoMnAl-MMO 在低温区的还原性要强于CoAl-MMO 和Co3O4。Mn3O4在温度分别为267,309,371 ℃的峰分别为四面体Mn3+、 八面体长Mn3+~ 八面体短Mn3+或八面体长Mn3+、四面体Mn3+~八面体短Mn3+的还原峰[3]。说明Mn3O4在低温区的还原性能较强。
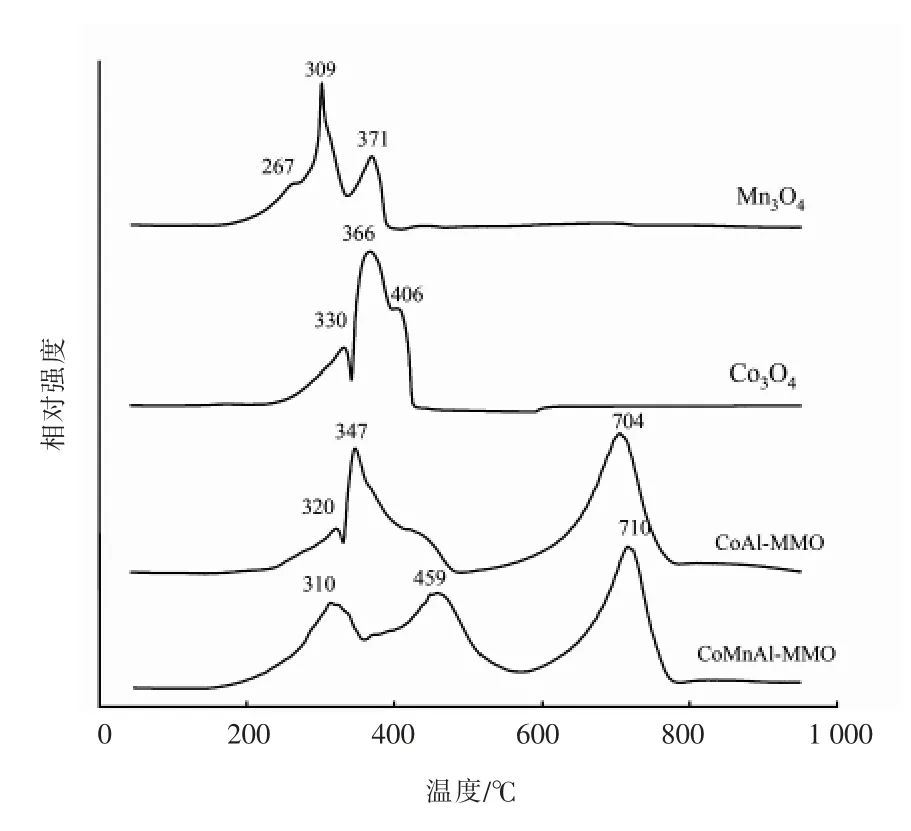
图4 钴锰氧化物的H2-TPR 谱图像
2.1.4 氧化性能
钴锰氧化物的O2-TPR 谱图像,见图5。 温度在50 ~200 ℃之间的峰属于Oα峰,为很弱的表面化学吸附氧脱附(O2-和O22-);温度在200 ~400 ℃之间的峰属于Oβ峰,为表面或羟基氧(O2-)脱附;温度在400 ℃以上的峰属于表面晶格氧脱附(晶格O2-)[21-22]。温度在50 ~400 ℃之间脱附的氧物种一般被认为是催化氧化的主要活性分子[22]。 由图5 可以看出,CoMnAl-MMO 和CoAl-MMO,Mn3O4均含有大量的Oα和Oβ。 CoAl-MMO 与Co3O4相比,在低温处显示更明显的氧脱附。 推断原因是由于铝的加入使尖晶石结构发生扭曲产生大量的氧空位和晶格空缺,有利于提高材料对氧物种的吸附。 对比Co3O4和CoMnAl-MMO,CoMnAl-MMO 当温度分别在200 与125 ℃左右的脱附峰相互叠加, 使其脱附量明显增强。 说明锰的加入增加了CoMnAl-MMO 的氧脱附量。 此外,Mn3O4的Oα峰峰型最强,说明其表面含有大量的化学吸附氧,具备较强的催化活性。
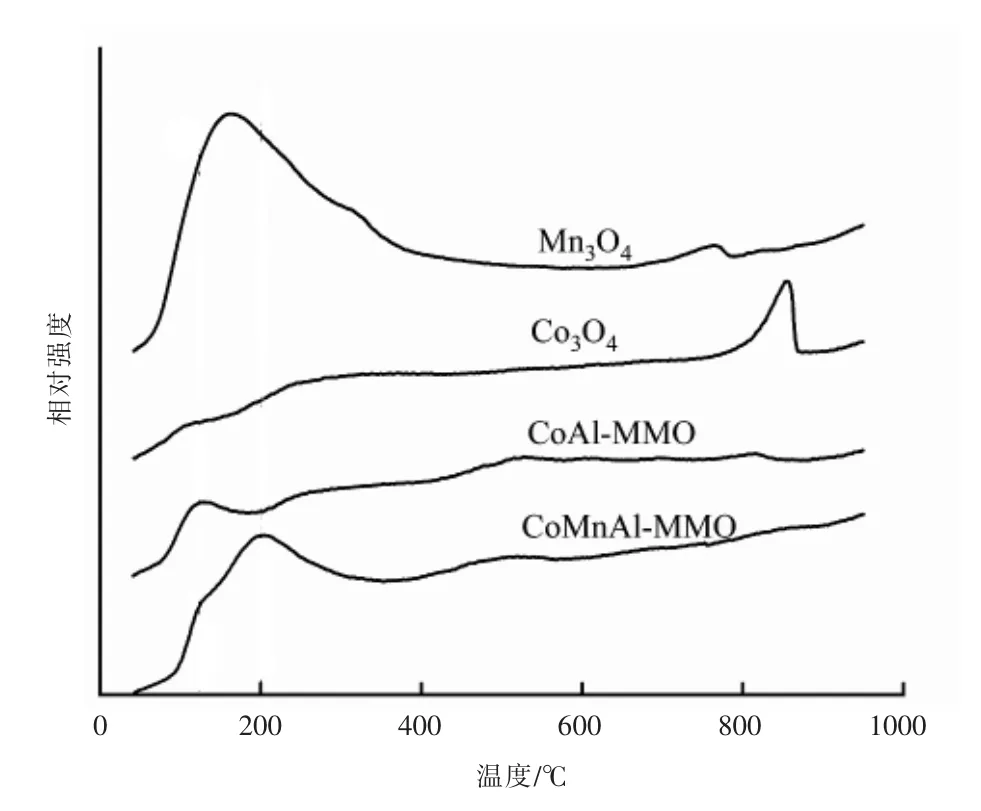
图5 钴锰氧化物的O2-TPD 谱图像
2.2 材料催化氧化甲苯的性能及机理
钴锰氧化物催化降解甲苯的性能见图6。 在低于200 ℃范围内所有催化剂对甲苯的转化率变化缓慢。 由图6 可以看出,CoMnAl-MMO,CoAl-MMO,Mn3O4对甲苯的催化氧化作用随温度的升高而增强,甲苯转化率也迅速升高。 其中CoMnAl-MMO 和Mn3O4对甲苯氧化表现出较高的催化活性, 当反应温度分别为232 和250 ℃时,CoMnAl-MMO 对甲苯的催化转化率分别为50%和90%;Mn3O4对应的反应温度分别为235 ℃(催化转化率为50%),258 ℃(催化转化率为90%)。 Co3O4对甲苯的催化氧化作用较弱, 反应温度为290 ℃。 同属于尖晶石结构的CoMnAl-MMO,CoAl-MMO,Co3O4三者的催化活性相差较大。 通过XRD 分析,由于锰和铝的晶格置换作用,CoMnAl-MMO 和CoAl-MMO 的晶格发生扭曲。尤其是锰的Jahn-Teller 效应,使分子的几何构型发生畸变,产生更多的结构缺陷。这也是在只掺杂少量锰的前提下,CoMnAl-MMO 的催化活性在温度为230 ℃后优于Mn3O4的原因之一。 其次,Al3+置换了Co3+,使晶格常数变小,阴离子空穴浓度增加。
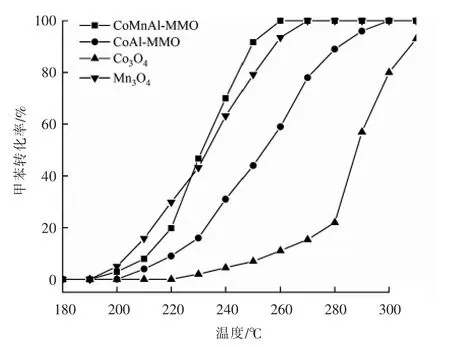
图6 钴锰氧化物催化降解甲苯的性能
GABROVSKA[13]认为在氧化还原过程中,Co2+与Al3+毗邻的阴离子空穴(°Al3+)反应见公式1:
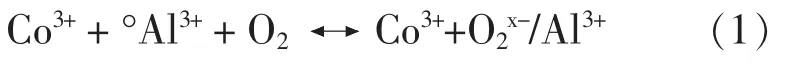
由公式(1)可以看出,该反应有利于Co3+/Co2+和O2/O2x-,从而产生更多的O2-/O-活性组分。 根据电中性原理,含有锰的催化材料中高价态锰(Mn4+)有利于表面吸附:O2/O2-的增加,Mn3+可产生氧空穴促进Olatt 的迁移。 因此,Mn4+/Mn3+之间的转化促进了Osurf 和Olatt 产生。钴和锰之间的协同作用。进一步加强了氧化还原过程中的电子转移。 故CoMnAl-MMO 相对于其他CoMn 氧化物显示出更强的催化活性。 钴和锰之间的协同作用见公式2。
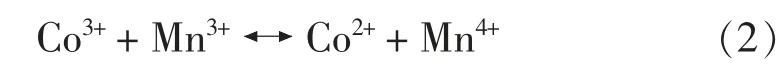
3 结论
(1) 相比CoAl-MMO 和Mn3O4,CoMnAl-MMO显示较强的催化氧化甲苯的活性,CoMnAl-MMO 对甲苯的催化转化率分别为50%和90%时的反应温度分别为232 和250 ℃。
(2)Co3+和Mn3+/Mn4+有利于钴锰氧化物催化氧化甲苯。 钴锰的协同作用加速了氧化还原过程中的电子转移。此外,多金属掺杂使晶体具备更多的结构缺陷,使晶格发生扭曲,有利于Osurf 空穴的产生,加快氧物种在催化剂的内部及表面的流动传输,使由水滑石衍生的CoMnAl-MMO 在低温区表现出略强的氧化还原性能。
