环状RNA circ_0036176结合miR-218-5p发挥抑制心肌纤维化的作用
2022-02-28黄智琪严钰敏郭继深朱杰宁方咸宏徐金东单志新
黄智琪,严钰敏,郭 晶,郭继深,朱杰宁,方咸宏,徐金东,单志新,
(1.华南理工大学生物科学与工程学院,广东广州 510006;2.南方医科大学药学院,广东广州 510515;3.华南理工大学医学院,广东广州 510006;4.南方医科大学第二临床医学院,广东广州 510280;5.广东省心血管病研究所,广东省人民医院//广东省医学科学院,广东广州 510080)
目前,心血管疾病已占所有疾病死因的31%,是全球患者死亡的主要原因之一。心肌纤维化是导致心力衰竭的主要病理基础,是公认的导致高发病率和高死亡率的病因[1]。心肌纤维化是病理性细胞外基质(ECM)重塑的过程[2]。最初的心肌纤维化可促进心肌伤口愈合和组织再生,细胞外基质沉积可起到保护作用,但持续性的细胞外基质沉积,尤其是I 型胶原分泌,导致基质组成和质量异常,进而心肌功能受损[1-2]。已知多种疾病都会促进心肌纤维化的发生,如高血压性心脏病、糖尿病性肥厚型心肌病和特发性扩张型心肌病[2-3],而心肌梗死后也常会引起心肌纤维化疤痕。环状RNA经反向剪接而成,相对于线性形式,circRNA 在细胞中有着丰富且稳定的存在[4-5]。越来越多的证据表明circRNA 参与包括心肌纤维化[6-7]、心肌缺血/再灌注损伤[8-9]、心力衰竭[10-11]及其他多种心血管疾病过程[12]。因此,深入研究circRNAs 调节心肌纤维化的作用机制,可为心力衰竭的治疗研究提供科学资料,具有重要意义。我们已证实小鼠源性的circRNA_005647 可吸附miR-27b-3p,并解除miR-27b-3p对靶基因PPAR-γ的抑制作用,进而发挥抑制心肌纤维化的作用[13]。有趣的是,我们发现与circRNA_005647 同源的人circ_0036176 在心衰病人心肌组织中表达亦上调,但circ_0036176 对心肌纤维化的调节作用尚未见报道。本研究旨在初步探讨circ_0036176 在心肌纤维化中的生物学功能,并了解其发挥作用的分子机制,或可为心肌病的临床治疗提供潜在干预靶点。
1 材料与方法
1.1 组织标本
利用心衰患者和健康器官捐献者的心肌组织进行circ_0036176 和宿主基因Myo9a 表达的RTqPCR 检测。本文所涉及的临床样本实验均经广东省人民医院伦理委员会批准[批准号No.GDREC20 19238H(R1)],所有患者均签署知情同意书,相关心肌组织标本均由广东省心血管病研究所进行提供,病例资料信息同以往报道[14]。
1.2 动 物
SPF 级出生日龄1-3 d 的C57BL/6 乳小鼠,雌雄不限,由广州中医药大学的实验动物中心进行繁育与提供,乳小鼠的生产许可证号为SCXK(粤)2013-0034。
1.3 主要试剂
特级澳洲胎牛血清与DMEM/F12 细胞培养基(BioInd);miR-218-5p、-100-5p、-27b-3p 等mimic(广州锐博);转染试剂Oligofectamine(Invitrogen);逆转录试剂盒(TaKaRa);RNase R(ribonuclease R)(广州吉赛生物);放线菌素D(生工有限公司);RIPA 裂解液(碧云天);SDS-PAGE 凝胶配制试剂盒(碧云天);抗GAPDH 抗体、抗TGF-β1抗体(Protein Technology);抗Ⅰ型胶原蛋白α1 链(type Ⅰcollagen α1,COL1A1)、抗Ⅲ型胶原蛋白α1 链(typeⅢcollagen α1,COL3A1)抗体(Invitrogen);抗α 平滑肌肌动蛋白(α-smooth muscle actin,α-SMA)抗体(Abcam);BCA 蛋白定量试剂盒(Thermo);蛋白Marker(Fermentas);ECL 发光液(Millipore);PVDF膜(What-man);血管紧张素Ⅱ(Sigma);其他生化试剂均为进口分装或国产分析纯。
1.4 主要方法
1.4.1 Masson 三色染色 从浸泡于冰生理盐水中的人心肌组织标本中切取出大小适宜的组织块,放置在多聚甲醛中做固定处理,后将固定好的组织块进行脱水、透明、浸蜡和石蜡包埋操作,静置凝固后进行连续性切片,将切片厚度控制在4 μm。获得组织切片后,利用Masson 染色试剂盒染色,最终将切片标本置于显微镜下,观察健康组与心衰病人组之间胶原纤维的沉积差异,并对其进行拍照。
1.4.2 人心房肌成纤维细胞的原代分离、培养 从手术室中取得的左心耳用冷PBS清洗干净,用灭菌的剪刀和镊子清除脂肪及筋膜后将心耳组织剪碎,参照我们已报道的方法进行HAF 的原代分离和培养[14]。本文实验使用的人心房肌成纤维细胞(human atrial fibroblasts,HAFs)为第3~5代。
1.4.3 小鼠心肌成纤维细胞的原代分离、培养、处理 基于已有报道的方法[15]并进行适当优化,将小鼠心肌成纤维细胞的进行原代分离、培养。准备适龄的SPF 级别的C57BL/6 小鼠,利用眼科剪从乳鼠体内取出完整心脏,随后立即对组织进行适当修剪与破碎,添加浓度为2×104U/L DNA 酶和2.5 g/L 胰酶的混合液,在37 ℃的条件下进行反复数次酶消化,随后把分离得到小鼠心肌成纤维细胞(mouse cardiac fibroblasts,mCFs)做离心处理,并利用含有10%血清浓度(100 mL 完全培养基中含10 mL 胎牛血清)的DMEM培养基对离心获得的细胞沉淀进行轻柔的重悬,而后将其置于洁净无菌的培养瓶中。当小鼠成纤维细胞的接触密度增长到接近90%的时候,即可进行传代处理,细胞实验中所用的mCFs代数均为P2。
1.4.4 Circ_0036176 重组腺病毒的构建和包装根据人circ_0036176 模板DNA 序列和腺病毒穿梭质粒pAd-Track-cmv 多克隆位点序列,设计合成引物,通过PCR扩增得到circ_0036176模板的DNA插入片段。参照已报道方法[12],将circ_0036176 模板DNA利用定向插入的方式,在pAd-Track-cmv载体上实现重组构建。并进一步将pAd-Track-cmvcirc_0036176 与pAd-Easy-I 在BJ5183E.Coli中 进行重组。而后,利用PacI 酶将重组circ_0036176 腺病毒载体进行酶切,利用转染试剂将其转染至293T细胞中,给予体积分数5%血清的DMEM 培养基并于37 ℃恒温下培养,待绿色荧光蛋白显著表达则提示该重组腺病毒完成包装,并做进一步的病毒扩增。实验时以rAd-GFP 作为对照组腺病毒(circ_0036176和rAd-GFP的MOI均是5)。
1.4.5 RT-qPCR 利用Trizol 法提取CFs 的总RNA,而后取800 ng,将其与5×逆转录试剂进行充分混合,同时使用Oligo(dT)15和random primers 进行RNA 的逆转录,获得cDNA。选择GAPDH 作内参照,用相应的引物检测TGF-β1 以及纤维化相关基因的mRNA 表达水平。在ViiA 7 Quantitative PCR System(Applied Biosystems)进 行PCR 反 应后,TGF-β1 和纤维化相关基因的相对表达程度用2-ΔΔCt法进行计算。所涉及引物均经Invitrogen 进行合成,具体序列见图1。
1.4.6 Western blot 取适量的1×PBS 对处理后的成纤维细胞进行清洗,将蛋白裂解液分别均匀滴加入每个板孔中,静置于冰上10 min,轻轻刮取、裂解细胞,用移液枪收集裂解液,于10 000×g的转速下4 ℃离心13 min 使细胞沉淀聚集,随后分装上层澄清蛋白裂解液,沉淀弃去。蛋白质定量18 μg,加入等量的4×SDS-PAGE 缓冲液,99 ℃金属浴加热10 min,使蛋白质完全变性。取样品在恒压条件下进行SDS-PAGE 凝胶电泳,在恒流条件下进行PVDF膜转膜,在室温环境下利用5%脱脂牛奶进行封闭处理。按照蛋白对应的不同位置,裁剪PVDF 膜条带,并分别利用相应的特异性抗体[COL1A1(1:2 000)、COL3A1(1:2 000)、TGF-β1(1:2 000)、α-SMA(1:2 000)]在4 ℃环境下缓慢均匀孵育过夜后将其取出,于常温条件下分别与对应的二抗稀释液充分孵育1 h。最后利用ECL 发光试剂盒对目的蛋白进行显影处理。本文均使用GAPDH(1:5 000)作为内参,借助ImageJ 对其灰度值做分析处理,对各目的蛋白进行表达情况分析。
1.4.7 双萤光素酶报告实验 利用特异的引物扩增出circ_0036176 碱基片段,并将扩增得到的片段通过定向克隆的方式,连接至pGL3-promoter 载体上,构建双萤光素酶报告质粒pGL3-circ_0036176。将HEK293 细胞均匀接种于24 孔板中,稳定培养24 h 后,利用Lipofectamine 2000 对400 ng重组萤光素酶报告质粒、0.9 ng pRL-TK(可在细胞中表达出海肾萤光素酶,作为内参照质粒)、100 nM miRNA 进行包裹,20 min后分别共转染至细胞,恒温培养24 h。测定萤火虫萤光(Firefly luciferase,FL)和海肾萤光(Ranilla luciferase,RL)强度,由FL/ RL 比值推断circ_0036176 与不同微小RNA间的结合能力的强弱。

表1 PCR引物序列Table.1 The sequences of the primers for PCR
1.5 统计学处理
采用Image J 和GraphPad Prism8 分析与作图,用SPSS 21.0 进行统计分析。实验数据用均数±标准差表示,当两组间作比较时,采用t检验;当多组间作比较时,采用单因素方差分析;在组间两两做比较时,则用Bonferroni 校正的t检验。当P<0.05时,则为数据间的差异具有统计学意义。
2 结果
2.1 Circ_0036176在心衰心肌组织中表达增加
Masson 染色结果显示心衰病人心肌组织中的微血管外周及细胞间质胶原沉积,较健康人组有增加趋势,并出现了较高程度的心肌纤维化(P<0.001;图1A)。RT-qPCR 结果显示,circ_0036176在心力衰竭患者心肌组织中表达上调(P<0.05),而其宿主基因Myo9a 的表达变化不明显(图1B)。在Ang-Ⅱ处理的HAFs 心肌纤维化的细胞模型中,发现circ_0036176 和Myo9a 的表达一致性降低(P<0.01;图1C)。分别以人cDNA 和基因组DNA 为模板,PCR结果显示,从人cDNA和gDNA中可PCR扩增到Myo9a 基因产物,而circ_0036176 只能从人cDNA 中扩增到(图1D)。通过DNA 测序的方法,在PCR 产物中成功检测出circ_0036176 的特异接头序(TATGACTCTGAGCCGTTATTTTACCAAGAA)(图1E)。

图1 Circ_0036176在心衰心肌组织中表达增加Fig.1 Upregulation of circ_0036176 in the myocardium of patients with heart failure
2.2 Circ_0036176 在AC16 心肌细胞中的分布及稳定性鉴定
定量PCR 和FISH 检测结果显示,circ_0036176除了富集于细胞质中,在细胞核内也有分布(图2A、B)。RT-qPCR 结果显示,在放线菌素D 和RNase R 处理的人心肌细胞AC16 中后,Myo9a mRNA 水平相对于circ_0036176,发生较大程度的下降,此结果表明circ_0036176 具有较好的环状RNA典型的稳定性(P<0.05;图2C、D)。
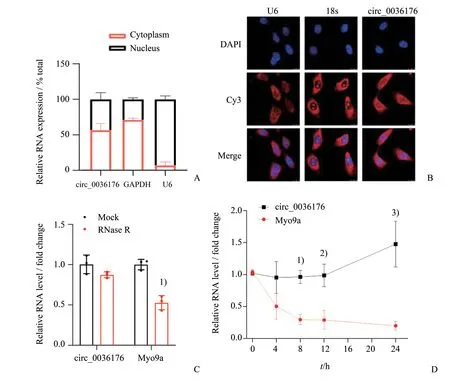
图2 Circ_0036176在AC16心肌细胞中的分布及RNA稳定性鉴定Fig.2 Cellular distribution and RNA stability of circ_0036176 in AC16 cardiomyocytes
2.3 Circ_0036176抑制心肌成纤维细胞纤维化表型
利用重组circ_0036176 腺病毒感染HAFs 24 h后,共表达的绿色荧光蛋白(GFP)提示circ_0036176 已在成纤维细胞中成功过表达(图3A)。通过RT-qPCR 对HAFs 中纤维化相关基因的表达进行检测,结果显示,过表达circ_0036176 后可起到明显的抑制作用(P<0.05;图3B)。进一步的,利用Western-blot,发现过表达circ_0036176 后,COL1A1、COL3A1、TGF-β1 和α-SMA 的蛋白表达同样受到了抑制(P<0.01;图3C)。

图3 circ_0036176在HAFs中具有下调纤维化相关基因表达的生物学功能Fig.3 Circ_0036176 inhibited the expression of fibrosis-related genes in HAFs
2.4 miR-218-5p 介导circ_0036176 抑制纤维化相关基因的表达
生物信息学预测(https://circinteractome.nia.nih.gov/index.html;http://starbase.sysu.edu.cn/starbase2/index.php)结果显示,circ_0036176 序列上有多个潜在的miRNAs 结合位点,并选择12个心肌中高表达miRNAs,分别为:miR-7-5p、miR-99b-5p、miR-100-5p、miR-154-3p、miR-200b-3p、miR-200c-3p、miR-218-5p、miR-330-3p、miR-429、miR-485-3p、miR-487a-3p 和miR-665 进 行鉴 定(图4A)。以miR-27b-3p 作为无关对照组,将上述miRNA 的模拟物和pGL3-circ_0036176 共转染至HEK293 细胞中进行检测。双萤光素酶报告基因实验提示,circ_0036176 与5 个微小RNA 发生较为明显的结合,其分别为miR-154-3p、miR-200b-3p、miR-218-5p、miR-487a-3p 和miR-665(P<0.05;图4B)。
进一步通过RAP 实验检测circ_0036176 与miR-154-3p、miR-200b-3p、miR-218-5p、miR-487a-3p 和miR-665 间结合能力的差异,利用circ_0036176 特异的生物素标记寡核苷酸探针下拉AC16 细胞中circ_0036176,提取RNA 检测circ_0036176 结合的相关miRNA 水平。RAP 实验发现circ_0036176 可有效地结合miR-218-5p 和miR-665,而结合miR-218-5p 量的相对更多(P<0.001;图4C)。
为了明确miR-218-5p 是否参与介导circ_0036176发挥抑制心肌纤维化表型的作用,将miR-218-5p 模拟物转染mCFs。Western blot 结果显示,与Scramble 组相比,过表达miR-218-5p 可以促进COL3A1、COL1A1、TGF-β1 和α-SMA 的表达(P<0.01;图4D)。而在mCFs 中同时过表达circ_0036176 和miR-218-5p,miR-218-5p 可有效逆转circ_0036176 对心肌纤维化相关基因表达的抑制作用(P<0.05;图4E)。

图4 circ_0036176以结合miR-218-5p方式抑制mCFs中纤维化相关基因表达Fig.4 Circ_0036176 inhibited fibrosis-related gene expression through sponging miR-218-5p in mCFs
3 讨论
本文中,我们发现circ_0036176 在心衰心肌中表达上调,但在经AngII 处理的HAFs 中表达下调。与之相似的,课题组前期工作中发现微小RNA miR-214-3p 在Ang-Ⅱ刺激下的小鼠整体模型与细胞模型中的表达出现相反趋势[16-17];KLHL20 是环形RNA circRNA_100395 的宿主基因,两者在发生纤维化的人心耳组织中表达一致降低,而在经过了Ang-Ⅱ处理的人心耳成纤维细胞中,两者的表达一致增加[15]。针对circ_0036176在AngⅡ刺激下的HAFs 中表达下调,而在心衰心肌中表达增加的现象,其可能的原因是,相对于原代分离出来的细胞,整体水平的心肌中存在多种类型的细胞和复杂的病理刺激因素,如氧化应激、急慢性炎症等,在这些因素综合作用,最终引起心衰心肌中circ_0036176 表达增加,但其中具体的调节机制仍有待深入探讨。
我们以往报道了小鼠源性circRNA_005647 具有抑制纤维化相关基因表达的作用[13],而本文证实来自同一宿主基因Myo9a 的人源性circ_0036176同样可以抑制心肌纤维化。我们既往已明确circRNA_005647可以特异吸附miR-27b-3p的方式发挥其生物学功能,尽管circRNA_005647 与人circ_0036176 的碱基序列比较相似(92.75%),但本文未发现circ_0036176 上具有miR-27b-3p 潜在的结合序列,提示同源的circRNA 即使有相同的生物学功能,但介导其生物学功能的分子机制可能不同。
在细胞RNA 的核质分离实验中,我们证实circ_0036176 主要存在于mCFs 细胞质中,这提示了此环形RNA 可能会通过经典的特异吸附微小RNA 途径来抑制心肌纤维化[18-19],因此,我们借助生物信息学对circ_0036176 上潜在的miRNA 结合位点进行分析,筛选了12 个可在心肌中高表达的miRNAs 进行鉴定。根据双萤光素酶实验的结果,发现circ_0036176 可与12 个潜在微小RNA 中的5个发生有效结合,其分别为miR-154-3p、miR-200b-3p、miR-218-5p、miR-487a-3p 和miR-665;而RAP 实验进一步确认circ_0036176 对miR-218-5p 的结合作用最显著。功能实验结果表明miR-218-5p 具有促进心肌纤维化相关基因表达的作用,并能有效逆转circ_0036176 起到的抑制作用。因此,微小RNA miR-218-5p 可介导环形RNA circ_0036176 行使抑制纤维化的功能。既往研究证实miR-218-5p 可通过靶向RE1 沉默转录因子(RE1-silencing transcription factor,REST)发挥促进心肌肥厚的作用[20];降低miR-218-5p 的表达可以有效减缓大鼠心肌损伤及纤维化的发生进程,同时可促进血管生成[21]。但对于本文中参与生物学功能调控的miR-218-5p下游中起主导作用的目的基因,仍需进一步探究。
综上,本文明确了人源circ_0036176 可特异吸附miR-218-5p 来抑制纤维化相关基因的表达,不同于同源的小鼠circRNA_005647 发挥抑制心肌纤维化作用的分子机制,目前尚未见有关同源circRNA 通过结合不同miRNA 发挥一致生物学作用的报道。本文尚存在一定局限性,还需在细胞水平明确circ_0036176 对mCFs 增殖和迁移的影响,并且我们拟继续在整体动物水平验证circ_0036176对心肌纤维化的抑制作用,并进一步明确其下游作用靶基因和相关信号通路。
