石墨烯作为硫载体在锂硫电池中的研究进展
2022-02-26张梦迪陈蓓吴明铂
张梦迪,陈蓓,吴明铂
重质油国家重点实验室,中国石油大学(华东)新能源学院,化学工程学院,山东 青岛 266580
1 引言
随着新能源的大规模开发与使用、电动汽车以及智能电网的快速发展,开发高性能、低成本的电化学储能体系势在必行1,2。锂硫电池理论能量密度高达2600 Wh·kg-1,是目前商业化锂离子电池能量密度的5倍以上。而且,硫还具有储量丰富、成本低廉、无毒的优点。因此,锂硫电池被认为是极具发展潜力与应用前景的新一代电池体系3,4。
锂硫电池的工作原理如图1a所示5。在放电过程中,负极锂失去电子生成锂离子,正极硫接收通过外电路传递来的电子并与锂离子结合生成Li2S。充电过程与之相反。实际上,在充放电过程中,锂硫电池正极经历了一个复杂的多电子反应过程。如图1b所示,放电时,环状的S8分子首先开环并与Li+结合生成可溶性的多硫化锂(Li2Sx,4 ≤x≤ 8),然后继续被还原生成固态的Li2S2和Li2S。该“固-液-固”转化过程为正极带来了诸多挑战:(1)硫及其放电产物Li2S2/Li2S的电子绝缘性导致活性物质利用率较低6,7;(2)由硫生成Li2S的过程伴随着80%的体积膨胀,严重损害了电极结构稳定性8,9;(3)中间产物多硫化锂易溶于电解液并在正负极之间来回往复,即发生所谓的“穿梭效应”,导致正负极活性物质损失、电池容量衰减以及库仑效率降低10-12。
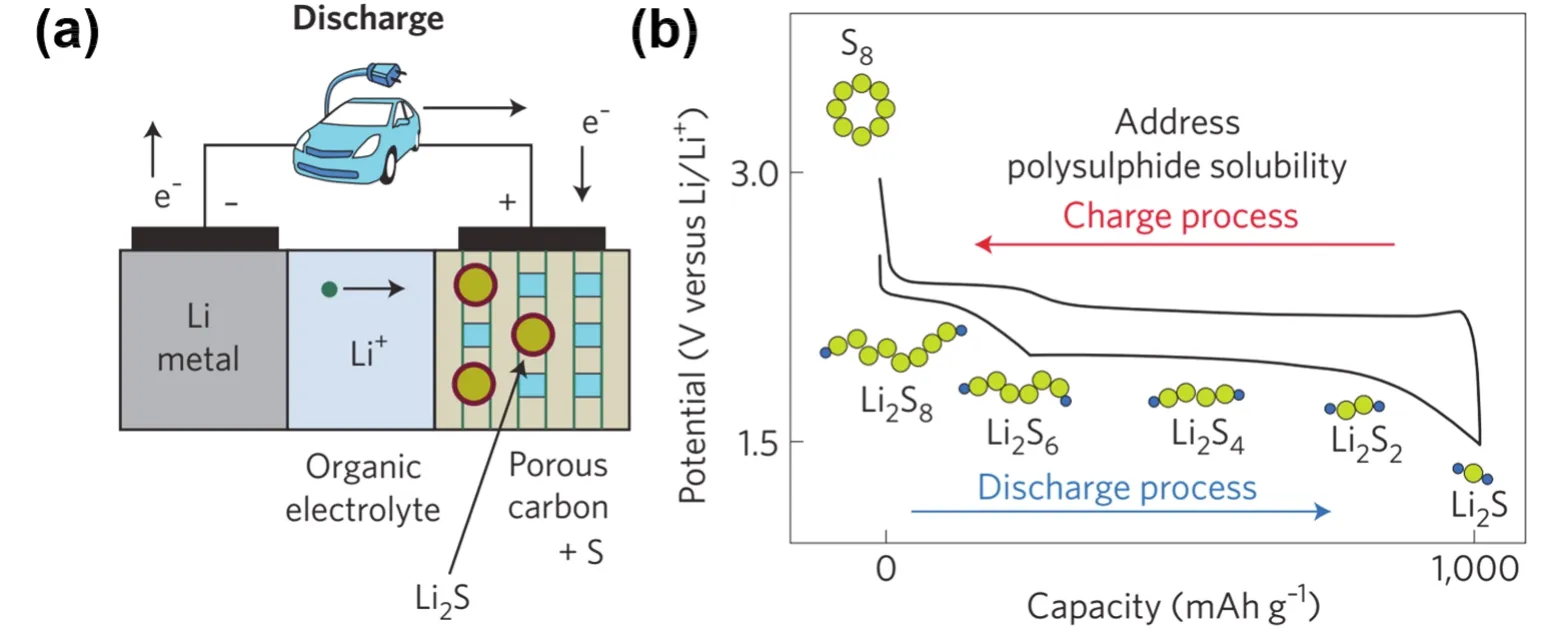
图1 锂硫电池的(a)工作原理图和(b)正极充放电过程示意图5Fig.1 (a)Schematic diagram and (b)charge/discharge process of lithium-sulfur battery5.
优化锂硫电池正极最常用的策略是将碳基材料作为活性物质硫的载体13-15。理想的硫载体材料应具备以下特点:(1)具有高的比表面积和发达的孔隙结构,能够为硫及其放电产物提供充足的储存空间,并且为锂离子提供快速传输通道;(2)具有优异的导电性,能够为活性物质提供良好的电化学接触;(3)具有优异的结构稳定性,能够缓解充放电过程中的电极结构应变;(4)对多硫化锂具有强的吸附作用以及催化转化作用,加快正极氧化还原反应动力学,抑制穿梭效应。
石墨烯,作为一种由单层sp2杂化碳原子构成的二维碳材料,具有高的理论比表面积(2630 m2·g-1)、极高的本征载流子迁移率(200000 cm2·V·s-1)以及优异的柔韧性和机械稳定性16,17。因此,石墨烯作为硫载体在锂硫电池正极中具有极大的应用潜力18-20。遗憾的是,石墨烯片层的少孔、开放结构并不利于约束循环过程中多硫化锂的扩散,也就无法有效缓解穿梭效应。早期,研究者们主要通过对石墨烯进行三维结构设计、表面化学修饰以及与多孔碳材料复合等策略来解决这一难题。例如,Wang等21将碳黑纳米颗粒分散在被轻度氧化的石墨烯表面。同时,通过化学反应沉积策略得到聚乙二醇包覆的亚微米级硫颗粒。最终,将两者混合分散即可得到石墨烯包覆硫颗粒的复合材料。该材料作为锂硫电池正极,在0.5C电流密度下,第10圈到第100圈的容量衰减率仅为9%。Ji等22利用化学反应沉积方法将硫固定在二维氧化石墨烯上,得到了氧化石墨烯-硫复合材料(GO-S)。GO表面丰富的含氧官能团能够有效吸附硫物种,限制多硫化物的溶解,从而使得GO-S正极具有较好的电化学性能。Yang等23通过水热和化学活化方法在石墨烯表面均匀包覆了多孔碳层,其丰富的孔道作为多硫化锂的“蓄液池”,抑制了多硫化锂的扩散,从而提高了循环性能。石墨烯另一突出的优点是可以作为生长基底诱导各种高电化学活性材料在其表面成核生长24-27。最近,各种石墨烯/金属化合物复合材料被作为硫载体应用于锂硫电池正极,其中的极性金属化合物能够有效吸附多硫化锂并加快其转化反应速率,从而进一步提升锂硫电池的电化学性能28-30。另外,石墨烯优异的柔韧性令其在柔性锂硫电池应用中也得到了广泛关注与研究31,32。
本文主要综述了近年来三维石墨烯、表面化学修饰的石墨烯、石墨烯基复合材料以及石墨烯基柔性材料作为硫载体在锂硫电池正极中的研究进展,并展望了石墨烯载体在锂硫电池正极中的发展趋势。
2 石墨烯作为硫载体在锂硫电池中的研究进展
2.1 三维石墨烯
如前所述,石墨烯开放的二维平面结构无法有效约束多硫化锂的扩散,会导致锂硫电池容量快速衰退。而且,石墨烯片层之间的π-π相互作用令石墨烯片相互堆叠,导致其实际比表面积大大减小,无法完全发挥出性能优势。研究表明,将片层石墨烯组装成三维多孔结构,能够为硫及其放电产物提供相对封闭的储存空间,一定程度上可以抑制穿梭效应,改善锂硫电池的电化学性能。清华大学魏飞和张强教授团队在这方面做了很多代表性工作。例如,他们利用真空辅助热膨胀方法制备了分级多孔石墨烯,石墨烯片层之间松散堆叠弯曲形成相互连通的三维大孔结构,比表面积为434 m2·g-1。然后,将硫封装在这些多孔导电网络中得到了多孔石墨烯/硫复合材料,在0.5C和10C下能够分别表现出1068和543 mAh·g-1的倍率容量33。他们还利用煅烧过后的介孔层状双金属氢氧化物(Mg-Al LDH)作为模板,采用化学气相沉积(CVD)法在其表面沉积石墨烯层,其中部分碳被沉积在LDH的介孔中形成突起,将模板去除后即可得到被大量突起分隔的两片未堆叠石墨烯(DTG),比表面积高达1628 m2·g-1。这些片层之间介孔尺寸的突起能够封装多硫化锂,抑制穿梭效应。因此,DTG与硫的复合材料(DTG/S)表现出优良的倍率性能,在5C和10C的大电流密度下,初始比容量分别高达1034和734 mAh·g-1,循环1000圈后仍然保持530和380 mAh·g-1(图2a,b)34。另一工作是以CaO作为模板,通过CVD法制备了比表面积为572 m2·g-1的分级多孔石墨烯(HPG)。石墨烯表面分布着丰富的平面微孔,能够限制多硫化锂扩散;片层弯曲褶皱形成了大量介孔,有利于离子的快速传输和多硫化锂的限域;片层之间构建了大孔尺寸的空腔,能够进一步为锂离子传输提供畅通通道。将HPG与硫复合并用于锂硫电池正极,在5C大电流密度下表现出357 mAh·g-1的比容量(图2c,d)35。
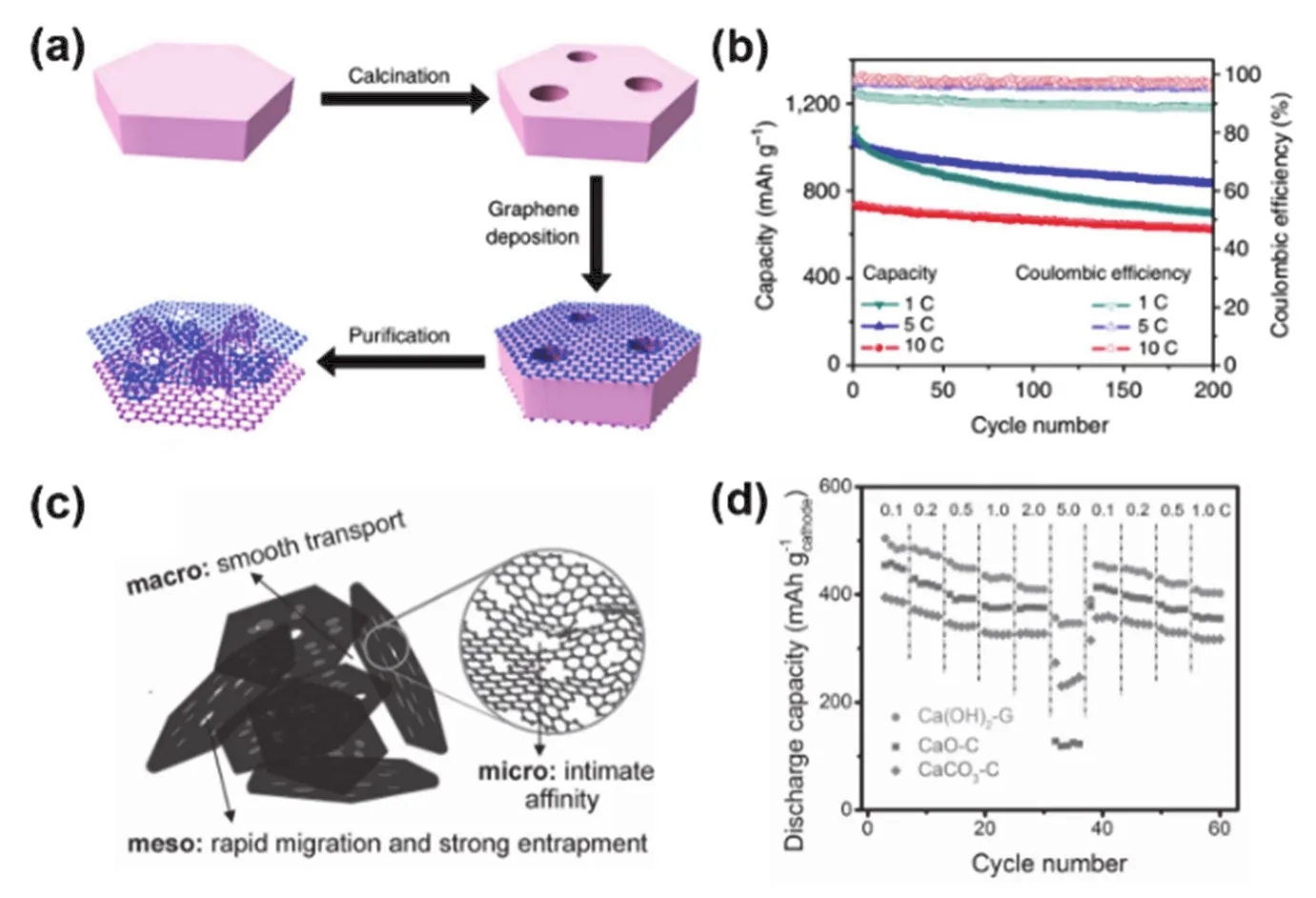
图2 (a)DTG的合成示意图;(b)DTG/S正极的循环性能34;(c)HPG的孔结构图示图;(d)HPG/S正极的电化学性能35Fig.2 (a)Schematic for the synthesis of unstacked DTG;(b)Cycling performance of the DTG/S cathode34;(c)Illustration for the pore structure of HPG;(d)Rate performance of HPG/S cathode35.
2.2 表面化学修饰的石墨烯
极性多硫化锂与非极性石墨烯之间的相互作用较弱,因而仅依靠空间限域并不能有效阻止多硫化锂从石墨烯基底逃逸。研究者们发现,通过表面化学修饰可以提高石墨烯基底的极性,从而对多硫化锂产生较强的化学吸附作用。
2.2.1 官能化石墨烯
在石墨烯表面嫁接亲水性官能团有利于多硫化锂在石墨烯基底上锚定。Zu等36首先通过水热方法在石墨烯表面均匀生长了丰富的羟基基团,然后以羟基作为硫的成核位点,通过氢键作用将化学反应得到的无定型硫均匀负载在羟基化石墨烯表面。硫如此高的分散状态使其与导电基底充分接触,从而表现出优异的倍率性能。在2C大电流密度下,初始比容量高达647 mAh·g-1,循环100圈后仍然保持647 mAh·g-1。Chang等37通过一锅法制备了功能化多孔石墨烯/硫复合材料。石墨烯表面被H2O2氧化刻蚀形成了丰富的微孔,同时沿着孔边缘掺杂了丰富的含氧官能团,这些极性含氧官能团对多硫化锂具有强的锚定作用。该正极材料在0.2C电流密度下循环300圈后,比容量保持429 mAh·g-1。Wang等38通过在石墨烯表面嫁接乙二胺官能团有效抑制了固体放电产物从石墨烯基底脱离。理论计算证明,Li2S中的锂原子能和乙二胺中的氮原子形成共价键,从而增强其与石墨烯基底之间的结合能(图3)。将乙二胺功能化石墨烯与硫复合用于锂硫电池正极,在0.5C电流密度下循环350圈后,仍具有80%的容量保持率;在4C大电流密度下仍具有480 mAh·g-1的高比容量。
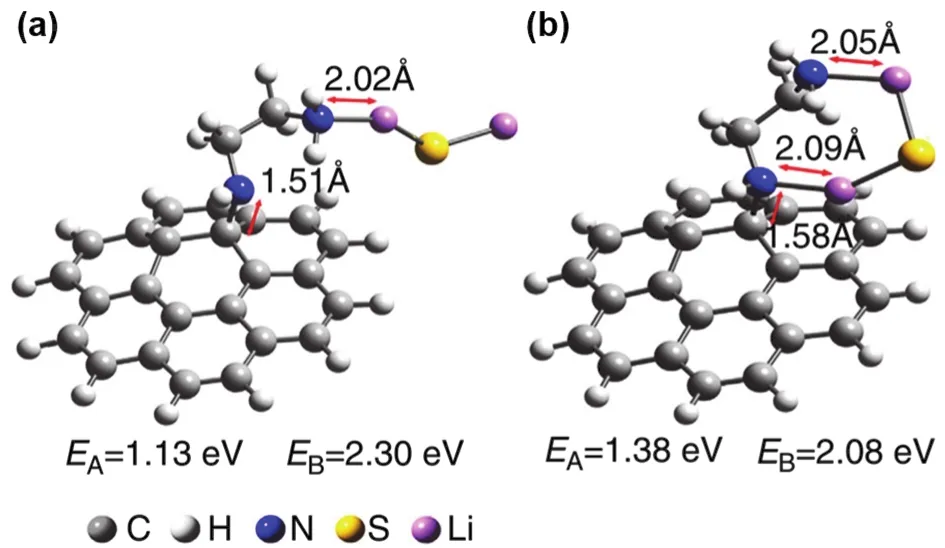
图3 Li2S与EFG的相互作用示意图38Fig.3 The interaction between Li2S cluster and EFG38.
2.2.2 杂原子掺杂石墨烯
除了在石墨烯表面引入官能团,对石墨烯进行杂原子掺杂也能加强石墨烯基底对极性多硫化锂的吸附能力。Qiu等39首先通过将GO在NH3气氛下热处理制备了氮掺杂石墨烯(NG),然后通过化学反应沉积在NG表面均匀负载小尺寸的硫纳米颗粒,得到了S@NG复合材料。NG不仅具有优异的导电性,而且其中的N原子可作为多硫化锂的极性吸附位点,有效抑制穿梭效应。因此,该S@NG正极在不添加碳黑导电剂的情况下仍表现出良好的电化学性能。在5C大电流密度下,比容量高达606 mAh·g-1,且在2C下循环2000圈后,容量衰退率仅为0.028%每圈。Xie等40采用一步水热法制备了三维硼掺杂石墨烯气凝胶(BGA),掺杂的硼原子能够有效提高材料的导电性和对多硫化锂的吸附能力,将BGA作为硫载体应用于锂硫电池正极表现出良好的电化学性能,在2C电流密度下循环200圈后,仍有600 mAh·g-1的比容量。Xu等41将聚吡咯官能化的石墨烯进行K2CO3活化得到了三维氮、硫共掺杂多孔石墨烯(A-NSG),碳晶格中掺入的吡啶氮和噻吩硫能够调控局域电子排布,从而增加石墨烯基底与多硫化锂的结合能力,提高多硫化锂转化的可逆性。将A-NSG与硫复合并应用于锂硫电池正极,在0.2C电流密度下初始比容量为1178 mAh·g-1,在5C大电流密度下仍保持651 mAh·g-1。Hou等42通过第一原理计算研究了不同杂原子掺杂的石墨烯对多硫化锂的吸附作用及机制。结果表明,具有孤对电子的氮原子和氧原子能够通过与多硫化锂中的锂离子之间的偶极-偶极相互作用显著增强石墨烯基底对硫物种的吸附,从而实现高的比容量和库伦效率。相反,B、F、S、P和Cl杂原子对增强石墨烯与硫物种之间的相互作用的效果不尽人意(图4)。由此可见,对石墨烯进行氮掺杂、氧掺杂或者多原子掺杂是提高锂硫电池电化学性能行之有效的方法。
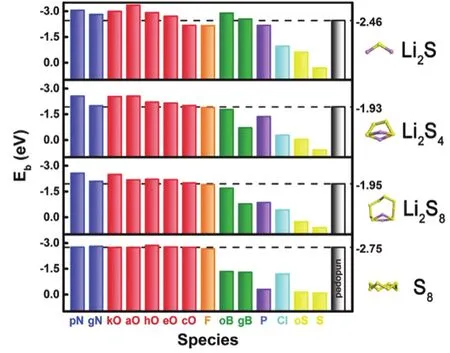
图4 基于DFT计算的Li2S、Li2S4、Li2S8和S8分别与原始石墨烯和X原子(X = N、O、F、B、P、Cl、S)掺杂的石墨烯之间的结合能42Fig.4 Binding energies of Li2S,Li2S4,Li2S8 and S8 with X-doped (X = N,O,F,B,P,Cl,S)graphene based on DFT calculations42.
2.2.3 金属单原子修饰的石墨烯
最新研究表明,金属单原子修饰的石墨烯在锂硫电池中具有广阔的应用前景。一方面,金属单原子具有100%的原子利用率、不饱和的配位环境和独特的电子结构,不仅能有效吸附多硫化锂,而且能显著加快其氧化还原反应动力学43-48。另一方面,石墨烯的二维平面结构有利于实现金属单原子的高载量分散,进一步提高其吸附和催化转化能力49。Du等50将吸附有钴离子的氧化石墨烯在氨气气氛下高温热解制得了单原子Co修饰的N掺杂石墨烯(Co-N/G)。DFT理论计算表明,所形成的Co-N-C配位结构能够有效促进放电和充电过程中Li2S的形成和分解,加快其反应动力学(图5)。在硫面载量为2 mg·cm-2时,在0.2C电流密度下,S@Co-N/G复合材料初始比容量为1210 mAh·g-1;当硫面载量增加到6 mg·cm-2时,在0.2C电流密度下循环100圈后,其面积比容量高达5.1 mAh·cm-2。Wang等51将GO与Fe(OH)3溶胶混合并在Ar/H2/NH3混合气中高温煅烧得到FeN0.056/Fe3C纳米颗粒嵌入的氮掺杂石墨烯复合材料,经过酸洗去除这些纳米颗粒最终得到了多洞的Fe、N共掺杂石墨烯(HFeNG)。多洞结构可以提供离子快速传输通道,加快Li+扩散,从而提高电化学反应速率。Fe单原子分别以Fe-N4结构锚定在石墨烯面内和以Fe-N2配位结构位于洞的边缘处。值得注意的是,Fe-N2配位中心与多硫化物的结合能力更强。将HFeNG载硫后用作锂硫电池的正极,在5C大电流密度下,比容量高达810 mAh·g-1。Zhou等52通过实验与理论计算分析了一系列金属单原子(包括Fe、Mn、Ru、Co、Zn、V、Cu和Ag)修饰的氮掺杂石墨烯对多硫化锂的吸附能力和催化转化能力。结果发现,除单原子Ag和Cu之外,其他金属单原子在循环过程中均能保持结构稳定。通过理论计算可知,Li2S在各种基底上的分解能垒由小到大依次排列为V <Mn < Ru < Fe < Co < Zn,而与Li2S6的结合能由大到小依次排列为V > Ru > Co > Zn > Fe > Mn。综合以上结果可知,SAV@NG对多硫化物具有最强的吸附能力和催化转化能力。实验合成的SAV@NG/S复合材料也表现出最佳的电化学性能,在3C大电流密度下,放电比容量高达645 mAh·g-1。
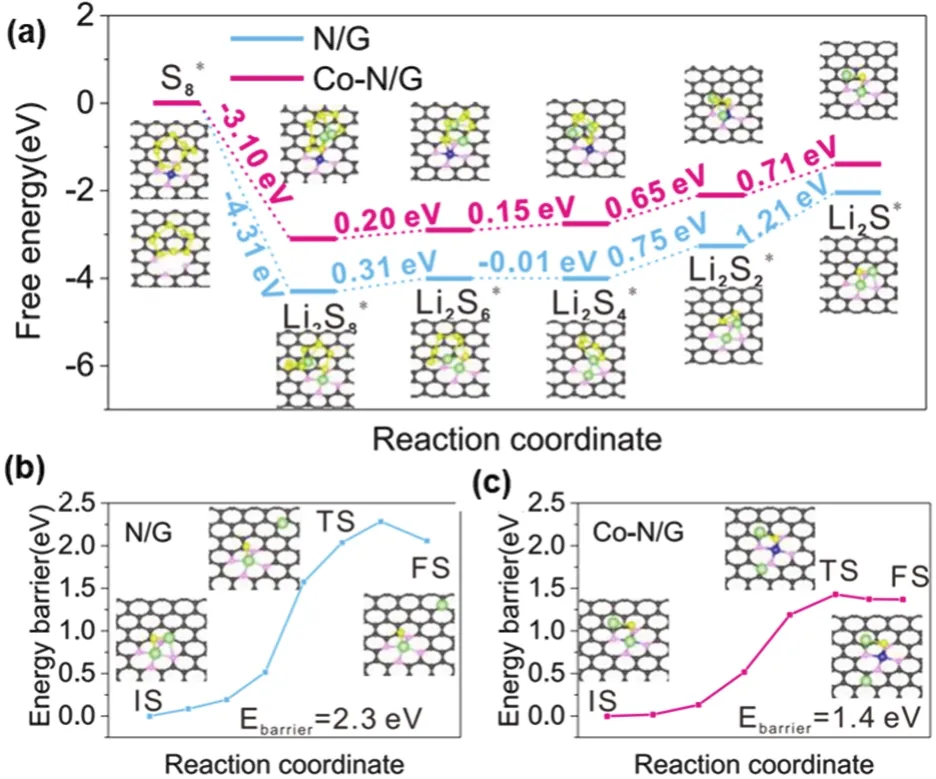
图5 (a)硫物种在N/G和Co-N/G基底上的还原反应吉布斯自由能曲线;Li2S在(b)N/G和(c)Co-N/G上的分解能垒曲线50Fig.5 (a)Energy profiles for the reduction of sulfur species on N/G and Co-N/G substrates;Energy profiles of the decomposition of Li2S cluster on (b)N/G and(c)Co-N/G50.
2.3 石墨烯基复合材料
2.3.1 石墨烯/碳复合材料
通常,单一的一种碳材料难以全部满足正极硫载体的要求,将具有不同优点的碳材料复合是实现锂硫电池正极性能优化的有效策略。石墨烯无可比拟的导电性和优异的结构稳定性令其在碳复合材料中广受欢迎53,54。其他类型的碳材料,如多孔碳、杂原子掺杂碳等也可弥补石墨烯开放的片层结构无法有效约束多硫化锂的缺点55,56。除了各组分的本征优势之外,复合碳材料还可被设计成各种独特结构,能够进一步改善锂硫电池电化学性能57-60。Zhang等61利用模板法在导电石墨烯表面构筑了丰富的孔状/管状碳通道(NTPC-G),这些氮掺杂碳通道不仅为硫和固体放电产物提供了充足的储存空间,而且对多硫化锂起到了多重限域作用(图6a)。因此,NTPC-G与硫的复合材料在6C大电流密度下,初始比容量仍高达563 mAh·g-1,循环600圈之后容量衰减率为0.07%每圈。Tang等62通过两步CVD法制备了垂直生长的氮掺杂碳纳米管与石墨烯复合材料(N-ACNT/G)。碳纳米管与石墨烯片相互垂直形成类三明治的多级结构,为电子转移和离子扩散提供了快速通道,而且氮掺杂进一步提高了该碳复合材料对多硫化锂的吸附能力。因此,N-ACNT/G与硫的复合材料表现出了优异的循环性能和倍率性能,即使在5C大电流密度下,其可逆比容量仍高达770 mAh·g-1(图6b,c)。Lu等63首先制备了硫包覆的碳纳米纤维(S-CNFs),然后利用静电自组装策略将石墨烯包裹在S-CNFs表面,得到了石墨烯硫-碳纳米纤维同轴复合材料(G-S-CNFs)。该材料作为锂硫电池正极时,在1C电流密度下具有745 mAh·g-1的初始比容量,循环1500圈后保留273 mAh·g-1,容量衰减率为0.043%每圈。Yuan等64将石墨烯与离子液体[Emim]BF4混合并经过两步热解得到了石墨烯支撑的富N/B碳层(G-NBCL)。该复合材料不仅继承了石墨烯优异的导电性,而且其表面碳层中的N=B/N=B结构对多硫化锂的吸附能力明显强于吡咯氮和吡啶氮。将G-NBCL与硫复合作为锂硫电池正极,在2C电流密度下,循环1500圈之后容量衰退率仅为0.035%每圈,且在3C大电流密度下,具有480 mAh·g-1的可逆比容量。

图6 (a)NTPC-G的合成示意图61;(b)N-ACNT/G的合成示意图;(c)载硫N-ACNT/G的倍率性能62Fig.6 (a)The synthesis process of NTPC-G61;(b)The synthesis process of N-ACNT/G;(c)The rate performance of sulfur-loading N-ACNT/G62.
2.3.2 石墨烯/金属化合物复合材料
最近,各种石墨烯负载的金属化合物被广泛应用于锂硫电池正极。在该类复合材料中,石墨烯不仅可作为导电网络和柔性框架来提高电极的导电性和结构稳定性,还可为金属化合物提供原位成核位点,实现其小尺寸高分散。这些金属化合物能够暴露丰富的极性吸附位点,将多硫化锂锚定在石墨烯基底上,通过快速的离子与电子传输进一步促进多硫化锂的转化,提高锂硫电池的循环性能和倍率性能。Yu等65通过原子层沉积方法在载硫氮掺杂石墨烯基底上生长TiO2(NG/S-TiO2)。尽管TiO2对多硫化锂具有强的结合能力,然而其较差的导电性降低了多硫化锂的转化反应动力学,因此调控导电石墨烯基底上TiO2的负载量对提高载硫正极的电化学性能至关重要。最终,原子层沉积20圈得到的NG/S-TiO2复合材料实现了最优的电化学性能。在1C电流密度下,初始比容量高达1102 mAh·g-1,经过500圈循环后,容量衰减率仅为0.024%每圈。与金属氧化物相比,金属硫化物、金属氮化物、金属硒化物的电子导电性更高,更有利于促进多硫化锂的转化反应,提高锂硫电池的倍率性能。Cheng等66通过水热法在还原氧化石墨烯表面均匀负载了VS2纳米片(VS2-rGO),然后通过熔融扩散策略将硫封装在VS2-rGO的夹层中,形成弹性的三明治结构。这种结构不仅能够嵌入更多的活性物质,而且还能为Li2S沉积提供充足的空间以有效缓解体积膨胀。另外,具有强极性且高导电性的VS2-rGO基底能够有效锚定多硫化锂,并加快界面电荷转移,提高其转化反应动力学。硫载量高达89% (w)的VS2-rGO/S复合材料在0.1C电流密度下表现出高达1182 mAh·cm-3的体积比容量。Sun等67将GO和NH4VO3作为前驱体进行水热处理并在NH3气氛下热解得到了VN/G复合材料。介孔VN纳米带与石墨烯相互连接形成的三维网络结构,不仅能够加快锂离子传输和电子转移,还能够有效容纳硫化锂的体积膨胀。而且,VN能通过与多硫化锂形成S―V键和Li―N键有效将多硫化锂锚定在导电基底上,进而加快其转化反应动力学。将VN/G应用于锂硫电池正极时,在0.2C电流密度下,初始比容量高达1461 mAh·g-1,在2C大电流密度下,比容量仍能保持956 mAh·g-1。Chen等68结合软模板法和肼还原法制备了中空CoSe2纳米球与还原氧化石墨烯复合材料(RGO-CoSe2)。CoSe2中空纳米球均匀分散在石墨烯片层之间,既能有效阻止石墨烯堆叠,又能有效吸附多硫化锂。而且,CoSe2由于其本身的金属属性能够促进电荷转移,加快多硫化锂的电化学转化(图7)。因此,载硫的RGO-CoSe2复合材料在1C电流密度下具有1037 mAh·g-1的初始比容量,循环400圈后,仍能保持741 mAh·g-1。

图7 RGO-CoSe2在锂硫电池中的作用机制68Fig.7 The function mechanism of RGO-CoSe2 nanohybrid in Li-S batteries68.
2.4 石墨烯基柔性自支撑正极
柔性、可穿戴的电子设备的广泛应用对电化学储能器件的设计提出了更多的要求。与传统的电池体系相比,柔性电池必须在经历弯曲、折叠、拉伸挤压之后仍能恢复原始状态,并保持原有电化学性能。锂硫电池因其极高的理论能量密度在轻便、柔性电池设备中具有极好的应用前景。石墨烯具有优异的导电性、机械强度和柔韧性,已经被广泛应用于柔性锂硫电池正极32。
Jin等69首次将柔性自支撑石墨烯/硫复合材料(GS/S)应用于锂硫电池正极。首先,通过硫代硫酸钠和盐酸之间的化学反应将硫纳米颗粒均匀沉积在石墨烯层,然后经过真空抽滤即可得到GS/S膜。在0.1C电流密度下循环100圈之后,该GS/S柔性电极的比容量仍保持600 mAh·g-1,容量保持率高达83%。Zhou等70通过CVD方法在泡沫镍上生长石墨烯,然后在其表面包覆一层聚二甲基硅氧烷(PDMS),酸洗去除镍即可得到PDMS/GF柔性薄膜。最终将含硫浆料过滤在PDMS/GF薄膜上得到了柔性S-PDMS/GF电极。在石墨烯泡沫表面的PDMS包覆层有效提高了柔性骨架的机械强度,相互连通的石墨烯泡沫不仅提供了电子快速传输路径,而且提供了足够大的空间容纳活性物质。当硫载量高达10.1 mg·cm-2时,该柔性电极面积比容量高达13.4 mAh·cm-2,而且在0.15 A·g-1电流密度下,经过1000圈循环之后,容量衰退率仅为0.071%每圈(图8a,b)。与石墨烯相比,氧化石墨烯具有丰富的含氧官能团,更易于在水溶液中分散和组装,并得到与硫的柔性复合材料,后续再经过还原即可得到石墨烯/硫柔性电极。例如,Wang等71将硫纳米颗粒和氧化石墨烯均匀混合分散,然后通过冷冻干燥以及低温热处理过程制备了柔性纳米硫/石墨烯复合膜(S-rGO)。冷冻干燥方法导致氧化石墨烯片层褶皱弯曲,形成丰富的大孔结构。后续高温热处理过程中,氧化石墨烯被还原成石墨烯,同时硫纳米颗粒熔融分散,均匀包覆在石墨烯表面。该S-rGO复合膜作为自支撑电极,在0.3 A·g-1的电流密度下,初始比容量为957 mAh·g-1,经过200圈循环,容量仍保持93% (图8c,d)。Cao等72利用化学反应沉积策略在氧化石墨烯表面沉积硫纳米颗粒,尺寸仅为9-22 nm。然后,将锌箔浸渍到以上GOS分散液中,利用rGO/GO与Zn/Zn2+的还原电势差,将GO还原成rGO。在还原过程中,电子易从锌箔表面转移到GO片层,导致锌箔表面离子化,产生的Zn2+能够吸附更多带负电的GO片,诱导其进一步的还原与组装(图8e)。最终剥离的rGO-S膜具有突出的柔性与机械强度,因而利用该电极组装的柔性软包电池和电缆型电池均表现出优异的电化学性能,在0.1C电流密度下,初始比容量分别高达1187和1360 mAh·g-1,并且经过弯折之后容量仍然保持稳定。
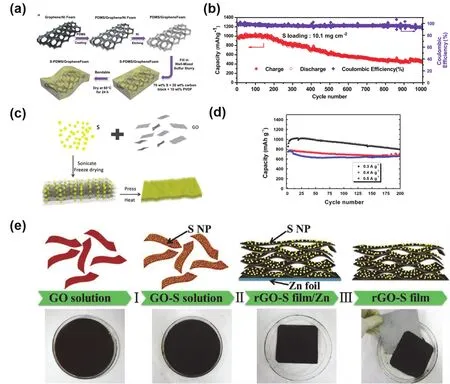
图8 S-PDMS/GF电极的(a)合成示意图和(b)循环性能图70;S-rGO膜的(c)合成示意图和(d)循环性能图71;(e)rGO-S复合膜的合成示意图72Fig.8 (a)Synthesis schematic and (b)cycling performance of S-PDMS/GF electrodes70;(c)Synthesis schematic and(d)cycling performance of S-rGO paper70;(e)Schematic process of fabricating rGO-S composite films70.
与石墨烯在常规锂硫电池正极中的应用思路类似,其他各种类型的碳材料、导电聚合物以及极性材料也被引入到柔性石墨烯基电极中。石墨烯在这些复合电极中充分发挥了其高柔韧性和高导电性的优势31,73。Shi等74将氧化石墨烯和碳纳米管混合,经过冷冻干燥制备了氧化石墨烯/碳纳米管气凝胶,之后通过自蔓延燃烧被快速还原成石墨烯/碳纳米管气凝胶。将该气凝胶同时作为硫的柔性、致密载体以及正极和隔膜之间的夹层组装成锂硫电池,表现出优异的循环性能。在2C电流密度下,经过500圈循环之后,比容量仍高达445mAh·g-1,容量衰退率仅为0.06%每圈。同时,该电池的体积比容量高达1841 Ah·L-1,体积能量密度高达2134 Wh·L-1。Zhou等53利用TiO2中空球作为模板,多巴胺作为碳源,合成了氮掺杂双壳中空碳球(NDHCS),然后通过熔融扩散策略将硫封装在其空腔中,得到NDHCS-S复合材料,最后通过包覆石墨烯、真空抽滤得到了柔性G-NDHCS-S复合膜(图9a)。在2C大电流密度下,该膜比容量高达600 mAh·g-1,并且循环200圈之后库伦效率仍接近100%。Xiao等75在沉积硫纳米颗粒的氧化石墨烯外部包覆PEDOT:PSS,后续经过热还原以及真空抽滤过程得到了致密、柔性的硫-石墨烯-导电聚合物(SGP)膜(图9b)。该膜作为锂硫电池正极,在0.1C电流密度下,体积比容量高达1432 Ah·L-1;在1C电流密度下,循环500圈之后容量仍保持80%。He等76通过水热法在石墨烯表面原位生长少层MoS2纳米片,制备了自支撑的三维石墨烯/1T MoS2异质结。1T MoS2具有丰富的活性位点,有利于促进多硫化锂转化;通过冷冻干燥石墨烯形成的大量孔隙结构有利于加快电解液渗透和锂离子传输;三维石墨烯框架和金属性1T MoS2具有优异的导电性,有利于加快电子转移。基于以上优点,面载量高达10 mg·cm-2的柔性载硫三维石墨烯/1T MoS2正极在0.1C电流密度下,初始比容量高达1181 mAh·g-1,经过200圈循环之后,容量保持率为96.3%。在1C大电流密度下循环500圈容量衰退率仅为0.08%每圈(图9c)。Ghosh等77首先通过溶液分散混合方法得到了S/Mn3O4/石墨烯复合物,然后以海藻酸钠作为掺杂剂,通过苯胺的原位聚合反应得到聚苯胺/海藻酸钠粘结的S/Mn3O4/石墨烯(PRGO/S/Mn3O4@PANI-SA)柔性薄膜(图9d)。聚苯胺/海藻酸钠作为粘结剂不仅具有高的机械强度和电子/离子导电性,而且对多硫化锂具有一定的化学吸附作用。以该柔性薄膜作为锂硫电池正极,在5 A·g-1电流密度下,初始比容量高达1015 mAh·g-1,经过500圈循环之后,容量保持率为71%。

图9 (a)G-NDHCS-S复合膜的合成示意图53;(b)SGP复合膜的合成示意图75;(c)多硫化锂在石墨烯/1T MoS2表面的转化过程76;以及载硫石墨烯/1T MoS2电极的循环性能;(d)PRGO/S/Mn3O4@PANI-SA正极的合成示意图77Fig.9 (a)Schematic illustration of the fabrication of the G-NDHCS-S hybrid paper53;(b)Schematic illustration of the SGP cathodes75;(c)The conversion process of lithium polysulfides on a graphene surface with 1T MoS2 and cycling performance of S-loading graphene/1T MoS2 electrode76;(d)Schematic illustration of the synthesis of the PRGO/S/Mn3O4@PANI-SA cathode77.
3 结论与展望
本文总结了三维石墨烯、表面化学修饰的石墨烯、石墨烯基复合材料以及石墨烯基柔性材料在锂硫电池正极中的研究进展。各种载硫石墨烯材料的电化学性能汇总于表1。石墨烯及其复合材料作为硫载体的优势在于:(1)具有高的导电性以及结构稳定性,能够有效提高活性物质利用率和缓解放电过程中的体积膨胀;(2)三维网络以及丰富的孔结构一方面可以加快电子转移和离子传输,另一方面可以对多硫化锂起到物理限域作用;(3)表面官能团改性和杂原子掺杂,特别是金属单原子掺杂,能通过与多硫化锂之间的化学相互作用有效吸附多硫化锂,并加快其转化反应动力学;(4)高导电性石墨烯与强极性金属化合物复合能够协同促进基底对多硫化锂的吸附能力与催化转化能力;(5)具有高的柔韧性以及易于组装的特性,非常适合构筑柔性锂硫电池电极。
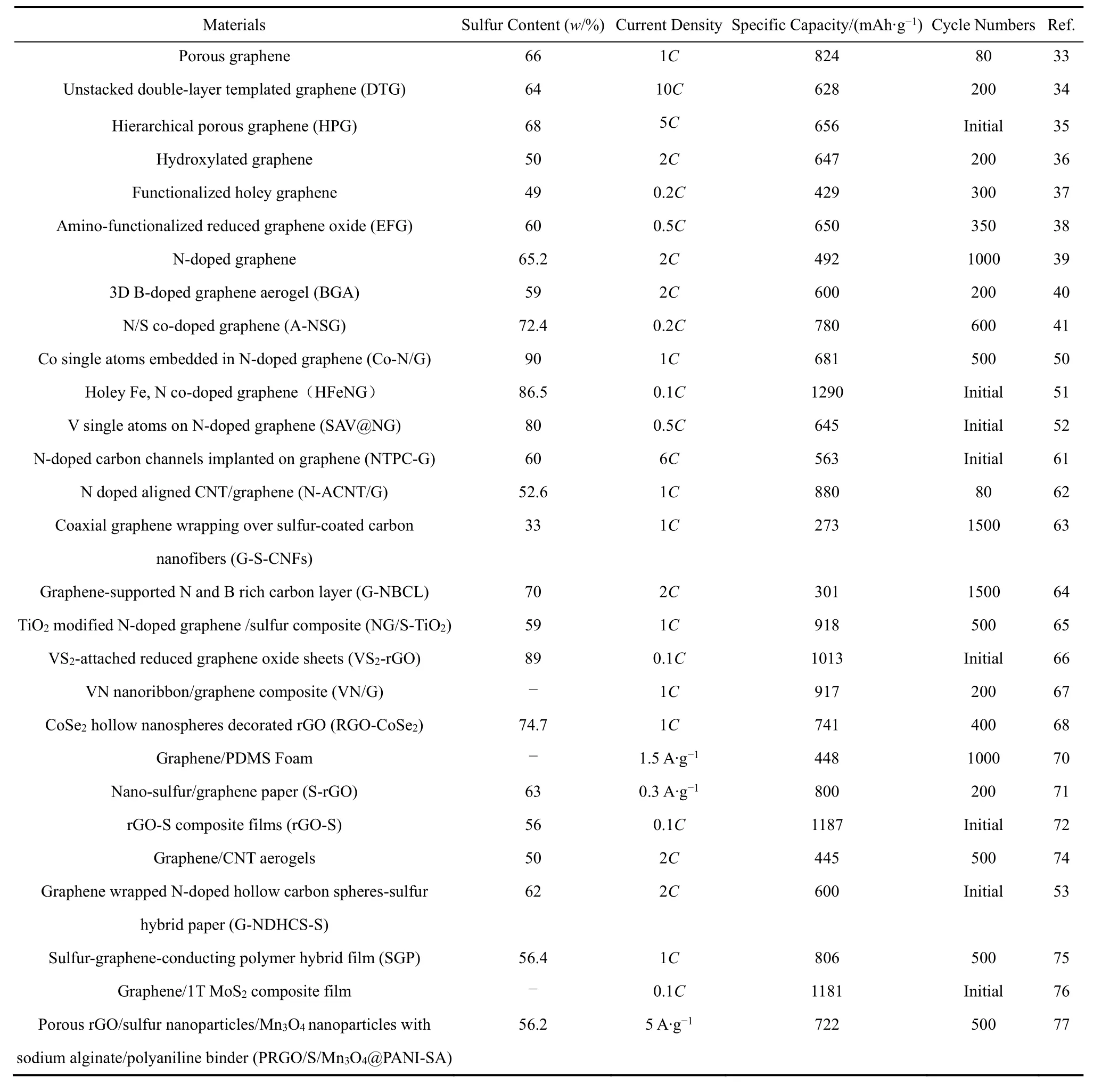
表1 载硫石墨烯材料的电化学性能Table 1 Electrochemical performance of sulfur-loading graphene materials.
尽管石墨烯在锂硫电池正极中的研究已经取得了很大进展,但是距离锂硫电池实用化还有很大差距,目前存在的主要问题有:(1)石墨烯的高品质、大规模制备较为困难,通过CVD或者特殊的剥离方法得到的石墨烯品质较高,但生产成本也随之上升,而通过氧化石墨烯还原策略得到的石墨烯的物理结构性质会大打折扣;(2)高硫载量条件下,硫在石墨烯基底中分散不均匀甚至严重团聚。低液硫比条件下,锂硫电池循环寿命明显衰减;(3)电极内部的表界面化学反应过程尚不清晰,石墨烯与其他材料的协同作用机理仍不明确。由此可见,未来在低成本制备高品质石墨烯、提高硫载量和降低液硫比实现锂硫电池高能量密度、探索石墨烯在锂硫电池中的储能增强作用机制等领域亟待取得突破。研究者们可从新型石墨烯制备技术开发、电池材料与结构设计、先进原位表征结合理论计算等方面来突破以上难题。
