AI肺结节筛查准确率及结节风险评估准确率分析
2022-02-25陈巧一通信作者
陈 均,陈巧一(通信作者)
(重庆市永川区人民医院放射科 重庆 402160)
随着医学影像检查技术不断发展,特别是多层螺旋CT的广泛应用,肺结节的检出率明显增高。CT扫描层厚越来越薄,由之前双排、16排的1.5 mm/层发展到现在超高端螺旋CT的0.5 mm/层,虽然层厚越来越薄,提供的诊断信息越来越多,但图像层数也越来越多,影像诊断医生的工作量及压力显著增大。普通成年人行常规胸部CT检查,如层厚0.6 mm/层,平扫肺窗将会有500张左右图像,再加上软组织窗、骨窗图像,诊断人员每完成1例胸部CT检查诊断,将调阅上千张图像资料,很难避免微小结节的漏诊、误诊。越小的结节越容易漏诊,尤其是放射科医师在长时间工作产生疲劳之后,这符合临床上对肺结节检测的普遍经验[1]。随着科学技术的发展,计算机辅助人工智能诊断系统(AI)逐渐应用于影像诊断领域,其中肺结节的计算机辅助人工智能诊断应用最早、也最广泛。随着影像科医生阅片对AI的应用逐渐增多,AI影像辅助诊断系统对减少漏、误诊,提高阅片速度及诊断正确率发挥了巨大的作用,使肺结节的检出率明显提高[2]。AI分析的准确性成为广大影像科阅片医生关注的重点。本研究旨在探讨AI对肺结节的筛查准确率及风险评估准确率,推动AI辅助诊断技术在胸部CT检查中的应用。
1 资料与方法
1.1 一般资料
回顾分析重庆市永川区人民医院2019年12月—2021年5月收治的以肺部症状就诊的行胸部或者胸腹部联合CT扫描、AI与影像诊断医生共同诊断的90例肺结节患者。AI诊断结节阈值3 mm。排除标准:尘肺粟粒结节、转移瘤、双肺间质性病变、严重肺气肿等患者;常规体检、常规术前检查、外伤患者。90例患者中男性52例,女性38例,年龄17~78岁,平均年龄(57.6±8.4)岁。患者均对本试验知情并签署同意书。
1.2 方法
所有病例均使用飞利浦(极速之心)Ingenuity core 64排128层螺旋CT扫描。患者取仰卧位,头先进,嘱患者屏气后一次性完成全肺扫描。扫描参数:管电压120 kV,管电流 50~200 mA,层厚5.0 mm,层距5.0 mm。扫描结束后,使用Reduce Dose 18算法行肺组织窗薄层重建,层厚1.0 mm,层距1.0 mm,由肺尖重建至肺底(包含全部肺野)[3]。
1.3 图像分析与处理
所有病例分别由诊断医师及AI进行分析诊断。诊断医师由中级诊断医师按日常工作状态进行阅片分析(使用卫宁健康PACS系统阅片);AI分析由医准智能公司提供的肺结节人工智能诊断系统V5.0版本软件自动识别和标记肺结节。结节大小以6 mm为分界标准(参照《中国肺癌筛查标准(T/CPMA013-2020)》实性结节或部分实性结节LDCT随访分界标准)[4]。由2名高年资中级医师在参照AI的结果上通过薄层(1 mm)横断面图像及多平面重组等技术,判断结节的真实性,以2名医师的一致性意见作为参照标准,意见不统一时,由高级职称医师组织共同讨论,得出统一诊断金标准。结节风险评估以高风险结节(AI)和拟诊恶性肿瘤结节(诊断医师)为统计数据,以手术、穿刺病理结果为金标准[5]。
1.4 统计学方法
所得数据采用SPSS 22.0统计学软件处理,计数资料以率(%)表示,行χ2检验,若P<0.05则表示数据差异具有统计学意义。
2 结果
所选90例病例中,AI识别结节总数689个,>6 mm结节432个,高风险(拟诊肿瘤)患者30例;诊断医师识别结节总数547个,>6 mm结节401个,高风险(拟诊肿瘤)患者25例。两组结论与金标准对照可以得出:AI诊断肺结节灵敏度高于诊断医师,特别是6 mm以下小结节不易漏诊,但存在少量假阳性,经分析假阳性结节主要为局部胸膜增厚、血管转折、局灶性炎性渗出等;AI识别高风险结节灵敏度高于诊断医师,特异度稍低;诊断医师6 mm以下小结节漏诊较多,漏诊主要为细小结节及小磨玻璃结节。见表1。

表1 结节总数、>6 mm结节及高风险(拟诊肿瘤)结节
AI识别30例高风险结节,诊断医师拟诊25例肿瘤结节(肿块),手术、穿刺确诊恶性肿瘤22例,3例排除恶性肿瘤;AI对于高风险结节的检查准确率高于影像诊断医师,灵敏度高,但特异度低于诊断医师。AI误判的8例高风险结节中有结核空洞1例,尘肺结节2例,炎性团块4例,叶间裂积液1例。
患者17岁,青年,右肺上叶空洞,病灶邻近多发粟粒结节及小片状影,最终诊断为肺结核。如图1、图2所示。

图1 结核空洞
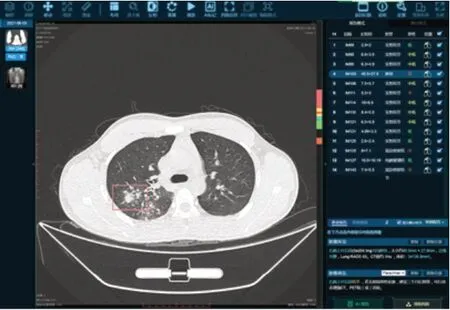
图2 结核空洞
薄层观察病灶密度较高,CT值在80 HU左右,内见钙化,双肺散在细小结节,结合患者有粉尘接触使,诊断尘肺团块。如图3、图4所示。
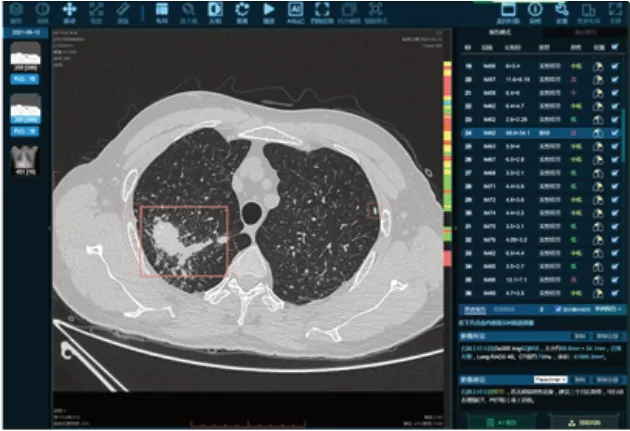
图3 尘肺团块(肺窗)
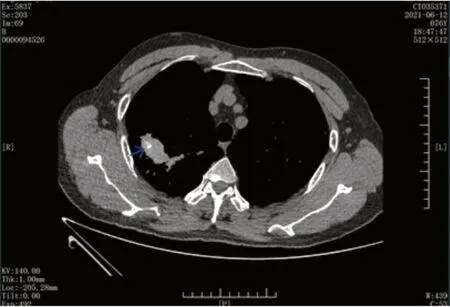
图4 尘肺团块(纵隔窗)
薄层观察病灶呈片状,内可见细支气管通行良好,抗炎治疗后病灶吸收,为炎性病灶。如图5所示。

图5 炎性病灶
3 讨论
肺癌是我国最常见的恶性肿瘤,病死率高于发达国家,但研究表明ⅠA期肺癌患者中,原位癌和微浸润性癌术后五年生存率可接近100%[6-7],早发现、早诊断和早治疗是延长肺癌患者生存期的唯一有效方法[8]。
目前胸部CT检查是肺结节检出的重要手段[9],胸部HRCT检查成为体检及临床筛查肺部病变的常规检查方法,区县级以上医院每天有大量CT检查患者。胸部HRCT检查人员日益增多,图像数量较以前的常规螺旋CT明显增多,对肺部细微结构显示更加清晰,肺结节的显示也越来越准确,但同时也明显增加了诊断医师的工作量,每位诊断医师每天将调阅大量薄层CT图像,长时间的工作及紧张的节奏会加剧视疲劳,对细小肺结节容易漏诊[10]。同时,患者不同时间段检查或到不同医院检查,不同诊断医师对细小肺结节的诊断率会有一定差异,患者不理解时则存在医疗纠纷的风险。计算机辅助人工智能诊断系统可较为精准地诊断肺结节,特别是数毫米的微小结节,不易漏诊,且系统可自动前后对照结节大小,在检出率及结节随访中具有较大优势。AI的出现不仅降低了早期肺癌的漏诊率,也在一定程度上解放了影像科医生的双眼,使其可将有限的精力用于更高难度的工作中[11]。
在本研究中,AI识别肺小结节灵敏度高,特别对于<6 mm的细小结节不易漏诊,诊断医师对小结节特别是6 mm以下小结节漏诊较多,AI在肺小结节的诊断上有较大优势。AI对于高风险结节的检查准确率高于影像诊断医师,灵敏度高,但存在一定比例假阳性,且特异度低于影像诊断医师。现目前AI对肺结节诊断的假阳性率仍较高,需进一步改善其算法、结合临床信息等因素,以提高其特异度。经初步分析,AI高风险结节误判主要原因为:①不能良好结合患者年龄等临床资料,只凭借影像征象判定,如青年患者结核球及结核空洞判定为高风险;②未结合CT值等后处理手段综合分析,如尘肺团块判定为高风险结节;③不能结合患者双肺其他情况综合分析,把部分炎性病灶判定为高风险肿块。与普通图片不同,影像学图像更为复杂,疾病的影像表现多样,对AI也是极大的挑战[12]。下一步应提供更多数据,建立更可靠的模型,加强AI的深度学习,提高AI诊断的准确性及特异度。
本研究仍有不足的地方:①样本量相对较少,相对日常大批量的胸部CT检查,本次研究仅选取小部分病例,还需要进一步结合大批量样本研究;②缺少相同或相近病种、影像表现相近的AI分析结果。
综上所述,AI能够有效协助影像科诊断医生阅片,但不能完全替代,只有将人工智能阅片和人工阅片有机结合,互相取长补短,才能发挥最大能效。
