氢氟醚电解液在锂金属电池中的应用研究
2022-02-22刘佩莹
陶 锴,刘佩莹,王 灿
应用研究
氢氟醚电解液在锂金属电池中的应用研究
陶 锴,刘佩莹,王 灿
(武汉船用电力推进装置研究所,武汉 430064)
无负极锂金属电池存在容量损失快和循环寿命短的缺点。本文设计制备一种氢氟醚电解液,探究其在无负极锂金属电池中的应用。采用X射线衍射仪(XRD)和扫描电子显微镜(SEM)进行分析,结果表明该氢氟醚电解液对高面容量银碳基无负极锂金属电池的循环性能有着优良的改善作用。氢氟醚电解液减少了锂枝晶的产生,提高了沉积锂的致密性,在大于3 mAh/cm2的高面容量下,银碳基无负极锂金属电池在0.5C的倍率下50次循环后仍保持96.2%的平均库伦效率,展现了优良的循环性能和良好的倍率性能,1C倍率下容量保持率≥85%。
氢氟醚电解液无负极锂金属电池循环性能倍率性能
0 引言
船用装置和无人装备的应用越来越广泛。为了保证其电源在有限体积下具备更长的工作时间,要求电源具备高体积比能的特性。与传统锂离子电池相比,无负极锂金属电池体积能量密度可提高约60%,在锂离子电池材料中得到广泛的关注和研究[1-3]。在无补充锂的条件下,无负极锂金属电池通常会出现快速的容量损失。电池失效可归因于锂和电解液的副反应形成固体电解质界面(SEI)和电绝缘锂,导致“死”锂形成和活性锂损失。电解液优化是提高锂循环寿命的有效策略之一,因为它们促进了沉积锂的致密化,锂形貌的保持,提高了锂的循环寿命[4-10]。
通过精确调节电解液的成分,可以形成有利于锂沉积的SEI,使锂沉积变得均匀平坦,减少副反应,减少电解液的分解。Qian[11]等人用4mol/L的LiFSi/DME来稳定负极,50圈后容量保持率约60%,平均CE大于99%,优异的电性能表现归因于溶剂和盐的更高程度的配位,形成紧密离子对,FSI-阴离子的分解形成了富含LiF的SEI等。在这之后,研究人员又通过改变电解液成分来进行电池负极的优化,例如,Beyene[12]用双盐(2mol/L LiFSI+1mol/LLiTFSI)溶于DME/DOL中,Hagos[13]用2mol/L LiPF6溶于EC/DEC加50%FEC的电解液中。除了对电解液成分优化之外,采用添加剂来优化也有许多研究工作,Sahalie[14]等人采用KNO3作为添加剂,实现了50圈40%的容量保持。Brown[15]报道了磷酸三乙酯作为共溶剂加到1mol/LLiDFOB的EC/DMC电解液中,及VC作为添加剂加入到1mol/L LiPF6的 EC/EMC电解液中,提高了Cu/LFP全电池的循环容量。
近几年来,无负极锂金属电池的研究越来越多[14-20],但面向应用的无负极锂金属电池研究较少。本工作研究了一种氢氟醚电解液,制备了高面容量银碳基无负极锂金属电池,比较了不同电解液在高面容量银碳基无负极锂金属电池中的性能表现。
1 试验方案
1.1 银碳纳米复合层的制备
银纳米颗粒(Ag NPs, D50 =300 nm)和炭黑粉末 (SP,D50 =35 nm) 作为活性物质材料。银粉和炭黑粉按1:3的重量比混合N-甲基吡咯烷酮(NMP),其中含7 wt%的聚偏二氟乙烯(PVDF)作为粘结剂。将NMP溶液使用混合器不断搅拌以制备浆料,之后将所制备的银碳复合浆料采用丝网印刷的方式印刷在铜箔上,便得到银碳铜复合集流体,其中银碳(Ag-C)纳米复合层的厚度为5~10 μm。
1.2 氢氟醚电解液的配置
原材料主要包括氟代碳酸乙烯酯 (FEC)、1,1,2,2-四氟乙基-2,2,2-三氟乙基醚(HFE)、三氟乙基甲基碳酯 (FEMC)、碳酸二甲酯(DMC)、碳酸乙烯酯(EC)及六氟磷酸锂(LiPF6)等。氢氟醚电解液由1mol/L LiPF6溶解在质量比HFE:FEMC:FEC为2:6:2的混合溶液中制备而成。作为所有三种溶剂中极性最强的,FEC 作为主要溶剂以确保锂盐浓度,而FEMC和HFE都用作稀释剂以增加离子电导率。
1.3 电极的制备和纽扣电池的组装
高载量银碳基无负极锂金属电池的电化学测试需要将制备的银碳铜复合集流体组装成电池。其中银碳铜复合集流体作为负极,NCM811作为正极(面密度20 mg/cm2, 压实密度3.7),1mol/L LiPF6的HFE/FEMC/FEC (质量比为2:6:2)作为电解液,组装成扣式电池。
1.4 性能表征
用X射线衍射仪(XRD)对制备的材料进行分析,通过X射线打入晶体后产生的特征X射线衍射线的强度和空间分布来确定相组成。以Cu靶为射线源,在5°~90°范围内以5°/min的扫描速率对样品进行扫描。测试设备为XRD-7000,测量电压为30 kV。通过扫描电子显微镜(SEM)对其形貌结构进行表征,设备型号为FEQ250。样品元素分析采用元素分析仪型号为Perkin-Elmer2400CHNelementalanalyzer。电池测试采用蓝电电池测试柜,型号CT3001A,测试电压范围2.8V~4.2V。
2 结果与讨论
2.1 物相分析与形貌结构及元素组成

图1 银碳铜复合集流体的XRD图谱
图1表示合成的银碳铜复合集流体材料的XRD图谱,从图中可以看出合成的银碳铜复合集流体材料的XRD图谱中呈现出Cu,Ag和非晶碳的峰,强烈的Cu峰对应于基底,SP仍保持其非晶态,Ag峰对应于银碳纳米复合层。

图2 银碳纳米复合层不同放大倍数下的扫描电镜图
图2为银碳纳米复合层材料的形貌和结构表征,从图中可以看到银纳米颗粒为约300nm的无规则形状,炭黑呈现35nm无定型结构。经过丝网印刷的方式印刷在铜箔上时银纳米颗粒基本均匀分布于由炭黑形成的基底中,证明了Ag的良好分散性。
3.2 银碳铜复合集流体沉积锂的形貌及电性能
图3为银碳铜复合集流体分别使用1mol/L LiPF6的EC/DMC和1mol/L LiPF6的HFE/FEMC/FEC沉积锂的形貌图,其中a,b采用1mol/L LiPF6的EC/DMC为电解液,c,d,e,f为1mol/L LiPF6的HFE/FEMC/FEC氢氟醚电解液。银碳铜复合集流体在1mol/L LiPF6的EC/DMC中表现较差,沉积锂为大量枝晶,各处都出现了明显的死锂,而采取氢氟醚电解液沉积锂表现较好,虽然存在些许孔隙,但是整体表现致密,无锂枝晶,证明该氢氟醚电解液对于金属锂具有良好的相容性,保证了电极的完整性。
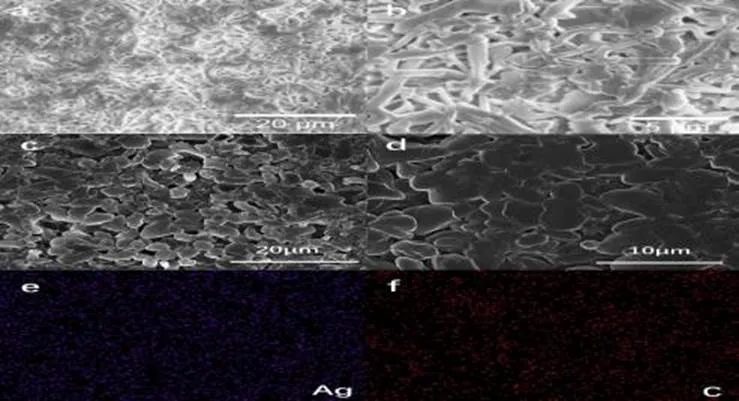
图3 银碳铜复合集流体沉积锂的形貌图
本文同时还探索了银碳铜复合集流体在高载量下即面容量超过大于3 mAh/cm2条件下,不同电解液对无负极锂金属电池循环性能的影响。利用不同电解液匹配电极载量大于20 mg/cm2的NCM811正极片,组装成的Ag-C||NCM811的全电池按0.5C的倍率进行循环充放电,充放电区间为2.8 V~4.2V。其性能表现如图4所示,在0.5C的倍率条件下,采用1mol/L LiPF6的EC/DMC电解液沉积锂,首次放电比容量达到2659mAh/g,第二次循环放电比容量为1739mAh/g,在前5圈的时候便出现容量的断崖式下跌。原因是由于传统碳酸脂类作为电解液循环时会产生大量的锂枝晶及死锂,锂的孔隙率增加,导致需要更多的电解液填充,以完全湿润电池的所有组件,由于电解质分散而导致的电极润湿不足,也被称为电解液耗尽[20]。电解液的耗尽也会导致电荷转移电阻和溶液电阻快速增加,导致容量的快速衰减。以1mol/L LiPF6的HFE/FEMC/FEC作为电解液所沉积的锂首次放电比容量达到2733mAh/g,第二次循环放电比容量为2033mAh/g,50次循环平均库伦效率为96.2%,且库伦效率稳定。以上现象表明该氢氟醚电解液对于银碳基无负极锂金属电池循环性能有着很大的改善[21],使用氢氟醚的电解质,固液电解质界面(Sei)的外层包含更多的LiF,它们对化学和电化学反应非常稳定。相反,在富含EC的电解质中形成的SEI膜会产生不稳定的物质,基于这种原因氢氟醚电解液循环效率相较于传统酯类电解液大大提升。

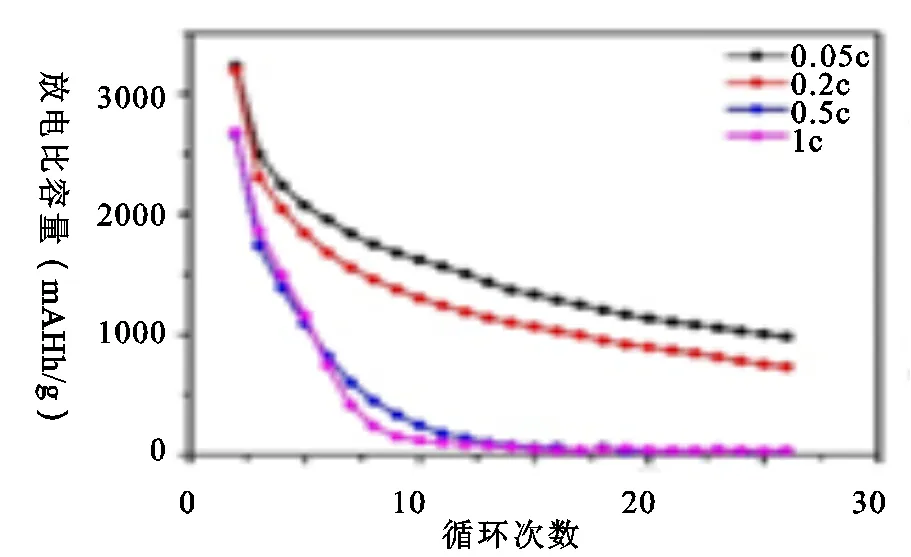
根据上述结果,本文中还测试了使用不同的电解液下银碳基无负极锂金属电池的倍率性能,如图5所示,在高面载量Ag-C||NCM电极中,采用氢氟醚电解液不同倍率下的第一次放电比容量分别为0.05C倍率下3227mAh/g,0.2C倍率下2992mAh/g,0.5C倍率下2871mAh/g,1C倍率下2733mAh/g,不同倍率下循环下放电比容量均相比于采用1mol/L LiPF6的EC/DMC都有明显提升,倍率性能较为优异。图a采用1mol/L LiPF6的EC/DMC为电解液,图b为1mol/L LiPF6的HFE/FEMC/FEC氢氟醚电解液。
3 结论
本文利用氢氟醚电解液搭配银碳铜复合集流体制备出一种无负极锂金属电池。该氢氟醚电解液在高载量无负极锂金属电池中对循环有优良的改善作用,显著减少了锂枝晶及死锂的产生。通过对不同电解液在银碳铜复合集流体电极对NCM811的全电池测试中,该氢氟醚电解液表现出更优异的循环性能,在0.5C的倍率下50次循环后平均库伦效率为96.2%,相比于传统酯类电解液的前5圈容量的断崖式下跌具有显著提升。同时在高载量的电极条件下,1C倍率放电容量保持率≥85%,表现出优异的倍率性能。综上,本文所述的氢氟醚电解液可显著提高无负极锂金属电池的综合性能,对新型高体积比能锂离子电池的应用研究具有积极意义。
[1] Nanda S., Gupta A., Manthiram A., Anode‐free full cells: A pathway to high‐energy density lithium-metal batteries[J]. Adv. Energy Mat.,2021, 11:2000804.
[2] Cheng, X. B., Hou, T. Z., Zhang, R., et al. Dendrite-free lithium deposition induced by uniformly distributed lithium ions for efficient lithium metal batteries[J]. Adv. Mater., 2016, 28: 2888-2895.
[3] Miao, R., Yang, J., Feng, X., et al. Novel dual-salts electrolyte solution for dendrite-free lithium-metal based rechargeable batteries with high cycle reversibility[J]. J.Power Sources 2014, 271:291-297.
[4] Lin, D., Liu, Y., Cui, Y. Reviving the lithium metal anode for high-energy batteries[J]. Nat. Nanotechnol. 2017, 12: 194.
[5] Yu Z., Wang H., Kong X., et al. Molecular design for electrolyte solvents enabling energy-dense and long-cycling lithium metal batteries[J]. Nature Energy, 2020, 5:526-533.
[6] Yu H., Zhao J., Ben L., et al. Dendrite-free lithium deposition with self-aligned columnar structure in a carbonate-ether mixed electrolyte[J]. ACS Energy Letters, 2017, 2(6):1296-1302.
[7] Peng Z., Song J., Huai L., et al. Enhanced stability of Li metal anodes by synergetic control of nucleation and the solid electrolyte interphase[J]. Adv.Energy Mat., 2019, 9(42):1901764
[8] Zhang J G., Xu W., Xiao J., et al. Lithium metal anodes with nonaqueous electrolytes[J]. Chem. Rev., 2020, 120, 13312-13348.
[9] X Cao, X Ren, Zou L, et al. Monolithic solid-electrolyte interphases formed in fluorinated orthoformate-based electrolytes minimize Li depletion and pulverization[J]. Nature Energy., 4(9):796-805.
[10] AB Gunnarsdóttir, Amanchukwu C V, Menkin S., et al. Noninvasive in situ NMR study of "Dead Lithium"formation and lithium corrosion in full-cell lithium metal batteries[J]. J. Am. Chem. Soc., 2020, 142(49):20814-20827.
[11] Qian, J., Adams, B. D., Zheng, J., et al. Anode-free rechargeable lithium metal batteries[J]. Adv. Funct. Mater., 2016, 26:7094-7102.
[12] Beyene T T., Bezabh H K., Weret M A., et al. Concentrated dual-salt electrolyte to stabilize Li metal and increase cycle life of anode free Li-metal batteries[J]. J. Electrochem. Soc., 2019, 166(8):1501-1509.
[13] Locally concentrated LiPF6in a carbonate-based electrolyte with fluoroethylene carbonate as a diluent for anode-Free lithium metal batteries[J]. ACS Appl. Mater. Interfaces, 2019, 11: 9955-9963.
[14] Sahalie N A, Assegie A A, Su W N, et al. Effect of bifunctional additive potassium nitrate on performance of anode free lithium metal battery in carbonate electrolyte[J]. Journal of Power Sources, 2019, 437: 226912
[15] HeiskanenS , Lucht B L . Using triethyl phosphate to increase the solubility of LiNO3in carbonate electrolytes for improving the performance of the lithium metal anode[J]. J. Electrochem. Soc., 2019, 166(12):2523-2527.
[16] 肖岩, 王宏刚, 李线绒,等. 无枝晶金属锂负极用钨青铜改性碳纤维膜集流体[J]. 中国科学: 技术科学, 2020, 50(05): 84-96.
[17] 齐新, 王晨, 南文争,等. 人造固态电解质界面在锂金属负极保护中的应用研究[J]. 材料工程, 2020, 048(006): 50-61.
[18] Lee Y G., Fujiki S., Jung C., et al. High-energy long-cycling all-solid-state lithium metal batteries enabled by silver-carbon composite anodes[J]. Nature Energy, 2020, 5: 348
[19] Yang C., Yao Y., He S., et al. Ultrafine silver nanoparticles for seeded lithium deposition toward stable lithium metal anode[J]. Adv. Mat., 2017, 29(38): 1702714
[20] Louli A J., Eldesoky A., Weber R., et al. Diagnosing and correcting anode-free cell failure via electrolyte and morphological analysis[J]. Nature Energy, 2020, 5(9): 1-10.
[21] Fan X., Chen L., Borodin O., et al. Non-Flammable electrolyte enables li-metal batteries with aggressive cathode chemistries[J]. Nature Nanotechnology, 2018, 13: 715-722.
Application study of hydrofluoroether electrolyte on anode-free lithium metal cells
Tao Kai, Liu Peiying, Wang Can
(Wuhan Institute of Marine Electric Propulsion, Wuhan 430064, China)
/cm, the silver-carbon anode-free cells maintain 96.2% average coulombic efficiency after 50 cycles at a rate of 0.5C, thereby ensuring excellent cycle performance. At the same time, the cells have a good capacity retention rate, the 1C rate discharge maintains an excellent capacity of no less than 85%.
TM912
A
1003-4862(2022)02-0043-04
2021-06-29
陶锴(1995-)男,硕士,研究方向:化学电源。E-mail:18627991757@163.com
