构树叶制备介孔TiO2/SiO2 复合材料的光催化性能及其动力学研究
2022-02-21李英萍高培元王美敬雷月香马永平
李英萍,高培元,王美敬,雷月香,陈 阵,马永平
(昆明理工大学 理学院,云南 昆明 650500)
二氧化钛(TiO2)具有较高的光催化活性、稳定的化学性质、无毒且成本低廉等优点[1-3],被广泛应用于空气净化[4]、污水处理[5]、太阳能转换[6]等多个研究领域,但TiO2因禁带宽度大(3.2 eV)、比表面积较低,对有机污染物的吸附性能差等特点,抑制了它的实际应用.研究者常通过贵金属沉积[7-8]、非金属掺杂[9]和半导体复合[10-12]等方法来提高TiO2的光催化活性,而且以化学模板制备TiO2/SiO2复合材料对TiO2进行改性[13-17].化学模板法制备方法简单,但所制备的催化剂不仅结构单一,成本较高,而且会进一步增加对环境的污染.然而,生物模板技术是一种几乎“零成本”、环境友好且高效的新技术,可以同时实现生模板材料的结构复制和元素自掺杂.因此,利用生物模板技术构建TiO2/SiO2复合材料是提高TiO2光催化活性的重要手段之一,在光催化领域有着广泛的应用前景.Ma 等[18]以玉米的叶、根、茎、丝和壳5 种聚硅组织为生物模板,合成了具有生物形态的分级多孔TiO2/SiO2复合材料,显著提高了其吸附和光催化活性.Fatimah 等[19]以竹叶提取的SiO2为原料,采用溶胶−凝胶法成功合成了TiO2/SiO2复合光催化材料,通过光催化降解亚甲基蓝(MB)以考察其光催化性能,结果表明,TiO2的增加有利于提高催化材料的光催化活性,其降解率均高于纯TiO2.Yan等[20]以芦苇、水葫芦和浮萍等水生植物叶片为模板材料,合成了具有介孔结构的生物形态TiO2/SiO2复合材料,实现了SiO2的自掺杂与结构的有效复制,在可见光范围内表现出较强的集光效率.Li等[21]以甘蔗叶、小麦、豇豆等绿叶为生物模板,把原始树叶中所含的氮自掺杂到样品中,制备出了具有生物形态的Morph-TiO2材料,与未添加模板的TiO2相比,不同叶片制备的生物形态TiO2在可见光范围内的吸收强度提高了103%~258%.尽管前人已经采用了多种生物模板制备TiO2/SiO2复合材料以提高其光催化性能,但以构树叶为模板制备TiO2/SiO2复合光催化材料却很少研究.构树叶具有速生、适应性强、分布广、易繁殖等优点,而且具有很好的饲用价值和药用价值,但是绝大部分构树叶还是处于未利用状态,造成了资源的重大浪费.
本研究以构树叶叶片为生物模板和硅源,以钛酸四丁酯为前驱体,通过改变前驱体浓度制备出了具有生物形态的介孔TiO2/SiO2复合光催化材料,并考察了其对罗丹明B 的光催化降解效果及动力学行为.本文的研究工作丰富了生物模板及光催化材料的种类和结构,为作物废弃物资源的利用探索新方法,并为解决水体中的有机染料污染问题提供新思路.
1 实验部分
1.1 试剂与仪器试剂:钛酸四丁酯(A.R.,天津市致远化学试剂有限公司),无水乙醇(A.R.,天津市致远化学试剂有限公司),罗丹明B(A.R.,海试剂产总第三分厂),盐酸(A.R.,成都市科隆化学品有限公司).
仪器:陶瓷纤维马弗炉(MFLC−7/10P 型,天津市泰斯特仪器有限公司),离心机(800 型,常州翔天实验仪器厂),紫外−可见分光光度计(UV−2500型,日本岛津),紫外灯(λ=254 nm,32 W),X 射线粉末衍射仪(XRD,Empyrean),X 射线荧光光谱仪(XRF,AxioSmAX),傅里叶变换红外光谱仪(FTIR,TENSOR 27),扫描电子显微镜(SEM,Phenom Prox),高分辨场发射透射电子显微镜(HRTEM,Tecnai G2 TF30),多功能扫描成像光电子能谱仪(XPS,PHI5000,ULVAC−PHI),多功能吸附仪(BET,MFA−140),紫外−可见近红外分光光度计(UV Vis−DRS,U−4100).
1.2 催化材料的制备将在校园内采摘的新鲜构树叶洗净表面灰尘后用蒸馏水润洗2~3 遍,自然晾干后,剪成约1 cm×1 cm 大小留存备用.将剪好的构树叶放入质量分数为5%的HCl 溶液中浸泡24 h 进行预处理,后取出蒸馏水洗至pH 成中性,放在托盘中自然晾干,把预处理且干燥的构树叶作为硅源.称取4 g 构树叶,依次放入混匀的钛酸四丁酯(TBOT)−乙醇体积比为0/80、2.6/80、4.0/80、5.5/80、7.0/80、8.6/80 的前驱体溶液中,然后放在避光环境下浸渍24 h,取出浸泡后的构树叶(TBOT/SiO2),用无水乙醇和蒸馏水洗去表面残留的离子,于50 ℃烘箱中干燥过夜.将干燥后的TBOT/SiO2放入马弗炉内以1 ℃/min 的速率升温至500 ℃并维持该温度3 h,共合成6 个催化剂,掺杂TiO2的质量分数w(TiO2)分别为0、2.6%、4.0%、5.5%、7.0%和8.6%,编号为:0−TiO2、2.6−TiO2、4.0−TiO2、5.5−TiO2、7.0−TiO2和8.6−TiO2.
1.3 光催化实验本实验通过对罗丹明B(RhB)染料的降解,考察所制备材料的光催化活性.向烧杯中加入50 mL 10 μmol·L–1的RhB 溶液和20 mg催化材料,在暗室中搅拌60 min,建立吸附−解吸平衡以消除吸附干扰因素.开启紫外灯(254 nm,32 W)对罗丹明B 溶液进行光催化实验.每隔15 min 后取适量溶液,高速离心后取上层清液,用紫外−可见分光光度计测定其在553 nm 处的吸光度A,根据公式(1)计算罗丹明B 的降解率(η):
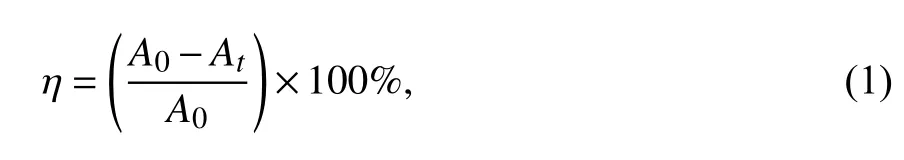
式中:A0和At分别表示暗吸附平衡和光照一定时间t后罗丹明B 的吸光度.
2 结果与讨论
2.1 XRF 分析通过X 射线荧光光谱(XRF)测量估算样品中的元素成分和质量分数如表1 所示.从表1 中我们可以看出,在0−TiO2材料中含有的大部分元素为O 和Si;然而,在5.5−TiO2材料中,除主要含有O 元素和Si 元素,Ti 元素质量分数也明显增加,其值为44.54%,说明TiO2成功浸渍到树叶模板中,并实现了模板元素的“自掺杂”,合成了TiO2/SiO2复合材料(因为树叶中离子含量多且较为复杂,经盐酸预处理并掺杂TiO2后还含有少量S、Ca、Mg、Fe、Na、K 等元素,其原因可能是用5%盐酸预处理后尚有离子残留).

表1 XRF 表征样品中的元素质量分数(%)Tab.1 The elementmass fraction of the samples estimated from XRF measurement(%)
2.2 XRD 分析为确定5.5−TiO2催化材料的晶相,本研究采用粉末X 射线衍射(XRD)对催化剂进行了表征,图1 为5.5−TiO2材料的X 射线衍射图.其中2θ值位于25.30°、37.79°、48.03°、53.88°、55.05°和62.68°处的衍射峰分别对应于(101)、(004)、(200)、(105)、(211)和(204)锐钛矿TiO2(JCPDS:21−1272)的晶相[22-24].在XRD 谱图中没有二氧化硅或硅酸盐的衍射峰,说明该样品材料中的二氧化硅结构与原始树叶一样,依然为非晶态.检测结果表明,样品中的TiO2主要相为锐钛矿相.
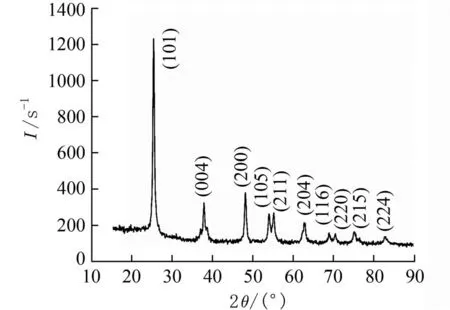
图1 5.5−TiO2 材料的XRD 谱Fig.1 XRD spectrum of 5.5−TiO2 material
2.3 FTIR 分析图2 为不同催化材料的FTIR 谱图.在500~600 cm−1范围内是典型Ti―O―Ti 的伸缩振动,对应锐钛矿相TiO2,而且随着TiO2含量的增加,Ti―O―Ti 峰强逐渐升高.在1 096 cm−1、803 cm−1和468 cm−1处的峰分别与Si―O―Si 不对称、对称伸缩振动以及弯曲振动有关[25].在3 000~3 500 cm−1范围内出现了较强的宽峰,归因于样品表面吸附O―H 引起的[26].最后,可以发现在952 cm−1处有一个非常微弱的因Ti―O―Si 键连接的吸收峰,进一步说明SiO2与TiO2的相结合[25,27-28].
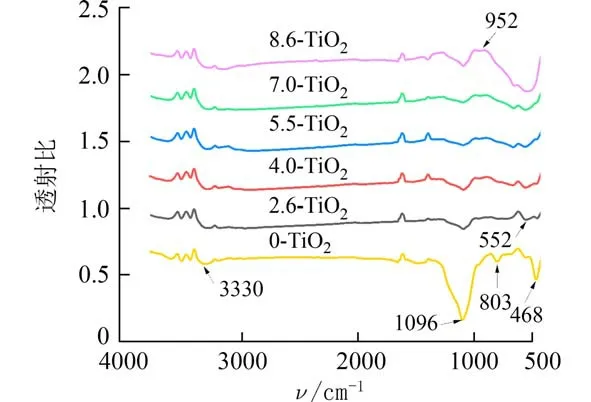
图2 不同催化材料的FTIR 谱Fig.2 FTIR spectra of different catalytic materials
2.4 SEM/EDS 分析图3(a)~(c)是0−TiO2样品的SEM 图,它的表面结构由微孔组成,由多个近似多边形的凹面形成了“莲蓬状”结构.图3(d)~(h)是5.5−TiO2催化剂的SEM 和EDS 图.如图3(e)所示,该材料也与图3(b)一样具有“莲蓬状”微观结构,与原始树叶相似,其结构不太完整,可能是由于高温煅烧过程导致莲蓬部分脱落.对比图3(c)与图3(f)的SEM 图可以发现,在w(TiO2)=0 时没有纳米球,掺杂w(TiO2)=5.5%后形成了较均匀的纳米球,而且从图3(h)可知,该纳米球中存在O、Ti 和Si元素,说明成功合成了TiO2/SiO2复合材料,与XRF 和FTIR 谱图分析结果一致.

图3 0−TiO2(a)~(c)和5.5−TiO2(d)~(h)催化剂的SEM/EDS 图Fig.3 SEM/EDS images of(a)—(c)0−TiO2 and(d)—(h)5.5−TiO2 catalysts
2.5 TEM 分析图4(a),(b)为5.5−TiO2样品的TEM 图.从图4(a)中可以观察到该催化材料主要由纳米小球组成,其平均粒径为500 nm,还可在图中隐约观察到小球周围有树叶的微观形貌镶嵌其中,与SEM 观察一致.图4(b)为催化材料的HRTEM图,在图中可以发现d=0.35 nm 的晶格条纹对应锐钛矿型TiO2的(101)晶格平面,与XRD 分析结果一致.

图4 5.5−TiO2 催化材料的TEM 图Fig.4 TEM image of 5.5−TiO2 catalytic material
2.6 BET 分析5.5−TiO2催化材料的氮气吸附−解吸等温线如图5(a)所示.根据IUPAC 的分类,该氮气吸附−解吸等温线为Ⅳ型,具有H3 滞后回线,其原因可能是颗粒聚集产生的堆积孔[29].测得该材料的BET 比表面积为50.42 m2/g.图5(b)为相应材料的Barrett-Joyner-Halenda(BJH)孔径d分布图,从图中可得知催化材料的平均孔径为7.2 nm,属于介孔材料.其介孔结构使光照与催化剂表面、催化剂表面与罗丹明B 目标分子的接触更加充分,从而有效促进了罗丹明B 有机废水的降解[30].
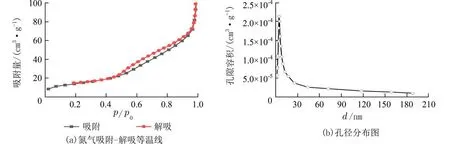
图5 5.5−TiO2 材料的氮气吸附−解吸等温线和孔径分布图Fig.5 Nitrogen adsorption−desorption isotherm and pore size distribution of 5.5−TiO2material
2.7 XPS 能谱分析为进一步研究所合成5.5−TiO2催化材料中元素的化学组成和状态,进行了X 射线光电子能谱(XPS)分析,结果如图6 所示.由图6(a)可知,材料中主要有C、O、Ti、Si 等元素存在.对于C1s 光谱(图6(b)),在283.39、284.86 和288.7 eV处观察到峰值,分别属于C―Si 键、C―C 或C―H 键、C=O 键和Ti―O―C 键[31-34].图6(c)所示的O1s 谱分为3 个峰,在532.49 eV 和530.95 eV 处属于Si―O―Si,在529.19 eV 处属于Ti―O―Ti 或Ti―O―Si,其低强度的信号峰归因于表面硅醇基团(Si―OH)引起的[35-36],与红外的结果一致.图6(d)为Ti2p 光谱,可以拟合为4 个组分(456.12、457.97、461.66 eV 和463.51 eV).其中457.97 eV 和463.21 eV 分别为Ti―O Ti2p3/2和Ti―O Ti2p1/2的峰,说明TiO2的存在.而456.12 eV 和461.66 eV 分别对应于Ti―S Ti2p3/2和Ti―S Ti2p1/2的峰,其归因于部分S 元素与Ti 元素形成了TiS2[37],综上2 个峰均相差5.6 eV,表明Ti 以Ti4+形式存在.

图6 5.5−TiO2 催化材料的XPS 谱图Fig.6 XPS spectrum of 5.5−TiO2 catalytic material
2.8 UV–Vis DRS 分析纯TiO2和5.5−TiO2催化材料的UV−Vis DRS 和带隙能谱如图7 所示.由图7(a)可知纯TiO2的光吸收范围主要在300~400 nm,其吸收边际在387.8 nm,5.5−TiO2催化材料吸收边际红移到404.2 nm 附近,吸收边际发生了约16 nm的红移.由图7(b)可知,纯TiO2和5.5−TiO2材料的禁带宽度分别为3.22 eV 和3.08 eV,可以看出其5.5−TiO2材料的禁带宽度较TiO2有所减小,拓展了可见光响应范围,提高了催化剂的量子产率,进而提高了其光催化活性.
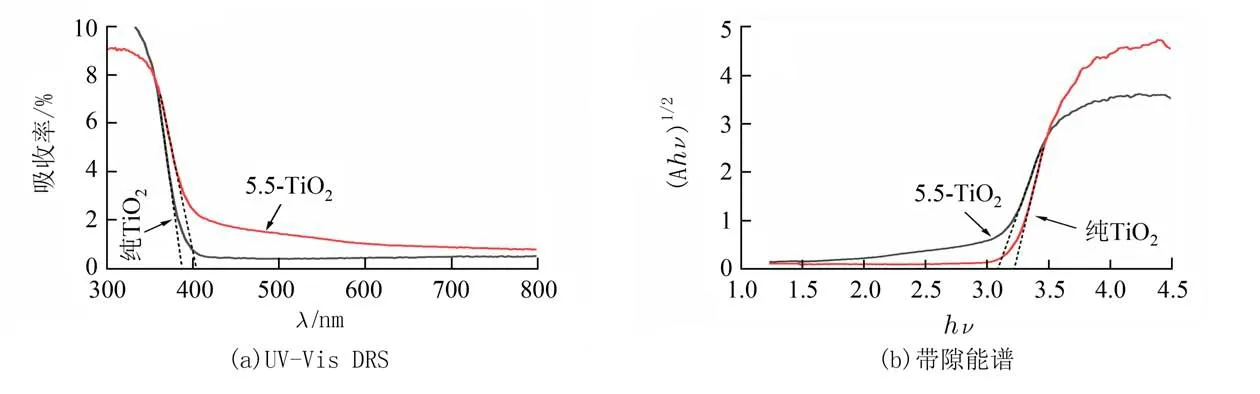
图7 5.5−TiO2 和纯TiO2 样品的UV−Vis DRS 和带隙能谱Fig.7 UV−Vis DRS and band gap energy spectra of 5.5−TiO2 and pure TiO2 samples
2.9 光催化性能分析图8 为在不同催化剂存在下罗丹明B 溶液的吸光度随光照时间的变化曲线.从图8(a)0−TiO2样品中可以看出,罗丹明B 的吸光度随着光照时间的延长变化较小,光照时间为90 min 时,罗丹明B 仅降解了39.8%.由图8(b)~(f)可以看出,在不同TiO2掺杂量合成的TiO2/SiO2催化剂存在时,随着光照时间的延长,罗丹明B 溶液的吸光度变化明显,光照时间为90 min 时,罗丹明B 的降解率均在90%以上.
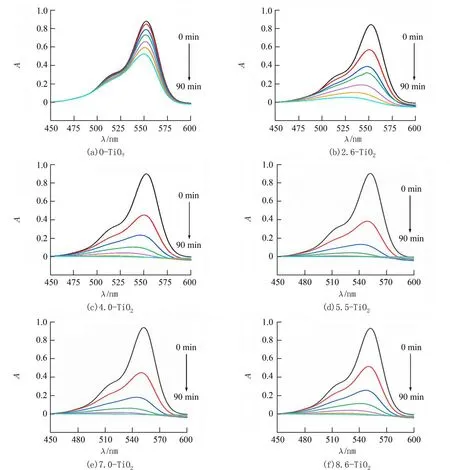
图8 在0−TiO2、2.6−TiO2、4.0−TiO2、5.5−TiO2、7.0−TiO2 和8.6−TiO2 催化剂存在下RhB 溶液的吸光度随光照时间的变化曲线Fig.8 The absorbance curve of RhB solution with light time in the presence of 0−TiO2,2.6−TiO2,4.0−TiO2,5.5−TiO2,7.0−TiO2 and 8.6−TiO2 catalysts
图9 表示不同催化剂存在下罗丹明B 溶液的降解率随光照时间的变化.由图9 中可以看出,不同催化剂在同一光照时间内对RhB 溶液的降解率不同.在光照时间为90 min 时,不同催化剂对RhB溶液的降解效果由高到低的顺序依次为:5.5−TiO2(99.7%)>7.0−TiO2(99.5%)>4.0−TiO2(99.1%)>8.6−TiO2(99.0%)>2.6−TiO2(91.9%)>0−TiO2(39.8%).
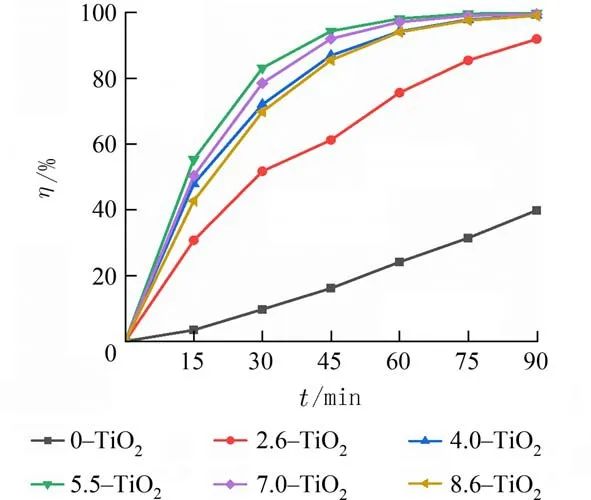
图9 在不同催化剂存在下RhB 溶液的降解率随光照时间的变化Fig.9 The change of degradation rate of Rhodamine B solution with different illumination time in the presence of different catalysts
其中5.5−TiO2催化剂对RhB 溶液降解效果最好,其光催化活性是0−TiO2样品的2.5 倍.结果表明,在以构树叶叶片为硅源中掺杂合适量的TiO2,可以增加对载流子的俘获数量,提高表面电荷迁移的速率,从而促进催化降解过程的进行[38].
2.10 动力学分析分别配制5、10、15、20、25 μmol·L−1和30 μmol·L−1RhB 溶液,测定其吸光度,得到标准曲线如图10(a)所示.从图中可以看出,本研究中所考察的罗丹明B 浓度均在线性范围以内.
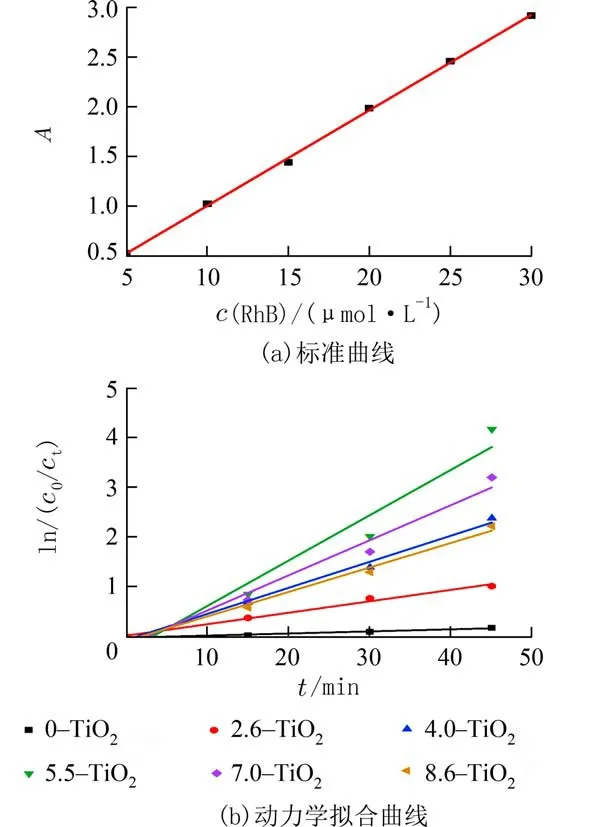
图10 RhB 溶液标准曲线和紫外光下不同催化剂降解RhB 溶液的动力学曲线Fig.10 Standard curve of RhB solution and the kinetics curves of RhB solution degradation by different catalysts under ultraviolet light
目前绝大多数的光催化反应动力学模型都符合一级动力学模型[21,36,39],满足方程

式中:c0和c分别是指光照反应前和反应t时罗丹明B 的浓度;k为一级反应速率常量,t为反应时间.
图10(b)是不同催化材料紫外光催化降解RhB溶液的动力学拟合曲线.从图可知,ln(c0/ct)~t具有较好的线性关系,说明该反应符合一级动力学模型.5.5−TiO2催化材料显示了最高的表观速率常量k=9.11×10−2min−1,分别是7.0−TiO2(7.05×10−2min−1)、4.0−TiO2(5.23×10−2min−1)、8.6−TiO2(4.92×10−2min−1)、2.6−TiO2(2.3×10−2min−1)和0−TiO2(4.2×10−3min−1)的1.29、1.74、1.85、3.96 倍和21.69 倍.上述结果表明,掺杂TiO2可以大大提高其光催化活性[34].
3 结论
(1)本文以构树叶为生物模板和硅源,以钛酸四丁酯为前驱体,采用浸渍法合成了不同TiO2掺杂量,具有介孔结构的生物形态TiO2/SiO2复合材料.形貌和结构分析表明,生物形态TiO2/SiO2复合材料成功地复制了树叶的微观形貌,并在其中形成了平均粒径为500 nm 的纳米球.
(2)TiO2/SiO2复合材料是一种有效的紫外响应光催化剂,在光照时间为90 min 时,5.5−TiO2催化材料对罗丹明B 的降解率可达99.7%,是0−TiO2材料的2.5 倍.生物二氧化硅的自掺杂、介孔结构以及纳米小球的形成等都有效提高了光催化活性.
(3)动力学研究表明,紫外光催化降解罗丹明B 符合一级动力学模型.
