三维重建在胸腔镜肺段手术的临床应用
2022-02-19汤天生
聂 军,周 伟,汤天生
(皖南医学院第一附属医院胸心外科二病区,安徽 芜湖 241001)
随着高分辨率螺旋CT(High-resolution spiral CT,HRCT)在肺癌筛查的广泛应用,越来越多的以磨玻璃影(Ground-glass opacity,GGO)为主的早期肺癌被筛查出。临床上的回顾性研究已证实,胸腔镜解剖性肺段切除术对于治疗早期肺病变具有独一无二的优势,它不仅能从肿瘤学上达到和胸腔镜肺叶切除术同等的疗效,更能最大限度保留患者的正常肺组织,能相对缩短患者术后恢复周期和提升术后生活质量[1-2].但肺段切除术较肺叶切除术技术更复杂[3],如何准确辨识肺段血管、支气管的分支及毗邻结构,准确定位肺结节所处肺段的空间位置成为手术困难所在。而三维重建技术能很好地帮助术者行术前手术规划及术中实时导航,进行精准肺段切除。
1 资料与方法
1.1 一般资料 回顾性分析我院胸心外科二病区2018年6月至2021年12月行胸腔镜肺段手术50例患者的临床资料。其中男21例,女29例。术前均行胸部薄层CT或胸部增强CT扫描,肺功能、心电图、肺癌相关及常规检查等均无手术禁忌证。纳入标准:⑴胸部CT示肺部结节直径≤2 cm且磨玻璃样成分≤50%;⑵术前检查评估均未发生肿瘤远处转移情况;⑶术前未接受新辅助放化疗患者;⑷术后组织病理学分期为良性或未超过Ⅰa期非小细胞肺癌(根据国际抗癌联盟第8版肺癌TNM分期);⑸临床病例资料完整;⑹病灶位于肺中野,不便于楔形切除。
1.2 手术方法 术前采集层厚为1 mm的胸部薄层CT或增强CT数据,将胸部二维CT图像信息以DICOM格式导入英库科技公司软件系统,通过图像加载处理,重建靶区肺段支气管、动静脉血管的三维模型,评估肺结节的三维空间毗邻关系,有无血管、支气管的变异,肺结节所处肺段的空间位置,进行精准的术前规划。术中结合术前三维重建,处理靶段血管、段支气管,使用“改良膨胀萎陷法”识别段间平面,使用切割缝合器处理段间平面,系统性纵隔淋巴结采样。要求切缘与肿瘤间距>2 cm,或大于肿瘤最长径。对于靠近肺段边界的肿瘤,则行联合肺段切除以保证足够切缘。当多发肺结节时,行肺段联合切除或肺段联合楔形切除术。术中、术后预防性使用2 d抗生素并给予化痰、镇痛等对症处理。复查胸部X线片显示肺复张良好、无明显漏气,24 h胸腔引流量≤200 mL即拔除引流管。所有患者术前均已签署知情同意书。
1.3 数据收集 查阅病例,收集50例患者的术前一般临床资料包括性别、年龄、吸烟史、症状、结节最大直径及部位、三维重建影像、术中手术方式及肺段切除分布、术后病理、围手术期数据(包括手术时间、术中出血量、术后胸管引流量、术后拔管时间、术后住院时间及并发症等)。
1.4 统计学方法 数据采用SPSS 22.0软件进行分析,计量资料采用±s表示,计数资料以n(%)表示,P<0.05为差异有统计学意义。
2 结 果
2.1 患者临床资料分析 本治疗组共纳入50例行肺段切除术、病变直径≤2 cm、病灶位于肺中野、不便于楔形切除患者。其中男性21例(42%),女性29例(58%),高龄患者(≥70岁)5例(10%),不吸烟患者37例(74%),无临床症状者32例(64%)。术后病理非典型腺瘤样增生2例(4%),原位腺癌10例(20%),微浸润型肺腺癌5例(10%),浸润型肺腺癌23例(46%),转移癌1例(2%)(系肾透皮细胞癌肺转移),其他良性病9例(包括炎性假瘤1例,硬化性血管瘤1例,结核球1例,淋巴结1例,其他炎性病变5例)。见表1。
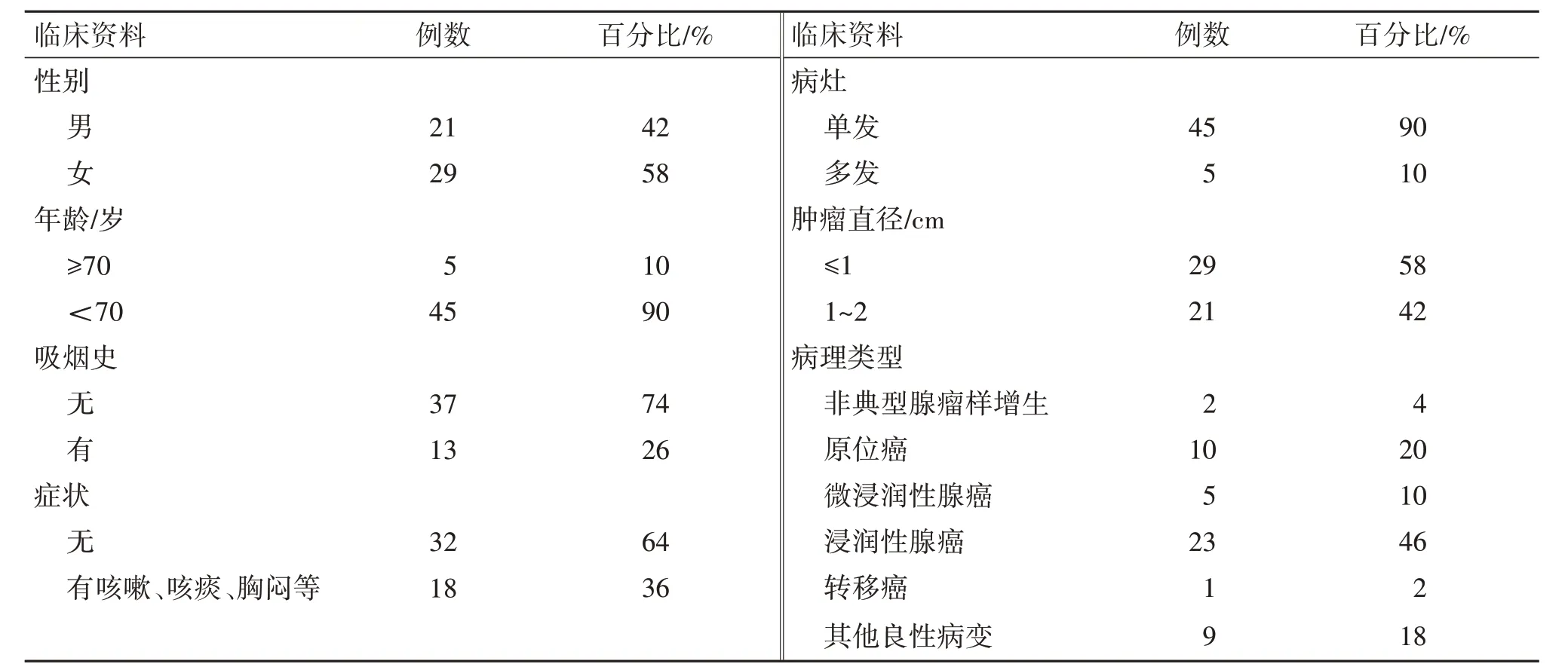
表1 术前患者临床资料
2.2 围手术期资料分析
2.2.1 术前手术规划 术前下载胸部CT影像的DICOM数据,使用英库科技公司软件进行三维重建。薄层CT平扫后重建29例,增强CT平扫后重建21例,辨识肺段血管、支气管的分支及毗邻结构,以结节为中心显示出2 cm安全切缘,手术小组进行术前讨论,规划出最佳的手术方案及手术路径(图1)。部分肺部结节较小、较淡,考虑术中难以快速定位病灶,则在CT引导下使用Hook-wire带钩钢丝进行术前定位。
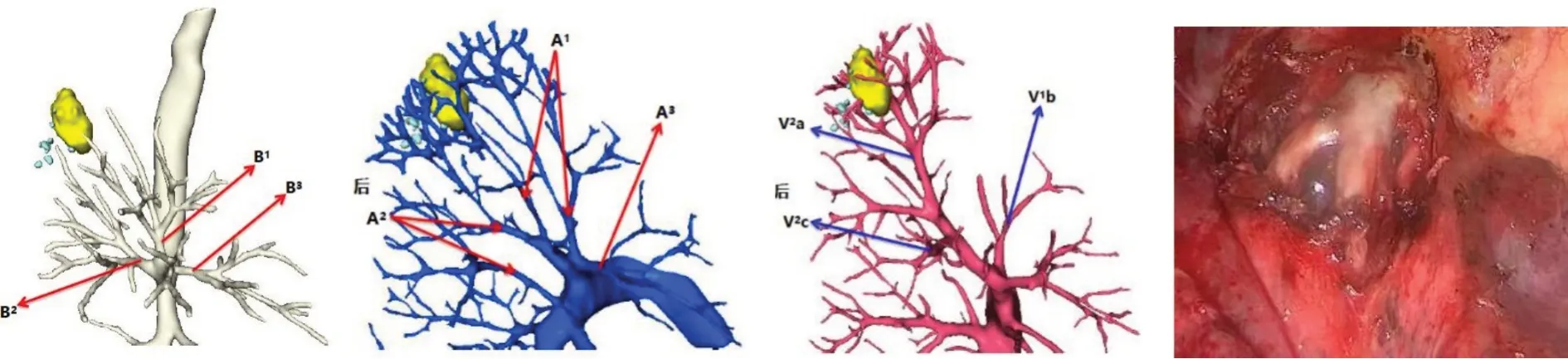
图1 术前三维重建及术中对比举例图片
2.2.2 术中手术方式 行单孔或单操作孔手术,使用“膨胀萎陷法”识别段间平面,使用切割缝合器处理段间平面。单个肺段切除43例(86%),联合肺段切除6例(12%),同期行双侧肺段切除术1例(2%)。见表2。

表2 术中肺段切除分布
2.2.3 术中情况 中位手术时间139(54~275) min,中位术中出血量80(25~600) mL。中转开胸1例(2%),原因为分离肺门血管意外出血。
2.2.4 术后并发症及随访 中位术后住院时间4.6(2~19) d。术后胸管引流量250(160~720) mL,术后拔管时间3.8(2.8~17)天,术后发生并发症患者8例(16%),其中最常见并发症为持续肺漏气3例(6%),其他并发症包括肺部感染2例(4%)、肺复张不全2例(4%)、胸腔积液1例(2%)。本组病例无围术期死亡。末次随访时间为2021年12月8日,术后随访0.5~30(13.6±9.8)月,无并发症发生,胸部CT等检查提示1例患者(肾透皮细胞癌肺转移)术后24个月出现左下肺0.7 cm新增病灶,转移待排,其余患者无肿瘤复发、转移。
3 讨 论
随着人们健康意识的不断增强及低剂量螺旋CT的普及化程度越来越高,肺部小结节包括磨玻璃样影不断被发现,因此早期肺癌检出率也越来越高[4]。近年来,部分学者发现肺癌患者中非吸烟女性比例较前升高,这种趋势在肺腺癌患者中表现更加明显。无症状肺癌患者比例明显升高,在本研究中也体现出这种趋势,且早期肺癌在70岁以下肺癌患者比例明显升高,这与胸部CT在体检普查的广泛应用有关。随着微创外科理念的不断深入发展及胸腔镜手术技术的不断提高,早期肺癌的治疗手段也不断进步,既往的标准肺叶切除加系统性淋巴结清扫部分被解剖性肺段切除术取代,国内外学者进行了探讨研究,结果提示对于直径<2 cm的Ⅰa期NSCLC行解剖性肺段切除是切实可行的,生存分析提示,其术后长期生存率与肺叶切除术并未显示出明显差异,特别是一些特殊病理类型比如原位癌及微浸润性腺癌,其术后特异性生存率甚至接近100%[5]。
近年来,胸腔镜下解剖性肺段切除技术不断进步,在完全切除病变的同时能最大化保留正常肺组织,特别是对于孤立性转移肿瘤、良性病变和周围型早期肺癌,因此肺段切除术是一种理想的胸腔镜手术治疗方法[6-8]。然而,肺段切除术也遇到一些技术困难,比如肺段之间缺少明显的解剖学间隙、解剖的深度、肺段动静脉及所属的支气管存在变异[6],结节所在肺段的位置不同,有时候无法保证保留足够的手术切缘,因而增加了术中准确且快速辨识肺段结构的难度,且进一步影响了手术时间,增加了手术并发症,这些问题亟待解决。解剖性肺段切除术在技术上比肺叶切除术要求更高,术中主刀医师必须能准确离断靶肺段支气管及肺段动静脉,确保肿瘤手术切缘阴性,进而降低肿瘤复发的可能性,这需要术者在术前对患者肺部解剖结构具备精准把握与理解。
三维重建技术通过采集CT扫描获取的图像进而利用软件实施精准的三维重建,最终还原出3D图像,术者还可利用软件将肺段所属的不同结构比如分支气管、肺静脉、肺结节和肺动脉等进行着色处理,所得到的图像能360°旋转,经多角度、多层次观察判断,术者能找到最佳手术路径,制定个性化的手术方案及缩短术中思考、判断时间,提高胸腔镜手术的精确性[9-11]。本研究中,重建得到的三维图像与术中解剖情况基本相符,且术前三维重建结节部位定位成功率为100%。术前根据三维重建图片识别判断结节与重建血管、支气管的关系,术中依据肺段血管、支气管相对固定解剖关系指导手术,达到直观、准确辨别所需切除的肺段、切除范围、需保留与切除的血管的目的。本研究提示,术前三维重建在肺间静脉判断上有明显优势,能最大限度避免误切及其可能会导致的术后咯血等并发症[12-13],本研究患者术后并发症中均无咯血现象。
综上所述,三维重建及虚拟手术规划在胸腔镜解剖性肺段切除中围术期疗效显著。不但可提高手术的准确率和安全性,且能降低技术门槛,更直观地展示解剖结构的空间关系,有助于肺段切除术的开展,具有临床应用和推广价值。
