听力损伤竟能逆转?双载体基因疗法,全球遗传性听力患者或将受益
2022-02-19
听力受损作为一种常见性疾病,正受到越来越多的关注。
2021年3月,《柳叶刀》曾公布一项关于听力受损的研究报告,“1990年~2019年全球听力损失患者逐年增加,预计2050年将达到24.5亿。”
由此可见,听力受损并不是我们想象中的只存在老年群体中,而是与所有人都息息相关。事实上,除了年龄增长这一关键因素外,基因遗传也是导致听力损伤的重要原因之一。
近日,波士顿儿童医院首创一种基因治疗技术,成功在小鼠体内实现了听力逆转,将其严重受损的听力恢复到正常水平。
2021年12月15日,相关研究结果以论文形式发表。该论文以《双载体基因治疗可恢复DFNB16听力损失小鼠模型的耳蜗放大和听觉灵敏度》为题,通讯作者由哈佛医学院耳鼻喉科和神经病学教授杰弗里·霍尔特担任。

相关论文
据了解,先天性听力受损的原因各不相同,至少与100个不同基因的突变有关,但高达16%的遗传性听力损失可以追溯到同一个基因,即著名的STRC基因。
“STRC是一种编码蛋白质立体纤毛蛋白的基因,同时,它也是DFNB16遗传性耳疾的第二个最常见的原因。”霍尔特表示。
哺乳动物的内耳已经进化出一种独特的能力,可以放大柔和的声音,减弱其对响亮声音的响应,并在频域中快速调整其响应,这种能力又被成为耳蜗放大功能。但携带STRC突变的患者却完全丧失了耳蜗放大能力,这导致他们听觉灵敏度降低,频率辨别和言语感知困难。
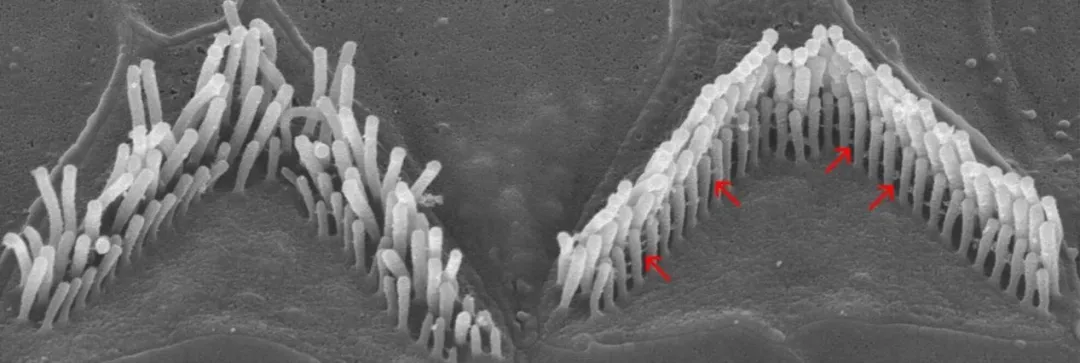
电子显微镜下的感觉外毛细胞
那么,该如何通过基因治疗来应对STRC突变呢?
说到这里,就不得不介绍一下人们能听到声音的原因。
我们之所以能够听到各种各样的声音,取决于耳蜗中感觉外毛细胞的活动。其一般都与耳朵的盖膜接触,盖膜会响应声音而振动,然后将这些振动转换为发送到大脑的信号。
而毛细胞若想和盖膜相接触,还需要立体纤毛蛋白的帮助,它会让毛细胞微绒毛以有组织的束形式聚拢起来,从而使它们的尖端可以接触盖膜。
“但如果立体纤毛素发生突变,你就没有这种接触,所以毛细胞不会受到适当的刺激。不过重要的是,毛细胞仍然保持功能,因此它们可以接受基因治疗。”霍尔特说。
为了提供健康的立体纤毛素基因,该团队使用了一种有效靶向毛细胞的合成腺相关病毒(AAV)。
然而,一个新的挑战摆在了该团队的面前。由于立体纤毛素基因的长度约为6200个DNA碱基对,但AAV的容量仅为4700个碱基对,这导致立体霉素的基因太大而无法放入基因治疗载体。
为了解决这一重大未满足的需求,研究团队设计了一种双载体蛋白质重组策略来替代野生型的STRC基因在小鼠的外毛细胞中。
首先,该团队将小鼠的STRC基因一分为二,并分别放入到两个独立的AAV中,再通过蛋白质重组技术将它们连接起来,但这种方法被发现是无效的。
“然后我们意识到蛋白质的开头有一小段氨基酸,就像一个‘地址’,将蛋白质引导到细胞中的适当位置。”
于是,该团队将这个氨基酸信号添加到被分成两半的蛋白质上,再将其成功地结合在一起。最终,研究人员发现小鼠的立体纤毛蛋白和能够接触盖膜的正常毛束得到了有力的恢复。

研究人员使用了两种类型的听力测试:一种类似于婴儿听力测试,另一种是使用头皮上的电极来测量听觉脑干对一系列声音频率和强度的反应。
在测试中,他们发现老鼠对微妙的声音更加敏感,并且耳蜗放大的功能在一定程度上得到了加强,而在一些DFNB16遗传性耳疾小鼠中,其听力恢复到正常水平。
对此研究结果,霍尔特表示,“结果非常显著,这是第一个使用双载体基因疗法靶向感觉外毛细胞来恢复听力的例子。我们认为这将为治疗提供一个广阔的机会窗口——从婴儿到听力损失的成年人。”
下一步,该团队将不再采用小鼠样本,而是选择在人类内耳细胞中进行测试,这些细胞全部来自STRC听力受损患者,并被完好地保存在培养皿中。相比于小鼠,该测试显然更能判断基因疗法的实用性。
如果该基因疗法能够再次发挥功效,使人类内耳细胞在组织水平上恢复听觉功能,霍尔特将向美国食品药品监督管理局申请在人体中进行测试的许可。
波士顿儿童医院耳鼻喉科医学博士艾略特·希勒表示,在美国,约有10万名患者携带STRC突变,而全球范围内大概有230万名患者,他们都将可能从这种疗法中受益。
