刺参(Apostichopus japonicus)幼参对高温和低盐协同胁迫的生理响应:生长和诱导型热休克蛋白基因表达
2022-02-18于姗姗李学玉何振平王青林孙桂清付仲
于姗姗 ,李学玉 ,何振平,王青林,,孙桂清,付仲
(1.河北科技师范学院 海洋资源与环境学院,河北 秦皇岛 066004;2.河北省海洋动力过程与资源环境重点实验室,河北秦皇岛 066004;3.秦皇岛市海洋生境与资源重点实验室,河北 秦皇岛 066004;4.河北省海洋生物资源与环境重点实验室,河北 秦皇岛 066004;5.河北省海洋与水产科学研究院(河北省海洋渔业生态环境监测站),河北 秦皇岛 066004)
1 引言
刺参(Apostichopus japonicus)为浅海底、温带物种,主要分布于35°~44°N 的西北太平洋沿岸[1]。作为海洋生态系统的重要组成部分,刺参能够分解海底生物碎屑,在碳循环中发挥着极其重要的作用[2-4]。此外,由于刺参具有极高的药用滋补作用,其消费市场需求不断升高,养殖产量和增养殖规模随之增长,其已成为我国北方和东南沿海重要的养殖种类之一[5]。据统计,2020 年全国刺参产量为1 965 64 t(占海水养殖总量的0.92%),年总产值高达315 亿元(占海水养殖总产值的8.20%)[6]。但是,作为一种水生变温生物,刺参对高温和低盐等环境胁迫非常敏感,2013 年、2016 年和2018 年夏季的极端高温天气和暴雨导致了池塘养殖刺参的大幅减产甚至绝产。然而,全球气候变化背景下的极端高温天气和短时强降雨频发,导致高温期大量淡水注入刺参池塘,从而使养殖海水盐度大幅降低,而且这种持续的高温和低盐状况在河口地区更严重[7-8],给刺参池塘养殖带来了严峻的挑战。因此,研究极端环境下刺参的生理响应,对刺参产业的绿色发展具有重要的指导意义。
刺参的适宜生长温度为10~20℃,且随着刺参规格的增大而降低,体长为5~15 cm 的刺参的最适生长温度为10~15℃[9]。诸多研究表明[1,10-13],温度对刺参的生长、耗氧率、酶活力、摄食行为、肠道质量、配子的受精能力、热休克蛋白(Heat Shock Protein,HSP)表达等各方面都有显著的影响。盐度是影响水生生物的另一个重要生态因子,作为狭盐性的棘皮动物,刺参对盐度的耐受程度有限,其适宜生长盐度为28~34[14]。盐度变化能显著影响刺参的呼吸代谢、能量转换和生长等,当盐度低于22 时,可造成刺参大量死亡[15-16]。在遭受温度、盐度等环境因子胁迫时,水生生物体内会诱导产生HSP[17-18]。诱导型HSP 是指生物体在不利环境因素刺激下应激合成的一组在结构上高度保守、具有重要生理功能的特殊蛋白质分子家族。它最主要的功能是作为分子伴侣,可修复错误折叠蛋白、降解变性蛋白等[19-20]。研究表明[10,21],hsp70和hsp90基因在刺参抵抗温度和盐度胁迫的过程中发挥重要的作用。热休克蛋白基因表达量与生物体的热耐受性有关,且生物前期经历的高温胁迫能诱导热休克蛋白高表达来防止蛋白损伤和聚集[22-23]。长期环境胁迫对生物来说是一种驯化,是指通过实验诱导,使生物对某种生态因子的耐受性增强的过程[10,24]。这种胁迫能增加生物对新环境的适应性,特别是细胞结构和生理生化能随着环境条件的改变而改变[25]。温度和盐度单因子胁迫对刺参的影响已有报道[10,22,26],但由于hsp基因具有交叉耐受性,一种环境胁迫诱导产生的hsp基因不仅能够提高机体对该种胁迫的耐受性,同时也能增加对于其他环境胁迫的耐受能力[27-28]。因此,有必要研究多环境因子尤其是极端天气导致的持续性高温和低盐协同胁迫对刺参生长和诱导型热休克蛋白基因表达的影响。
为应对极端天气带来的挑战,刺参从业者们采取了提高池塘水位、安装增氧降温设备、排表层淡水等一系列措施,起到了一定的效果。提高刺参自身抵抗逆境的能力也是非常关键的一个环节,这需要科研工作者加强多环境因素胁迫下刺参响应机制相关的研究,进而探索提高刺参抵抗逆境能力的途径。因此,本研究通过分析高温和低盐长期协同胁迫(40 d)对刺参幼参生长和诱导型hsp70和hsp90基因表达的影响,探讨两个外源性因子对刺参的交互影响,从而为指导极端天气下刺参生产实践,促进刺参养殖产业的健康持续发展提供一定的理论依据。
2 材料与方法
2.1 实验材料
实验用刺参幼参购自山东省青岛市养殖场。选取体表无损伤且活力好的刺参幼参在温度为16℃,盐度为32 的海水中暂养两周。暂养期间每天足量投喂1 次配合饲料(主要成分:粗蛋白(18.58±0.23)%、脂肪(2.67±0.06)%、灰分(42.66±0.54)%、水分(9.94±0.17)%)。每天更换1/3~1/2 温度为16℃,盐度为32 的新鲜沙滤海水以保证养殖水质。暂养期间持续充气,光照周期设置为14 h∶10 h(白天∶黑夜),pH为7.8~8.2,氨氮含量低于0.24 mg/L。
2.2 实验设计
实验设置4 个温度梯度(16℃、20℃、24℃和28℃)和3 个盐度梯度(22、27 和32),共12 个组合,每个组合3 个重复。将经过暂养的216 头刺参幼参随机分配到36 个规格为450 mm×250 mm×350 mm(长×宽×高)的玻璃缸中,每缸6 头。采用水浴法并每天升高0.5~1℃的温度,采用向自然海水中添加曝气自来水的方法每天降低1~2 的盐度,直至到达实验设定温度和盐度,并在设定温度和盐度下持续40 d。
2.3 不同温盐协同胁迫下幼参的生长
刺参幼参饥饿24 h 后称量初始湿体重,平均体重为(3.541±0.046)g。实验期间每天足量投喂1 次配合饲料,每日换水1 次,换水前将沙滤海水调整到实验所需的温度和盐度。每20 d 称量体重1 次,实验持续40 d。实验结束后,刺参幼参饥饿24 h 后称重,并计算幼参每天的特定生长率(Specific Growth Rate,SGR),公式为
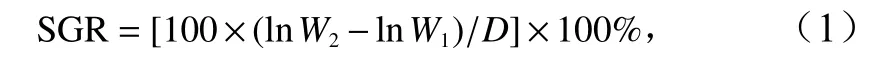
式中,W2和W1分别表示刺参幼参的末体重和初始体重;D为实验持续的时间。
2.4 诱导型热休克蛋白基因的表达
2.4.1 样品的获取
将经过40 d 高温和低盐协同胁迫的刺参幼参转移至温度为30℃,盐度为20 的海水中急性胁迫2 h,之后在温度为16℃,盐度为32 的自然海水中进行恢复。在恢复6 h 的每个处理组随机取4 头刺参,迅速保存于液氮中。并取自然海水中的刺参作为空白对照。带回实验室进行后续实验。
2.4.2 引物设计
本实验中选取的2 条基因(hsp70,hsp90)筛选自NCBI 刺 参cDNA 文 库(Ajhsp70,GH 985449;Ajhsp90,JF907619)。实验中使用的引物(Hsp70-F 和Hsp70-R,Hsp90-F 和Hsp90-R)见表1。以刺参的部分β-actin 序列(312 bp)作为内参基因,其引物序列来自文献[17]。

表1 用于本实验的引物序列Table 1 Primers used in this study
2.4.3 总RNA 提取和基因表达分析
利用Trizol 试剂从体重约为80 mg 刺参体壁组织中提取总RNA。cDNA 第一链利用Oligo dT18 作为引物合成。合成的第一链cDNA 通过内参基因PCR检验其是否可用。PCR反应体系25μL,包括:2.5μL10×PCR扩增缓冲液、1.6μLMgCl2(25mmol/L)、2.0μLdNTPs(2.5mmol/L)、各1μL的上下游引物(10pmol/mL)、15.875μL灭菌水、0.125μL(5U/μL)TaqDNA聚合酶以及1μLcDNA模板。hsp70和hsp90反应程序为94℃反应5 min,接着是94℃ 45 s,53℃ 45s,72˚C 1 min,30 个循环,最后72℃延伸10 min;内参基因反应程序为94℃反应5 min,接着是94℃ 45s,55℃ 45s,72˚C 1 min,28 个循环,最后72℃延伸10 min。PCR 产物使用EB 染色的1.2%琼脂糖凝胶电泳检测,为了确保PCR 反应的特异性,产物进行胶回收并测序。电泳图使用GeneTools 软件分析,基因相对表达量通过其电泳图中光密度值与内参基因光密度值的比值表示。
2.5 数据统计与分析
数据统计采用IBM SPSS Statistics 21.0 进行。用K-S 检验和Levene 检验分别对数据进行正态性和方差齐次性检验。应用双因子方差分析(Two-way ANOVA)分析温度和盐度协同胁迫对刺参体重、特定生长率以及热休克蛋白基因表达量的交互作用。采用Tukey’s 多重比较进行处理间的显著性检验,以p<0.05作为差异显著的标准。
3 结果与分析
3.1 高温和低盐协同胁迫对刺参幼参生长的影响
各组间刺参幼参的初始体重无显著差异(F11,24=0.401,p=0.942),经过40 d 实验,各组刺参幼参的末体重差异显著(F11,24=69.534,p<0.001)(表2)。在同一盐度下,刺参幼参的末体重随温度的升高而下降。在同一温度下,刺参幼参的末体重随盐度的降低也呈下降的趋势。其中温度为16℃、盐度为32 组的刺参幼参末体重最大,温度为28℃、盐度为22 组的末体重最小,并且在此处理组,刺参幼参出现死亡现象。双因子方差分析显示,温度和盐度对刺参幼参体重均有显著性影响(温度:F3,24=172.761,p<0.001;盐度:F2,24=114.546,p<0.001),且两者的交互作用显著(F6,24=2.917,p=0.028)(表3)。
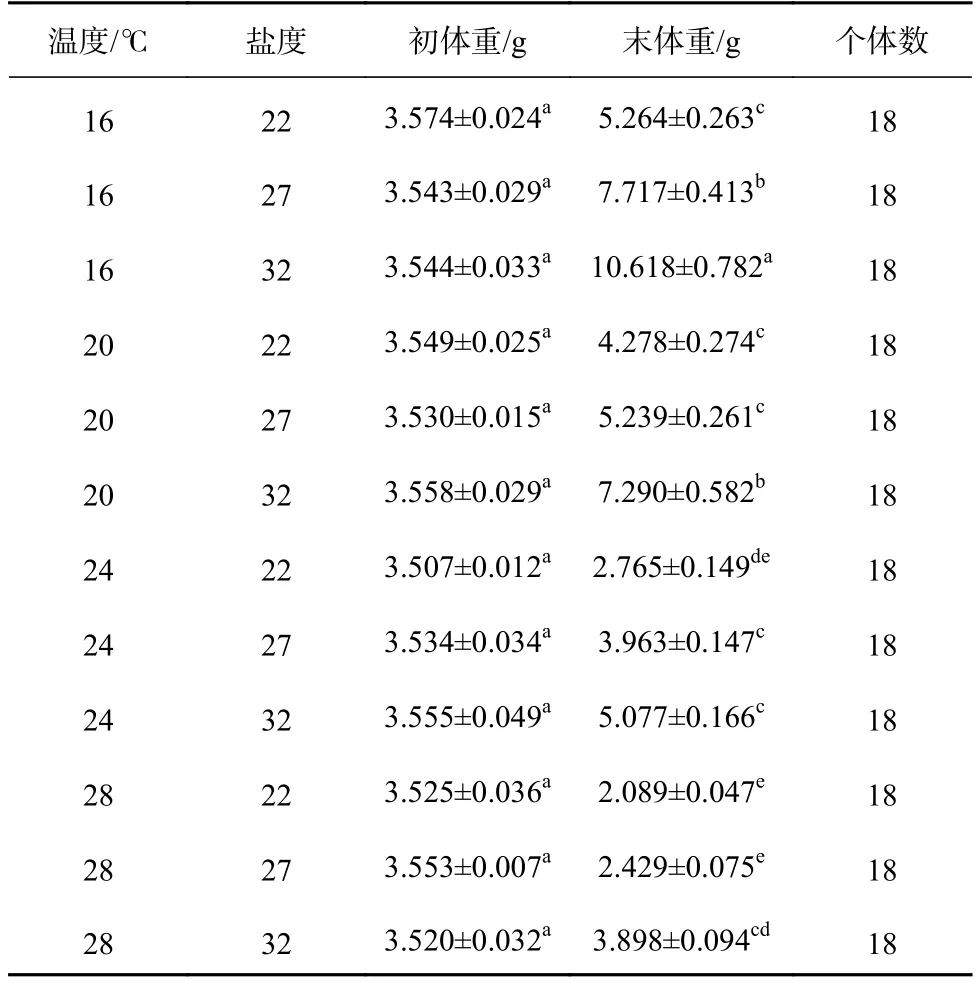
表2 高温和低盐协同胁迫对刺参幼参生长的影响Table 2 Effects of high temperature and low salinity collaborative stress on growth of juvenile Apostichopus japonicus
各处理组刺参幼参的特定生长率不同(图1)。从图上可以看出,经过40 d 实验,温度和盐度对刺参幼参的特定生长率影响差异显著(F11,24=87.132,p<0.001),在同一温度或盐度下,SGR 均随着盐度的降低以及温度的升高而下降。双因子方差分析显示,温度和盐度对刺参幼参的SGR 均有显著性影响(温度:F3,24=220.109,p<0.001;盐度:F2,24=143.439,p<0.001),但是两者的交互作用不显著(F6,24=1.874,p=0.127)(表3)。
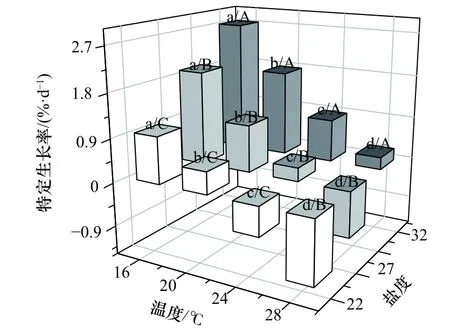
图1 高温和低盐协同胁迫对刺参幼参特定生长率的影响Fig.1 Effects of high temperature and low salinity collaborative stress on specific growth rate of juvenile Apostichopus japonicus
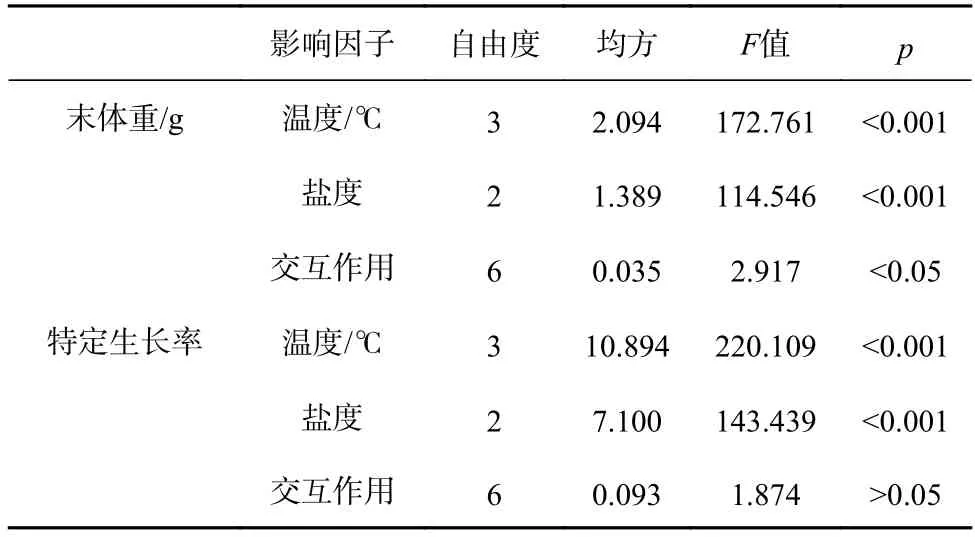
表3 温度和盐度对刺参幼参生长的双因子方差分析Table 3 Two-way ANOVA of growth for the juvenile Apostichopus japonicus maintained in different temperature and salinity
3.2 高温、低盐协同胁迫对刺参幼参诱导型hsp70 和hsp90 基因表达的影响
双因子方差分析结果表明,温度对hsp70和hsp90相对表达量具有显著影响(hsp70:F3,24=7.207,p=0.001;hsp90:F3,24=8.541,p<0.001)。但是盐度以及两者的交互作用对基因表达量的影响不显著(hsp70:盐度:F2,24=2.502,p=0.103;交互作用:F6,24=0.159,p=0.985;hsp90:盐度:F2,24=1.861,p=0.177;交互作用:F6,24=0.157,p=0.986)(表4)。
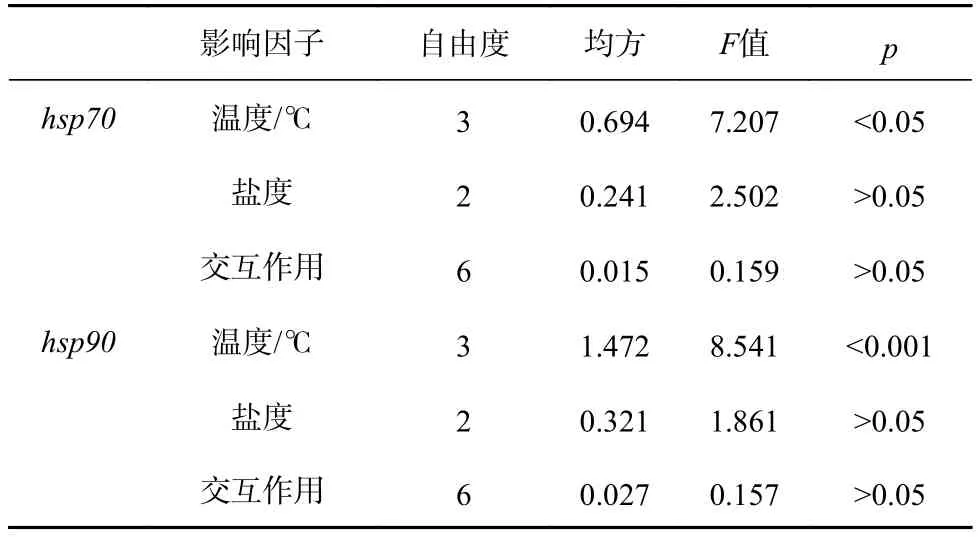
表4 温度和盐度对刺参幼参诱导型hsp 基因表达量的双因子方差分析Table 4 Two-way ANOVA of hsp gene expression for the juvenile Apostichopus japonicus maintained in different temperature and salinity levels
图2a 为刺参幼参hsp70基因的相对表达量,各组间表达量差异显著(F11,24=2.508,p=0.029)。在同一盐度下,不同温度组刺参幼参hsp70基因表达量均在温度为28℃时最大,并且表达量随着驯化温度的升高而上升(图2a)。在同一温度下,盐度为32 时,hsp70基因相对表达量最少。温度为16℃和20℃时,hsp70基因相对表达量随着盐度的降低而升高,但是温度为24℃和28℃时,盐度27 条件下的表达量最大,盐度22 时出现小幅度的下降。
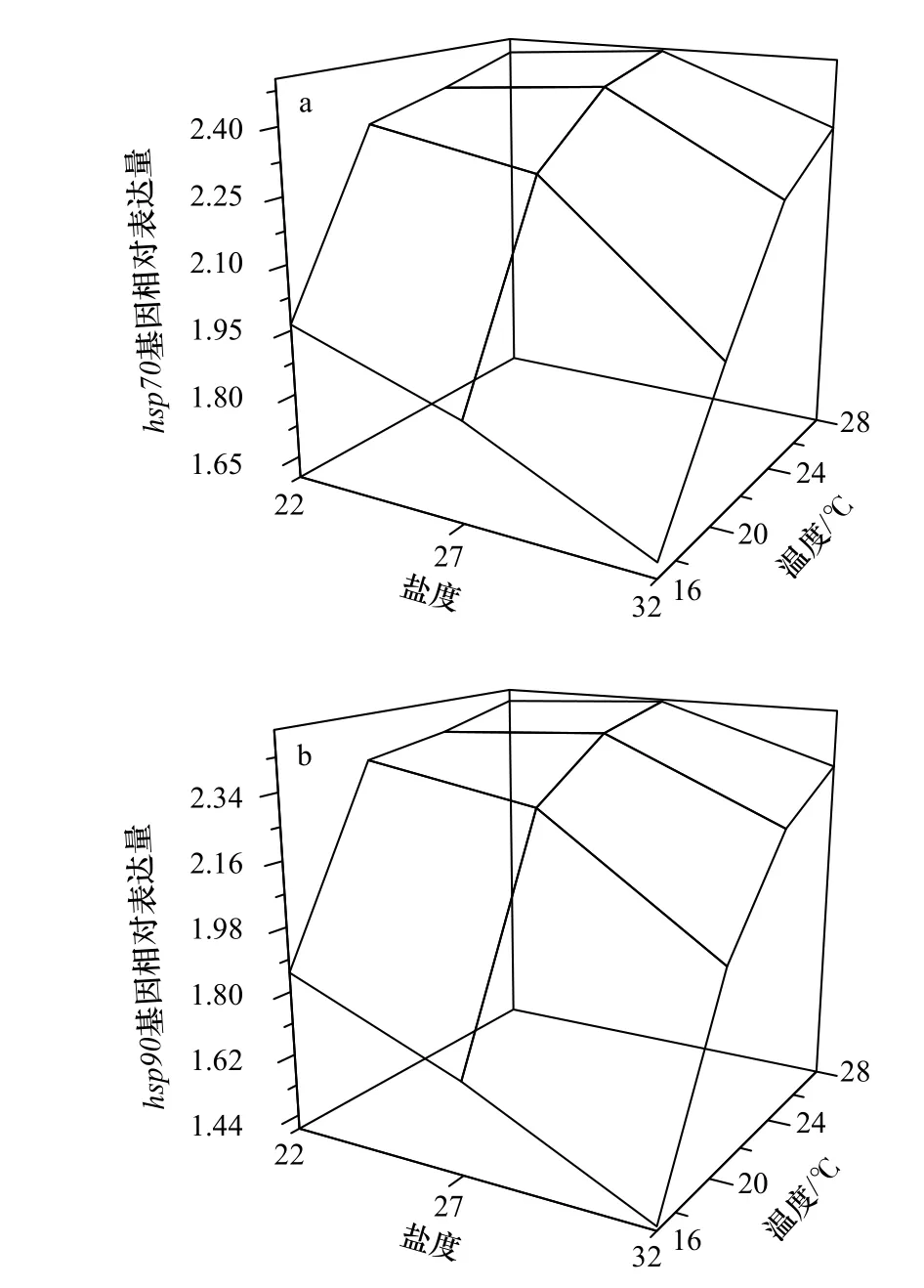
图2 高温和低盐协同胁迫对刺参幼参hsp70(a)以及hsp90(b)表达的影响Fig.2 Effects of high temperature and low salinity collaborative stress on hsp70 (a) and hsp90 (b) expression of juvenile Apostichopus japonicus
刺参幼参hsp90基因的相对表达量见图2b。从图上可以看出,hsp90的表达趋势与hsp70基本相同。即在同一盐度下,hsp90相对表达量随着驯化温度的升高而上升;在同一温度下,盐度从32 下降到27 时,hsp90相对表达量上升,盐度从27 下降到22 时,hsp90相对表达量或升或降。
4 讨论
我国刺参的养殖方式主要有池塘养殖、围堰养殖、工厂化养殖、底播养殖、吊笼养殖和网箱养殖,其中池塘养殖面积最大,主要集中在渤海和黄海的潮间带地区[29-30]。这种室外池塘的水质条件易受天气的影响,夏季高温期的持续暴雨天气会使大量淡水注入池塘,导致池塘海水盐度在十几个小时内从30 陡降至20 以下,而且这种高温、低盐的状况在河口地区更为突出,并且会持续相当长一段时间[31],给刺参池塘养殖造成了巨大的损失。
刺参属于一种温带和狭盐生物,温度、盐度过低和过高对其生长和存活都有很大的影响。本研究的结果显示,温度为16℃和盐度为32 时刺参幼参的体重以及特定生长率要明显高于其他处理组(表2,图1)。且随着温度的升高以及盐度的降低,幼参的体重增加量减少,甚至在温度为24℃、盐度为22 以及温度在28℃以下的盐度27 和盐度22 处理组,刺参幼参的体重下降。这说明,在高温胁迫下,刺参幼参对低盐胁迫的耐受能力降低。温度和盐度单因子胁迫对刺参生长影响的研究已有报道。Wang 等[22]研究表明,高温胁迫下刺参的生长速率降低,原因主要有3 个:(1)高温胁迫下摄食量较少;(2)高温胁迫下耗氧率升高,呼吸耗能增加;(3)高温胁迫下hsps合成以及发挥功能所产生的能量消耗高。赵斌等[32]对比5 个盐度梯度(23、27、31、35 和39)下刺参的生长发现,生长率随着盐度的升高呈现先上升后下降的趋势,并且在盐度为31 时达到最大值。王欠欠等[33]研究进一步表明,低盐度下刺参需要更多的能量来用于渗透压调节,这是导致低盐度下刺参负增长的一个重要的原因。本研究中,在高温和低盐的协同胁迫下,刺参幼参需要消耗更多的能量用于维持机体的正常机能,在外源能量摄入减少的前提下,体重下降成为一种必然结果。因此,在刺参池塘养殖过程中,高温暴雨季节要采取有效措施调节海水盐度,避免盐度的大幅降低。此外,高温季节池塘底部有机质、杂草等物质容易发酵,产生大量热量,造成底热。由于刺参属于底栖生物,要及时打破这种底热造成的养殖水体分层现象,促进上下层水体交换,避免造成更大的损失。
虽然随着胁迫温度的升高和胁迫盐度的降低,幼参的体重呈下降趋势。但是高温胁迫下刺参幼参的诱导型热休克蛋白基因的表达量要高于低温胁迫组(图2)。说明长期高温胁迫能提高机体在急性热胁迫下合成热休克蛋白的能力,并保持高水平的表达量来防止蛋白变性和聚集[25,34-35]。长期环境胁迫对生物来说是一种驯化,而驯化温度是影响生物耐热性的关键环境因素之一[10,36]。生活在不同区域的同一生物对温度的耐受程度不同,且生物体的致死温度受到其前期所经历环境温度的很大影响[11,37]。俞丹等[38]通过比较不同水温条件下驯化的尖头鳉(Rhynchocypris oxycephalus)的热耐受特征发现,尖头鳉耐受的最大临界温度随驯化温度的升高而升高,说明尖头鳉的热耐受性明显有赖于驯化温度。此外,生物体会对长时间的温度驯化产生适应机制,包括对环境因子变化的感知、将外界信号传递到细胞内以及细胞内分子伴侣的激活等[39]。作为重要的分子伴侣,当应对高温胁迫时,机体通过诱导和表达热休克蛋白来缓解热胁迫带来的损伤[17,34,40-41]。
hsp基因具有交叉耐受性,高温胁迫诱导的hsp可以增加机体抵抗氨氮[42]、弧菌[28]、盐度[27]等胁迫的能力。本研究中,在温度为24℃和28℃时,盐度为22 的处理组刺参幼参诱导型热休克蛋白基因的表达量较盐度为27 时低,但是差异并不显著(图2)。可能的原因是,经过长期高温胁迫,刺参诱导热休克蛋白表达的起始盐度以及表达量达到峰值时的盐度较低温胁迫的个体降低。因此对其进行盐度20 的胁迫,诱导热休克蛋白基因的表达量尚未达到最大值。这与前人报道的实验生物的诱导热休克蛋白开始表达的最低温度和达到峰值时的最高温度以及诱导热休克蛋白的最大表达量会随着驯化温度的升高而增加的研究结果相似[43-44]。但是,热休克蛋白的表达是耗能的过程[45],高温及低盐条件下热休克蛋白的表达量较高,需要消耗大量的能量,这也是在此条件下刺参生长缓慢的原因之一。
Wang 等[17]通过研究温度和盐度双因子急性胁迫下刺参渗透压和基因表达发现,盐度变化后,相对于低温处理组,高温处理组刺参体腔液渗透压变化速度更快,而且相较于盐度因子,温度因子对热休克蛋白表达的影响更为显著。本研究中,高温和低盐对特定生长率和诱导型热休克蛋白基因表达量的交互作用均不显著,并且盐度对诱导型热休克蛋白基因表达量也没有显著的影响(表3,表4)。这也说明高温比低盐对刺参幼参的影响更大。因此可以将高温作为选择压力开展刺参新品系选育工作,选育的个体在获得耐高温特性的同时可能对低盐也有一定的耐受能力。此外,刺参对温度和盐度的耐受性具有可塑性[26,46]。在高温和低盐条件下驯化的刺参幼参在遭受温度30℃、盐度20 的急性胁迫时,诱导型热休克蛋白表达量具有相对较高的水平。这说明经过高温和低盐驯化,刺参幼参具有较强的耐高温和耐低盐的能力,并能够增加在相应极端条件胁迫下的诱导型热休克蛋白的合成,防止胁迫导致的蛋白质变性和聚集,从而维持机体的正常功能。
综上所述,本研究通过分析长期高温和低盐协同胁迫下刺参幼参的生长以及诱导型热休克蛋白基因表达量,发现相较低盐,高温对刺参幼参的影响更大。长期高温、低盐协同胁迫增加了刺参幼参诱导型hsp70和hsp90基因表达量,进而在一定程度上提高了刺参幼参应对高温季节暴雨环境的能力。高温期应该采取有效措施降低海水温度,并防止养殖池塘底热造成的养殖水体分层,避免损失。该研究丰富了刺参生理生态学理论,为刺参良种选育工作提供思路,为指导极端天气下刺参生产实践活动提供一定的理论依据。
