某炼化污水处理厂水中可溶有机物的转化规律研究
2022-02-15吴百春李玉果
吴百春,李玉果,聂 凡,何 晨,史 权
(1.石油石化污染物控制与处理国家重点实验室,中国石油集团安全环保技术研究院有限公司,北京 102206;2.中国石油大学(北京)理学院,北京 102249)
炼化一体化企业产品多元化,生产工艺流程长,各单元排水水质差异大,使得进入污水处理厂的污水成分更为复杂,有机污染物种类多,除了石油烃类,还含有酚类、腈类、杂环类和聚合物等非烃类物质,污水处理难度和剂耗、能耗大大增加〔1-4〕。同时,这类非烃类物质导致废水中可溶性有机质(DOM)种类和数量增多,单纯以石油类、COD、BOD5等综合水质控制指标已难以有效指导处理工艺的设计及运行〔5〕,识别与分析污水中DOM 构成,掌握其在污水处理各工艺单元的转化规律,对炼化一体化企业污水处理厂长周期稳定运行和污染物控制达标升级具有重要指导意义。
目前,对废水中的DOM 研究有较多报导〔6-10〕。相比于生活污水,炼化废水水质更加复杂多样,其中,炼化废水中DOM 占总可溶有机碳(DOC)的82.6%~86.6%〔11〕,现有工艺难以完全去除,易造成废水水质波动大,冲击处理设备、增加处理负荷,大大增加了综合污水处理厂处理难度〔12〕,尤其在过滤、吸附和混凝过程,还易引起水的着色和异味、膜材料结垢,诱发致癌消毒副产物或其他污染物的形成,导致深度处理时氧化剂用量增加〔13-14〕。但是常规水质分析难以提供DOM 信息〔2,15〕,不利于来水水质的控制与处理工艺的优化。鉴于废水中DOM 分子层面的分析需求,近年来,一些光谱类分析技术应用于污水中污染物的快速识别屡见报道,三维荧光(3DEEM)技术可快速分析炼化污水污染物的组成类别〔16-17〕,但提供的信息难于精确到具体化合物。目前多采用质谱分析方法对废水中有机物进行精确定性与定量,例如Yijun YU 等〔18〕将废水中的有机物进行提取浓缩后,采用气相色谱质谱联用(GC-MS)技术对污水中挥发性和半挥发性的烷烃、芳香烃、酚类、有机酸类以及含氮类化合物进行了鉴别和分析。但由于GC-MS 气化温度上限、分辨率低等条件限制,难挥发大分子及极性杂原子化合物无法检测〔19-22〕,因此许多研究采用傅立叶变换离子回旋共振质谱(FT-ICR MS)手段,结合多种电离源,可对水体DOM 进行分子层面的定性分析。例如Yongyong LI 等〔23-24〕利用FT-ICR MS 对比研究了炼油污水处理过程中不同阶段水样中DOM 分布及相对含量变化,发现通过常规的隔油-气浮-生化方法较难去除类腐殖质物质。
总的来看,实际生产中对炼化一体化污水的认识大部分停留在综合指标(如pH、COD、BOD5)和单一污水的有机组成分析〔25〕,从分子层面跟踪不同处理过程对污染物降解的影响还缺乏较为系统的分析。本研究以某典型炼油化工一体化企业综合废水处理厂为研究对象,对处理厂3 种不同来水、两条处理工艺主要处理单元进出水中DOM 组成进行从常规参数到分子层面的分析。通过对比分析,确定各处理单元DOM 的去除特征。
1 样品采集及实验方法
1.1 样品采集
废水样品采集于东北某石化公司综合污水处理厂,该污水处理厂对于炼油和化工单元来水采用两条处理工艺,分别为:(1)酸性废水和化工污水混合后的高浓度污水处理工艺;(2)炼油废水和生活污水混合后的低浓度污水处理工艺。处理流程见图1。本研究选择了高浓度污水处理工艺中的水解酸化、生化、臭氧催化氧化处理单元和低浓度污水处理工艺中的生化处理单元为主要研究对象。图1 中三角形符号标识了本研究工艺废水的采样点。

图1 某石化企业综合污水处理厂工艺流程图及采样点Fig.1 Process flow chart and sampling points of a comprehensive sewage treatment plant in a petrochemical enterprise
其中,1#酸性废水来自电石厂、染料厂等酸性废水;2#化工污水主要来自生产汽油、柴油、航空煤油、聚乙烯、ABS、丙烯腈、乙丙橡胶、丁苯橡胶、甲基丙烯酸甲酯等115 种主要石油化工产品的60 余套化工装置排放的化工污水;7#炼油污水主要来自上游炼油厂各炼油装置排水。所有废水样品使用无菌样品袋采集,装满排尽空气,样品经0.45 μm 滤膜过滤后于4 ℃密封避光保存备用。
1.2 试剂及前处理方法
1.2.1 试剂及耗材
试剂:超纯水(LC-MS 级,韩国德山),浓盐酸(ACS 级,德国默克),重蒸甲醇,重蒸二氯甲烷。
耗材:Bond Elut PPL 固相萃取柱(500 mg,6 mL,美国安捷伦),0.45 μm 玻璃纤维滤膜(美国颇尔)。
1.2.2 样品预处理
DCM 萃取:取300 mL 经0.45 μm 滤膜过滤后的废水样品,加入50 mL 二氯甲烷(DCM)萃取,磁力搅拌5 min,充分混匀后转入分液漏斗进行DCM 相(下层)和水相(上层)的分离。重复萃取3 次,将3 次萃取后的DCM 相合并,旋蒸去除大部分的DCM,最后用DCM 定容至10 mL,于-18 ℃黑暗处保存备用。
固相萃取:对于DCM 萃余水相,先用20 mL 重蒸甲醇和20 mL 酸化至pH=2 的酸化超纯水淋洗固相萃取柱,将萃取后的水相用高纯盐酸酸化至pH=2后,注入固相萃取柱过柱;水样过完后,再用20 mL酸化超纯水淋洗固相萃取柱,接着用氮吹方式将柱子内的水分完全去除;最后用10 mL 重蒸甲醇洗脱固相萃取柱得到有机物,在-18 ℃黑暗处保存备用。
1.3 分析仪器及条件
COD、氨氮检测:采用美国哈希公司试剂管快速测定方法对原水水样进行了分析。
总有机碳(DOC)检测:采用总有机碳测定仪(DOC-500A,日本岛津)对原水水样进行可溶性有机碳含量测定。在对其进行检测之前,用超纯水将0.45 μm 滤膜过滤后的原水水样稀释20 倍后调节pH 至2.0 左 右。
石油四组分:DCM 相的饱和烃、芳烃、胶质、沥青质的分离分析依据石油天然气行业标准《岩石中可溶有机物及原油族组分分析标准》(SY∕T 5119—2008)。
3D-EEM 分析:采用Aqualog®三维荧光光谱仪(日本堀场)对原水、DCM 相与水相进行分析,激发波长λEx为220~800 nm,发射波长λEm为240~800 nm,狭缝宽度5 nm,CCD 电压medium。水样过0.45 μm滤膜,测试分原水水样直接测试和DCM 萃取测试两部分。若个别荧光峰浓度太强,稀释后测量。水样直接测试时,采样点1#、3#样品稀释10 倍,4#、7#、8#、9#样品稀释5 倍,其余样品直接测试;DCM 萃取测试时,水样和有机溶剂体积比为1∶1,取有机相进行三维荧光分析。
傅立叶变换离子回旋共振质谱(FT-ICR MS)分析:本实验采用型号为Apex-Ultra 9.4 T FT-ICR MS(美国布鲁克)的高分辨质谱,ESI 电离源为Apollo ⅡESI的负离子模式,进样流速为250 μL∕h。电离源:雾化气流速为2.0 L∕min,干燥气流速为3.0 L∕min,干燥气温度为200 ℃,电离电压为3 500 V,毛细管出口电压为-320 V,反射板电压为-300 V。源六级杆:离子在源六级杆中的累积时间为0.001 s,碰撞累积时间为0.2 s,飞行时间为0.001 0 s。采集质量范围为200~800 U,采样点数选用2 M,谱图平均扫描次数为128次。
2 结果与讨论
2.1 原水中有机污染物的特征分析
本研究对炼油废水、酸性废水、化工污水中可溶有机质进行分析,表1 列出了3 种污水综合水质指标、3D-EEM 与FT-ICR MS 分析结果。
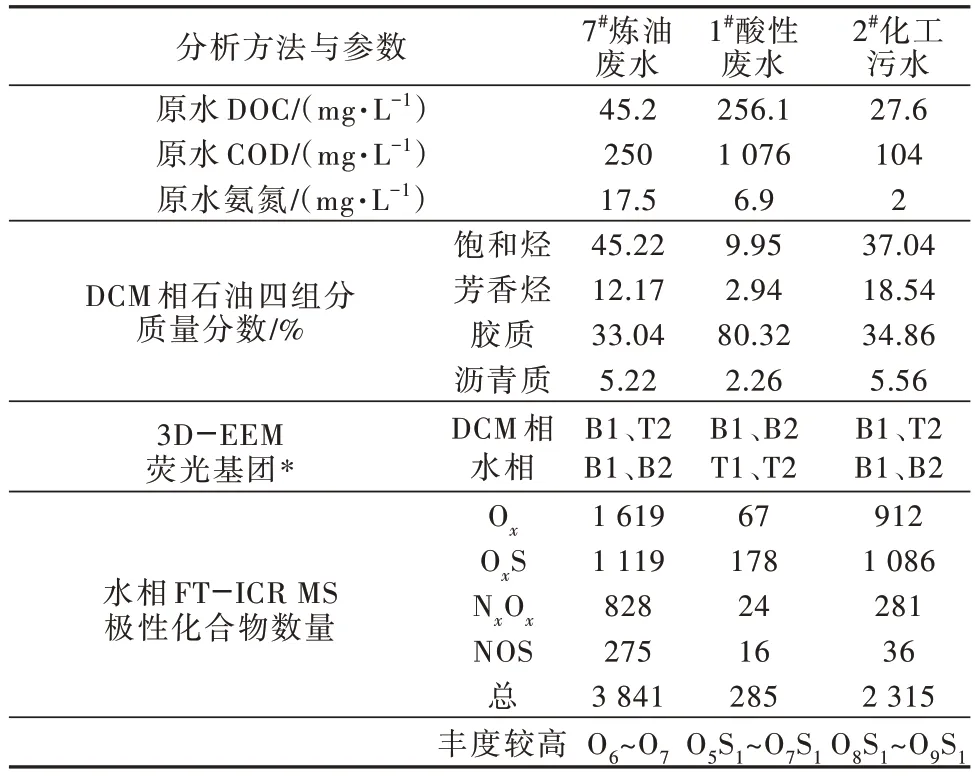
表1 不同废水水质特征及有机组成对比Table 1 Comparison table of water quality characteristics and organic composition of different wastewaters
由表1 可知,酸性废水中DOC 显著高于炼油废水和化工废水,与电石厂石油焦、染料废水中可溶有机质种类多且浓度高有关〔26-30〕;炼油废水的氨氮质量浓度高于酸性废水和化工废水,氨氮主要来自酸性水汽提后废水。根据石油四组分的质量分数得出炼油废水和化工废水以饱和烃、胶质为主,酸性废水DCM 相中的胶质质量分数达80.32%,主要为非烃类物质。
利用3D-EEM 分别对DCM 相和水相荧光基团进行分析,结果见图2。
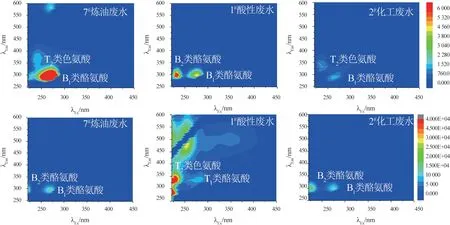
图2 3 种废水DCM 萃取有机相(上)及水相(下)可溶有机质的3D-EEMFig.2 3D-EEM of dissolved organic matter in organic phase and aqueous phase of three wastewaters
由图2 可知,三类废水检测到的荧光基团均为B类酪氨酸、T 类色氨酸,炼油废水和化工废水的DCM相与水相检测到的荧光基团一致,而酸性废水DCM相与水相荧光基团不同,分别为B 类酪氨酸、T 类色氨酸。其中B 类酪氨酸荧光基团是炼化废水的特征荧光基团,3 种污水均有检出〔31〕。
3种废水水相鉴定化合物种类的相对丰度见图3。
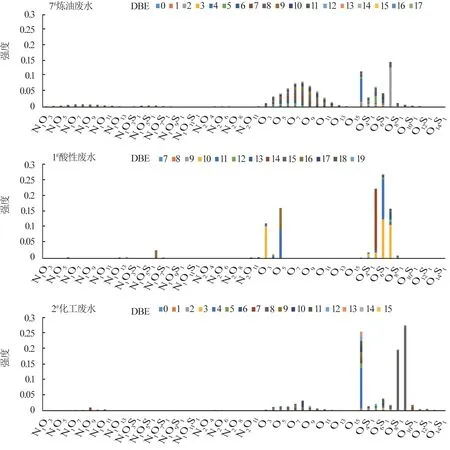
图3 3 种废水水相鉴定化合物种类的相对丰度图Fig.3 Relative abundance of the identified compounds in the aqueous phase for the wastewaters
由表1、图3 可知,样品炼油废水的极性化合物中含氧类化合物(CHO)峰数最多,酸性废水和化工废水中氧硫类化合物(CHOS)峰数最多。相比于化工废水,酸性废水检测到的极性化合物峰数最少,只有285 个分子式。
2.2 有机污染物在高浓度污水处理工艺中的转化规律
2.2.1 DOC、COD、氨氮分析
高浓度污水处理工艺主要单元进出水水质分析结果见表2。
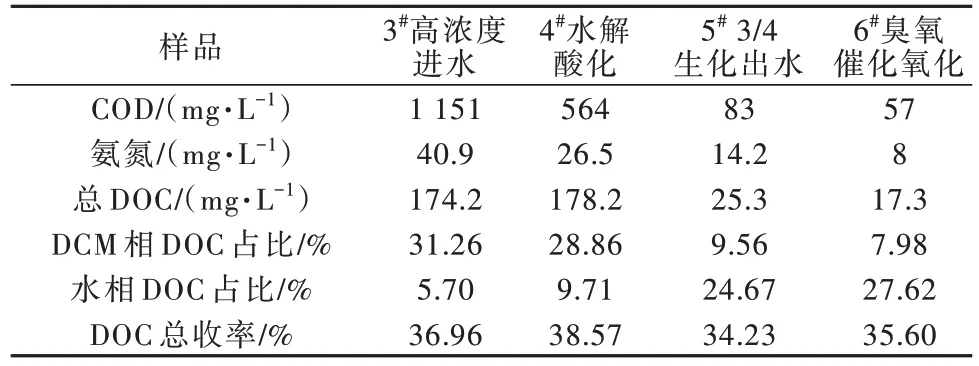
表2 高浓度污水处理工艺基础数据Table 2 Bulk properties of high-concentration wastewater treatment process
在整个处理流程中,DOC 主要在生化单元去除,去除率达86%;DOC 在水解酸化单元略有上升,主要是部分难降解DOM 被水解为小分子可生化DOM〔32-33〕。从DCM 相与水相中DOC 分析结果看,生化处理后,DCM 相中DOC 占总DOC 的比值从31.26%降低到了9.56%,水相中DOC 占总DOC 的比值从5.70%增加到了24.67%,说明DCM 相中DOC更易生化降解,而原水中残余的DOC 主要源自水相中难降解DOM。本实验方法的DOC 两相收率较低,这可能是由于样品中一些易挥发的化合物损失和部分无法萃取或易残留物质引起的〔34-37〕。
2.2.2 荧光光谱分析
高浓度污水处理工艺中各水样萃取后的水相和DCM 相的3D-EEM 光谱图见图4~图5。
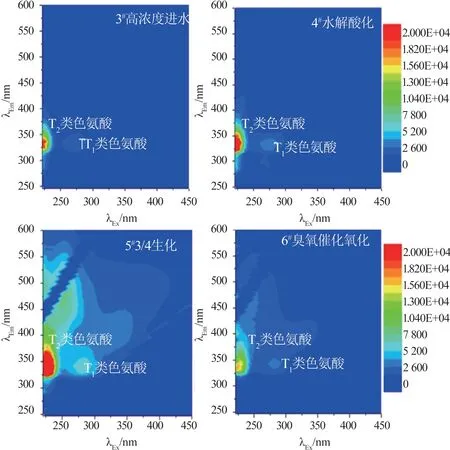
图4 高浓度处理工艺水相可溶有机质的3D-EEMFig.4 3D-EEM spectra of aqueous phase DOM from the high-concentration wastewater treatment process
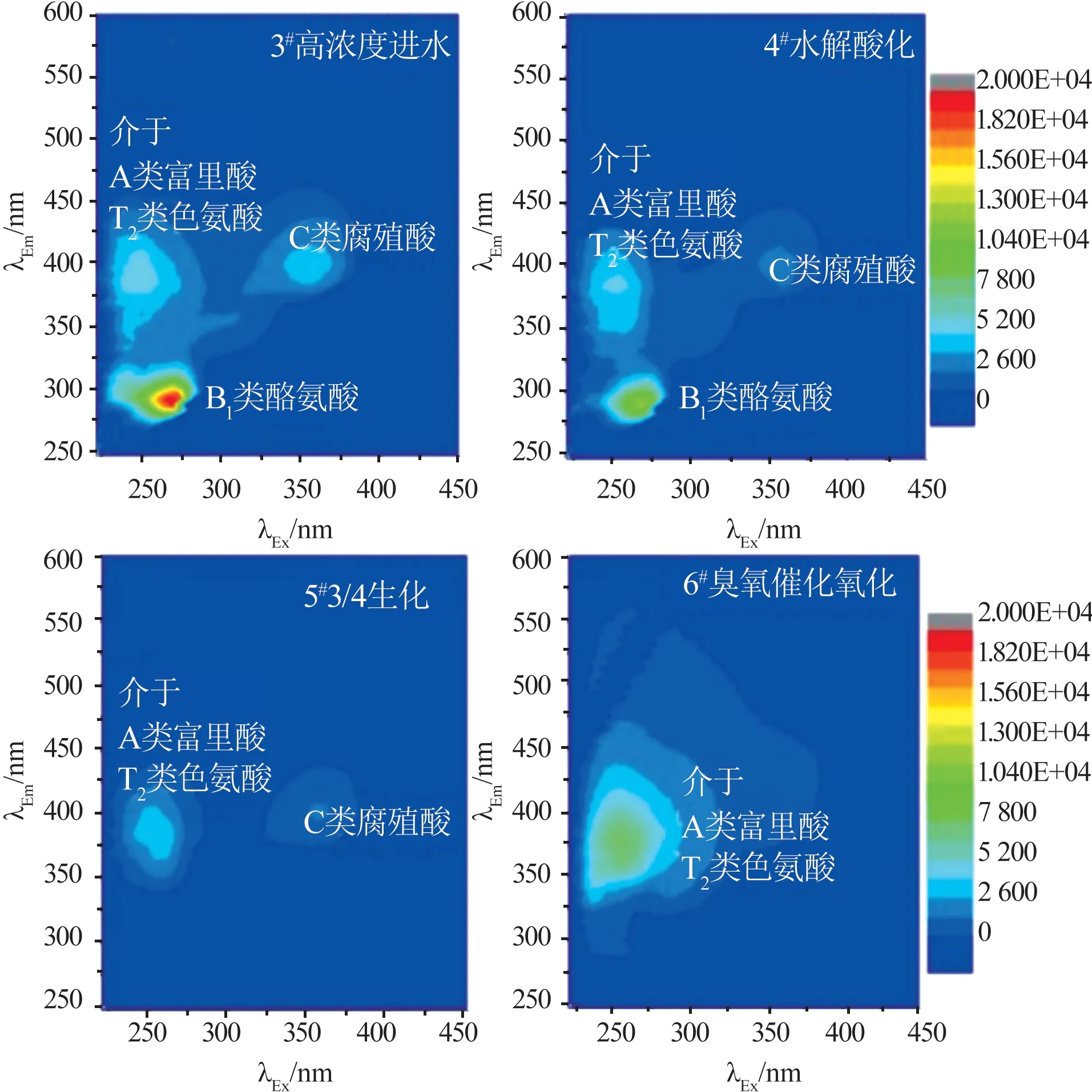
图5 高浓度处理工艺DCM 相可溶有机质的3D-EEMFig.5 3D-EEM spectra of organic phase DOM from the high-concentration wastewater treatment process
高浓度进水为酸性废水和化工废水混合水,水相中只检测到T1、T2 类色氨酸类荧光基团,推测是由于极性物质中的芳香结构共轭程度增加,发生红移而转化为T1、T2 类色氨酸荧光基团〔38〕,且在整个处理过程中未发生变化,说明T 类色氨酸类荧光基团性质稳定,难以去除〔39〕。DCM 相中主要检测到3组荧光基团,分别为B1 类酪氨酸、介于类富里酸和类色氨酸荧光基团、C 类腐殖酸。水解酸化出水荧光基团没有变化,3∕4 生化单元出水中B1 类酪氨酸荧光基团消失,相关有机物被有效去除;经过臭氧催化氧化处理后C 类腐殖质荧光基团消失,说明臭氧催化氧化对腐殖酸具有良好的去除效果〔2〕。与表2测得的DOC 占比结果类似,相对于水相,现有处理工艺更易降解DCM 相的DOC。
2.2.3 极性化合物分子组成分析
炼化废水极性化合物含量较高,采用FT-ICR MS 对高浓度污水处理工艺进出水萃取后的水相DOM 进行了分析,测得的各节点水样水相中DOM化合物的杂原子相对丰度见图6。
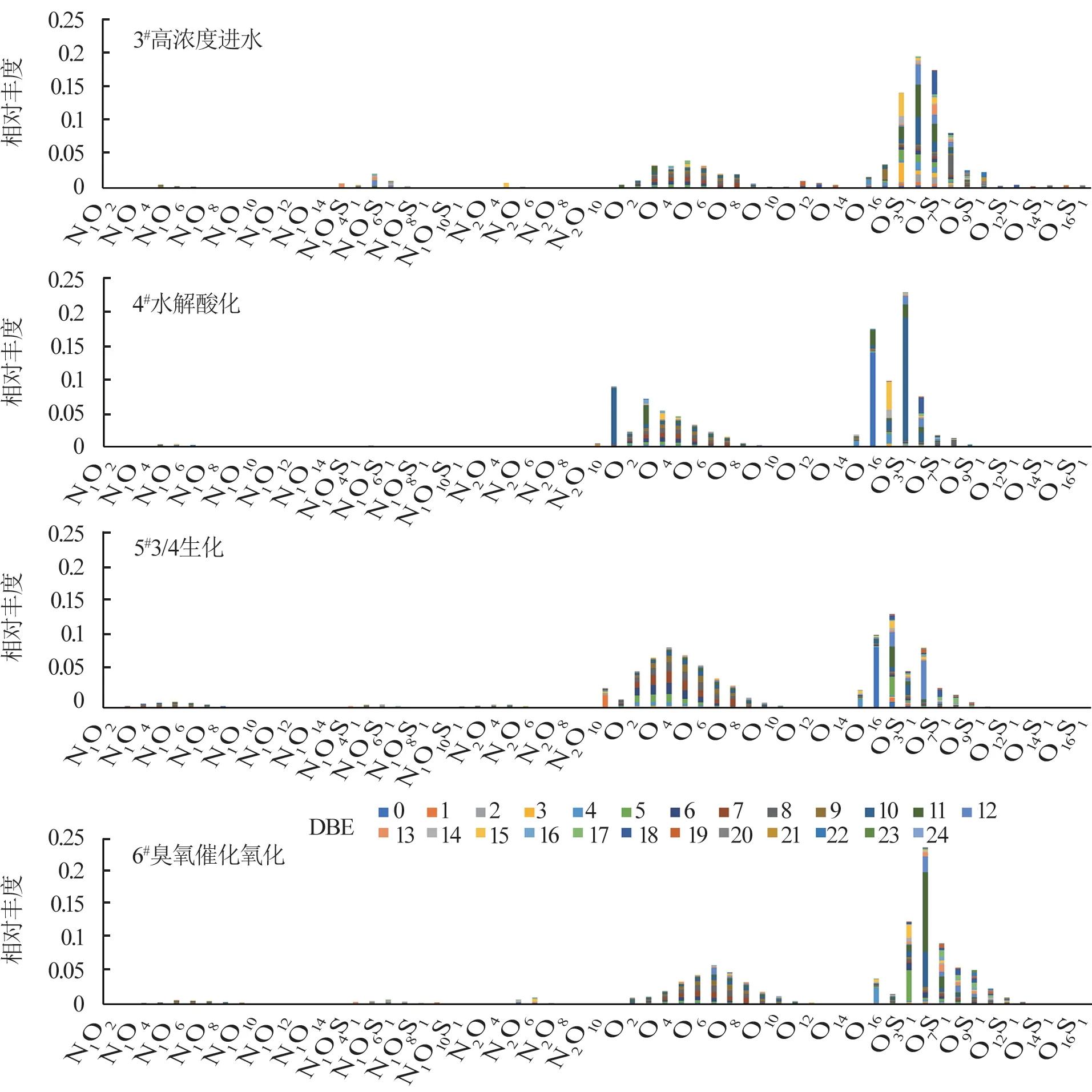
图6 高浓度处理工艺水相DOM 中所鉴定化合物的杂原子相对丰度Fig.6 Relative abundance of identified compounds in aqueous phase of the wastewaters from the high-concentration wastewater treatment process
总的来看,极性有机物主要包含CHO、CHOS、CHON、CHONS 共4 类化合物,其中CHO、CHOS 类化合物相对丰度较高。按照“水解酸化—生化处理—臭氧催化氧化”的现有工艺流程,CHO 类化合物丰度由低氧数O5向高氧数O8移动,说明低氧数化合物在过程中得到部分降解,但现有工艺对以腐殖质为代表的含高氧数的CHO 类化合物降解效果较差〔40〕。CHOS 类化合物中O5S1~O7S1化合物相对丰度较高,推测为表面活性剂类及其衍生物为主的聚合物类含氧硫类化合物〔40-42〕。
为了进一步对比CHO、CHOS 类化合物在水解酸化(3#)、3∕4 生化(4#)、臭氧催化氧化(6#)处理过程中化合物发生的变化,对FT-ICR MS 检出物质按原子比(H∕C、O∕C)进行了划分,结果见图7。图中红色代表在该处理单元去除的化合物的分子式,紫色代表该处理单元新生成的化合物的分子式。由芳香指数(AI)和元素比(H∕C、O∕C)对化合物进行分类〔43-44〕:饱和化合物(H∕C>2),脂肪族化合物(2.0≥H∕C>1.5)〔45〕,高度不饱和及酚类化合物(AI<0.50,H∕C<1.5),类多酚类化合物(0.66≥AI≥0.50)和多环芳烃类化合物(AI≥0.66)〔46〕。
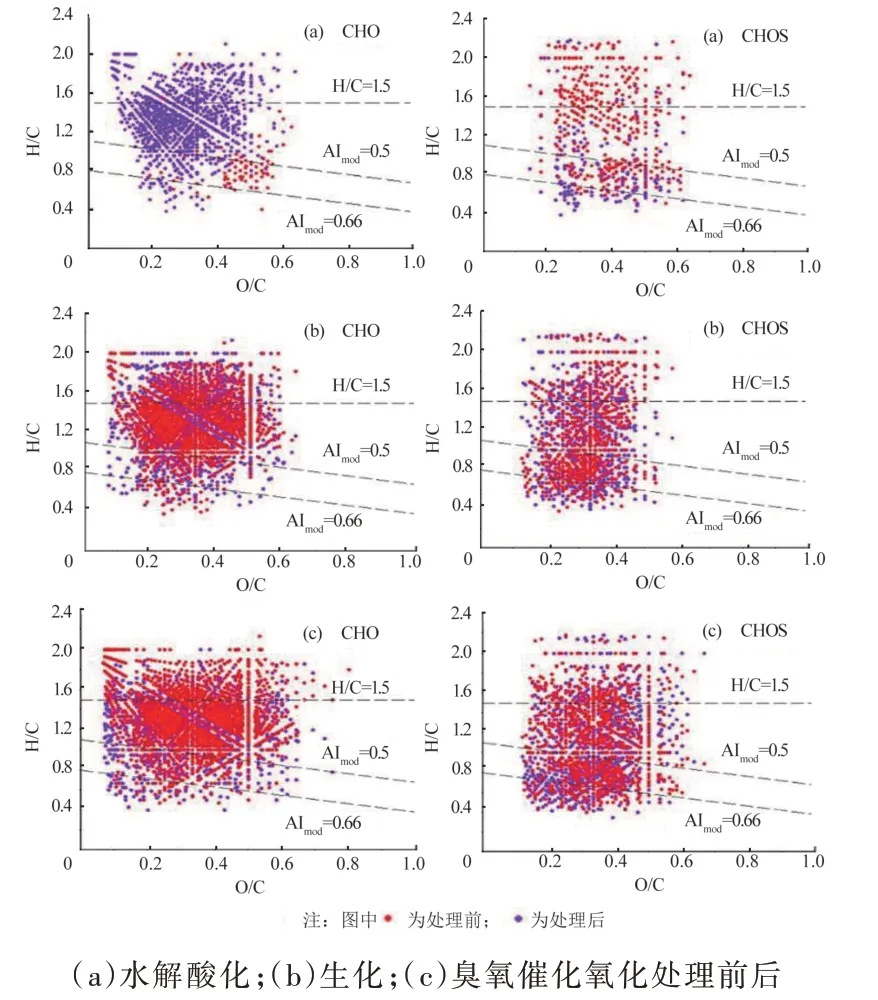
图7 高浓度处理工艺流程CHO 和CHOS 类化合物的VK 图Fig.7 van Krevelen diagrams of removed and newly formed CHO and CHOS formulas in the aqueous phase of high-concentration wastewater treatment process
各处理单元进出水中萃取后水相中极性化合物种类和相对含量变化见表3。
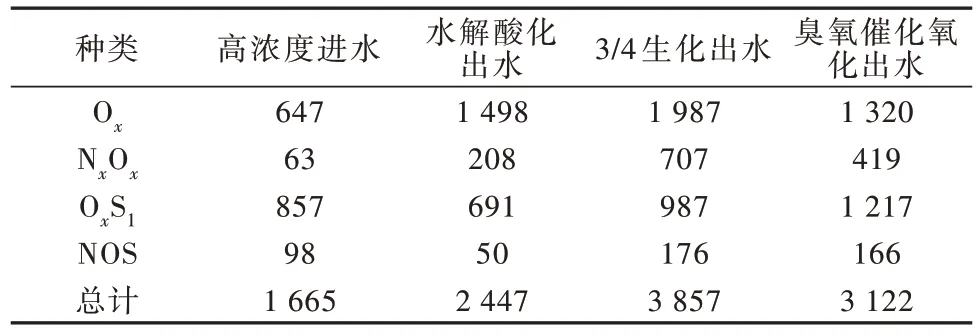
表3 高浓度处理工艺极性化合物在水处理过程中种类和数量的变化Table 3 Variations in the types and quantities of polar compounds in high-concentration treatment processes
由图7、表3 可知,高浓度废水萃取后水相中含有大量的水溶性氧硫类化合物,主要为饱和化合物、脂肪族化合物、高度不饱和酚类化合物及多酚类化合物。经水解酸化后,生成了大量的CHO 类可溶性有机物,且相对含量增加,主要分布在O∕C<0.5、H∕C>0.6 的区域,包括饱和化合物、脂肪族化合物、高度不饱和及酚类化合物、多酚类化合物,同时CHOS中生成了一些O∕C>0.2、0.6<H∕C<1.0多酚类化合物,说明该处理单元对H∕C较高的脂肪族及不饱和的酚类CHOS类化合物具有明显降解效果。对于生化及臭氧催化氧化单元,处理前后水相中的CHOS类化合物、CHO类化合物类型和分布变化不大,其中CHOS类化合物分布范围集中在0.1≤O∕C≤0.5、0.4≤H∕C≤2.2和0.1≤O∕C≤0.6、0.4≤H∕C≤2.2;CHO类化合物分布范围集中在0.1≤O∕C≤0.6、0.4≤H∕C≤2.0和0.1≤O∕C≤0.7、0.4≤H∕C≤2.0。经过生化处理后,脂肪族等的CHO、CHOS 类化合物的相对丰度有所降低,但检测到的化合物种类数量有所增加。臭氧催化氧化过程主要去除了部分的水溶性CHO 类化合物,但CHOS 类化合物的种类和相对丰度略有增加。由检测到的化合物总峰数变化可以说明,水解酸化和生化增加了水溶性分子多样性,而臭氧催化氧化使分子多样性降低,可能是部分化合物转化成CO2造成的〔33,47-48〕。
2.3 高、低浓度污水处理工艺中生化单元作用效果对比
污水中有机污染物主要依靠生化单元降解去除,本研究对该污水厂两条处理工艺中生化单元作用效果进行了对比分析。低浓度污水处理工艺1∕2生化单元进出水中DOC、COD、氨氮的变化见表4。

表4 低浓度污水处理工艺生化处理前后DOC、COD、氨氮质量浓度变化Table 4 Changes of DOC,COD and NH3-N before and after biochemical treatment of low-concentration sewage treatment process
由表4 可知,COD 与氨氮质量浓度在生化处理后明显降低,生化单元有机质去除率达83%,与表2高浓度污水处理工艺生化单元有机质去除率86%接近,均是有机污染物去除的主要单元。
高、低浓度污水处理路线生化出水DCM 相与水相的荧光基团对比见图8。

图8 高、低浓度污水处理工艺生化单元出水可溶有机质的3D-EEM 图Fig.8 3D-EEM of dissolved organic matter in effluent of biochemical unit of high and low concentration wastewater treatment process
由图8 可知,与高浓度污水处理生化单元相比,低浓度污水中萃取DCM 相中未检测出腐殖酸;萃取水相中出水荧光峰强度要低一个数量级,但荧光基团均为T 类色氨酸类荧光基团,荧光变化一致,说明生化单元处理这两类污水对荧光基团物质的作用效果一致。
利用FT-ICR MS 对高、低浓度污水处理工艺生化单元出水可溶有机质进行了分析,生化处理后水相中CHO、CHOS 类化合物分布见图9。
由图9 可知,高、低浓度废水生化处理后化合物种类一致,主要为CHO、CHOS、CHON、CHONS 四类杂原子化合物,其中CHO、CHOS 类化合物中O6、O7类高氧数化合物丰度较高。图10 为两条处理工艺中CHO 及CHOS 类化合物在生化处理前后化合物变化的VK 图。对于CHO 类化合物,由于生化处理的废水不同,两个生化单元在VK 图中反映出的O∕C、H∕C 的分布有所不同,但两者在去除CHO 类化合物的同时,均伴有大量CHO 类化合物的生成,分子多样性也有所增加。对于CHOS 类化合物,低浓度污水在生化单元水溶性化合物的O∕C 分布范围较高浓度污水生化广,为0.1≤O∕C≤0.8。由此可知,通过FT-ICR MS 分析,对于两类不同性质组成的污水,生化单元对可溶有机质的作用效果基本一致。
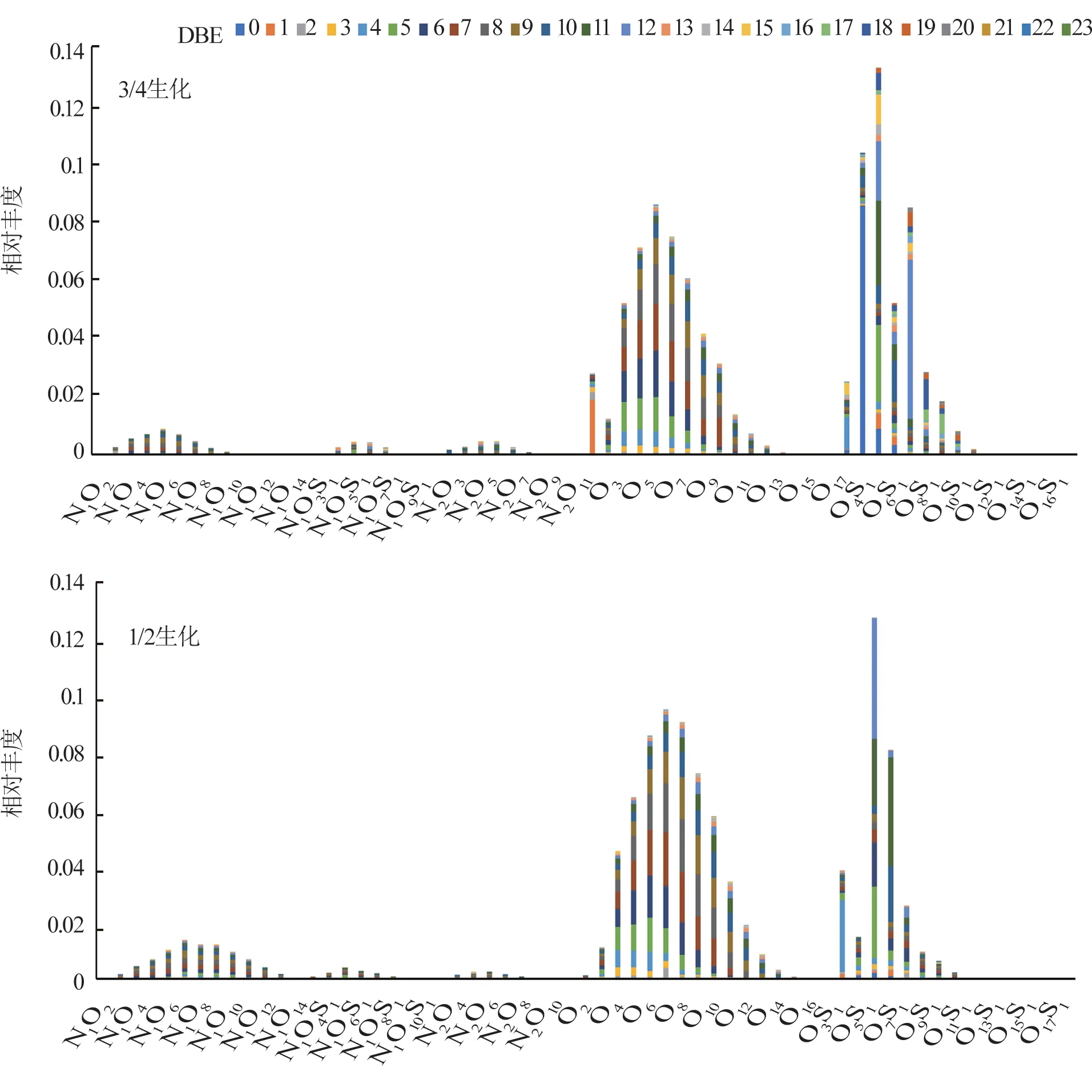
图9 高、低浓度处理工艺生化出水可溶有机质的杂原子丰度图Fig.9 Relative abundance of assigned compound classes in the aqueous phase DOM from biochemical treatment processes
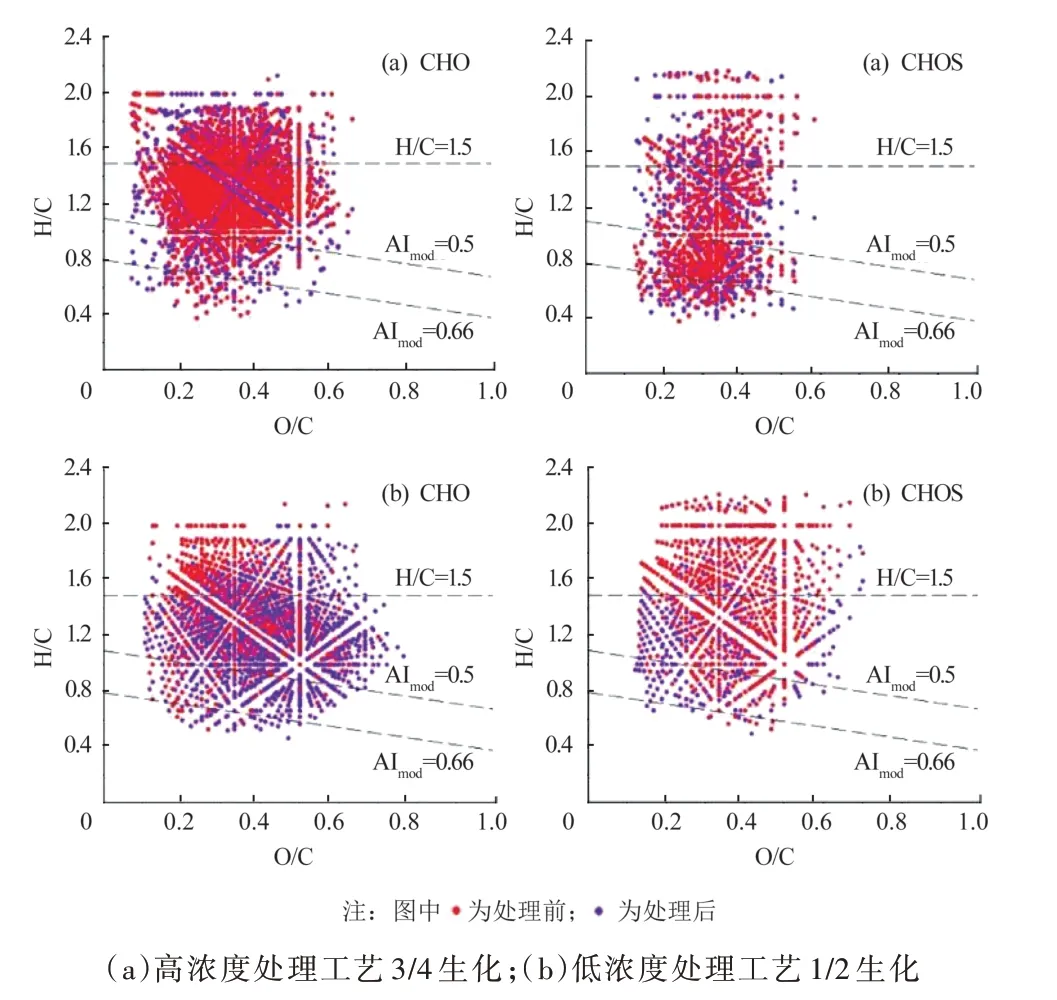
图10 高、低浓度污水处理工艺生化处理过程CHO、CHOS 类的生成和去除的VK 图Fig.10 van Krevelen diagrams of removed and newly formed CHO and CHOS formulas in the biochemical treatment process of high and low concentration wastewater treatment routes
3 总结与展望
通过对某炼油化工一体化企业废水处理厂水样分析,发现:(1)炼油废水、酸性废水和化工废水水质差别较大,但检测到的荧光基团均以类蛋白质为主,其中炼油废水DOC 质量浓度低、氨氮浓度高,极性化合物以含氧类化合物为主;酸性废水DOC 质量浓度高,酸性废水及化工废水中极性化合物以表面活性剂类及其衍生物为主的聚合物类含氧硫类化合物丰度较高,主要为高氧数的多氧含硫类化合物。(2)炼化废水处理工艺中,水解酸化能有效降解H∕C 较高的脂肪族及不饱和的酚类CHOS 类化合物,同时生成大量小分子含氧类化合物;生化处理后86%的可溶有机质得到降低,其中类酪氨酸、脂肪族等CHO 类化合物在生化单元中得到有效去除;臭氧催化氧化工艺有效去除C 类腐殖酸物质。T1、T2 类色氨酸荧光基团较为稳定,和高氧数多氧含硫类化合物均难以去除,是出水中难降解有机物的主要贡献者。(3)对比不同性质污水生化单元处理效果,处理前后DOC 去除效率、荧光基团及极性化合物的种类及其变化规律基本一致,说明炼化废水经生化处理后,水质差异性较小。
