肢端肥大症性心肌病1例
2022-02-14王雅兰谢家和
王雅兰,谢家和
(1.赣南医学院;2.赣南医学院第一附属医院章贡心内科,赣州 341000)
肢端肥大症性心肌病临床罕见,国内外相关文献较少。近期赣南医学院第一附属医院收治1例肢端肥大症性心肌病,现相关报告如下。
临床资料:患者,男性,59岁,因“反复胸闷、气促半年余,加重伴呼吸困难3天”入院,患者自诉缘于近半年来无明显诱因反复有胸闷、气促,2020年3月因左侧腹股沟疝至当地医院就诊,行胸片示心影增大,未做特殊处理,3天前突发症状加重,伴呼吸困难,伴有咳嗽,无头痛、头晕,无胸痛、心悸,无腹痛、腹胀,遂至当地医院就诊,心脏彩超示“射血分数28%,全心增大(左房55 mm,左室75 mm),左室壁弥漫性动度明显减弱,左室后壁运动低平,三尖瓣中度返流,二尖瓣、主动脉瓣轻度返流”,考虑“心力衰竭”,给予强心、利尿、抗心衰等对症治疗,症状有所改善,考虑瓣膜病变入住我院心胸外科。既往史:否认心肌炎、哮喘、先天性心脏病、恶性心律失常等病史,高血压病史6年余,未服药,收缩压最高200 mmHg,有左侧腹股沟疝气及双侧股骨头坏死2年余。个人史:有吸烟史30余年,约2两烟叶/日,未戒烟,有饮酒史30余年,2~3两/日。入院查体:面貌粗犷、四肢宽大、指间关节增粗,双肺呼吸音稍粗,未闻及干湿啰音。心前区无隆起,心尖搏动范围第5肋间左锁骨中线外1cm,心前区未触及震颤和心包摩擦感,叩诊心脏相对浊音界扩大,心率78次/分,心律齐整,心音正常,心脏各瓣膜听诊区未闻及杂音。入院诊断:慢性心力衰竭,非风湿性三尖瓣关闭不全,高血压病3级(极高危),冠状动脉粥样硬化,心功能Ⅲ级,左侧腹股沟疝,右肾结石,入院后完善相关检查:性激素,生长激素(Growth Hormone,GH):睾酮141.8 ng/dL,雌二醇12.86 pg/mL,生长激素(GH)>50.00,心脏彩超(左房前后径/横径:46 mm/46 mm,左室前后径:77 mm,右房横径:46 mm,右室前后径:26 mm,射血分数36%)。(1)全心增大;左室后壁运动减弱。(2)升主动脉增宽并主动脉硬化;主动脉瓣反流(轻度)。(3)二尖瓣反流(轻度);三尖瓣反流(轻度)(图1)。(4)左室收缩功能受损。选择性冠状动脉造影结果示:冠状动脉分布呈右冠优势型,左主干无明显狭窄,前降支无明显狭窄,前向血流TIMI3级,回旋支无明显狭窄,前向血流TIMI3级,右冠无明显狭窄,前向血流TIMI 3级。垂体MRI平扫+增强:蝶鞍无扩大,垂体增大,大小约16 mm×23 mm×14 mm,考虑侵袭性垂体大腺瘤可能性大,Knosp 2级(图2)。内分泌科会诊建议加用醋酸奥曲肽,用药期间定期监测生长激素水平,若心功能允许可转神经外科手术治疗,神经外科会诊建议转科行垂体瘤切除术,尊重患者及家属意见,转神经外科行内镜下经鼻蝶鞍区病损切除术+视神经减压术,术后病理诊断:(鞍区)垂体腺瘤(图3)。术后复查垂体MRI:(1)垂体大腺瘤术后改变,术区积液(血),右侧鞍旁结节软组织,肿瘤部分残留可能,请结合临床;(2)鼻窦炎。术后停用强心、利尿、扩血管药物,出院三个月后电话随访患者诉胸闷较前明显好转,外院复查心脏彩超(左房(前后径/横径39 mm/45 mm),左室内径(舒张末期/收缩末期60 mm/43 mm),右房横径41 mm,右室横径24 mm,射血分数54%)左房左室增大,室间隔增厚,左室壁向心运动不协调,收缩幅度减低,二尖瓣轻度反流,主动脉窦部稍宽,肺动脉稍宽,左室舒张功能减低,收缩功能正常值下限)。

图1 心脏彩超
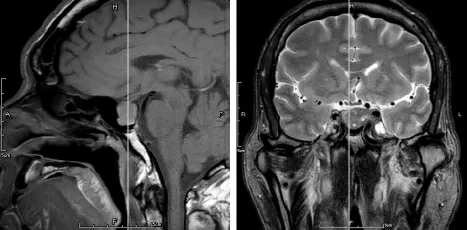
图2 垂体磁共振:瘤体大小约16mm×23mm×14mm
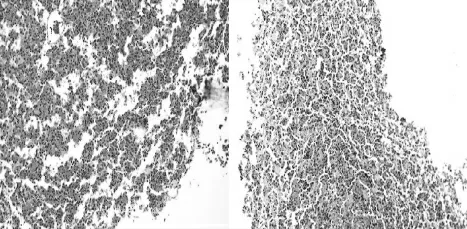
图3 (鞍区)垂体腺瘤
讨论
肢端肥大症是身体发育不成比例的疾病,每年的发病率约为每百万人中有5例,虽然这种疾病很早就被认识到了,但垂体“肢端扩张症”的病理最早是由Andrea Verga在1864年描述的,而肢端肥大症的临床特征则是由Pierre Marie在1886年首先描述的,该病主要涉及肿瘤垂体生长激素(GH)细胞分泌的GH[1-3],垂体瘤GH分泌过多,GH可直接或间接通过胰岛素样生长因子(Insulin like growth factor-I,IGF-I)作用于心肌细胞中存在的GH和IGF-I受体,涉及一系列心脏结构和功能以及血管系统的异常,一项对大约600名患者的研究确定,肢端肥大症的临床表现为肢端和面部改变、多汗(出汗异常增加)、头痛、感觉异常(“针刺感”)、性功能障碍、高血压、甲状腺肿以及视野缺陷[4],但以心力衰竭为主要临床表现的少见,本例患者以轻度体力活动即感胸闷、气促不适为主要临床表现。
肢端肥大症心肌病在其生理病理发展过程复杂,在早期,高动力心脏表现为心肌功能增强,外周血管阻力降低,心输出量增加;中间阶段以心肌肥大为特征,由于炎症反应导致心肌纤维组织增生,这导致进行性间质重塑及心脏舒张和收缩功能的恶化;晚期肢端肥大症心肌病的特征是腔显著扩张,伴有严重的收缩和舒张功能障碍以及高外周血管阻力,最终导致充血性心力衰竭[5],短期GH过量以及长期GH暴露导致最终心力衰竭的确切机制目前尚不清楚,尽管它们似乎与心肌纤维化和炎症的发展有一定联系,GH慢性过量影响心脏形态和性能,导致双心室向心性肥大,这是由于心肌细胞宽度增加,这表明新的肌节紧密并置,最相关的组织学异常是细胞外胶原沉积增加,肌原纤维紊乱,单核细胞坏死和淋巴单核细胞浸润,所有这些都会逐渐损害整个器官结构,最终导致收缩或舒张功能障碍[6],GH/IGF-I过量还可增加钠水储留在肾脏、增加交感神经紧张、胰岛素抵抗、血脂异常等导致心脏结构改变最终心力衰竭[7]。
肢端肥大症心肌病治疗有很多种方法,其包括原发病的治疗及心肌病的定向治疗,原发病的治疗包括药物治疗、手术治疗、放射治疗等[8],方案的选择应该根据患者瘤体性质,生化特征,代谢状态等个体化治疗,当然经蝶手术仍然是此疾病的首选治疗方案,垂体生长激素腺瘤的切除在技术上是有挑战性的,因为在解剖学上肿瘤是难以接近的,而且切除时容易伤及周围组织,有些肿瘤侵犯大脑旁边组织时手术时不易被发现,导致肿瘤残遗,继续分泌GH,这时候就需要技术及仪器上的发展,但经手术治疗不能控制疾病或无法手术的时候,药物治疗显得尤为重要,如生长抑素受体配体(Somatostatin receptor ligands,SRLS)、生长激素受体拮抗剂、多巴胺激动剂等,第一代SRLS对生物指标的控制率为55%[9],在实际中由于各种因素如样本人的选择、初始GH/IGF-I水平、依从性等都会影响GH/IGF-I控制,对第一代SRLS的生化反应低于早期实验,但高于过去10年的发表的实验[10],在第一代SRLS治疗控制不充分的患者,第二代SRLS被推荐为二线治疗,但其主要不良反应为血糖升高,所以应监测糖化血红蛋白及空腹血糖[11],生长激素受体拮抗剂生化控制率受剂量影响大,所以我们推荐临床医学监测患者IGF-I水平来调整剂量的使用,使其获益达到最大,其与SRLS联合使用时显示出很高的有效率,在SRLS治疗不足时,可添加多巴胺受体激动剂即卡麦角林也有类似的益处[12],主要在IGF-I水平轻度升高的患者体现。不管什么治疗方案最终目的都是将生化指标控制及临床症状改善[13]。肢端肥大症所导致心肌病的治疗,包括戒烟、生活方式改变、控制血压、心力衰竭药物治疗等,本例病人虽然已经出现慢性心力衰竭,但给予积极手术治疗后,三个月后心功能情况明显改善,提示肢端肥大症性心肌病病人即使出现了慢性心力衰竭,积极治疗原发病仍会有所获益,但是肢端肥大症所导致心肌病少见,临床医生容易误诊为冠心病、高血压性心脏病、瓣膜病导致的心肌病而得不到有效治疗,强调临床上的医生需要有意识去关注患者体征及必要时完善垂体相关检查。
