宫颈高级别鳞状上皮内病变锥切术后接种HPV疫苗预防复发的临床研究
2022-02-14汪美容舒宽勇谢彤王艺
汪美容,舒宽勇,谢彤,王艺
(1.江西省妇幼保健院健康管理体检科;2.肿瘤科,南昌 330006)
宫颈高级别鳞状上皮内病变(HSIL),被认为是进展为宫颈浸润癌的第一步[1],如果不能及时发现或者治疗很容易发展成浸润癌[2]。临床上对CIN2及以上癌前病变的治疗主要是保守生育功能的宫颈锥切术,经过锥切术后,去除CIN病灶,可以阻断宫颈浸润癌的发展,但其术后仍存在病灶残留和疾病复发的风险[3]。有报道[4-5]显示CIN宫颈锥切术后两年内复发率约为1%~25%不等。因此治疗后除需密切随访外,如何减少疾病复发也至关重要。近期Joura EA[6-8]等研究表明向宫颈CIN2-3锥切术后的患者提供HPV预防性疫苗,能有效预防CIN2-3的复发。虽然预防性HPV疫苗国内也已经大规模用于临床且对相关型别生殖道癌前病变和癌预防效果显著[9-10],但对其预防复发的研究国内尚无相关报道。本研究旨在探讨宫颈高级别鳞状上皮内病变锥切术后的患者接种二价HPV疫苗能否有效降低疾病的复发。
1 资料与方法
1.1 资料来源 选取2019年1月至2020年1月体检筛查经病理组织确诊为宫颈高级别鳞状上皮内病变(CIN2-CIS)并行宫颈冷刀锥切术,年龄21~45岁,257例患者进行随访观察。其中110名患者自愿接种进口二价HPV疫苗,按0/1/6程序进行接种;未接种HPV疫苗患者147例。
1.2 方法 有其他恶性肿瘤、免疫缺陷等患者;因故未能按时随访或失访者;术后子宫切除患者均排除在外。锥切术后3个月、6个月、12个月、18个月对患者行人乳头瘤病毒(HPV)和宫颈液基细胞学(TCT)检查。 如果HPV检测阳性,或细胞学检查显示非典型意义的鳞状上皮细胞(ASCUS)及以上,则进行阴道镜检查,活检或宫颈管取样组织经病理学诊断。治疗后3个月检查有CIN2以上的病变认为病灶残余予以排除在外,6个月后则认为是疾病复发。比较术后HPV疫苗接种者与未接种者随访期间病变的复发及高危型HPV感染情况。
1.3 统计学处理 采用SPSS 19统计软件,计算95%的置信区间,P值均为双侧,当P<0.05时,差异有统计学意义。接种疫苗和未接种疫苗的患者之间的比较采用卡方检验或Fisher精确检验。
2 结果
2.1 共有257例患者被纳入随访研究,平均随访时间为1.5年。接种疫苗组和未接种疫苗组患者在年龄、CIN分级、切缘阳性情况、HPV16/18相关型别感染差异无统计学意义(P>0.05)。见表1。
2.2 257例患者中,随访期复发9例(3.50%),组织学检查显示CIN2 3例,CIN3 6例。未接种疫苗和接种疫苗组疾病复发分别为7例(4.76%)和2例(1.82%)。术后患者接种HPV疫苗较未接种疫苗患者复发风险降低,为保护因素,但差异无统计学意义(比值比(OR)=0.37;p值=0.571)。但随访截止时发现未接种疫苗组高危型HPV感染者14例(9.52%),接种HPV疫苗组3例(2.27%),差异有统计学意义(P<0.05)。见表2。
2.3 剔除切缘阳性后,疫苗接种组复发3例,非疫苗接种组0例,两组比较差异无统计学意义(P>0.05)。剔除切缘阳性后高危型HPV感染非疫苗接种组9例(6.47%),疫苗接种组1例(0.96%),差异显著(P<0.05)。见表3。
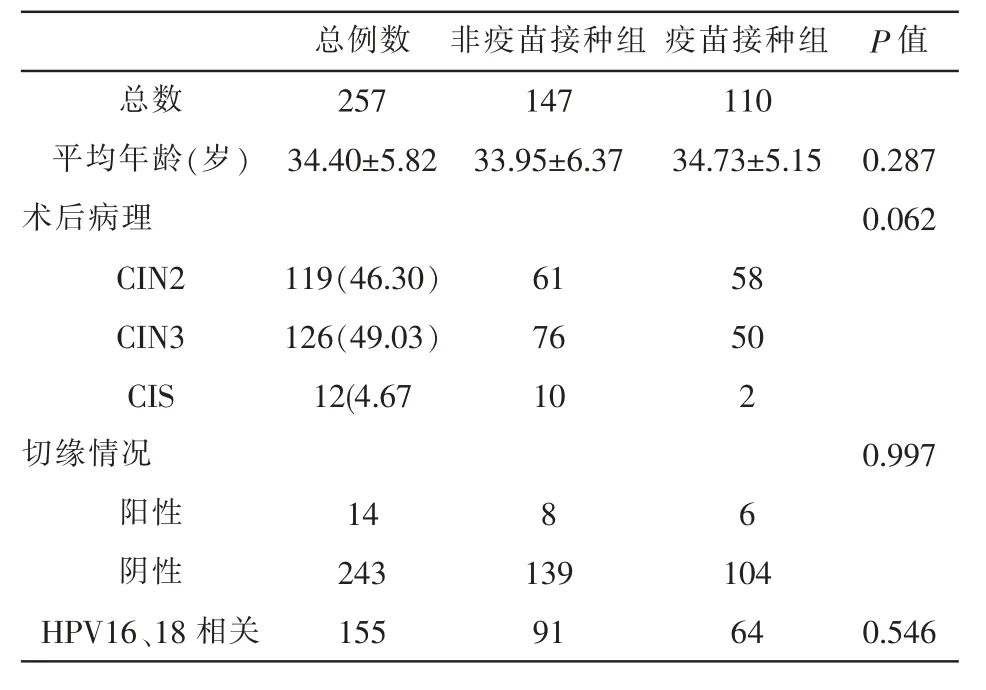
表1 CIN患者临床基本特征
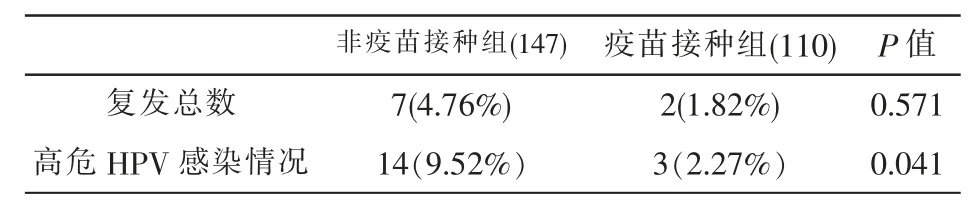
表2 疫苗接种组与非疫苗接种组随访情况比较

表3 切缘阳性剔除后疫苗接种组与非疫苗接种组随访情况比较
3 讨论
致癌型人乳头瘤病毒(HPV)是宫颈癌及其癌前病变发生的主要病因[11]。基于这些知识,在过去几十年里,随着预防性疫苗的开发,一级预防和通过在宫颈筛查中使用初级HPV核酸检测进行二级预防都取得了重大进展[12],其次是治疗筛查发现的宫颈高级别鳞状上皮内病变(HSIL))[13]。宫颈环形电切术(LEEP)和宫颈冷刀锥切术(CKC)是临床治疗HSIL的主要手段,可将病变组织切除,保留宫颈的解剖功能与结构。但是无论哪种方法还是存在一定的病灶残留和疾病复发的风险。研究表明影响复发的因素有病变程度、病变面积、术前HPV高载量、切缘受累情况等[14-15]。而减少疾病的复发一直是临床医师努力研究的方向。
既然HPV的持续感染是疾病发生发展的基础,HPV预防性疫苗的接种成功实施显著降低了宫颈癌的发病率[16]。那么对HPV疫苗作为手术切除后的预防辅助治疗是否也能起到一定作用呢?虽然CIN病灶得到治疗,低水平持续感染或潜在HPV感染的再激活,或治疗后又出现新感染,都有可能再次导致病变复发从而进展为宫颈浸润癌。自然感染后约50%产生低水平抗体,对再次感染仅仅能提供部分而不是全部的保护[7]。所以经诊断和治疗后CIN的妇女接种预防性HPV疫苗,可预防HPV再次感染,从而使疾病复发的风险降低,这在生物学上也是合理的。有学者提出宫颈CIN治疗后接种HPV疫苗预防复发的机制可能包括:1.抑制潜伏感染的HPV再激活2.预防新发感染3.增强机体免疫。即CIN治疗后的感染可能是既往HPV感染的持续,也可能是新发感染[17]。
目前越来越多的证据支持宫颈高级别病变锥切术后接种HPV疫苗,可降低宫颈病变的复发率。2013年,W.D.Kang[10]等人对737名LEEP术后的妇女进行了回顾性分析,其中360名接种四价HPV疫苗,377名未接种HPV疫苗,复发率分别为2.5%和7.2%。研究显示锥切术后不接种HPV疫苗是LEEP术后复发的独立危险因素(p<0.001)。2018年意大利前瞻性随机对照研究表示接种HPV疫苗可显著降低宫颈病变治疗后HPV相关疾病的复发[18]。2020年西班牙真实世界研究显示接种疫苗可使病变持续或者复发的风险降低4.5倍[19]。基于此,我们对临床现有资料进行了随访探究,包括110名接种了进口二价HPV疫苗的锥切术后患者和147名未接种HPV疫苗术后患者,发现接种HPV疫苗组术后复发率较未接种疫苗组确实有降低,接种疫苗是保护因素(分别为1.82%和4.76%,(OR)=0.37);但两组之间差异无统计学意义(P>0.05)。分析原因可能与我院总体术后复发率相对较低,研究的病例总数较少,随访时间不够,限制了疫苗的效力有一定的关系。但值得重视的是随访结束时高危型HPV感染率疫苗接种组较非疫苗接种组是显著下降的(P<0.05),因此我们可以推测,随着时间的发展,接种HPV疫苗组术后复发率将会明显下降。
综上,对现有证据的回顾表明宫颈高级别病变锥切术后的妇女接种预防性HPV疫苗复发风险将会降低,但这也需要更大样本的前瞻性随机对照数据来评估其最终的有效性和成本效益,值得探究。
