全自动移液工作站在肺炎疫苗多重调理吞噬实验中的应用
2022-02-12杜慧竟张全仓李江姣叶强
杜慧竟,张全仓,李江姣,叶强
1.中国食品药品检定研究院卫生部生物技术产品检定方法及其标准化重点试验室,北京102629;
2.帝肯(上海)贸易有限公司,上海200122
肺炎链球菌寄居在人体鼻咽部,通过呼吸道飞沫进行传播,可引起肺炎、菌血症、脑膜炎、中耳炎等疾病,是儿童和老年人获得性感染的主要病原菌[1]。接种肺炎链球菌疫苗可有效预防肺炎链球菌感染[2]。为了保证疫苗质量,所有肺炎链球菌疫苗上市前均需对其免疫保护效力进行测定。目前针对该疫苗,普遍采用的体外效力检测方法是酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)和体外调理吞噬实验(opsonophagocytic assay,OPA)。前者利用抗原-抗体的特异性结合特性对待测血清中的抗体水平进行检测[3],ELISA方法操作流程较为简便快捷,可用全自动移液工作站替代手动操作完成大部分实验步骤[4-5],但只能检测抗体的总含量,无法将功能性抗体甄别出来,不能真实反应疫苗的免疫保护效果[6-7]。OPA法通过检测抗体的调理吞噬活性,能够直接反映功能性抗体含量,实现对疫苗保护效力的准确评估[8-9]。近年来已有多项研究指出,通过直接检测抗体的调理能力来评估疫苗效力更为可靠,因为抗体是通过促进吞噬细胞对肺炎球菌的调理吞噬作用来提供保护力的[10-11]。
美国阿拉巴马大学通过长期探索,建立了优化的多重调理吞噬实验(multiplexed opsonophagocytic killing assay,MOPA),可同时对4种血清型的肺炎球菌功能抗体进行检测,减少了工作量,并节约了血清样本,提高了OPA技术的检测通量[12]。但与ELISA实验相比,MOPA的操作流程较为复杂,技术要求高,影响因素较多,目前国内外实验室仍以手动操作为主。为了提高效率,减少人力投入,本研究旨在将全自动移液工作站应用于MOPA中,探索由机械臂代替手动操作完成部分实验流程的可行性。
1 材料与方法
1.1细胞、菌株及血清样本 HL-60细胞系购自美国ATCC(CCL-240);13个血清型的肺炎链球菌菌株(带有特定抗生素抗性)由美国阿拉巴马大学伯明翰分校Moon H Nahm实验室提供;11份血清样本来自23价肺炎球菌多糖疫苗免疫后的健康人群(企业惠赠)。
1.2主要试剂及仪器 补体来自SPF级新西兰3~4周龄乳兔,由本室制备;标准血清007sp来自于美国FDA;BactoTMTodd Hewitt Broth(THB)(批号:725-0806)和酵母提取物购自美国Becton Dickinson公司(批号:8015615);RPMI1640购自美国Gibco公司(批号:8118152);胎牛血清购自澳大利亚ExCell公司(批号:1428479);二甲基甲酰胺(dimethylformamide,DMF,批号:BCBW2583)、2,3,5-氯化三苯基四氮唑(triphenyltetrazoliumchloride,TTC,批号:BCCB1241)、4种抗生素:奥普脱欣(optochin,批号:BCBV2536)、奇霉素(spectinomycin,批号:122K0561)、甲氧苄氨嘧啶(trimethoprim,批号:BCBN2518V)和链霉素(streptomycin,批号:SLBX2654)均购自美国Sigma公司;1号全自动移液工作站(型号Freedom EVO150,MCA机械臂,简称1号工作站)和3号全自动移液工作站(型号Freedom EVO150,LIHA机械臂,简称3号工作站)购自瑞士帝肯公司;菌落计数器(型号:ProtoCOL 3)购自英国Synbiosis公司。
1.3M OP A手动操作方法 血清样本于56℃放置30 min后,在96孔板的H行中进行5~20倍预稀释,之后由H向A行进行3倍系列稀释为8个梯度,每孔20μL;血清稀释板中加入10μL按一定比例混合的带特定抗生素抗性的各型肺炎球菌,每次混合4种血清型的肺炎球菌,置于振动器上室温孵育30 min;每孔加入10μL补体和40μL用DMF诱导分化5 d的HL-60细胞[13-14],置于37℃,5%CO2培养箱中振荡孵育45 min;将96孔板冰上放置20 min;各孔取10μL反应液,分别点至4个含THY琼脂培养基的方形平皿内,室温吸收20 min;分别覆盖含4种不同抗生素及TTC的上层培养基,37℃,5%CO2培养箱中过夜培养后,利用菌落计数器计数各平板上的菌落数;用Opsotiter 3软件计算样本的OPA滴度。详细操作步骤见文献[15]。
1.4M OP A工作站操作方法
血清样本、肺炎球菌混合菌液、补体和细胞液的处理和配置均与手动操作相同。仪器操作步骤分为1号工作站和3号工作站两部分。
1.4.11号工作站 在96孔板的H行中将血清样本进行5~20倍预稀释后放入1号工作站中。在1号工作站中编入操作程序:依次进行每孔稀释液分装;从H行向A行进行3倍系列稀释共8个梯度;每孔加入10μL混合菌液,振动孵育30 min;每孔加入50μL补体和细胞混合液。从工作站中取出96孔板,置于37℃,5%CO2培养箱中振荡孵育45 min;之后冰上放置20 min。点样、培养、计数和结果计算均与上述手动操作方法相同。参数设置:分装稀释液、菌液和细胞悬液的液体类型为MCA加液模式(MCA add dilution),吸液速度150μL/s,喷液速度600μL/s;血清吸液和混匀的液体类型为MCA混匀模式(MCA mix),吸液速度30μL/s,喷液速度100μL/s。
1.4.23号工作站 在3号工作站上编入程序:将稀释液和血清分别按照设定好的预稀释倍数加入到稀释板上,并混匀;再从稀释板上分装到实验板的H行,每份血清平行分装2孔,30μL/孔。参数设置:分装稀释液的液体类型为非接触性喷液(water free dispense),吸液速度150μL/s,喷液速度600μL/s;血清吸液和混匀的液体类型为血清(serum-s-Ep),吸液速度30μL/s,喷液速度100μL/s。
1.5结果分析
1.5.1相关系数计算 将手动操作结果与工作站操作结果均转换为以2为底的对数,进行线性回归分析,计算相关系数。
1.5.2差值分析 手动操作与工作站操作分别检测11份样本,计算两种方法的各型别滴度差在3倍以内的样本比例。
1.5.3试验内精密性 工作站在一次试验内对6份样本进行5次重复检测或3份样本进行6次重复检测,计算每份样本重复检测结果的均值,比较每次结果是否在均值的上下3倍之内。
1.5.4试验间精密性 工作站对11份样本进行5次平行试验,计算每份样本平行检测结果的均值,比较每次结果是否在均值的上下3倍之内。
2 结果
2.1梯度稀释、菌液分装、细胞液分装(1号工作站实验部分)验证
2.1.1PCV13免疫血清样本手动操作与工作站操作结果的相关性 11份血清样本的13个型别手动操作结果与工作站操作结果的相关系数均在0.90以上,除6B和9V型,11份样本两种操作方式检测结果的差值80%以上均在3倍以内,见表1。
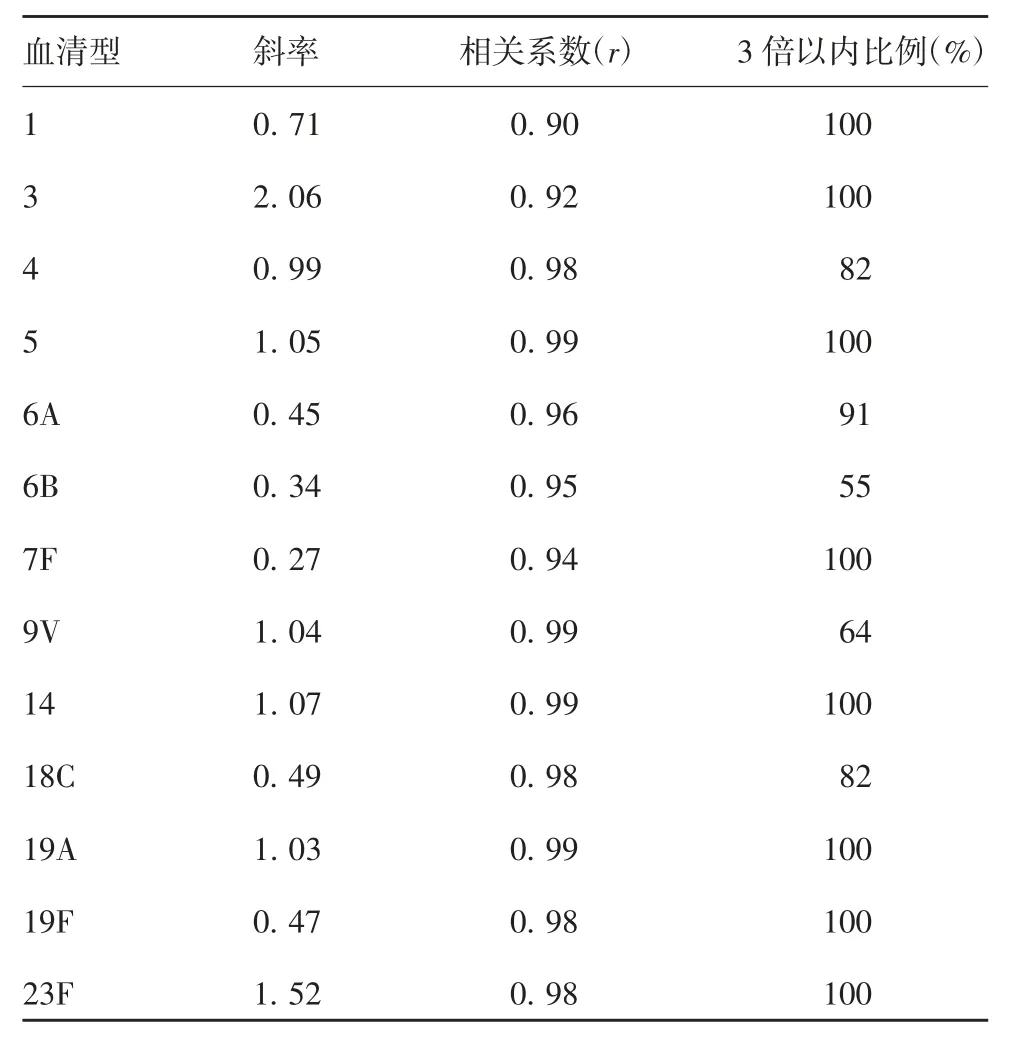
表1 1号工作站实验部分与手动操作结果的相关性和差值Tab.1 Correlation and difference of determination results by robot No.1 and by manual operation
2.1.2试验内精密性 用1号工作站同时对6份样本13个型别进行5次平行试验,每份血清的滴度结果都在均值的上下3倍以内,重复性良好,见图1。
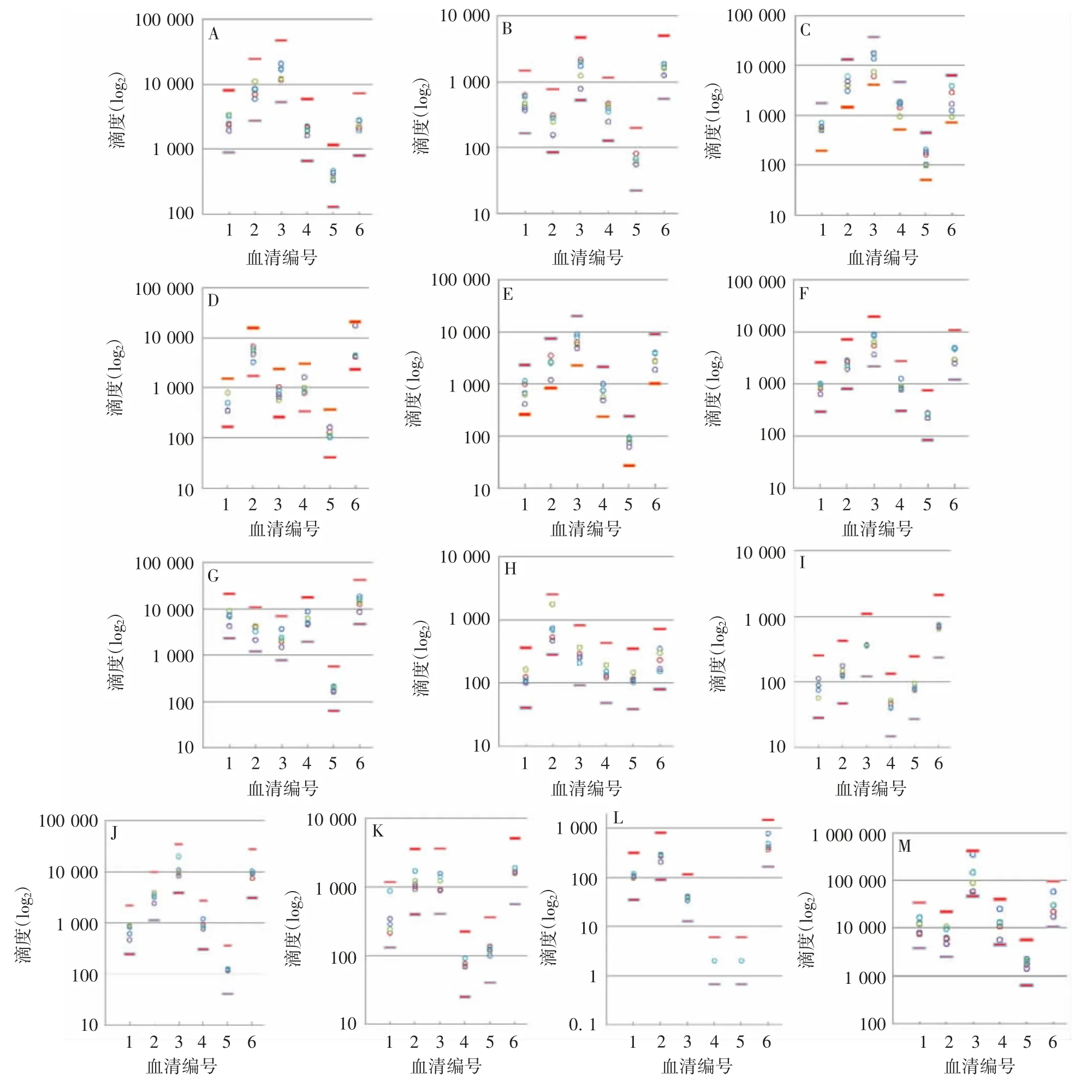
图1 1号工作站对6份样本13个型别进行5次平行试验的结果Fig.1 Results of five parallel assays on six samples of 13 types by robot No.1
2.2预稀释验证(3号工作站实验部分)
2.2.1预稀释手动操作与工作站操作结果的相关性 分别用3号工作站和手动操作对11份血清进行预稀释并分装在实验板H行中,之后一同用1号机进行后续实验步骤,所有血清两种方法检测的滴度值相差均在3倍之内,相关系数均在0.7以上,见表2。

表2 3号工作站实验部分与手动操作结果的相关性和差值Tab.2 Correlation and difference of determination results by robot No.3 and by manual operation
2.2.2预稀释试验内精密性 用3号工作站同时对3份样本进行6次平行预稀释试验,每份血清的滴度均在均值的上下3倍以内,重复性良好,见图2。

图2 3号工作站对3份样本4个型别进行6次试验内精密性验证结果Fig.2 Verification for precision in six intra-assays on three samples of four types by robot No.3
2.3试验间精密性验证 用3号工作站进行血清预稀释,之后用1号机进行稀释液分装、血清梯度稀释、菌液和细胞液分装,对11份样本4个型别重复5次平行检测试验,每份血清5次检测的滴度均在均值的上下3倍以内,重复性良好,见图3。
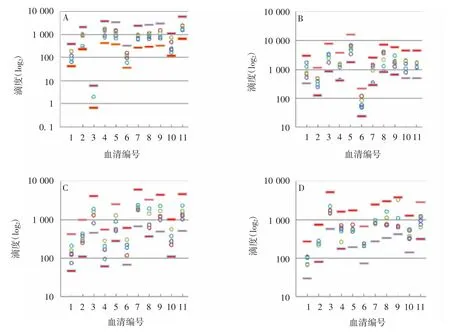
图3 3号和1号工作站对11份样本4个型别进行5次试验间精密性验证结果Fig.3 Verification for precision in five inter-assays on 11 samples of four types by robots No.3 and No.1
3 讨论
MOPA目前已成为WHO推荐使用的肺炎球菌疫苗效力评价方法,但其操作复杂繁琐,且系统体积较小,对每一步的操作误差要求较高。因此,该方法一直难以用自动化代替人工。但随着肺炎疫苗的发展,国内肺炎疫苗的临床检验项目日益增加,本研究首次尝试用全自动移液工作站进行MOPA部分操作步骤,旨在节约人力,提高实验效率。
本研究使用了两台全自动移液工作站进行OPA技术操作,通过对11份13价肺炎球菌结合疫苗血清效价的检测,与手动操作进行比较。其中3号工作站进行血清预稀释和分装,1号工作站进行稀释液分装、血清梯度稀释、菌液和细胞液的分装。经前期多次试验摸索,将工作站的加液模式设定为血清类型的系列模式,对吸液和喷液速度进行调试,并确定了每一步的合适数值,以达到误差和残留最少。
1号工作站对11份血清样本13个型别的检测结果与手动操作结果的相关系数均高于0.90,各型的滴度差值80%以上样本均在3倍以内(6B和9V型分别只有55%和64%的样本在3倍以内,可能由于机器和手动操作所在实验室不同而温湿度不同,两个操作方法也不可能做到完全同步,而影响到补体的非特异杀伤力、细胞活力和菌株的生长速度,个别型的菌株对补体和温湿度更为敏感,从而在本次实验中表现出较大的差异),因此,在血清梯度稀释和稀释液、菌液、细胞液分装过程,工作站与手动操作无明显差异。用3号工作站对11份血清进行预稀释并分装在实验板中,与手动操作比较,各血清的效价均在3倍以内,处于可接受误差范围内。
1号工作站MCA机械臂为单通道分成96个分液孔,出液几乎不存在显著误差;而在操作过程中,实验板均平铺于操作台面上,不同板之间因位置不同而在加液和梯度稀释过程中可能产生细微误差,因此选择板(6个样本/板)之间的平行试验进行精密性验证。3号工作站的LIHA机械臂为8个独立通道,每个通道之间可能存在细微误差;而血清预稀释操作均在同一块96孔板中进行,因此选择在同一板内进行6次平行试验进行精密性验证。此外,3号工作站只进行血清预稀释步骤,不涉及型别和菌株操作,因此,验证3号机精密性和准确性时只是代表性地随机选择了4个型别(MOPA一次试验可同时检测4个型别的滴度)。两台工作站对平行板或平行样本检测的滴度值均在均值上下3倍以内。
经前期的实验条件摸索和后续的方法验证,在保证实验准确性和重复性良好的条件下,自动化工作站能够完成除点样和计数外的全部实验步骤,替代了1~2人的工作量,且实验用时也与人工操作基本相同。目前只有点样环节因略为复杂尚未找到机械替代方法,将在后续研究中继续探索机械化点样方法,并对工作站进行MOPA准确性、线性、特异性、稳定性等系统性验证,以实现工作站替代人工投入到临床样本的检验过程中。
