低氧诱导因子1α和长链非编码RNA-SNHG15在脑梗死发生发展中的表达及临床意义
2022-02-11张晨昕沈越刘瑞雪张赫楠赵阳
张晨昕,沈越 ,刘瑞雪,张赫楠,赵阳
1.齐齐哈尔医学院附属第三医院神经内科三病房,黑龙江齐齐哈尔 161000;2.齐齐哈尔医学院附属第三医院泌尿外科病房,黑龙江齐齐哈尔 161000;3.齐齐哈尔医学院附属第三医院内科,黑龙江齐齐哈尔 161000
脑梗死(cerebral infarction)作为临床上常见的脑血管疾病,具有极高的致死率与致残率,并且严重的影响着人类的健康生活,其发病率也随着社会的发展在不断增长。脑梗死在临床上又称为缺血性脑卒中,主要是由各种原因导致的脑部血液循环发生障碍,使脑部组织局部缺血缺氧甚至坏死,而出现的一种神经功能缺损的临床综合征[1]。长链非编码RNA是长度大于200个核苷酸的非编码RNA[2],参与各种细胞生命活动的调控,与多种疾病的发生发展关系密切[3]。在前期研究中,发现长链非编码RNA—核仁小RNA宿主基因15(SNGH15)在脑梗死患者的外周血中呈异常高表达,并且在低氧胁迫条件下表达明显上调,这提示SNGH15可能与脑梗死的发生有着密切关系。低氧诱导因子-1是一种转录因子,其在机体抗缺血缺氧方面发挥着重要作用[4],目前研究表明,低氧诱导因子-1与靶基因特定序列结合从而调控它们的转录与表达,并可能参与对低氧反应的信号转导,以维持机体氧的自我平衡与氧的稳态,从而在缺血缺氧脑损伤中发挥重要作用。2021年7—9月本研究通过制备30只大鼠缺血性脑损伤模型,采用qPCR检测上述样本HIF-1α、SNHG15动态表达水平,分析其表达时间关系及表达水平的相关性。现报道如下。
1 对象与方法
1.1 研究对象
成年SD大鼠30只,体质量250~280 g,雌雄不限,随机分为模型组(24只):接受动脉结扎和断开手术;假手术组(3只):只接受动脉分离,并不结扎和断开动脉,直接缝合;正常对照组(3只):不接受任何手术。模型组再分为缺血2 h、再灌注4 h、再灌注12 h和再灌注24 h组,每组6只。
1.2 方法
1.2.1 制备大鼠缺血性脑损伤模型 模型建立参照Belayev改良Longa法。在室温(25℃)条件下,用3.6%的水合氯醛腹腔麻醉动物,在颈部正中做切口,结扎左侧颈外动脉远端,颈总动脉及颈内动脉置动脉瘤夹,断开左侧颈外动脉后插入末端涂有一层1%的左旋多聚赖氨酸的直径0.25 mm的尼龙线,深度为距颈总动脉分叉处18 mm,2 h后再次麻醉动物并拉出尼龙线。假手术组尼龙线插入深度为15 mm,余步骤相同。手术期间保持大鼠肛温在36.5~37.5℃。假手术组动脉分离后不结扎不断开,直接缝合切口。
1.2.2 取材 分别在2、4、12、24 h采集大鼠外周血,在24 h采集大鼠脑缺血区组织。采用qPCR检测上述样本低氧诱导因子1α(hypoxia-inducible factor 1α, HIF-1α)、SNHG15动态表达水平,分析其表达时间关系及表达水平的相关性。
1.2.3 荧光定量qPCR检测 按照RNA反转录试剂盒说明合成cDNA。使用实时聚合酶链式反应(polymerase chain reaction, PCR)系统进行实时逆转录PCR(qPCR)。以甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase, GAPDH)作为内参照,用 2-ΔΔCt方法计算各组样本的 SNGH15、HIF-1α的相对表达量,实验重复3次。
1.2.4 TTC染色 将脑组织放入-20℃冰箱速冻20 min,取出后按照实验要求进行切片,切片后将组织放入2%氯化三苯基四氮唑(triphenyltetrazolium chloride, TTC)中,并用锡箔纸盖住,置于37℃温箱中存放25 min,每5分钟翻动1次切片。然后用10%甲醛溶液固定,留置过夜,观察脑组织切片呈色情况。
1.2.5 EMSA检测 将设置好的探针反应体系加入同位素后,用Vortex混匀,再加入T4 Polynucleotide Kinase,混匀。使用水浴或者PCR仪,73℃反应10 min,加入1 μl探针标记终止液,混匀,终止标记反应,再加入89 μl TE,混匀,存于-20℃冰箱备用。核蛋白样本提取与蛋白定量。生物素标记DNA3’端并去吹TdT。Super-Shift反应,配制6.5%聚丙烯酰胺凝胶,配制好各反应体系,凝胶阻滞实验(electrophoretic mobility shift assays, EMSA)室温结合反应20 min,电泳上样。电转膜,操作方法同常规Western blot转膜操作。紫外交联,将核酸交联于PVDF膜上。化学发光法检测生物素标记的探针。
1.2.6 荧光素酶报告基因检测 合成SNGH15的3’非编码区,退火后插入荧光素酶基因下游的pCheck2报告荧光素酶载体的Xho1和NotⅠ位点。为了引入突变,将与3’UTR中HIF-1a的结合位点互补的序列(位点 1:5’-UGUUCUAGCUUCUCCC-3’,位点 2:5’-UU CCCCAACCUUCCU-3’,位点3:5’-UUCAUAGCCU UCUCCU-3’)替 换 为 位 点 1:5’-UGUUUCUAG UUACACCC-3’,位 点 2:5’-UUCCU-3’。经核苷酸测序证实构建成功。将SNGH15的阴性对照空载质粒或HIF-1a模拟质粒共转染细胞。荧光素酶检测采用双荧光素酶报告分析系统(PROMEGA)。
1.2.7 染色质免疫共沉淀(Chip) 在细胞生长状态下,加入交联剂,对蛋白-染色质复合物进行交联固定,裂解细胞,释放蛋白-染色质复合物,通过超声或酶解打断长染色质片段,用抗体进行免疫沉淀,富集特异蛋白-DNA复合物,洗脱特异蛋白-DNA复合物,解交联并消化蛋白,进行核酸纯化,纯化后的核酸进行PCR分析。
1.3 统计方法
采用SPSS 20.0统计学软件进行数据分析,计量资料符合正态分布,以(±s)表示,比较采用t检验;两变量之间相关性采用Spearman相关性分析,P<0.05为差异有统计学意义。
2 结果
2.1 SNGH15和HIF-1α的表达情况
与假手术组和正常对照组比较,模型组大鼠外周血与脑组织中SNHG15的表达水平明显升高,且随着时间的推移表达水平在不断升高,12 h达到最高峰,随后迅速下降,24 h时表达仍高于假手术组和正常对照组,差异有统计学意义(P<0.001);正常对照组与假手术组之间SNGH15的表达水平比较,差异无统计学意义(P>0.05)。见表1。与假手术组和正常对照组比较,模型组大鼠 2、4、12、24 h的HIF-1α表达水平明显升高,差异有统计学意义(P<0.001);而假手术组和正常对照组之间HIF-1α表达水平比较,差异无统计学意义(P>0.05)。见表2。
表1 SNHG15的表达情况(±s)

表1 SNHG15的表达情况(±s)
组别模型组2 h (n=6)4 h (n=6)12 h (n=6)24 h (n=6)假手术组(n=3)正常对照组(n=3)F值P值表达情况138.33±1.818 152.30±1.417 168.58±1.654 122.03±1.243 53.20±2.331 53.96±1.059 3 729.676<0.001
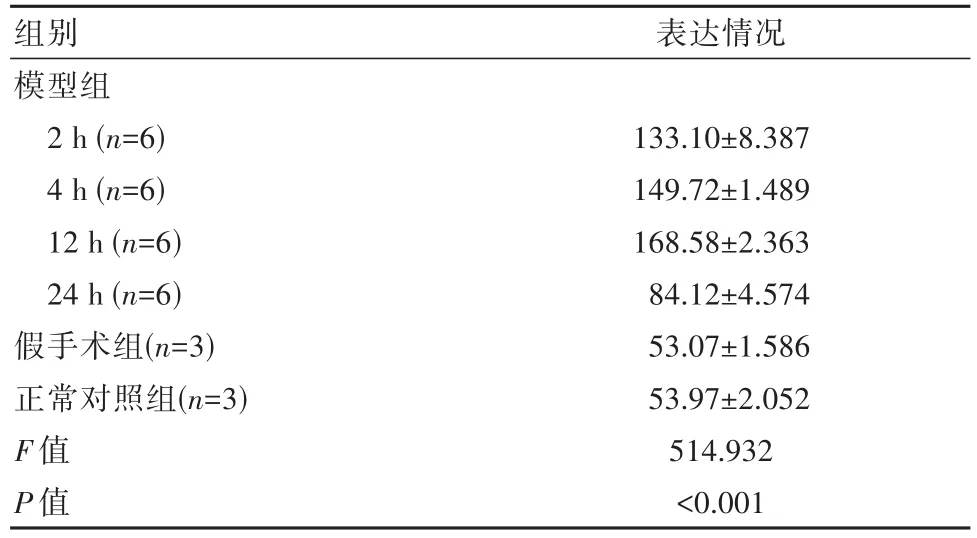
表2 HIF-1α的表达情况
2.2 大鼠脑梗死灶的呈色情况
TTC染色检测结果可见,正常对照组和假手术组大鼠脑组织呈砖红色,且未发现梗死灶的存在。模型组大鼠脑组织呈苍白色,并且与周围正常组织之间边界清晰,具有明显的梗死区域。见图1。

图1 TTC染色检测大鼠脑梗死灶的呈色情况
2.3 SNHG15调控细胞增殖凋亡的信号通路
荧光素酶报告基因检测:将过表达的HIF-1α质粒和空载质粒分别同SNHG15启动子质粒一起转染细胞,检测报告基因转录活性,发现模型组启动子的活性超过正常对照组的2倍,SNHG15启动子区域具有转录因子HIF-1α的结合位点。见图2。

图2 荧光素酶报告基因检测SNHG15启动子与转录因子HIF-1α结合位点情况
EMSA及染色质免疫共沉淀(Chip)检测:Thermo Scientific Plerce琼脂糖Chip试剂盒显示,NeuroD、C/ebp和RNA聚合酶Ⅱ与近端SNHG15的启动子结合。稳定的过表达克隆细胞因子在0.2%炭葡聚糖处理的培养基中培养3 h,然后用100 ng/mL的HIF-1α处理细胞15 min,使用适当的抗体和Pierce Chip Kit对3个靶点进行染色质免疫沉淀,发现HIF-1α处理后与SHNG15的启动子结合增加。见图3。

图3 EMSA及染色质免疫共沉淀(Chip)检测SNHG15启动子与转录因子HIF-1α结合情况
3 讨论
小核仁RNA宿主基因15(SNHG15)是一种产生短半寿命lncRNA的snoRNA宿主基因[5],在肿瘤细胞中上调并参与多种癌症的发生发展,涉及到肿瘤细胞的侵袭、转移等生物学过程[6],在细胞的增殖凋亡调控中发挥着重要的作用。
本研究中,在低氧条件下SNHG15的含量升高,并且与缺氧的程度有着密切关系,与正常对照组比较,模型组大鼠外周血中SNHG15的表达水平在2、4、12、24 h分别为(138.33±1.818)、(152.30±1.417)、(168.58±1.654)、(122.03±1.243),4个时间点上都显著增高,其表达从2 h开始发生,随着时间的推移不断升高,12 h达到峰值,随后迅速下降,24 h时SNHG15的表达水平仍然高于正常对照组大鼠(P<0.05);而假手术组大鼠(53.20±2.331)与对照组大鼠(53.96±1.059)之间SNHG15的表达水平比较,差异无统计学意义(P>0.05);而模型组大鼠SNHG15的表达水平在上述十个时间点也均高于假手术组大鼠(P<0.05)。这与冀方超等[7]的研究结果一致,其研究中,SNHG15在急性脑梗死患者的外周血中异常高表达,表达量为(5.94±1.05),尤其是重症患者最高,SNHG15异常表达的表达量(6.76±0.61)与NIHSS评分呈正相关(r=0.730,P<0.05),与神经功能缺损程度以及多项病理参数有着密切的关系。同时,相关研究显示,低氧培养时可促进SNHG15表达(5.877 5±0.365 97)上调(P<0.05)[8],这与本文研究结果基本一致,这说明SNHG15的含量与脑细胞缺氧程度之间关系密切。
HIF-1α作为HIF-1的调节亚基,其蛋白转录活性和稳定性都是受到细胞内氧的含量浓度调节[9],HIF-1α的N端的bHLH域,与下游PAS域共同构成HIF-1α的氧张力感受区[10],JAK2/STAT3/HIF-1α信号通路的激活或抑制对脑缺血再灌注的影响是复杂的,并不是单一的保护或者损害作用[11]。邓文骞等[12]在对大鼠缺血再灌注脑梗死的实验中发现,大脑局灶性缺血2 h再灌注后,大鼠大脑HIF-1α mRNA的水平和蛋白水平均比对照组高,缺血缺氧激活脑神经细胞HIF-1α基因的表达。本研究中:与正常对照组比较,模型组大鼠2、4、12 h外周血中HIF-1α的表达水平都显著增高(133.10±8.387)、(149.72±1.489)、(168.58±2.363),到 24 h时 HIF-1α的表达水平(84.12±4.574)虽然没有达到显著水平,但是仍然高于正常对照组大鼠(53.97±2.052)(P<0.05);而假手术组大鼠与正常对照组大鼠之间HIF-1α的表达水平差异无统计学意义(P>0.05)。这与顾霞等[13]研究结果:发现不同时间点,观察组HIF-1α浓度均显著高于对照组,分别以1、5 d后为例,1 d后大面积梗死组(3 287.6±1 472.1)、小面积梗死组(1 645.7±472.4),5 d后大面积梗死组(1 514.7±329.8),小面积梗死组(920.9±271.4),血清HIF-1a浓度与脑梗死面积存在显著正相关关系(r=0.754,P<0.05),HIF-1α参与了急性脑梗死的发生、发展过程的研究结果一致。表明在低氧相关疾病及高原病发生过程中,低氧诱导因子1α和相关信号通路中的关键因子的表达水平会发生不同程度变化[14]。表明在缺血缺氧胁迫条件下能够刺激HIF-1α的表达,调控其下游靶基因的表达,而发挥脑保护作用。急性脑梗死患者血清中低氧诱导因子-1α的表达呈动态变化规律,在脑梗死的发生发展中发挥着重要的作用[15];Notch信号通路在缺血再灌注损伤中被激活,其机制可能与HIF-1α有关[16],而且高原适应具有遗传学基础,尤其与HIF通路及低氧反应基因密切相关[17]。因此,HIF-1α和SNGH15可作为脑梗死诊断标记分子,能够对脑细胞增殖与凋亡进行调控,并且参与脑梗死的发生发展,LncRNA常常通过竞争性的结合并抑制microRNA而影响其下游基因的表达发挥作用。
综上所述,本研究利用体内动物模型,鉴定SNHG15的启动子区域,发现具有转录因子HIF-1α的结合位点,从而明确HIF-1α和SNHG15在脑梗死中的作用及其机制。有望为临床治疗脑梗死患者提供新的靶点,具有重要的科学意义和应用价值。
