NOACs与华法林用于心脏瓣膜置换术后患者抗凝有效性和安全性的Meta分析
2022-02-07周强吴思凡王熙尧杨元素陶瑛瑛黄晓晖魏萌
周强 吴思凡 王熙尧 杨元素 陶瑛瑛 黄晓晖 魏萌



中圖分类号 R542.5;R973 文献标志码 A 文章编号 1001-0408(2022)02-0230-06
DOI 10.6039/j.issn.1001-0408.2022.02.17
摘 要 目的 比较新型口服抗凝药(NOACs)与华法林用于心脏瓣膜置换术后患者抗凝的有效性和安全性,旨在为临床用药提供循证参考。方法 计算机检索PubMed、Cochrane图书馆、Embase、Web of Science、中国知网、万方数据、维普网,收集NOACs(试验组)对比华法林(对照组)用于心脏瓣膜置换术后患者抗凝的临床研究,检索时限均为建库起至2021年7月。筛选文献、提取资料后,采用Cochrane系统评价员手册5.2.0推荐的偏倚风险评估工具对纳入的随机对照研究(RCT)进行质量评价,采用纽卡斯尔-渥太华量表(NOS)对纳入的队列研究进行质量评价,采用RevMan 5.3软件进行Meta分析和敏感性分析。结果 共纳入9项研究,包括7项RCT和2项队列研究,共计4 962例患者。Meta分析结果显示,生物瓣膜置换/修复术后,试验组患者的卒中/系统性栓塞(SSE)发生率[OR=0.71,95%CI(0.52,0.97),P=0.03]、大出血发生率[OR=0.40,95%CI(0.30,0.54),P<0.000 01]、颅内出血发生率[OR=0.20,95%CI(0.04,0.95),P=0.04]均显著低于华法林组,两组患者的全因死亡率比较差异无统计学意义[OR=1.25,95%CI(0.88,1.79),P=0.22]。机械瓣膜置换/修复术后,两组患者的SSE发生率[OR=1.52,95%CI(0.04,60.29),P=0.82]、全因死亡率[OR=0.26,95%CI(0.04,1.84),P=0.18]比较差异均无统计学意义。按随访时间进行的亚组分析结果显示,生物瓣膜置换/修复术后,当随访时间≤3个月时,试验组患者的SSE发生率显著低于对照组[OR=0.20,95%CI(0.06,0.74),P=0.03],而两组患者大出血发生率比较差异无统计学意义[OR=0.67,95%CI(0.19,2.38),P=0.53];当随访时间>3个月时,两组患者的SSE发生率比较差异无统计学意义[OR=0.74,95%CI(0.54,1.02),P=0.07],而试验组患者的大出血发生率显著低于对照组[OR=0.39,95%CI(0.29,0.52),P<0.001]。按研究类型进行的亚组分析结果显示,生物瓣膜置换/修复术后,RCT研究中试验组患者的SSE发生率显著低于对照组[OR=0.51,95%CI(0.29,0.92),P=0.03],而两组患者大出血发生率比较差异无统计学意义[OR=0.58,95%CI(0.33,1.03),P=0.06]。队列研究中两组患者的SSE发生率比较差异无统计学意义[OR=1.03,95%CI(0.40,2.66),P=0.95],而试验组患者的大出血发生率显著低于对照组[OR=0.20,95%CI(0.06,0.74),P<0.001]。敏感性分析结果显示,所得结果较稳健。结论 对于生物瓣膜置换/修复术后患者,NOACs的有效性和安全性均优于或与华法林相当;对于机械瓣膜置换/修复术后患者,NOACs与华法林的有效性和安全性均无显著差异。
关键词 新型口服抗凝药;华法林;心脏瓣膜置换术;术后抗凝;疗效;安全性;Meta分析
Anticoagulant effectiveness and safety of new oral anticoagulants versus warfarin after heart valve replacement: a meta-analysis
ZHOU Qiang1,WU Sifan2,WANG Xiyao3,YANG Yuansu4,TAO Yingying1,HUANG Xiaohui1,WEI Meng1(1. Dept. of Clinical Pharmacy, General Hospital of Eastern Theater Command, the Chinese People’s Liberation Army, Nanjing 210002, China; 2. College of Pharmacy, Nanjing Jiangbei Hospital, Nanjing 210032, China; 3. School of Pharmacy, Nanjing Medical University, Nanjing 210029, China; 4. Dept. of Research Training Division, General Hospital of Eastern Theater Command, the Chinese People’s Liberation Army, Nanjing 210002, China)
ABSTRACT OBJECTIVE To compare the anticoagulant effectiveness and safety of new oral anticoagulants (NOACs) and warfarin after heart valve replacement, and to provide evidence-based reference for clinical drug use. METHODS Retrieved from PubMed, Cochrane Library, Embase, Web of Science, CNKI, Wanfang database and VIP, clinical studies about the use of NOACs versus warfarin after heart valve replacement were collected during the inception to July 2021. After literature screening and data extraction, the quality of included randomized controlled trials (RCTs) were evaluated by bias risk assessment tool recommended by Cochrane system evaluator manual 5.2.0. After the quality of the included cohort studies was evaluated by Newcastle-Ottawa scale (NOS), RevMan 5.3 software was used for meta-analysis and sensitivity analysis. RESULTS A total of 9 studies involving 4 962 patients were included, of which 7 were RCTs and 2 were cohort studies. Results of meta-analysis showed that after biological valve replacement/repair, the incidence of stroke and systemic embolism (SSE) [OR=0.71, 95%CI (0.52, 0.97), P=0.03], major bleeding [OR=0.40,95%CI(0.30,0.54),P<0.000 01] and intracranial hemorrhage [OR=0.20,95%CI(0.04,0.95),P=0.04] in trial group were significantly lower than warfarin group; there was no significant difference in all-cause mortality between 2 groups [OR=1.25,95%CI(0.88,1.79),P=0.22]. After mechanical valve replacement/repair, there were no significant difference in the incidence of SSE [OR=1.52,95%CI(0.04,60.29),P=0.82] or all-cause mortality [OR=0.26,95%CI(0.04,1.84),P=0.18] between 2 groups. The results of subgroup analysis according to the follow-up time showed that after biological valve replacement/repair, the incidence of SSE in trial group was significantly lower than that in control group when the follow-up time was ≤3 months [OR=0.20, 95%CI (0.06, 0.74), P=0.03]; but there was no significant difference in the incidence of major bleeding between 2 groups [OR=0.67, 95%CI (0.19, 2.38), P=0.53]; when the follow-up time was longer than 3 months, there was no statistical significance in the incidence of SSE between 2 groups [OR=0.74,95%CI(0.54,1.02),P=0.07], while the incidence of major bleeding in trial group was significantly lower than control group [OR=0.39,95%CI(0.29,0.52),P<0.001]. Subgroup analysis by study type showed that after biological valve replacement/repair, the incidence of SSE in the RCT in trial group was significantly lower than that in control group [OR=0.51, 95%CI (0.29, 0.92), P=0.03], but there was no significant difference in the incidence of major bleeding between 2 groups[OR=0.58,95%CI(0.33,1.03),P=0.06]. In cohort study, there was no significant difference in the incidence of SSE between 2 groups [OR=1.03,95%CI(0.40,2.66),P=0.95], while the incidence of major bleeding in trial group was significantly lower than control group [OR=0.20,95%CI(0.06,0.74),P<0.001]. Sensitivity analysis results showed that the results of the above-mentioned meta-analysis were relatively robust. CONCLUSIONS For the patients underwent biological valve replacement/repair, the effectiveness and safety of NOACs are better than or similar to those of warfarin; for the patients underwent mechanical valve replacement/repair, there is no significant difference in the effectiveness and safety between NOACs and warfarin.
KEYWORDS new oral anticoagulant; warfarin; heart valve replacement; postoperative anticoagulation; efficacy; safety; meta-analysis
心脏瓣膜病(valvular heart disease,VHD)是指因先天性发育异常或由其他各种疾病(如风湿、退行性病变、感染等)引起的心脏瓣膜及其附属结构解剖学或功能异常,最终可引发心力衰竭、心律失常等临床综合征[1]。该疾病影响着全球1亿以上的人口,每年有数十万严重的VHD患者需要进行心脏瓣膜置换术以提高生存质量和延长生存期,但由于心脏瓣膜置换术后易出现血栓,故患者需要接受抗凝治疗[2]。华法林为维生素K拮抗剂(vitamin K antagonists,VKAs),主要用于心脏瓣膜置换术后血栓的预防性治疗,虽然抗凝效果明确,但其体内代谢过程易受遗传和环境因素(食物、药物等)的影响,且治疗窗窄,临床用药时需要通过频繁调整剂量来达到目标治疗浓度[3]。
新型口服抗凝药(new oral anticoagulants,NOACs)主要包括凝血因子Ⅹa抑制剂(如利伐沙班、阿哌沙班、依度沙班)和直接凝血酶抑制剂(如达比加群)。与华法林相比,NOACs具有更快的药动学行为、更少的副作用,且无需频繁调整剂量及监测患者凝血功能[4]。2021年欧洲心律协会相关指南指出,对于生物瓣膜置换/修复术后合并房颤的患者,尤其是在术后8~12周,NOACs可作为其有效的治疗选择,但缺乏相关的循证证据;而对于机械瓣膜置换/修复术患者,VKAs是上述指南唯一推荐的用于该类患者预防卒中/系统性栓塞(stroke and systemic emblism,SSE)的口服抗凝药[5]。最新临床研究发现,NOACs可用于预防机械瓣膜性心脏病患者SSE的发生[6]。在近年来的研究中,对于非瓣膜性房颤患者,NOACs已逐步替代华法林,但NOACs用于心脏瓣膜置换术后抗凝有效性和安全性的结果不一[7]。基于此,本研究采用Meta分析的方法比较了NOACs与华法林用于心脏瓣膜置换术后患者抗凝的有效性和安全性,旨在为临床用药提供循证参考。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型 研究类型为国内外公开发表的随机对照研究(randomized controlled trial,RCT)和队列研究;语种限定为中文和英文。
1.1.2 研究对象 研究对象为接受心脏瓣膜置换术(包括机械瓣膜和生物瓣膜置换/修复术)且术后需要进行抗凝治疗的患者。
1.1.3 干预措施 试验组患者给予NOACs,包括利伐沙班、阿哌沙班、依度沙班或达比加群。对照组患者给予华法林,需根据患者的国际标准化比值(international normalized ratio,INR)调整剂量,INR目标范围为2~3。两组患者的疗程或剂量不限。
1.1.4 结局指标 本研究的结局指标包括:(1)有效性指标,如SSE发生率(主要疗效指标)、全因死亡率(次要疗效指标);(2)安全性指标,如大出血发生率(主要安全性指标,大出血标准参照国际血栓形成和止血学会相关指南定义[8])、颅内出血发生率(次要安全性指标)。
1.1.5 排除标准 排除标准包括:(1)系统评价/Meta分析、病例分析、会议摘要或综述;(2)重复发表的文献;(3)无相应结果数据的文献。
1.2 文献检索策略
计算机检索PubMed、Cochrane图书馆、Embase、Web of Science、中国知网、万方数据、维普网等,同时补充搜索未公开发表的临床试验或交流会议。中文检索词为“新型口服抗凝药”“直接口服抗凝药”“利伐沙班”“达比加群”“阿哌沙班”“依度沙班”“华法林”“维生素K拮抗剂”“生物瓣膜”“机械瓣膜”;英文检索词为“new oral anticoagulant”“direct oral anticoagulant”“rivaroxaban”“dabigatran”“apixaban”“edoxaban”“warfarin”“vitamin K antagonist”“bioprosthetic valve”“mechanical heart valve”。检索时限均为各数据库建库起至2021年7月。以PubMed为例,具体检索策略见表1。
1.3 文献筛选与资料提取
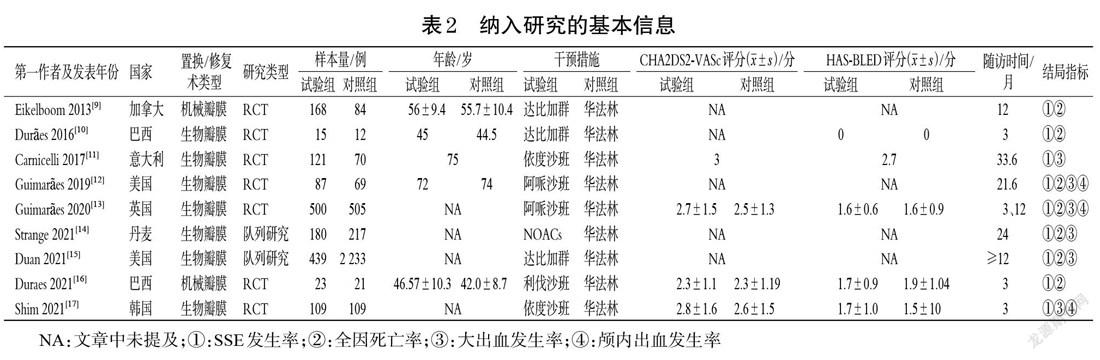
由2位研究者严格按照文献纳入与排除标准独立筛选文献,提取有效数据并交叉核对,如遇分歧则与第3位研究者商议。提取资料包括:第一作者及发表年份、国家、手术类型、研究类型、患者例数、年龄、干预措施、CHA2DS2-VASc评分、HAS-BLED评分、随访时间和结局指标等。
1.4 纳入文献质量评价
采用Cochrane系统评价员手册5.2.0推荐的偏倚风险评估工具对纳入的RCT进行质量评价,包括随机方法、分配隐藏、盲法实施、数据完整性、报告偏倚和其他偏倚,每个方面均分为高偏倚风险、低偏倚风险和不清楚[9-13]。采用纽卡斯尔-渥太华量表(Newcastle-Ottawa scale,NOS)对纳入的队列研究进行质量评价,包括研究对象选择(0~4分)、组间可比性(0~2分)、结果/暴露因素测量(0~3分);1~3分为低质量,4~9分为高质量[14-15]。
1.5 统计学方法
采用RevMan 5.3软件进行Meta分析。计数资料采用相对危险度(odds ratio,OR)及其95%置信區间(confidence interval,CI)表示。若各研究间无统计学异质性或异质性较小(I 2≤50%,P>0.1),采用固定效应模型进行分析;反之,则进行亚组分析或逐一剔除纳入研究后进行敏感性分析,寻找异质性来源,明确是否存在临床和方法学异质性,若无明显的临床和方法学差异,则采用随机效应模型进行分析。对结果的稳定性进行敏感性分析。检验水准α=0.05。
2 结果
2.1 文献检索结果与纳入研究基本信息
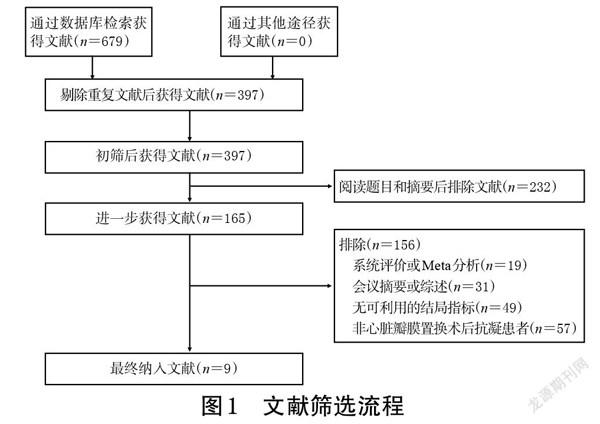
初检共获得相关文献679篇,经阅读题目、摘要和全文后,最终纳入9篇文献[9-17],其中7项RCT[9-13,16-17]、2项队列研究[14-15];共计4 962例患者,其中试验组1 642例、对照组3 320例。文献筛选流程见图1,纳入研究的基本信息见表2。
2.2 纳入研究质量评价结果
7项RCT分别采用区组随机化、交互式语音应答系统或计算机随机数字发生器等随机分组方法[9-13,16-17];7項RCT均采用了分配隐藏和双盲试验,结果数据均完整[9-13,16-17],其中4项研究存在报告偏倚[9-10,12,16];7项RCT均不清楚是否存在其他偏倚来源[9-13,16-17]。2项队列研究的NOS评分均为8分,为高质量研究[14-15]。结果见图2、图3。
2.3 Meta分析结果
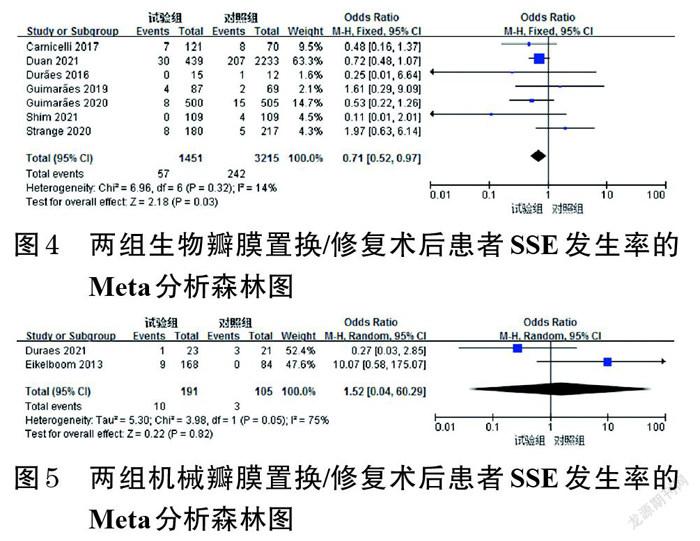
2.3.1 SSE发生率 9项研究(包括7项生物瓣膜置换/修复术和2项机械瓣膜置换/修复术)报道了SSE发生率[9-17]。生物瓣膜置换/修复术后患者中,各研究间无统计学异质性(P=0.32,I 2=14%)[10-15,17],采用固定效应模型进行Meta分析,详见图4。Meta分析结果显示,试验组患者的SSE发生率显著低于对照组[OR=0.71,95%CI(0.52,0.97),P=0.03]。机械瓣膜置换/修复术后患者中,各研究间存在统计学异质性(P=0.05,I 2=75%)[9,16],排除临床和方法学异质性后,采用随机效应模型进行Meta分析,详见图5。Meta分析结果显示,两组患者的SSE发生率比较,差异无统计学意义[OR=1.52,95%CI(0.04,60.29),P=0.82]。
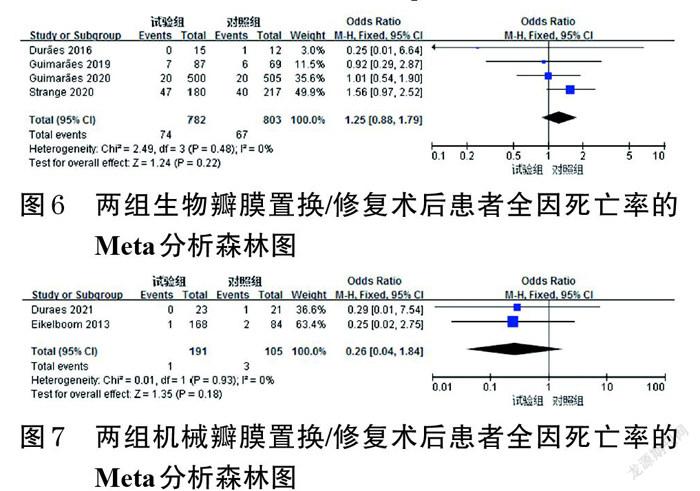
2.3.2 全因死亡率 7项研究(包括5项生物瓣膜置换/修复术和2项机械瓣膜置换/修复术)报道了全因死亡率[9-10,12-16]。生物瓣膜置换/修复术后患者中,各研究间有统计学异质性(P<0.1,I 2=84%)[10,12-14];排除Duan等[15]的研究后,异质性降低(P=0.48,I 2=0),考虑到异质性可能为该研究纳入的两组样本量差异较大,故删除该研究,对其余4项研究采用固定效应模型进行Meta分析,详见图6。Meta分析结果显示,两组患者的全因死亡率比较,差异无统计学意义[OR=1.25,95%CI(0.88,1.79),P=0.22]。机械瓣膜置换/修复术后患者中,各研究间无统计学异质性(P=0.93,I 2=0)[9,16],采用固定效应模型进行Meta分析,详见图7。Meta分析结果显示,两组患者的全因死亡率比较,差异无统计学意义[OR=0.26,95%CI(0.04,1.84),P=0.18]。
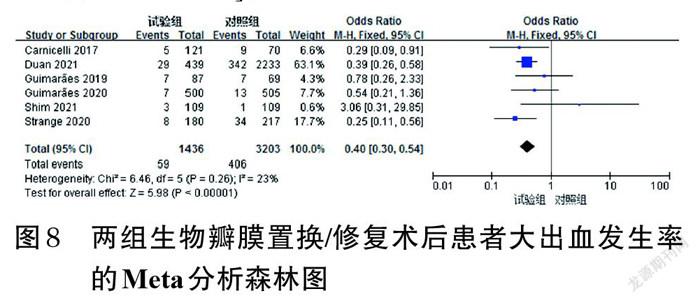
2.3.3 大出血发生率 6项研究(均为生物瓣膜置换/修复术)报道了大出血发生率[11-15,17],各研究间无统计学异质性(P=0.26,I 2=23%),采用固定效应模型进行Meta分析,详见图8。Meta分析结果显示,试验组患者的大出血发生率显著低于对照组[OR=0.40,95%CI(0.30,0.54),P<0.000 01]。
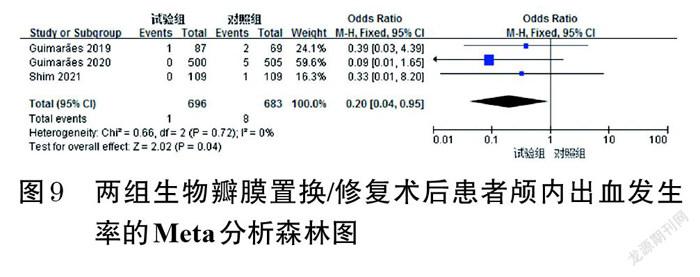
2.3.4 颅内出血发生率 3项研究(均为生物瓣膜置换/修复术)报道了颅内出血发生率[12-13,17],各研究间无统计学异质性(P=0.72,I 2=0),采用固定效应模型进行Meta分析,详见图9。Meta分析结果显示,试验组患者的颅内出血发生率显著低于对照组[OR=0.20,95%CI(0.04,0.95),P=0.04]。
2.3.5 亚组分析 因纳入的机械瓣膜置换/修复术相关文献的样本量较小,故未对其进行亚组分析,本文仅对生物瓣膜置换/修复术后患者的主要疗效和安全性指标进行亚组分析。首先,将生物瓣膜置换/修复术后患者按随访时间进行亚组分析。当随访时间≤3个月时,试验组患者的SSE发生率显著低于对照组[OR=0.20,95%CI(0.06,0.74),P=0.03],而两组患者的大出血发生率比较差异无统计学意义[OR=0.67,95%CI(0.19,2.38),P=0.53]。当随访时间>3个月时,两组患者的SSE发生率比较差异无统计学意义[OR=0.74,95%CI(0.54,1.02),P=0.07],而试验组患者的大出血发生率显著低于对照组[OR=0.39,95%CI(0.29,0.52),P<0.001]。其次,将生物瓣膜置换/修复术后患者按研究类型进行亚组分析。在RCT研究中,试验组患者的SSE发生率显著低于对照组[OR=0.51,95%CI(0.29,0.92),P=0.03],而两组患者的大出血发生率比较差异无统计学意义[OR=0.58,95%CI(0.33,1.03),P=0.06]。在队列研究中,两组患者的SSE发生率比较差异无统计学意义[OR=1.03,95%CI(0.40,2.66),P=0.95],而试验组患者的大出血发生率显著低于对照组[OR=0.20,95%CI(0.06,0.74),P<0.001]。结果见表3。
2.4 敏感性分析
分别以SSE发生率、全因死亡率、大出血发生率和颅内出血发生率为指标进行敏感性分析。结果显示,分别逐一剔除单项原始研究后,各结局指标均未发生显著变化,提示所得结果较稳健。
3 讨论
无论是接受机械瓣膜还是生物瓣膜置换/修复术,患者术后均需长期服用抗凝药物,其中无房颤患者在生物瓣膜置换/修复术后需服用3~6个月的抗凝药物,而生物瓣膜置换/修复术后合并房颤和机械瓣膜置换/修复术后患者,则需终生服用抗凝药物[18]。NOACs主要包括直接凝血酶抑制剂和凝血因子Ⅹa抑制剂,前者能特异性阻滞凝血酶活性,后者通过与凝血因子Ⅹa的活性位点结合来阻止凝血酶原转变为凝血酶,从而发挥抗凝作用[5]。但心脏瓣膜置换术后,NOACs是否可以替代华法林用于抗凝治疗仍存在争议[19]。Malik等[20]一项关于生物瓣膜置换术后合并房颤患者的Meta分析结果显示,NOACs与华法林的有效性和安全性均相当。Adhikari等[21]的Meta分析结果发现,对于生物瓣膜置换术后合并房颤患者,NOACs与华法林的有效性相似,但安全性更高。虽然上述两项Meta分析结果均表明,服用NOACs与华法林患者的SSE发生率无显著差异,但随后韩国的一项临床研究发现,华法林组有4例患者发生SSE,依度沙班组未有患者发生SSE[17]。美国的一项回顾性研究结果显示,利伐沙班引起的卒中发生率显著低于华法林[15]。上述研究结果提示,在SSE发生风险上,NOACs可能优于华法林。而本研究结果显示,在生物瓣膜置换/修复术后患者中,服用NOACs患者的SSE、大出血、颅内出血的发生风险均显著低于服用华法林患者,但两组患者的全因死亡率比较差异无统计学意义。这提示,生物瓣膜置换/修复术后患者使用NOACs的抗凝效果优于华法林。
有研究认为,心脏瓣膜置换术后患者早期(≤3个月)的血栓发生风险较高,但缺乏临床试验数据[5]。早期已发表的关于生物瓣膜置换术后合并房颤患者的Meta分析虽然认为,NOACs与华法林的有效性相当,但均未观察患者术后3个月内NOACs与华法林的抗凝疗效[20-21]。本研究以随访时间的不同进行了亚组分析,结果显示,当随访时间≤3个月时,NOACs组患者的SSE发生率显著低于华法林组,而NOACs组患者的大出血发生率与华法林组比较差异无统计學意义;当随访时间>3个月时,NOACs组患者的SSE发生率与华法林组比较差异无统计学意义,而NOACs组患者的大出血发生率显著低于华法林组。可见,无论是术后早期还是长期随访,NOACs在降低SSE发生率和大出血发生率方面均与华法林相当或优于华法林。按研究类型进行的亚组分析结果显示,无论是RCT还是队列研究,NOACs在降低患者SSE发生率和大出血发生率方面也与华法林相当或优于华法林。
有研究比较了机械瓣膜置换/修复术后患者使用达比加群与华法林的有效性和安全性,但因达比加群组患者发生SSE和大出血事件过多,使得该研究被提前终止[9]。但2020、2021年发表的两篇前瞻性研究发现,患者于机械瓣膜置换/修复术后服用利伐沙班抗凝,随访3个月内未有严重血栓或者大出血事件发生[6,16],虽然这2项研究纳入的样本量少,但所得结果提示可就该领域进行更大样本量的临床试验[22-23]。本研究结果显示,机械瓣膜置换/修复术后患者中,两组患者的SSE发生率、全因死亡率比较,差异均无统计学意义。这提示NOACs或许可以作为机械瓣膜置换/修复术后抗凝治疗的方案之一。
综上所述,对于生物瓣膜置换/修复术后患者,NOACs的有效性和安全性均优于或与华法林相当;对于机械瓣膜置换/修复术后患者,NOACs与华法林的有效性和安全性均无显著差异。本研究的局限性为:(1)研究纳入的NOACs种类不同,且给药剂量也不尽相同,可能会增加结果的异质性;(2)纳入的机械瓣膜性心脏病抗凝和生物瓣膜性心脏病早期抗凝(≤3个月)文献较少,且样本量较小;(3)部分纳入文献的结局指标发生率较低,可能会对结果造成一定的偏倚;(4)由于纳入的文献数较少,故未进行发表偏倚分析。因此,所得结论尚需更多大样本、多中心的临床研究进一步验证。
参考文献
[ 1 ] 沈卫峰,杨震坤.心脏瓣膜病诊治进展[J].中华老年心脑血管病杂志,2009,11(12):905-907.
[ 2 ] NKOMO V T,GARDIN J M,SKELTON T N,et al. Burden of valvular heart diseases:a population-based study[J]. Lancet,2006,368(9540):1005-1011.
[ 3 ] DI B L. Use of direct oral anticoagulants in patients with atrial fibrillation and valvular heart lesions[J]. J Am Heart Assoc,2016,5(2):e002776.
[ 4 ] GELOSA P,CASTIGLIONI L,TENCONI M,et al. Pharmacokinetic drug interactions of the non-vitamin K anta- gonist oral anticoagulants(NOACs)[J]. Pharmacol Res,2018,135:60-79.
[ 5 ] STEFFEL J,COLLINS R,ANTZ M,et al. 2021 European Heart Rhythm Association practical guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation[J]. Europace,2021,23(10):1612- 1676.
[ 6 ] ROOST E,WEBER A,ALBERIO L,et al. Rivaroxaban in patients with mechanical heart valves:a pilot study[J]. Thromb Res,2020,186:1-6.
[ 7 ] LI H J,LIN S Y,LIN F J,et al. Effectiveness and safety of non-vitamin K antagonist oral anticoagulants in Asian patients with atrial fibrillation and valvular heart disease[J]. Curr Med Res Opin,2021,37(4):535-542.
[ 8 ] SCHULMAN S,ANGERÅS U,BERGQVIST D,et al. Definition of major bleeding in clinical investigations of antihemostatic medicinal products in surgical patients[J]. J Thromb Haemost,2010,8(1):202-204.
[ 9 ] EIKELBOOM J W,CONNOLLY S J,BRUECKMANN M,et al. Dabigatran versus warfarin in patients with mecha- nical heart valves[J]. N Engl J Med,2013,369(13):1206-1214.
[10] DURÃES A R,DESOUZA RORIZ P,DEALMEIDA NUNES B,et al. Dabigatran versus warfarin after bioprosthesis valve replacement for the management of atrial fibrillation postoperatively:DAWA pilot study[J]. Drugs R&D,2016,16(2):149-154.
[11] CARNICELLI A P,DE CATERINA R,HALPERIN J L,et al. Edoxaban for the prevention of thromboembolism in patients with atrial fibrillation and bioprosthetic valves[J]. Circulation,2017,135(13):1273-1275.
[12] GUIMARÃES P O,POKORNEY S D,LOPES R D,et al. Efficacy and safety of apixaban vs warfarin in patients with atrial fibrillation and prior bioprosthetic valve replacement or valve repair:insights from the ARISTOTLE trial[J]. Clin Cardiol,2019,42(5):568-571.
[13] GUIMARÃES H P,LOPES R D,DE BARROS E SILVA P G M,et al. Rivaroxaban in patients with atrial fibrillation and a bioprosthetic mitral valve[J]. N Engl J Med,2020,383(22):2117-2126.
[14] STRANGE J E,SINDET-PEDERSEN C,STAERK L,et al. All-cause mortality,stroke,and bleeding in patients with atrial fibrillation and valvular heart disease[J]. Eur Heart J Cardiovasc Pharmacother,2021,7(FI1):f93-f100.
[15] DUAN L W,DOCTOR J N,ADAMS J L,et al. Compa- rison of direct oral anticoagulants versus warfarin in patients with atrial fibrillation and bioprosthetic heart valves[J]. Am J Cardiol,2021,146:22-28.
[16] DURAES A R,DE SOUZA LIMA BITAR Y,SCHONHOFEN I S,et al. Rivaroxaban versus warfarin in patients with mechanical heart valves:open-label,proof-of-concept trial:the RIWA study[J]. Am J Cardiovasc Drugs,2021,21(3):363-371.
[17] SHIM C Y,SEO J,KIM Y J,et al. Efficacy and safety of edoxaban in patients early after surgical bioprosthetic valve implantation or valve repair:a randomized clinical trial[J]. J Thorac Cardiovasc Surg,2021,S0022-5223(21)00228.
[18] 江文.理性选择机械瓣膜和生物瓣膜[J].中国胸心血管外科临床杂志,2015,22(4):361-365.
[19] DE SOUZA LIMA BITAR Y,NETO M G,FILHO J A L,et al. Comparison of the new oral anticoagulants and warfarin in patients with atrial fibrillation and valvular heart disease:systematic review and meta-analysis[J]. Drugs R D,2019,19(2):117-126.
[20] MALIK A H,YANDRAPALLI S,ARONOW W S,et al. Oral anticoagulants in atrial fibrillation with valvular heart disease and bioprosthetic heart valves[J]. Heart,2019,105(18):1432-1436.
[21] ADHIKARI G,BARAL N,RAUNIYAR R,et al. Syste- matic review and meta-analysis:can we compare direct oral anticoagulants to warfarin in patients with atrial fibrillation and bio-prosthetic valves? [J]. Cureus,2021,13(4):e14651.
[22] AIMO A,GIUGLIANO R P,DE CATERINA R. Non-vitamin K antagonist oral anticoagulants for mechanical heart valves:is the door still open? [J]. Circulation,2018,138(13):1356-1365.
[23] 李詩思,李松,张永.非维生素K拮抗剂口服抗凝剂在机械心脏瓣膜置换术后治疗中的应用进展[J].中国药业,2020,29(18):96-98.
(收稿日期:2021-09-14 修回日期:2021-12-09)
(编辑:陈 宏)
