商业可行的质子交换膜制氢催化剂制备和评价
2022-02-03任航星丁睿李黎明宋时莉袁先明张世渊
任航星, 丁睿, 李黎明, 宋时莉, 袁先明, 张世渊
(中国船舶集团有限公司第七一八研究所, 邯郸 056027)
目前,对于酸性介质中的析氢反应(hydrogen evolution reaction,HER),可用的电催化剂通常是铂黑或碳负载的铂纳米颗粒;而对于析氧反应(oxygen evolution reaction,OER)来说,IrO2是目前商业上最常用的稳定析氧催化剂[8-9]。由于阳极侧OER的缓慢动力学和高过电位,其占据了大部分的电解槽电压损失,这就导致阳极侧电催化剂负载(1~3.0 mg/cm2)要高于阴极侧(0.3~1.0 mg/cm2)[10]。因此,当前对于PEM制氢催化剂的研究多集中在阳极侧析氧催化剂上。为尽快实现PEM电解水制氢的规模化应用,开发商业可行的PEM析氧催化剂,仍然需要以IrO2为主要活性物质,通过晶体形貌调控、杂元素掺杂或引入载体等手段来实现性能上的提升[11-13]。考虑到贵金属铱的高价格和稀缺性,以简便、具有成本效益和可高效放大(公斤级)的方式合成具有高活性和优异稳定性的电催化剂是PEM电解水发展的关键。
迄今为止,已被报道的用于贵金属基氧化物电催化剂的合成方法主要有Adams法[14-15]、溶胶-凝胶法[16-17]、磁控溅射法[18]和模板法[19]。Liu等[14]采用Adams法制备出IrO2电催化剂,煅烧温度为550 ℃,IrO2比表面积达到126.4 m2/g,在1.5 V时OER活性为90 mA/cm2。Li等[20]开发了一种无模板氨络合物方法来合成高度多孔的IrO2,在450 ℃热处理后,其最高表面积为363.3 m2/g,在电流密度10 mA/cm2时的过电位为282 mV。如文献报道,电催化剂中钌的存在有助于促进析氧反应(OER)。然而,众所周知,RuO2的稳定性远不如IrO2[21-23]。最近,一些研究人员在阳极电催化剂中引入了适量的钌,以在活性和稳定性之间达到良好平衡[24-27]。Siracusano等[24]采用改进的Adams法制备了IrO2基和Ir0.7Ru0.3O2基电催化剂,证明IrRuOx混合氧化物在1.85 V和90 ℃下具有更好的催化活性,电流密度达到3.2 A/cm2,但并未给出稳定性结果。尽管已经开发出诸多纳米尺寸的氧化物电催化剂合成方法,然而其中一些方法可能会涉及复杂的设备和步骤,因此可能会在放大制备过程中存在技术和成本障碍。
现运用简单且易于放大的Adams法合成纳米IrO2和IrxRu1-xO2电催化剂,考察煅烧温度、煅烧时间、元素掺杂对催化材料晶体结构和形貌等的影响,并通过电化学测试以及工业级别的PEM电解槽测试方法评估这些催化剂的性能,为具体的商业应用提供参考。
1 实验
1.1 材料制备
1.1.1 电催化剂的制备
IrO2电催化剂采用Adams法合成,以H2IrCl6·xH2O(Ir:35%,Macklin)、NaNO3(分析纯,国药化学试剂有限公司)为原料。合成过程如下:称取0.5 g H2IrCl6·xH2O,并溶解在70 mL去离子水中,然后向该溶液中加入7.5 g NaNO3。将混合溶液在室温下磁力搅拌1 h以确保前体完全溶解,然后在80 ℃油浴下加热搅拌直至完全干燥。将得到的干盐放入坩埚电阻炉中,在450 ℃下煅烧1 h,得到熔融盐氧化物,用去离子水对其进行彻底洗涤以除去多余的可溶解盐,离心分离收集IrO2产物,最后在80 ℃空气氛围中干燥过夜。为了确定煅烧温度和煅烧时间的影响,分别测试了450 ℃下煅烧0.5 h,450 ℃下煅烧1 h和500 ℃下煅烧0.5 h,将所得IrO2命名为IrO2-450 ℃-0.5 h、IrO2-450 ℃-1 h、IrO2-500 ℃-0.5 h。
使用上述类似的步骤合成IrxRu1-xO2电催化剂。唯一的区别是贵金属前体使用H2IrCl6·xH2O和RuCl3·xH2O(Aladdin)的混合物。Ir与Ru的原子比为3∶1。将含有Ir和Ru的干盐在450 ℃下煅烧1 h,得到Ir0.75Ru0.25O2-450 ℃-1 h。
1.1.2 膜电极的制备
采用Nafion®117(ChemoursTM)膜(183 μm)作为制备膜电极的固体聚合物电解质膜。使用前,将Nafion®117膜在80 ℃过氧化氢溶液(质量分数5%)中预处理1 h。用去离子水冲洗后,转移到0.5 mol/L硫酸溶液中,在80 ℃下再煮1 h,然后用去离子水洗涤。
2.1吸烟组与不吸烟组(对照组)高频听力损失检出率的比较 吸烟组高频听力损失检出率为25.8%,二线接噪组高频听力损失检出率12.3%,经统计学分析,差异有统计学意义(X 2=33.079,P<0.05)。见表1。
使用所合成的IrO2或IrxRu1-xO2作为析氧电催化剂,用Hispec 4100 Pt/C(40% Pt,Johnson Matthey)作为析氢电催化剂。催化剂油墨配制是将一定量的催化剂粉末分散到异丙醇、去离子水和Nafion溶液的混合液中,然后超声处理1 h。使用SONO-TEK Exacta Coat 超声喷涂系统将分散良好的阳极和阴极催化剂油墨喷涂在Nafion®117膜的两侧得到CCM膜电极。阳极催化剂的负载量为1.5 mg/cm2的IrO2或IrxRu1-xO2,阴极催化剂的负载量为0.4 mg/cm2。所制备的膜电极有效面积为50 cm2。
1.2 物理表征
样品的粉末X射线衍射(X-ray diffraction,XRD)图谱在Brucker D8 Advance衍射仪上测试,以Cu Kα(波长λ=1.541 8×10-10m)射线为辐射源,工作电压为40 kV,工作电流为30 mA。N2吸附-脱附实验在ASAP 2460表面积和孔隙率分析仪上进行,吸附前先将样品在200 ℃、10-3Torr下脱气处理12 h,然后用高纯氮作为吸附介质,在液氮温度(-196 ℃)下进行氮吸附-解吸等温线测试。用Philips-FEI Tecnai G2S-Twin透射电子显微镜(transmission electron microscope,TEM)对材料的微观结构、颗粒大小等进行分析。粉末样品用无水乙醇进行超声分散,取两滴分散液至镀有碳膜的铜网上,用红外灯烘干后再测试。
1.3 性能评价
1.3.1 半电池测试
催化剂样品的电化学测试是利用CHI 760e电化学工作站,在实验室级别三电极体系下完成的。其中,以铂片作为对电极,以饱和甘汞电极(saturated calomel electrode,SCE)作为参比电极。工作电极是将所得的催化剂样品载到玻碳电极(glass carbon electrode,GCE)上,其制备过程为:将粉末状催化剂(5 mg)分散到包含异丙醇(380 μL)和质量分数为5% Nafion溶液(20 μL)的混合溶液中,并在室温下超声处理30 min制得催化剂墨水溶液。用移液枪将1.5 μL催化剂墨水滴在直径为3 mm的玻碳电极上,在空气中进行干燥。最后工作电极上催化剂的担载量约为0.26 mg/cm2。
所有的电化学测试温度为室温,电解液为0.5 mol/L H2SO4溶液。为避免电催化反应过程中电容电流的干扰,进行线性扫描伏安法(linear sweep voltammetry,LSV)测试时,扫速为1 mV/s,并进行了85%的内阻(internal resistance,iR)补偿。将测试所得电位全部转换为相对于可逆氢电极的电位,计算公式为
Evs.RHE=Evs.SCE+ 0.244 V + 0.059 1pH
(1)
式(1)中:Evs.RHE为相对可逆氢电极(reversible hydrogen electrode,RHE)的电位;Evs.SCE为相对饱和甘汞电极电位;pH为电解液的pH。
最后用电极面积S将电流值进行归一化得到几何电流密度jgeo。每个样品至少独立测量3次。
1.3.2 电解槽测试
所得催化剂样品的实际电解性能以基于膜电极的形式在自制PEM电解槽中进行评价。电解槽按照工业电解槽的规格要求进行设计,主要由端压板、极板、多孔气体扩散层、膜电极等组成,其结构如图1所示。其中,膜电极有效面积为50 cm2。为避免强酸性、大电流和高电位腐蚀的工作环境所引起的电解槽内阻增加对测试结果的影响,对膜电极以外的其他部件选择性进行特殊涂层处理。测试时,用蠕动泵以50 mL/min的流速将去离子水(18.2 MΩ·cm)输送至阳极室,并从氧气出口随氧气一起输送回水箱。在整个测试过程中,保持电解槽温度为60 ℃,为避免管路输送过程中热量损耗,水箱温度比电解池温度高约2 ℃。在极化曲线测试之前,首先对膜电极进行24 h激活处理,之后,在一系列电流密度(由0.01 A/cm2逐步升高至2 A/cm2)下采集电解槽小室电压,每个电流密度至少保持恒流10 min,并以电压稳定阶段采集的电压平均值作为最终电压。绘制得到电流密度-电压曲线。

图1 PEM电解槽结构Fig.1 PEM electrolytic cell structure
2 结果与讨论
2.1 XRD图谱
商用IrO2、不同煅烧温度和煅烧时间合成的IrO2纳米粒子和Ir0.75Ru0.25O2纳米粒子的XRD图谱如图2所示。与标准商业IrO2和Ir相比,所有IrO2样品都显示了IrO2粉末的典型衍射谱图,这表明成功制备了IrO2晶体结构,较宽的布拉格衍射峰则可能是由于形成的晶体晶粒较小所致。布拉格角为28.01°、34.67°、54.07°的3个主要衍射峰分别对应于IrO2的(110)、(101)和(211)晶面。然而,在商业IrO2中出现了单质铱的衍射峰,但在本实验合成的IrO2样品中却未发现,这表明合成样品为高纯度的IrO2。由于IrO2和RuO2具有相同的结构和相似量级晶格参数,并且铱和钌的离子半径非常相似,因此认为这些金属氧化物可以以固溶体形式存在。实际上,在Ir0.75Ru0.25O2催化剂的XRD图中观察到相对于参考IrO2向更高布拉格角的移动,这表明晶格收缩,暗示了固溶体的形成。

图2 商业IrO2、自制IrO2和Ir0.75Ru0.25O2样品的XRD谱图Fig.2 XRD patterns of commercial IrO2, in-house IrO2 and Ir0.75 Ru0.25 O2 samples
2.2 N2物理吸附
通过N2吸附-脱附(BrunauerEmmett-Teller,BET)实验测量了在不同煅烧温度和煅烧时间制备的IrO2纳米粒子的比表面积、孔容和平均孔径。结果如图3(a)和表1所示。在450 ℃煅烧温度和1 h煅烧时间的合成条件下所制得的IrO2具有最大比表面积,即182 m2/g。对比IrO2-450 ℃-0.5 h和IrO2-450 ℃-1 h的结果如表1所示,可以看出在450 ℃煅烧温度下,随着煅烧时间的延长,比表面积和孔容呈增加趋势,平均孔径的减小可以用大孔数的减少和孔径小于4 nm的孔数增加来解释[图3(a)]。当煅烧温度升至500 ℃时,比表面积介于IrO2-450 ℃-0.5 h和IrO2-450 ℃-1 h,可以看出延长煅烧时间比提高煅烧温度更有利于提高比表面积。图3(b)为在优化的煅烧温度和时间下所制备的Ir0.75Ru0.25O2-450 ℃-1 h的N2吸附-脱附结果,其比表面积为176 m2/g,具有典型的微孔特征。

表1 IrO2和Ir0.75Ru0.25O2纳米粒子的比表面积、孔体积和平均孔径Table 1 The values of specific surface area, pore volume and pore size of the IrO2 and Ir0.75 Ru0.25O2 nanoparticles

图3 催化剂样品的N2吸附-脱附等温线Fig.3 N2 adsorption-desorption isotherms of the catalyst samples
2.3 样品形貌
通过TEM研究了这些催化剂的形貌,如图4所示。图4(a)显示IrO2-450 ℃-1 h催化剂由大量聚集的细颗粒组成,这与XRD图谱较宽的布拉格衍射峰非常吻合,明显观察到IrO2-450 ℃-1 h粒子的晶格条纹。Ir0.75Ru0.25O2-450 ℃-1 h的TEM图像如图4(b)所示,有趣的是,细颗粒的分散比IrO2-450 ℃-1 h更好。使用晶格条纹图像估计两种催化剂晶粒的平均尺寸,分别为3.3 nm和4.3 nm。

图4 TEM图像Fig.4 TEM images
2.4 OER性能测试
所合成的IrO2和Ir0.75Ru0.25O2催化剂在0.5 mol/L H2SO4溶液中的OER电催化性能测试结果如图5所示。由线性扫描伏安(LSV)曲线可以看出,IrO2-450 ℃-1 h在10 mA/cm2时的OER过电位为274 mV,与IrO2-450 ℃-0.5 h、IrO2-500 ℃-0.5 h和商用IrO2催化剂相比分别降低了18、11和39 mV。此外,所合成的IrO2也表现出与已报道的OER催化剂相当的催化活性(在10 mA/cm2时过电位为270~290 mV)[15,20]。Ir0.75Ru0.25O2-450 ℃-1 h在所有催化剂中表现出最高的活性,在10 mA/cm2时的过电势仅为230 mV,比商用IrO2催化剂低83 mV,是目前所报道的最高活性催化剂之一。
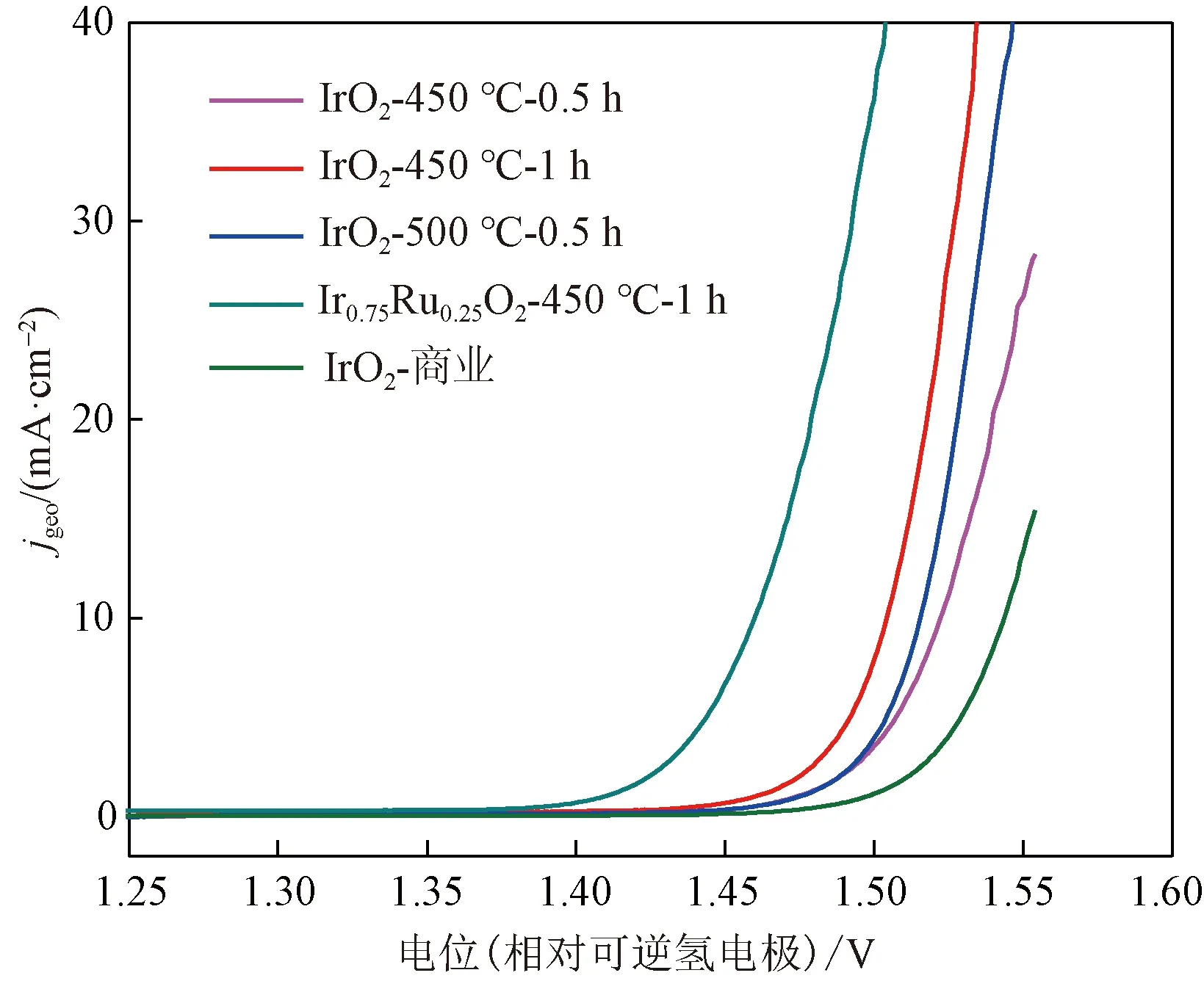
图5 IrO2和Ir0.75Ru0.25O2样品的LSV极化曲线Fig.5 LSV polarization curves of the IrO2 and Ir0.75Ru0.25O2 samples
2.5 电解槽性能及稳定性测试
在活性面积为50 cm2的PEM电解槽中测量了由不同阳极催化剂构建的MEA的电化学性能。典型极化曲线如图6所示,其中保持电解槽进水温度60 ℃,所测试的电流密度范围为0.01~2 A/cm2。与上述LSV曲线类似,IrO2-450 ℃-1 h表现出比使用IrO2-500 ℃-0.5 h更好的性能,达到1.77 V @ 1 A/cm2和2.02 V @ 2 A/cm2。这两种自制催化剂都显示出比商业IrO2更高的活性,在2 V电解电压下,IrO2-450 ℃-1 h的电流密度达到了商业催化剂的1.54倍。该结果可能与TEM结果推断的小粒径和表面粗糙度增加有关(图4)[28]。特别是在高电流密度范围内(>1 A/cm2),IrO2-450 ℃-1 h的性能明显提高,这可能是因为较小的孔径更利于水和氧气的快速传输。

图6 PEM电解槽中IrO2和Ir0.75Ru0.25O2的极化性能对比Fig.6 Comparison of polarization curves of the IrO2 and Ir0.75Ru0.25O2-based PEM electrolyzer
尽管在半电池测试时,Ir0.75Ru0.25O2-450 ℃-1 h在小电流密度下展现出的析氧过电位相比IrO2-450 ℃-1 h明显降低,然而在PEM电解槽中,前者所表现出来的电解性能仅略优于后者,电解电压仅达1.76 V @ 1 A/cm2和2 V @ 2 A/cm2,这与LSV极化曲线结果存在明显偏差。导致这一结果的原因可能是因为所合成的IrO2-450 ℃-1 h具有比Ir0.75Ru0.25O2-450 ℃-1 h更高的表面积和孔体积(表1)。还可以假设采用类似的合成方法引入钌可以提高MEA在活化极化区的活性,但在高电流密度下,由于欧姆极化和浓差极化开始发挥主要作用,这种改善并不显著[29]。因此,仅使用简单的实验室三电极体系来预测催化剂材料在实际商业应用中的性能,这一评价手段是否可靠还值得商榷,使用尽可能接近商业电解槽的电解装置进行电催化剂的评估可能更有意义。总体来说,开发高活性的铱基催化剂来降低贵金属铱的用量或许仍然是PEM电解水大规模应用的最佳选择之一。
在60 ℃下以1.2 A/cm2的恒定电流密度对IrO2-450 ℃-1 h和Ir0.75Ru0.25O2-450 ℃-1 h析氧催化剂进行了长期电解测试,同时监测了200 h电池电位变化,结果如图7所示。在整个电解操作中,电池电位没有明显增加,出现的小幅度波动可能是由于温度波动导致,该结果表明将电能转化为氢气的效率几乎没有损失。然而,需要更长的时间或加速应力测试(accelerated stress test,AST)来持续评估催化剂的稳定性。由于除催化剂活性外,催化剂的负载量、工作电流密度、膜(决定欧姆和离子电阻)和电解槽组成也是其中决定电解电位的最重要因素,因此同一催化剂在不同的测试工装和测试体系下可能得到的结果不同,在工业电解槽中验证催化剂的实际应用效果似乎是当前较为可靠的催化剂综合性能评价手段开发低铱负载的高性能强稳定性铱基催化剂是实现酸性OER催化性能瓶颈突破的关键,也是目前PEM电解槽工业应用的重点研发方向。利用杂原子或载体以金属掺杂、表面修饰、形成合金、固溶体氧化物、复合材料等来对氧化铱进行改进是目前快速实现商业应用的最为可行的方法之一。在今后的工作中,将继续进行低铱基析氧催化剂的设计和合成工艺优化,并对合成材料的商业可行性,特别是放大制备后的性能进行全面评估。

图7 IrO2和Ir0.75Ru0.25O2的寿命测试曲线Fig.7 Voltage of single cell test of the IrO2 and Ir0.75Ru0.25O2 samples
3 结论
PEM电解水制氢将成为未来氢能系统的重要组成部分。为了降低制造成本和电力成本,构建具有高活性和高稳定性的电催化剂以提高PEM电解水的性能和效率尤为重要。采用改进后的Adams法合成了纳米级IrO2和Ir0.75Ru0.25O2催化剂。在半电池测试条件下,IrO2-450 ℃-1 h和Ir0.75Ru0.25O2-450 ℃-1 h的OER过电位分别为274 mV @ 10 mA/cm2和230 mV @ 10 mA/cm2,优于商业催化剂和大多数报道的催化剂;同时,在60 ℃电解槽和2 V电解电压下,电流密度较商业催化剂提高1.54倍,有望显著提升电解效率,降低PEM制氢成本。未来将进一步优化催化剂结构组成,开发低成本、高活性与强稳定性的阳极催化剂,实现成本与性能问题的协同解决,并评估放大制备后催化剂的性能和批次稳定性,真正实现高效、长寿命、低成本的PEM电解制氢设备的规模化应用。
