铝件抛光剂废液中铝浓度检测和除铝研究
2022-02-01杨军星
杨 庆,黄 颖,杨军星
(1 黔南民族职业技术学院,贵州 都匀 558022;2 桂林理工大学,广西 桂林 541004)
1996年以来,王文忠、冯承才等[1-2]研发了一种混酸体系化学抛光剂,具有良好的去油污,防锈,清洗和增光性能,增加金属铝材制品的光泽,但是此铝件抛光剂会产生主要成分是氮氧化物NOx的黄烟,造成空气污染。后来,李贤成[3]采用磷酸、硫酸加抛光剂的高温化学抛光,工艺稳定可靠,配方中不用硝酸,不产生黄烟,有利于工人身体健康和环境保护。但是,郭昌明[4]指出了抛光剂在多次使用后,金属杂质(主要是铝)不断积累,当其含量达到一定量后抛光剂便慢慢失效,成为失效液。
这些年来,多位学者不断对此问题进行研究,例如,2007年钟明峰[5]报道,采用石灰法处理失效抛光剂,不仅浪费大量资源,还污染环境;1978年Mikami Y[6]首先报道的盐析法;2009年张艳红[7]报道的沉淀法;2003年Shibata J[8]首次报道的萃取法以及2004年Motoda Y[9]报道的离子交换法等会消耗混酸而改变抛光剂酸度或成本太高,难实现大批量处理而实用价值不高。
本研究的意义不仅在于采用一种不消耗混酸、不改变原抛光剂酸度,且在强酸下快速有效去除铝离子的方法,而且可以大批量处理高酸度、高浓度的含铝抛光剂,避免了大量废酸的排放。这不但能有效降低环境污染,并给铝件抛光件重复利用带来可能,有一定学术意义。同时也具有一定的应用价值。
1 实 验
1.1 材料与仪器
实验原材料:失效的抛光剂,广东佛山某铝材厂提供,为淡绿色黏稠状液体。
实验试剂:氢氟酸,冰醋酸,醋酸铵,乙二胺四乙酸二钠,1-(2-吡啶偶氮)-2-奈酚,硫酸铜,硫酸,均为分析纯试剂,使用的水均为去离子水。
实验仪器:PB-10 pH计,赛多利斯科学仪器(北京)有限公司;BSA1124S电子分析天平,广州市深华生物技术有限公司;OD-98-003电热板,法国Analab;水银温度计,广州化学仪器公司;CQY-5m3酸回收设备。
1.2 实验方法
1.2.1 铝件抛光剂废液中铝浓度检测方法
取5.0 mL失效的抛光剂稀释至100 mL,然后移取10 mL稀释液加蒸馏水再稀释到350 mL(此时铝的总量相当于原抛光剂的1/2)。在溶液中加入2 mL缓冲液与25 mL 0.1 mol/L的EDTA溶液。温热后,加入1.0 mL PAN指示剂,加热至沸腾,冷却至60 ℃时用0.1 mol/L的硫酸铜溶液滴定。溶液由绿色变到深蓝色时,滴定终止消耗硫酸铜体积V1。加入1~2 g氟化钠,使Al-EDTA络合物分解,再加热至沸点,冷却至60 ℃时再用0.1 mol/L硫酸铜溶液滴定游离的EDTA,至蓝色为终止,消耗硫酸铜体积V2。然后由2.1计算出铝含量。
1.2.2 铝件抛光剂除铝方法
抛光剂在抛光铝件中会溶解越来越多铝离子,最终因铝过量而“中毒”,失去抛光性能。本原理为在氢氟酸作用下,以不改变抛光剂酸度为原则,铝离子与氟离子结合生成难溶的AlF3白色沉淀,不溶于强酸,去除铝离子,实现抛光剂的活化。反应式为Al3++3F-=AlF3↓,AlF3(Ksp=1.0×10-15)[10],可以实现铝的去除目的。
2 结果与讨论
2.1 铝离子浓度的计算方法
铝的返滴定反应如下[11]:
滴定前:2Al3++3H4Y2-(EDTA过量)=Al2(H4Y)3,滴定开始至计量点前:H4Y2-(剩余EDTA)+Cu2+=Cu(H4Y),计量点:Cu2++H3In4-(pH<6.3,黄色→绿色)=CuH3In2-(深蓝),终点:深蓝色。
Al2(H4Y)3+6F-=2AlF3+3H4Y2-3H4Y2-+Cu2+=3H4YCu
螯合反应时,EDTA、铜、铝之间的摩尔比为1∶0.3∶0.7时,终点颜色为亮紫色,颜色敏锐,服从n(EDTA)=n(Cu)+ n(Al);因为EDTA属于六齿配位体螯合剂[12],而Al-EDTA属于sp3d2外轨型配合物[13],是活性配合物,Al3+属d0型离子,其形成AlY八面体配合物时,Al3+仍有d空轨道,有利于接受第七个配体的电子对形成配位数为七的中间化合物,有利于按交换机理进行。所以Al2(H4Y)3+6F-=2AlF3+3H4Y2-可以进行反应,由于生成氟化铝沉淀而使反应向右进行。所以, n(Al)=2n(Cu),因此,抛光剂中铝含量=5.4V2(g/L)。
2.2 氢氟酸除铝
理论上氟化钠或六氟硅酸钠都可以与铝离子形成螯合物而去除铝离子,但是,本研究的高浓度含铝的抛光剂中添加不同浓度的氟化钠或六氟硅酸钠,都没有生成沉淀,可能原因是氟化钠或六氟硅酸钠与铝反应形成稳定的络合体系,难以沉淀,而向失效的抛光剂中添加氢氟酸会生成氟化铝难溶沉淀,使铝离子从抛光剂中分离,解除了抛光剂的铝中毒。
高浓度含铝的抛光剂中添加不等量氢氟酸,反应、静置沉降6 h后,按1.2的实验操作检测铝离子,氢氟酸投加量、滴定体积差、0.1 mol/L硫酸铜溶液消耗量、铝离子的去除率数据,如表1所示。
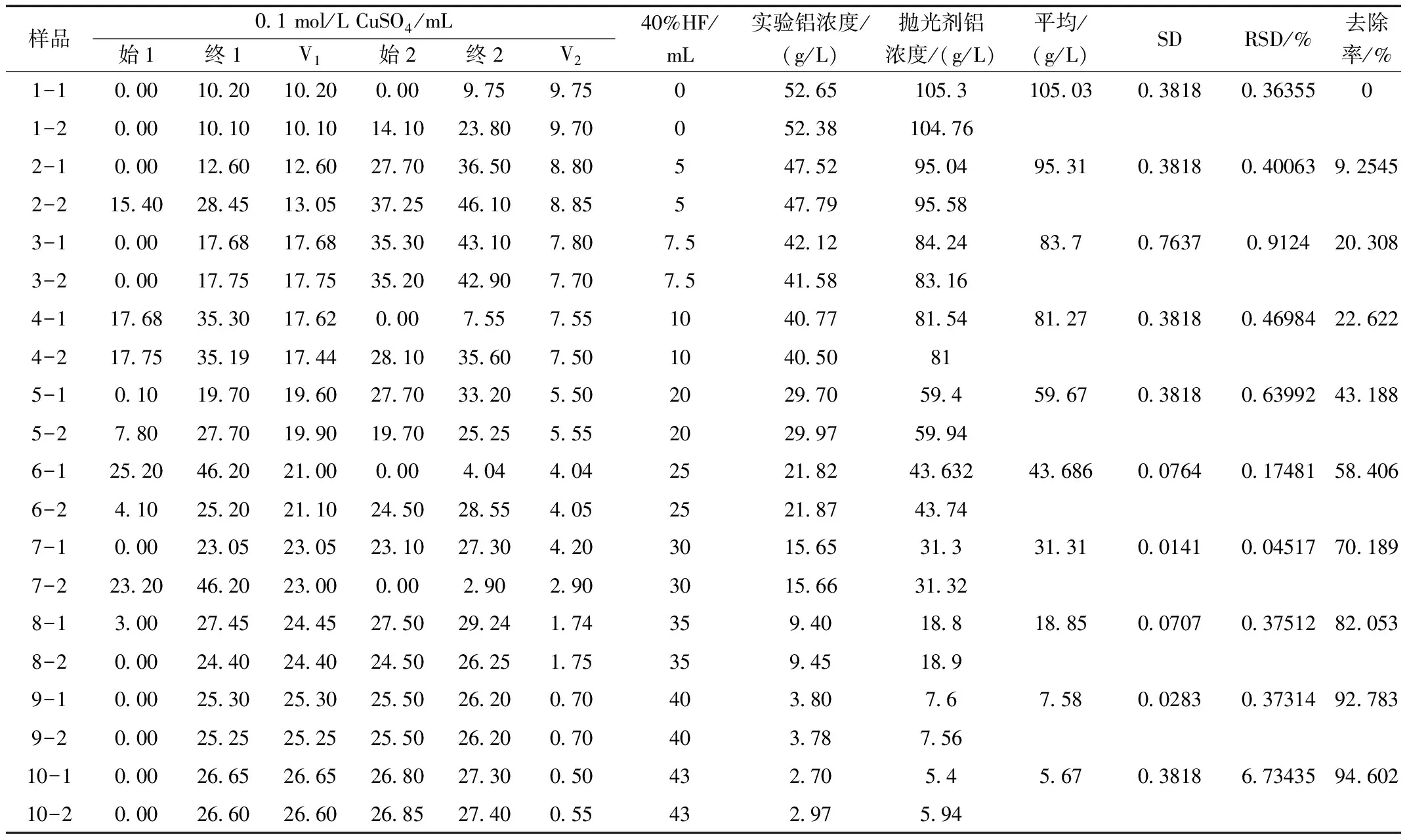
表1 添加氢氟酸后铝离子测定结果Table 1 Aluminum ion determination results after adding hydrofluoric acid
2.3 铜(II)的前后消耗关系分析
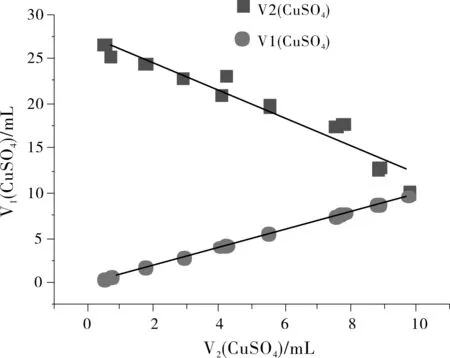
图1 硫酸铜的前后消耗曲线图Fig.1 Consumption curves of copper sulfate before and after
Al3+与EDTA完全络合后,加入PAN指示剂,然后用铜(II)去除过量的EDTA,指示剂变色指示多余的EDTA消耗完全。以利用氟离子置换出与铝离子等物质的量的EDTA,再与铝离子生成更稳定的络合物AlF3,再使用铜(II)滴定至终点,指示剂显色指示着铝离子等物质的量的EDTA,由第二次铜的消耗量可计算出铝含量。这两个过程中得到铜(II)的消耗关系曲线,如图1所示。由图2可见,铜的消耗量指示着铝的浓度的变化,随着铝浓度的降低,第一次消耗的铜(II)是呈线性下降的,同时,第二次消耗的铜(II)是呈线性上升的,最终两者会交叉。当溶液中铝离子的浓度无限接近0的时候,V1处在最大值,说明第一次消耗的铜(II)都与加入的EDTA形成螯合物了,后面加入的氟离子,没有再置换出EDTA,所以,第二次加入铜(II)后指示剂不变色,V2=0,从而验证了溶液中铝离子无限接近于0。
2.4 氢氟酸与铝离子去除关系分析
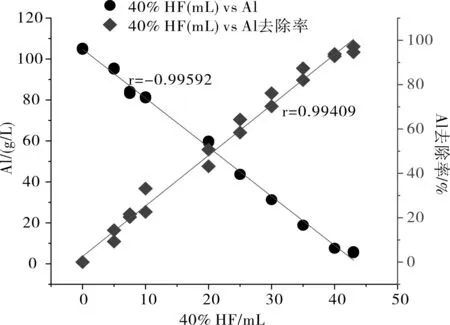
图2 氢氟酸的投加与铝的去除关系曲线图Fig.2 The relationship between the addition of hydrofluoric acid and the removal of aluminum
如图2所示,在失效抛光剂中定量加入氢氟酸试剂,溶液的铝离子明显下降,且氢氟酸投加量与铝离子浓度呈负相关性,线性关系r=-0.9959。同时,氢氟酸投加量与铝的去除率呈正相关关系,线性关系为r=0.99409。由此,可根据实际情况去除60%铝离子的需要(铝件抛光剂需要一定浓度的铝离子作为助剂),定量投加氢氟酸而达到除铝且活化抛光剂的目的。
2.5 实验可靠性分析
强酸下除铝与返滴定法测铝实验中,对氢氟酸的投加量设置10个梯度,分别为0.5 mL,7.5 mL,10 mL,20 mL, 25 mL,30 mL,35 mL,40 mL,43 mL,同时做一组平行样,记录下氢氟酸的投加量与硫酸铜溶液前后滴定的体积差,计算出氢氟酸对铝离子的去除率,数据如表1所示,除铝过程得到铝的浓度偏差为0.014 2009年,黎铉海等发现,往含高浓度铝的废酸液中添加氢氟酸,可显著生成白色沉淀AlF3,除铝效果明显[14]。但是,此法除铝只适用于没有温度或压强要求的耐腐蚀塑料或金属抛光槽。此外,氢氟酸会带进部分水分稀释了抛光剂,也会腐蚀玻璃制品,特别是对于负压蒸酸设备的耐高温耐高压玻璃内胆。对此,本研究在经过除铝工艺后采用加入定量硝酸镁的方法,使镁离子与多余氟离子结合生成氟化镁沉淀而再次去除氟离子,避免了氟腐蚀玻璃设备。 相关反应式为:Mg2++F-→MgF2↓,25℃时,MgF2的Ksp=7.42×10-11,有效去除剩余氟。 所以,经过除铝与除去余氟之后,通过酸回收设备的程序控温,使其负压低温蒸发多余水分再浓缩抛光剂,实现抛光剂有效成分的回收目的。 (1)氢氟酸可显著沉降抛光剂的铝离子,氢氟酸的投加量与铝的浓度关系呈良好的负相关性,相关系数r=-0.9959;使铝离子的浓度降低以除去铝离子。 (2)通过硝酸镁除余氟与负压浓缩抛光剂的方法,通过酸回收设备可以实现失效抛光剂的再生回收利用; (3)在返滴定法测铝的实验中,铜(II)的前后消耗量指示着铝浓度的变化,它们存在良好的负相关关系。 (4)EDTA返滴定测铝法,槽液中铝含量计算为5.4V2(g/L),V2是0.1 mol/L硫酸铜置换Al-EDTA络合物的铝而消耗的硫酸铜体积差,方法稳定、可靠,除铝曲线线性关系r=0.994。2.6 氢氟酸除铝的适用性
3 结 论
