基于网络药理学及分子对接技术探讨五苓散治疗慢性心力衰竭的作用机制
2022-01-27樊懿萱王心意鞠建庆
樊懿萱,王心意,鞠建庆,陈 卓,张 艳,徐 浩
慢性心力衰竭(chronic heart failure,CHF)是多种心脏疾病的终末期阶段。由于各种原因造成心脏结构和/或功能变化,心室的收缩和/或舒张功能障碍,从而引起以呼吸困难、劳累疲乏、液体潴留等为主要表现的一组复杂综合征[1]。至2019年,我国心血管病病人约3.30亿人,其中心力衰竭病人约890万人[2]。目前CHF的药物治疗以利尿剂、血管紧张素转换酶抑制剂(ACEI)、β受体阻滞剂、醛固酮受体拮抗剂为主。但是CHF病程较长,后期发展为多器官、多系统的损害,西药治疗受到一定限制,且长期应用西药副作用较多[3],治疗效果不佳。CHF属于中医学“心衰病”的范畴,根据主要症状不同,分属中医学“水肿”“痰饮”“虚劳”等范畴。五苓散出自“医圣”张仲景所著《伤寒论》,原文中8处提及五苓散,以温阳化气利水为主。现代研究证实,在CHF基础用药上加用五苓散,心力衰竭症状明显缓解,同时降低脑钠肽(BNP)等心力衰竭实验室指标水平,提高心脏收缩能力,具有降脂、降压、利尿等功效,可有效改善心脏功能[4]。网络药理学融合了网络信息学、系统生物学及药理学相关知识,而研究中药时又结合了中医哲学,包括中药与方剂学的相关知识。中药复方的研究在网络信息中量化,通过寻找药物中多种化合物成分,建立药物-疾病-靶点网络,体现了中药多成分、多靶点、多途径的特点[5]。分子对接主要运用计算机技术,立足于现代药理学基础,验证网络药理学相关结果[6],同时从分子机制分析中药复方,为实验验证提供参考。本研究借鉴网络药理学方法,探讨五苓散对CHF作用的相关分子机制,同时运用分子对接方法进行验证,为五苓散治疗CHF提供依据。
1 资料与方法
1.1 药物与疾病靶点网络的建立
1.1.1 五苓散药物靶点筛选 应用中药系统药理学技术平台(Traditional Chinese Medicine Systems Pharmacology,TCMSP),分别以“白术”“泽泻”“猪苓”“茯苓”“桂枝”为关键词检索五苓散组成药物的主要成分,根据TCMSP中的口服生物利用度(oral bioavailability,OB)≥30%及生物活性分子类药性(drug likeness,DL)≥0.18为标准,筛选五苓散组方药物中符合条件的化合物作为活性成分,同时在TCMSP平台中筛选出活性成分对应的靶点,将相应靶点输入UniProt数据库(http://www.uniprot.org/)、STRING数据库(https://string-db.org)及DisGeNET数据库(https://www.disgenet.org/)。STRING及DrugBank数据库作为补充,挖掘相应靶点信息。3个数据库中均选择物种为“人”(Homo sapiens),将靶点转化为相应的靶基因。
1.1.2 疾病靶点筛选 以“chronic heart failure”为关键词,分别检索GeneCards数据库(https://www.genecards.org/)、TTD数据库(http://db.idrblab.net/ttd/)、DrugBank数据库(https://www.drugbank.ca/drugs),DisGeNET数据库(https://www.disgenet.org/)。总结已有报道的CHF相关靶点基因,GeneCards与DisGeNET数据库由于提取基因较多,通过Relevance score取二倍中位数筛选与疾病相关度较高的基因靶点,合并所有数据库,去除重复基因,得到疾病基因库,作为交集网络构建的基础。
1.1.3 五苓散药物-化合物-靶点网络构建 建立五苓散药物-化合物-靶点网络文件,将五苓散药物中的活性成分及其对应靶点导入Cytoscape 3.8.0软件中,进行可视化处理,通过软件自带Analyze Network功能分析网络,根据自由度(Degree)值筛选出关键药物成分。
1.1.4 寻找药物与疾病交集靶点并构建韦恩图 将药物与疾病靶点导入在线数据分析与可视化网络平台(http://www.bioinformatics.com.cn),构建交集韦恩图,得到五苓散与CHF的交集基因。
1.1.5 五苓散药物成分-交集靶点网络建立与关键化合物选取 将药物有效成分及交集靶点导入Cytoscape 3.8.0中,构建成分-交集靶点网络,分析网络,通过Degree值与中位数筛选五苓散关键化合物。
1.1.6 蛋白相互作用网络构建分析及关键靶点筛选 将交集基因导入STRING平台,选择物种为Homo sapiens,自动生成蛋白-蛋白相互作用(PPI)网络。同时将生成的蛋白节点信息以tsv文件导入Cytoscape 3.8.0软件,通过Analyze Network及CytoNCA插件分析PPI,利用Degree、中心性(closeness)及介数(betweenness)与中位数筛选关键靶点。
1.2 基因本体(GO)分析与京都基因与基因组百科全书(KEGG)富集分析 利用Metascape平台(http://www.metascape.org/)分析交集基因,导入基因后选择物种为H.sapiens,通过平台进行GO及KEGG分析,得到关键生物过程(biological processes,BP)、细胞组成(cellular components,CC)、分子功能(molecular functions,MF)及KEGG通路(KEGG pathway),结果筛选后导入可视化平台得到GO及KEGG直方图。
1.3 分子对接 在TCMSP平台中搜索关键化合物结构,保存为mol2文件。阳性对照药物选择利尿剂托伐普坦。该药物通常在CHF病人使用呋塞米等常规利尿剂发生抵抗或者出现肾脏损害时应用[7]。研究发现,在常规药物和呋塞米基础上加用五苓散,治疗后病人呋塞米用量减少,且利尿剂抵抗发生率明显降低[8],故将五苓散与托伐普坦对比。在DrugBank平台中得到托伐普坦化学结构式,保存为mol2文件,为分子对接做准备。将筛选出的关键靶点与KEGG通路富集的基因进行比较,选择主要靶点;将靶点导入PDB网站(http://www.rcsb.org/),得到对应的靶点蛋白及PDB编码(PDB ID),保存蛋白结构为pdb文件。将mol2及pdb文件导入CB-Dock在线对接平台(http://cao.labshare.cn/cb-dock/),平台基于Autodock vina 1.1.2版本进行在线对接,对接过程相对快速,且成功概率较大。对接结果中得到Vina分数(Vina score)与腔体大小。Vina分数的数值越低,结合能力越强,受体和配体的亲和力越好,并且腔体的大小接近或大于配体,对接的准确性就会提高。
2 结 果
2.1 五苓散药物成分的筛选结果 得到五苓散药物成分共49个,分别为白术7个、泽泻9个、猪苓11个、茯苓15个、桂枝7个,去重后共有46个。详见表1。

表1 五苓散中化合物基本信息
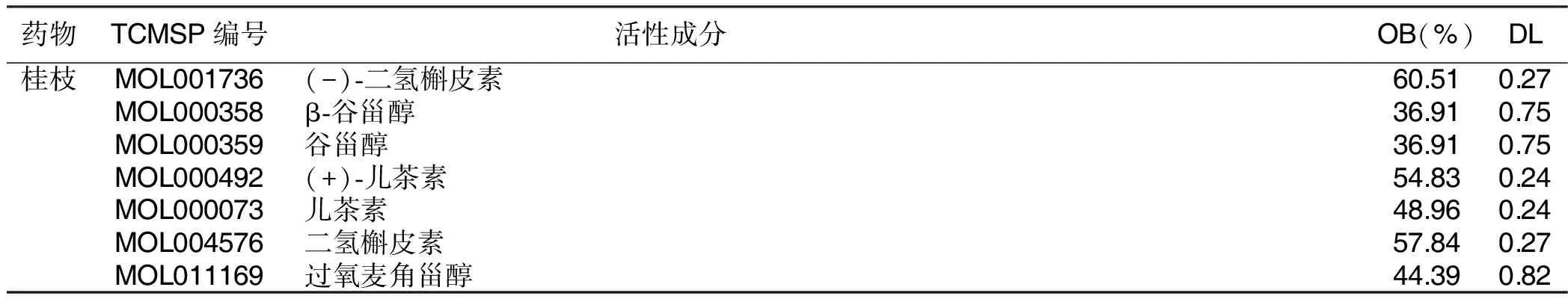
(续表)
2.2 五苓散药物-活性成分-靶点网络构建 筛选出对应靶点的五苓散活性成分共30个,对应的靶点去重后共计67个,标准化后得到靶基因共63个。构建药物-活性成分-靶点网络图,图中共包含95个节点、165条边,体现了五苓散多成分、多靶点的特点。详见图1。
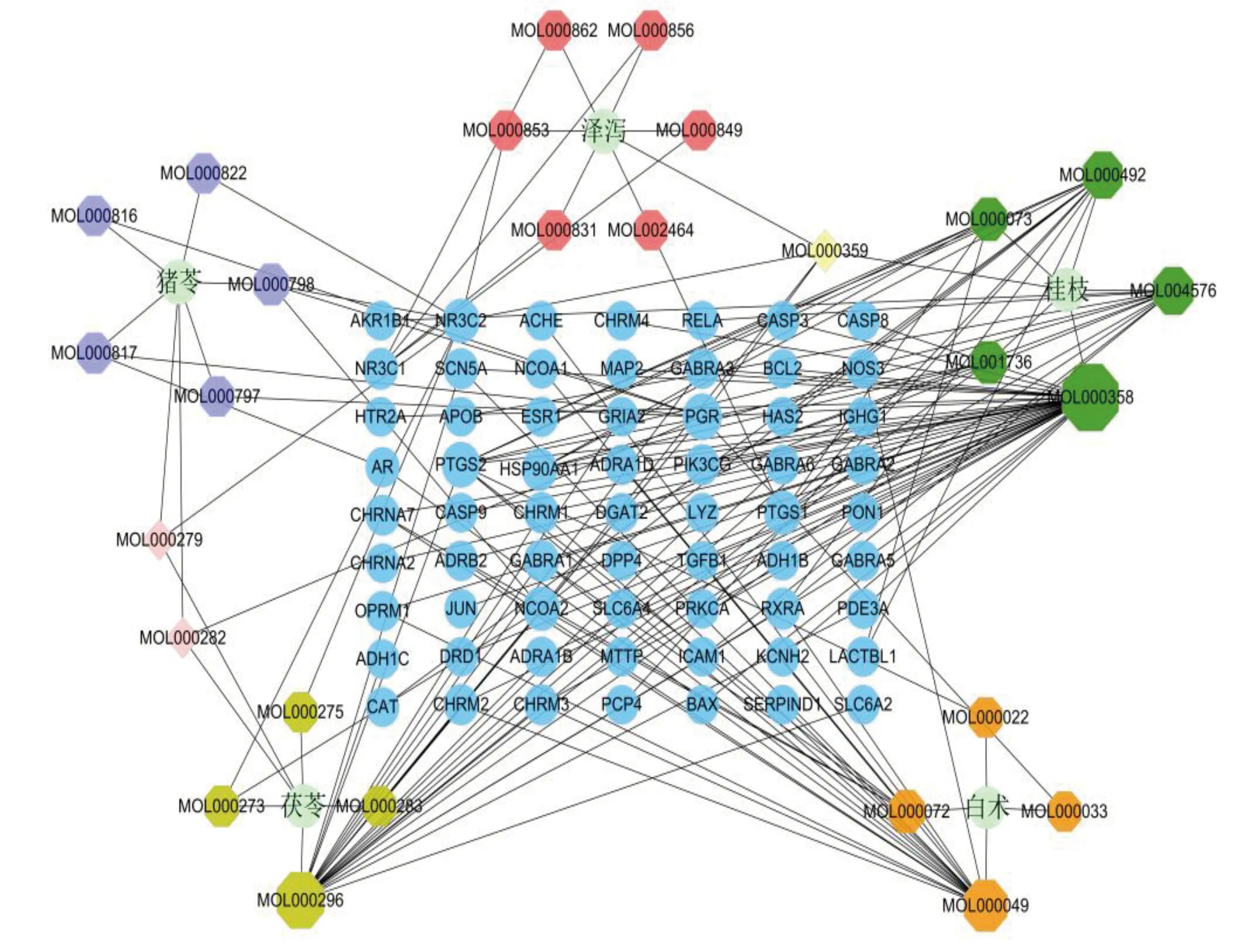
图1 五苓散药物-活性成分-靶点网络(绿色圆形代表药物名称;六边形及菱形代表药物活性成分;蓝色圆形代表药物对应靶点)
2.3 CHF靶点筛选及交集基因 合并数据库并去重后得到CHF相关基因共1 529个,将药物和疾病基因导入在线可视化平台,得到五苓散与CHF交集靶点共36个。详见图2。

图2 五苓散与疾病交集韦恩图
2.4 药物成分-交集靶点网络构建及关键药物成分筛选 构建药物成分-交集靶点图,网络图共有63个节点、85条边,详见图3。共计有10个关键成分。五苓散5种药物囊括关键活性成分,且桂枝所占比例最多,可见在五苓散治疗CHF的过程中,桂枝发挥的治疗作用尤为突出。详见表2。

图3 药物成分-交集靶点网络图(圆形代表药物活性成分;菱形代表药物与疾病交集靶点)

表2 五苓散关键药物成分
2.5 PPI网络建立及关键靶点选取 将交集靶点导入STRING平台,得到PPI网络(见图4)。分析PPI网络,筛选出排名前10位的关键靶点,靶点以NOS3、CASP3、PTGS2、HSP90AA1、CAT等为主,具体靶点详见表3。
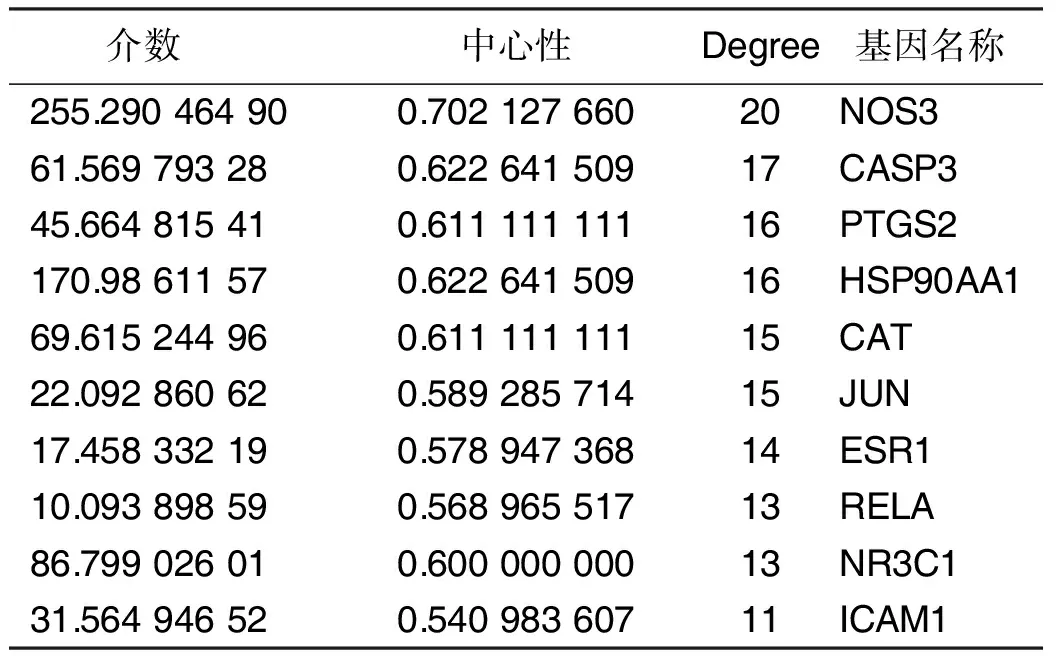
表3 蛋白相互作用网络分析(前10位基因)
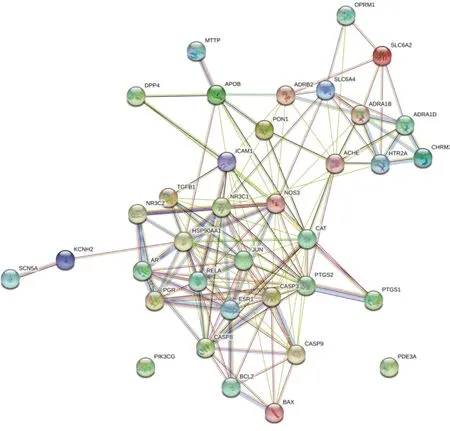
图4 交集基因PPI网络图
2.6 GO分析 GO分析结果富集在BP、CC、MF的分别有576个、32个、54个,分别选取前10位形成直方图。BP主要集中在血液循环(blood circulation)、循环系统流程(circulatory system process)、细胞对有机循环化合物的反应(cellular response to organic cyclic compound)、循环系统中的血管过程(vascular process in circulatory system)等,以循环系统作用为主,和CHF密切相关;CC富集结果主要与细胞膜相关;MF主要富集于蛋白质均二聚活性(protein homodimerization activity)、蛋白结构域特异性结合(protein domain specific binding)、类固醇激素受体活性(steroid hormone receptor activity)、支架蛋白结合(scaffold protein binding)、G蛋白偶联胺受体活性(G protein-coupled amine receptor activity)等多种功能。详见图5。
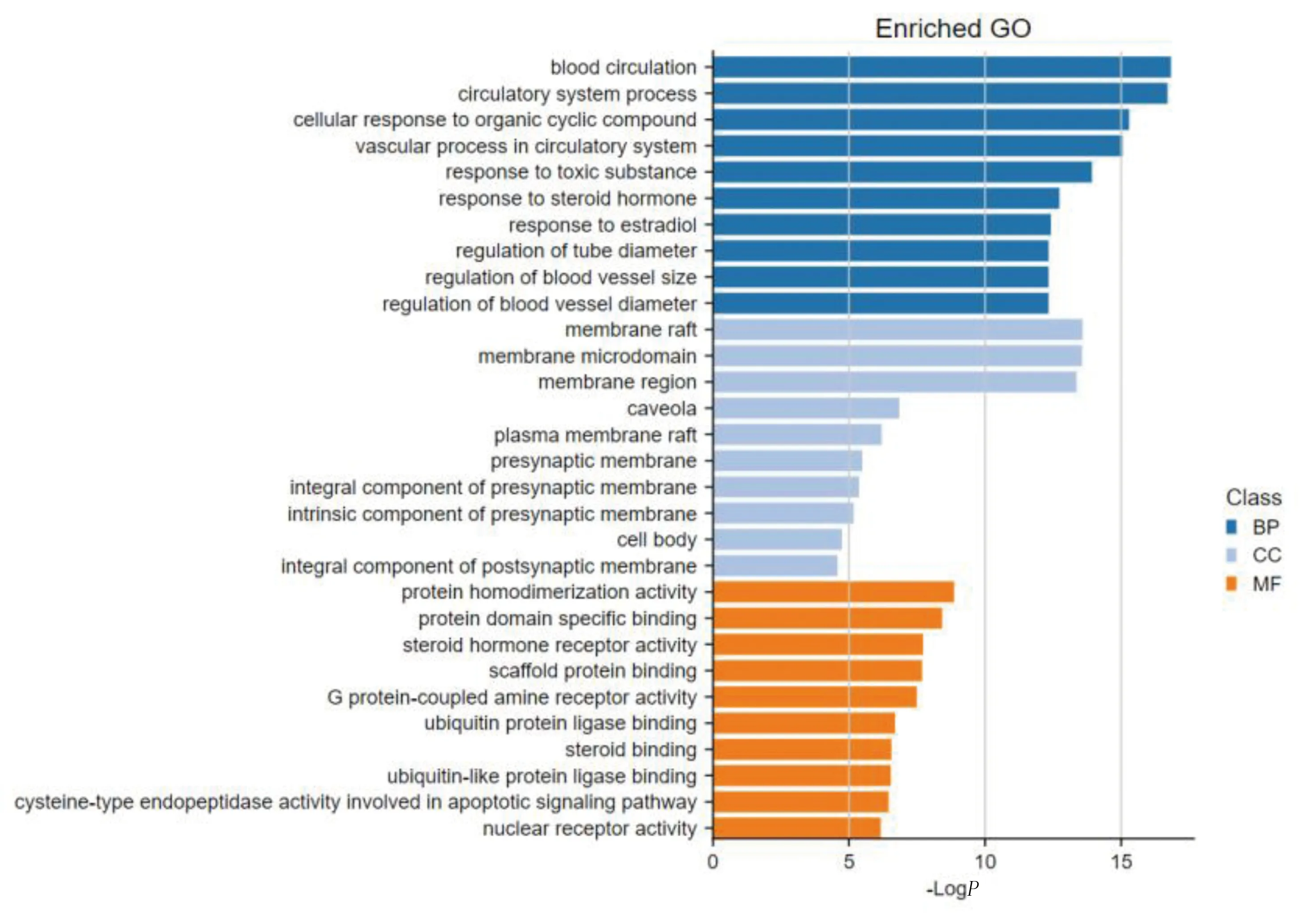
图5 GO生物过程、细胞组成、分子功能分析直方图(前10位)
2.7 KEGG富集分析及通路-靶点-药物成分网络构建 KEGG信号通路富集中靶点数居前20位的信号通路主要包括:AGE-RAGE信号通路、细胞凋亡、白细胞介素-17(IL-17)信号通路、肿瘤坏死因子(TNF)信号通路、液体剪切应力和动脉粥样硬化、心肌细胞的肾上腺素能信号通路、环磷酸鸟苷(cGMP)-蛋白激酶G(PKG)信号通路、刺激神经组织的中的交互、钙信号通路、雌激素信号通路、p53信号通路、点样受体信号通路、磷脂酰肌醇3-激酶(PI3K)-蛋白激酶B(Akt)信号通路、核转录因子-κB(NF-κB)信号通路,详见图6。每条通路富集多个基因,体现了五苓散多靶点、多通路的特点。

图6 KEGG通路富集分析(前20位)
2.8 分子对接验证 最终筛选出NOS3、CASP3、PTGS2、HSP90AA1、CAT、JUN、ESR1、RELA、NR3C1、CASP8共10个靶点。除CASP3没有对应的表达合适的PDB ID外,其余均有一定对接能力。并且Vina分数与腔体大小基本接近于托伐普坦,化合物与NOS3和PTGS2的结合力较好,详见表4、表5。可视化分析对接结果,可见靶点蛋白与活性成分对接结构,选择Vina分数后4位作图,共有5组对接,同时与托伐普坦比较,详见图7。
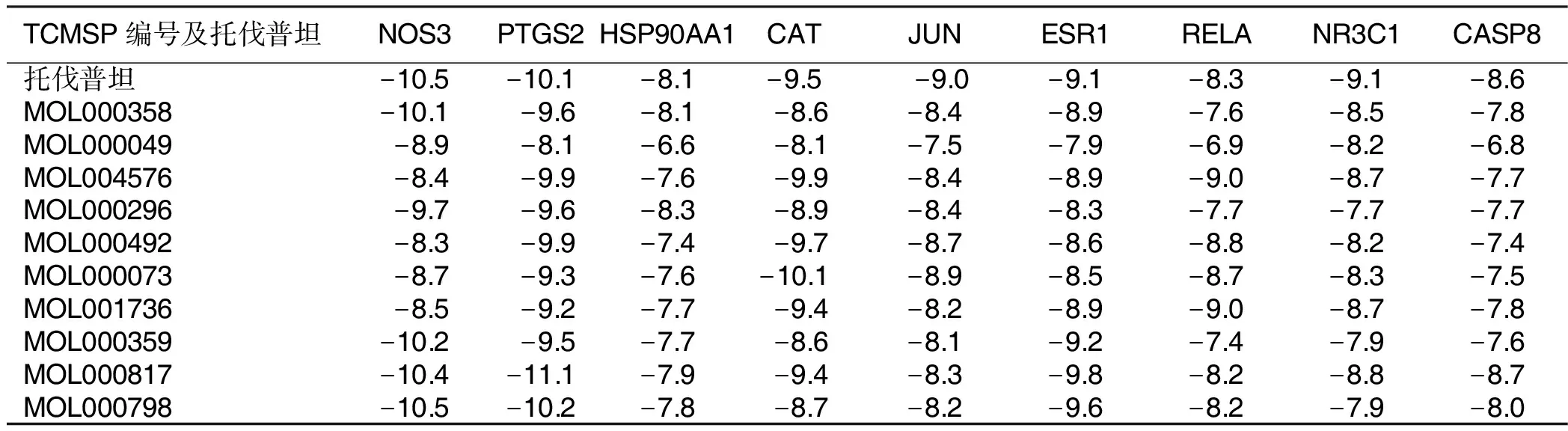
表4 化合物及托伐普坦与靶点对接的Vina 分数
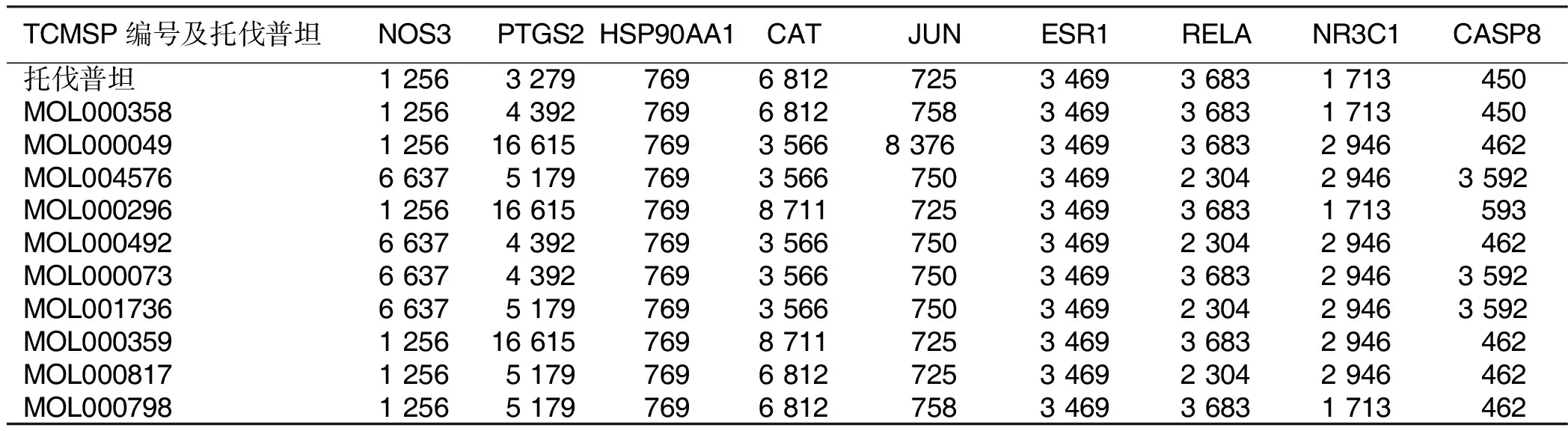
表5 化合物及托伐普坦与靶点对接的腔体大小

图7 配体与大分子对接结果可视化分析
3 讨 论
CHF的中医病机以“虚、瘀、水”为基础,以益气、养阴、温阳、活血、利水为主要治则,其中水饮内停的主要选方为五苓散[9]。现代医学认为心肌重构是CHF发生发展的重要病理生理学过程[1],心肌细胞凋亡、炎症反应、氧化应激是促进心肌重构的主要病理机制[10]。针对五苓散君药泽泻的药理研究,已明确其具有利尿、降低血脂作用,并且可以减少氧化应激中产生的活性氧(ROS),抵抗氧化损伤,还能通过抑制NF-κB通路起到抗炎作用[11]。含有关键化合物最多的桂枝,治疗心血管疾病的作用显著,具有良好的降血压、扩血管作用,同时也发挥抗炎作用[12]。本研究挖掘获得五苓散多个活性成分。动物实验表明,β-谷甾醇可以调节凋亡基因从而抑制心肌细胞凋亡,而二氢槲皮素具有抗氧化作用,通过调节心肌组织中的超氧化物歧化酶(SOD)、过氧化氢酶(CAT)活性,抑制氧化应激,防止心肌缺血损伤[13]。常春藤皂甙元可以降低高脂血症大鼠的血液黏度[14],改善血流动力学,降低心血管疾病风险。儿茶素具有抗氧化、抗炎及改善血管内皮障碍的作用[15],并且儿茶素竞争性抑制磷酸二酯酶,促进钙离子内流,具有扩张血管、产生正性肌力的作用,改善血流动力学,同时抑制心肌细胞凋亡。与米力农等磷酸二酯酶抑制剂相比,儿茶素属于天然药物,对心脏的副作用较小,应用于CHF更加安全[16]。
本研究筛选出NOS3、CASP3、PTGS2、HSP90AA1、CAT、JUN、ESR1、RELA、NR3C1、ICAM1等关键靶标,靶标通过相关通路发挥作用。血管中一氧化氮(NO)的释放,有赖于NOS3的诱导。NO可以帮助血管舒张,防止血小板聚集,阻止血栓的产生,起到了保护血管、防止动脉粥样硬化的作用[17-18]。通过实验基本确定调节NOS3可以改善左心室再灌注心肌损伤,有望减轻左心室不良重构[19]。CASP3属于细胞凋亡相关分子,与心肌细胞凋亡关系密切[20],抑制CASP3有利于防止细胞凋亡,延缓疾病进展。PTGS2编码产生环氧合酶-2(COX-2),抑制COX-2会导致心力衰竭的风险增加[21]。有研究发现,保护HSP90AA1有利于缺血-再灌注后心肌细胞的恢复[22]。CAT可以有效抑制神经内分泌系统激活时导致的氧化应激,过表达时可以抵抗缺血-再灌注导致的心肌损伤[23]。JUN是转录因子AP-1的主要组成成分,而AP-1同样介导细胞的增殖、分化与凋亡[24]。RELA通过翻译后的泛素化修饰,可以抑制NF-κB炎症通路[25]。NR3C1为糖皮质激素受体基因,容易变异,有研究发现,该基因的变异与心血管疾病常见的血压、血脂、血糖等危险因素相关[26]。
GO富集分析发现多生物过程主要富集于循环系统。分子功能主要包括蛋白质均二聚活性、泛素蛋白连接酶结合、类固醇结合、泛素样蛋白连接酶结合、半胱氨酸型内肽酶活性参与细胞凋亡信号通路,每种功能富集多个基因,说明五苓散相关靶点通过发挥多种分子功能作用于CHF。KEGG分析结果显示,富集的多条通路与心血管疾病关系密切,每条通路富集多个基因,五苓散通过调控相关通路作用于CHF。AGE-RAGE信号通路可以通过氧化应激反应激活NF-κB通路,引起异常炎症反应,同时也会引起细胞间黏附分子-1(ICAM-1)等基因的转录,易导致心血管疾病的发生[27]。研究发现,IL-17通过AP-1上调存在于心肌细胞中趋化因子C-C基序配体2(CCL2)的表达,加速了心肌损伤[28]。IL-17激活NF-κB信号通路[29]等多种炎症通路,促进心肌细胞凋亡[30]。研究表明,TNF-α导致左心室重塑,同时激活炎症通路,与心肌炎、心力衰竭多种心脏疾病相关[10],因此,调控TNF相关通路对心力衰竭的治疗有一定影响[31]。动物实验表明,激活cGMP-PKG信号通路可以减轻心肌损伤,抑制炎症反应[32]。心肌细胞的肾上腺素能信号可以介导钙信号通路,有效防止心律失常,起到保护心脏的作用[33]。
分子对接结果中,参与对接的主要药物成分与相关靶标有良好的对接,尤其是谷甾醇(sitosterol)、麦角甾-5,7,22-三烯-3-醇(ergosta-5,7,22-trien-3-ol)、麦角甾-7,22-二烯-3β-ol(ergosta-7,22-diene-3β-ol)与NOS3和PTGS2的结合力较为显著,且与阳性对照药物托伐普坦接近。托伐普坦对CHF液体潴留和利尿剂抵抗有效,并且有临床试验表明治疗后病人血清TNF-α、ICAM-1等炎症分子水平降低[34]。因此,本研究结果为五苓散用于CHF利尿剂抵抗病人提供了网络药理学依据。
通过网络药理学分析五苓散治疗CHF的作用机制,体现了五苓散药物多种成分、多个靶点、多条通路作用于疾病的特点,主要以炎症通路、氧化应激、心室重构、细胞凋亡等相关通路作用于CHF,研究挖掘出的药物成分与相关靶点为实验验证及新药的开发提供了基础。
