纳米金/硫堇/科琴黑修饰玻碳电极同时检测抗坏血酸和尿酸
2022-01-25张飞翔金葆康
张飞翔,金葆康
(安徽大学 化学化工学院,安徽 合肥 230601)
抗坏血酸(ascorbic acid,简称AA),通常称为维生素C,是人类和动物进行代谢反应所需的重要化合物.AA对正常组织的生长、健康的细胞发育和自由基清除具有至关重要的作用[1-2].尿酸(uric acid,简称UA)水平升高可能导致痛风、高尿酸血症、肥胖、非酒精性脂肪肝和慢性肾脏病[4-5].
快速准确地测定AA和UA含量,是人们普遍关注的问题.目前,已经报道了多种定量分析检测AA和UA的方法,例如,离子色谱法[6]、高效液相色谱[7]、比色法[8]和化学发光法[9]等.但是,这些方法费用高昂、费时和操作复杂.具有灵敏度高、检出限低、成本低等优点的电化学传感器受到了研究者的喜爱.抗坏血酸和尿酸都是电化学活性化合物,在水溶液中易被氧化,循环伏安法、差示脉冲伏安法、计时电流法和方波伏安法等电化学技术通常用于抗坏血酸和尿酸的检测.
硫堇(thionine,简称Thi)是一种噻嗪类碱性染料[10],它具有很好的电化学活性,是电化学传感器优良的基底材料和电催化剂[11].Lai等[12]将硫堇和磁性壳聚糖微球修饰在玻碳电极表面制备生物传感器来实现同时灵敏地对多巴胺和尿酸的检测,Sohrabnejad等[13]利用嵌入在聚氯乙烯(PVC)基体中的离子对络合物硫堇-钨磷酸盐修饰电极通过标准添加方法间接测定抗坏血酸.Sun等[14]报道了将尿酸氧化酶和硫堇-氧化石墨烯杂化纳米片固定在玻碳电极上来实现对尿酸的检测.
尽管已有报道对AA和UA进行灵敏度和选择性的检测,但在常规电极上由于AA和UA的氧化峰重叠,同时缓慢的电子转移动力学及由其氧化产物引起的严重电极污染给电化学选择性测量AA和UA的浓度造成了很大的困难[15].
笔者利用纳米金(gold nanoparticles,简称AuNPs)、硫堇/科琴黑(Ketjen black,简称KB)修饰玻碳电极,开展AA和UA浓度的电化学检测.结果表明,硫堇/科琴黑复合物因其良好的电化学活性,能够加快电子转移,纳米金具有良好的生物相容性和电催化活性[16],两者共同修饰,产生协同催化作用,实现较低的过电位下AA和UA的电催化氧化,以期得到分离明显的AA和UA的氧化峰,扩宽检测方法的线性范围,提高检测方法的抗干扰能力及灵敏度等.
1 实验部分
1.1 仪器与试剂
硫堇(Thi)、科琴黑(KB)、抗坏血酸(AA)、尿酸(UA)、氯金酸(HAuCl4·4H2O)、半胱氨酸、多巴胺、NaCl、葡萄糖,均为分析级试剂.用Milli-Q水(18.2 MΩcm,Millipore)配置溶液.
循环伏安法(CV)和差分脉冲伏安法(DPV)在CHI 660D电化学工作站(上海辰华仪器有限公司)上进行,采用传统的三电极体系,铂丝为对电极,Ag/AgCl电极用作参比电极,直径3 mm的修饰玻碳电极(glassy carbon electrode,简称GCE)用作基底电极.
1.2 Thi-KB纳米复合材料的制备
参考文献[17]制备Thi/KB纳米复合材料.将1 mg KB和2 mg Thi分散在1 mL蒸馏水中.通过在室温下至少6 h超声处理形成Thi/KB纳米复合材料.然后通过离心和连续水洗3次形成纳米复合材料.将获得的Thi/KB纳米复合物再分散在1 mL蒸馏水中用于进一步实验.
1.3 AuNPs/Thi/KB修饰的玻碳电极(GCE)的制备
在修饰Thi/KB纳米复合材料之前,先用0.05 μm和0.3 μm的氧化铝浆料抛光GCE(直径3 mm),然后用水冲洗,再分别于去离子水和酒精中超声清洗10 min,用氮气吹干后,将6 μLThi/KB纳米复合物悬浮液滴涂到GCE电极上,空气干燥.然后将Thi/KB/GCE在含有2 mg·mL-1的HAuCl4溶液中进行电化学沉积[18],电位为-0.2 V,持续300 s.将得到的电极标记为AuNPs/Thi/KB/GCE.电极使用前,二次水洗涤、氮气吹扫干燥.
利用类似方法,同时制备了纳米金修饰玻碳电极(AuNPs/GCE),Thi/KB/纳米金修饰的玻碳电极(先沉积纳米金,再修饰Thi/KB,最后得到Thi/KB/AuNPs/GCE),以及Thi/KB修饰的玻碳电极(Thi/KB/GCE).
2 结果与讨论
2.1 Thi-KB复合材料的形貌表征
利用SEM观察KB,Thi,Thi/KB和AuNPs/Thi/KB修饰电极的表面形貌,结果如图1所示.

图1 KB(a),Thi(b),Thi/KB(c),AuNPs/Thi/KB(d)修饰电极的SEM图
图1显示,KB修饰电极表面为小球状(图1(a)),而Thi在电极表面为典型的针状晶体(图1(b)),图1(c)显示制备的Thi/KB纳米复合材料在电极表面呈现为小球与针状晶体的组合体;进一步,在Thi/KB复合材料修饰电极上电沉积HAuCl4溶液后,可以观察到颗粒直径约60 nm的纳米金生成(图1(d)),表明电化学还原可成功将AuNPs均匀地修饰至复合材料表面,有利于提升电子转移速率[19].
2.2 修饰电极性能的研究
在0.2 mol·L-1PBS(pH 7.0)溶液中,利用循环伏安法研究1 mmol·L-1AA和1 mmol·L-1UA在几种不同修饰电极上的电化学行为,结果如图2所示.
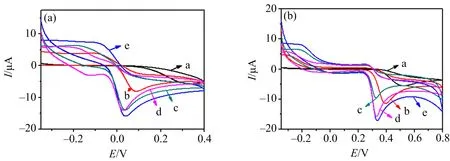
图中曲线a为GCE,b为AuNPs/GCE,c为Thi/KB/AuNPs/GCE,d为Thi/KB/GCE(d),e为AuNPs/Thi/KB/GCE;扫速为10 mV·s-1.
由图2可知,在实验条件下AA和UA在5种电极表面均发生不可逆的电化学氧化.相比于裸玻碳电极,在AuNPs/GCE和Thi/KB/GCE修饰电极上,AA和UA的氧化峰均发生显著正移,且氧化峰电流增大,表明AuNPs和Thi/KB的修饰,均降低氧化过电位,加速电子转移速率.AuNPs/Thi/KB/GCE(曲线e)与先电沉积修饰AuNPs再修饰Thi/KB(Thi/KB/AuNPs/GCE,曲线c)相比,前者在电化学氧化AA和UA均表现出更大的氧化电流.可能是在玻碳电极表面先电沉积的AuNPs被随后修饰的Thi/KB所覆盖,抑制了AuNPs对AA和UA催化氧化作用.而在AuNPs/Thi/KB/GCE电极上(曲线e),展现出更低的氧化峰过电位和更大的氧化峰电流.这可能得益于AuNPs大的比表面积、良好的导电性以及表面的快速电子转移[19],而Thi/KB上的NH2,通过氢键与AA和UA作用,电子通过N…H…O传递,降低了氧化过电位,促进了其电化学氧化还原.AuNPs和Thi/KB的协同作用,使得AuNPs/Thi/KB/GCE电极表现出最佳电催化性能.
进一步利用CV考察了AuNPs/Thi/KB/GCE电极上AA和UA电化学性能,结果如图3所示.
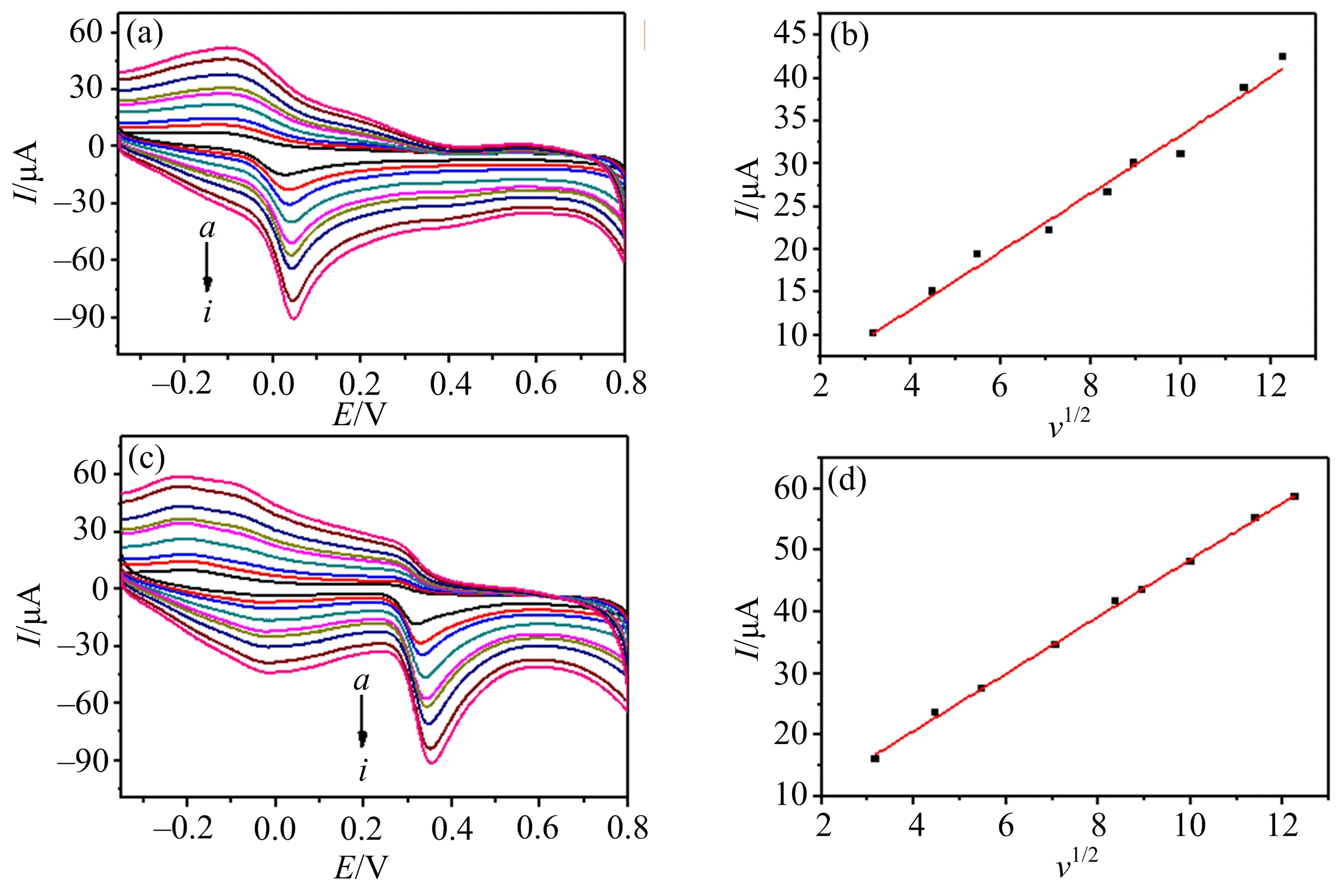
a→i扫速分别为10,20,30,50,70,80,100,130,150 mV·s-1.
由图3可知,AA和UA均呈现为不可逆氧化过程,随电位扫速增加,AA和UA的峰电位略有正移,氧化峰电流增大,且峰电流值与扫速的平方根呈线性关系,表明氧化电流受扩散控制.进一步说明AA和UA受AuNPs和Thi-KB的协同催化作用,在修饰电极上具有较快的电子转移速率.
2.3 条件优化
2.3.1 电沉积纳米金的时间
考察修饰纳米金的电化学沉积时间对电极电化学行为的影响.定义氧化电流变化值:△I=(Ip′-Ip0)/Ip0×100%(Ip0,Ip′分别表示纳米金修饰前、后氧化峰电流值).考察△I随沉积时间的变化关系,结果如图4所示.

图4 Thi/KB/GCE上沉积不同时间纳米金时在AA和UA缓冲溶液中的氧化峰电流值增大的比例曲线(电位为-0.2 V)
由图4可知,当电沉积纳米金时间小于300 s时,AA和UA在AuNPs/Thi/KB/GCE上氧化峰电流随沉积时间增加逐渐增大,在300 s时达到最大,当电沉积纳米金超过300 s时,氧化峰电流又逐渐减小.可能的原因是,当电沉积纳米金时间小于300 s时,随着电沉积时间的增加,电极表面的AuNPs颗粒逐渐增多,增大了修饰电极的表面积,加速了电子传递速率,当电沉积时间超过300 s时,随着纳米金的沉积,在电极表面形成致密的金膜,减小了Thi/KB与AA和UA的直接接触,从而降低其电催化能力,导致电流减小.故选取电沉积300 s为最佳沉积时间.
2.3.2 缓冲溶液pH
考察了缓冲溶液pH对AA和UA在修饰电极表面的电化学行为的影响.利用循环伏安法分别研究不同pH下,PBS溶液中AA和UA在修饰电极上的伏安行为,结果如图5(a)(c)所示.由图可知:随着缓冲溶液pH的升高,AA和UA的氧化峰电位负移,并且AA和UA的氧化峰电位与pH呈线性关系,斜率为-51.06 mV·pH-1(AA,图5(b))和-58.91 mV·pH-1(UA,图5(d)).该值接近-59.2 mV·pH-1的理论值.表明AA和UA在修饰电极上的电化学氧化为等质子等电子过程[19-23].

图5 不同pH下1 mmol·L-1AA(a)和1 mmol·L-1UA(c)在AuNPs/Thi/KB/GCE上的CV图;AA(b)和UA(d)氧化峰电位与pH的关系
2.4 定量分析
在优化条件下,利用差分脉冲伏安法研究AuNPs/Thi/KB/GCE对AA和UA的同时电化学检测,结果如图6所示.
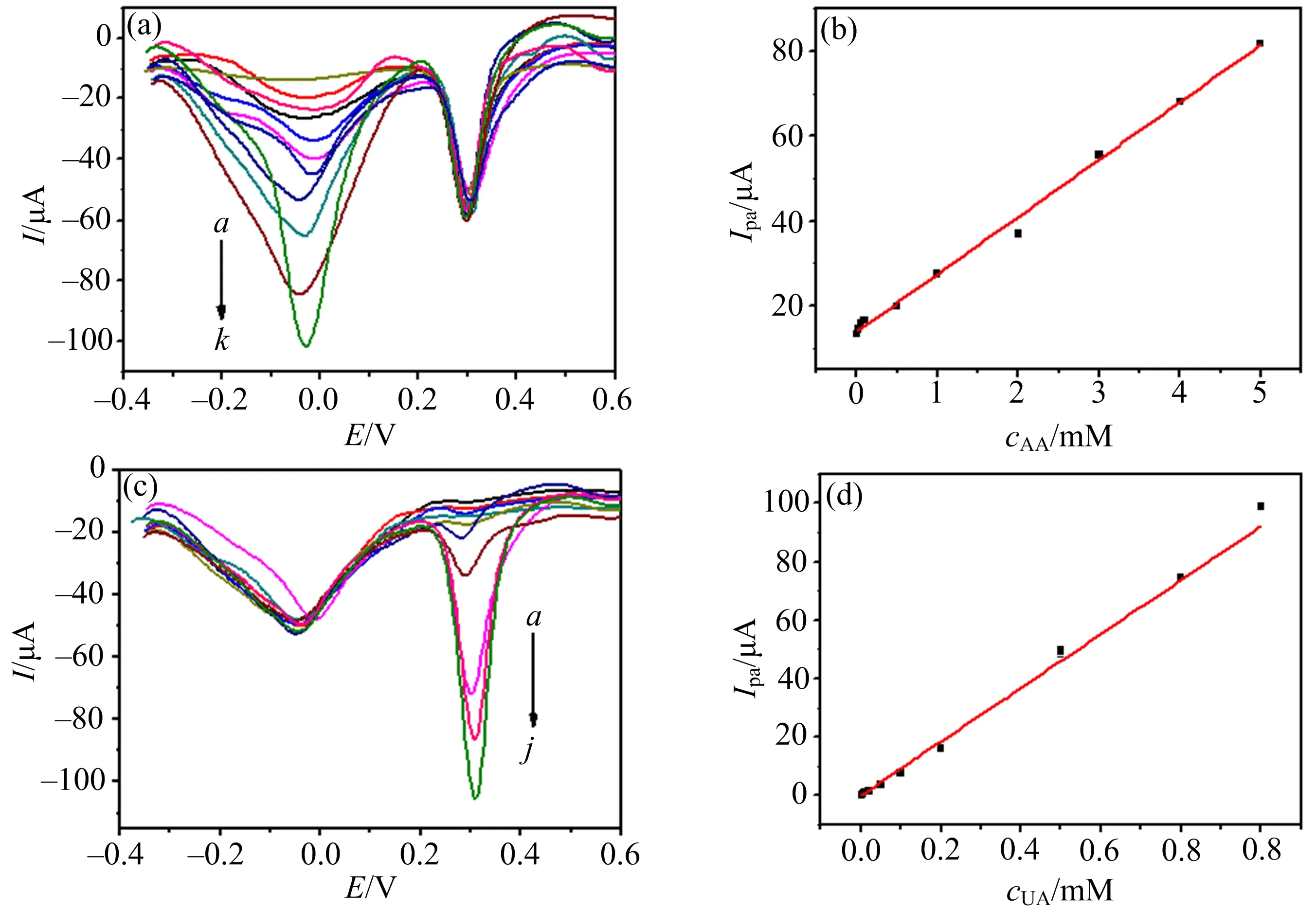
图(a)中a→k表示AA浓度分别为0.01,0.02,0.05,0.1,0.2,0.5,1,2,3,4,5 mmol·L-1;图(c)中a→j表示UA浓度分别为0.002,0.005,0.01,0.02,0.05,0.1,0.2,0.5,0.8,1 mmol·L-1.
图6表明,保持AA或者UA的浓度不变,另一种物质的峰电流值随着其自身浓度的升高而线性增大,AA氧化峰电位在0 V左右,UA氧化峰电位在0.3 V左右,两者氧化电位差达到300 mV,呈现完全独立的2个氧化峰.AA的氧化峰电流与其浓度在5×10-3~1×10-5mol·L-1范围内呈线性关系,线性方程为:i=13.885+13.512cAA,相关系数r=0.995,校准曲线的斜率为13.512 μA·(mol·L-1)-1,灵敏度为191.16 μA·(mol·L-1)-1·cm-2,检出限为1.30×10-6mol·L-1(S/N=3).UA的氧化峰电流与其浓度在1×10-3~2×10-6mol·L-1范围内呈线性关系,线性方程为:i=0.031+92.05cUA,相关系数r=0.992 6,校准曲线的斜率为92.05 μA·(mol·L-1)-1,灵敏度为 302.24 μA·(mol·L-1)-1·cm-2,检出限为6.32×10-7mol·L-1(S/N=3).
将笔者所制备的电化学传感器的性能与相关文献报道的AA和UA电化学传感器进行比较,结果如表1~2所示.

表1 不同AA电化学传感器的检测性能

表2 不同UA电化学传感器的检测性能
由表1~2可知,制备的电化学传感器具有较宽的线性范围和较低的检出极限,可以实现AA和UA的同时检测.表明所制备的传感器具有较好的同时检测AA和UA的能力.
2.5 传感器的抗干扰性、重复性和稳定性
利用差分脉冲伏安技术研究了葡萄糖、氯化钠、多巴胺和半胱氨酸对AA和UA测定的干扰.分别加入2.5倍浓度葡萄糖、氯化钠、多巴胺和半胱氨酸作为干扰物,考察干扰物的加入对峰电流的影响,结果如图7所示.
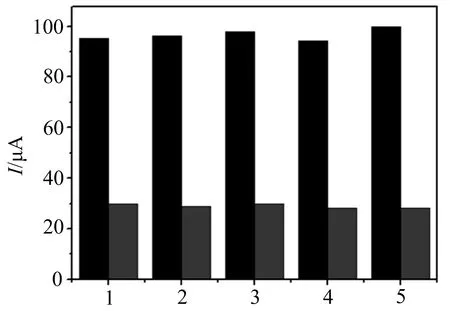
横坐标上1为加入干扰物前的UA(左侧柱)和AA(右侧柱);2~5分别为加入干扰物2.5 mmol·L-1葡萄糖、2.5 mmol·L-1氯化钠、1 mmol·L-1多巴胺、2.5 mmol·L-1半胱氨酸的UA(左侧柱)、AA(右侧柱).
由图7可以发现,干扰物加入前后,AA和UA氧化峰电流值变化均小于5%,表明该修饰电极对AA和UA的检测都具有良好的抗干扰性.
修饰电极回收率测试结果如表3~4所示.

表3 AA回收率的测定

表4 UA回收率的测定
由表3~4可知,AA回收率在97%~105%范围内,UA回收率在95%~103%范围内,表明修饰电极准确性良好,可应用于在实际样品中对AA和UA的检测.
修饰电极制备的平行性和长期稳定性结果如图8所示.
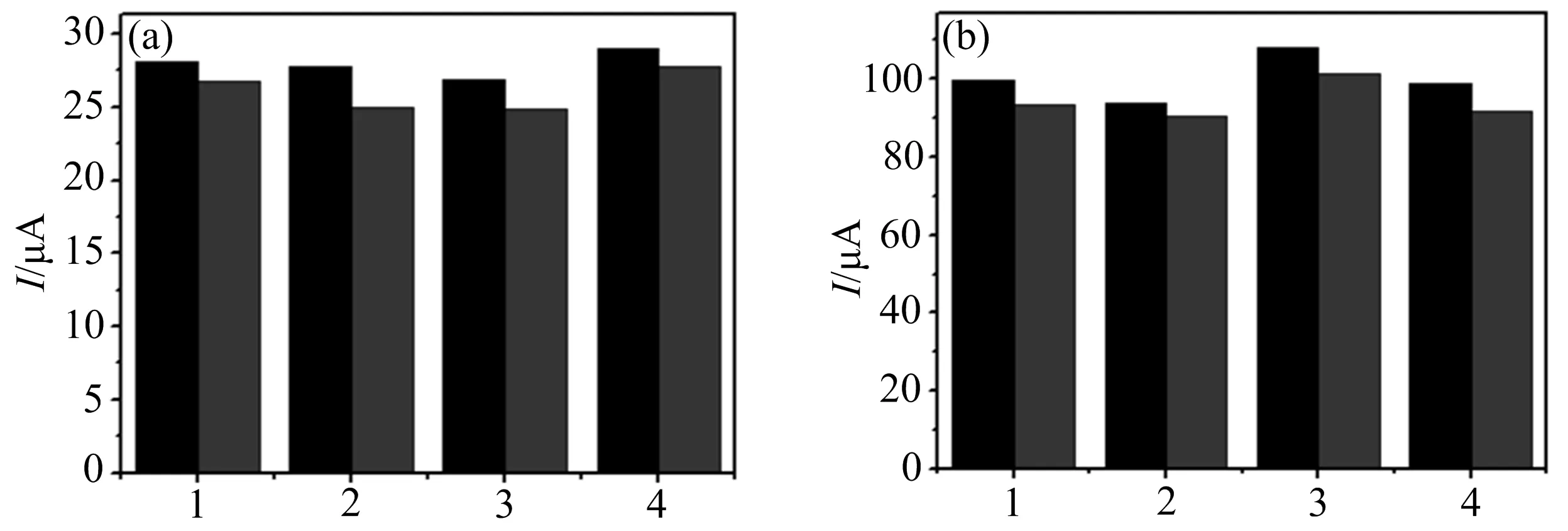
图8 AA(a)和UA(b)在4根平行AuNPs/Thi/KB/GCE上立刻测定(左侧柱)和放置一周之后(右侧柱)测定的氧化峰电流值
图8显示,对于AA和UA的检测,4根平行电极的氧化峰电流值相差小于8%,表明该电极具有很好的可重现性,在放置一周之后,AA和UA的氧化峰电流降低小于10%,显示修饰电极具有较好的稳定性.
3 结束语
基于硫堇/科琴黑复合物滴涂在玻碳电极上,然后电沉积纳米金,成功地制备了可同时定量检测抗坏血酸和尿酸的AuNPs/Thi/KB/GCE修饰电极.研究结果表明AuNPs和Thi/KB均可独自催化抗坏血酸和尿酸的电化学氧化,而AuNPs/Thi/KB/GCE修饰电极表现出更高的电催化氧化效果,表明两者可能存在协同催化作用.该传感器制作过程简单,具有较宽检测线性范围、较低的检出限和同时检测等优点.
