高强度聚焦超声消融联合GnRH-a治疗弥漫型子宫腺肌病患者的临床疗效分析*
2022-01-24戚莹莹潘礼洁
张 婷,戚莹莹,潘礼洁,姜 翙
(广州医科大学附属第五医院妇产科,广州 510700)
子宫腺肌病好发于30~50 岁妇女,发病率为10%~50%,常会导致继发性痛经及月经量增多等症状[1]。近20年来,高强度聚焦超声(HIFU)在子宫肌瘤及子宫腺肌病的治疗已经得到专业所认同而渐渐普及[2-3]。HIFU 治疗时采用一定聚焦方式将体外低能量的超声聚焦到体内形成一个能量高度集中的区域,通过超声在生物组织中的热效应和空化效应等使该区域病变组织产生不可逆转的凝固性坏死,而对焦域外的组织不产生明显影响[4]。在2020 年发布的“子宫腺肌病诊治中国专家共识”中提出,高强度聚焦超声可作为治疗子宫腺肌病的“介入”治疗[5],但因目前高强度聚焦超声在治疗子宫腺肌病范围划定、治疗剂量方面仍未形成统一的规范,故导致现治疗效果不一,功率过高易导致肠损伤、皮肤灼伤、血尿等并发症发生[6]。以往研究表明,在HIFU 治疗前或后联合促性腺激素释放激素激动剂(GnRH-a)治疗子宫腺肌病,效果明显比单纯HIFU治疗更好[7]。本研究通过对比单纯HIFU治疗及HIFU治疗前、后联合GnRH-a治疗子宫腺肌病的疗效差异,旨在探寻一种高效且优化治疗时长、降低累积功率的子宫腺肌病治疗策略。
1 资料与方法
1.1 一般资料
选取2018 年12 月至2020 年12 月在广州医科大学附属第五医院接受HIFU治疗的90例子宫腺肌病患者,病例纳入标准:(1)经超声及MRI确诊的为子宫腺肌病;(2)有HIFU治疗指征,如痛经,或经量增多;(3)要求保留子宫,不愿意手术治疗。排除标准:(1)妊娠妇女;(2)腹壁距离靶点边缘距离>13 cm;(3)可疑恶性变者;(4)疑有盆腔内广泛粘连者,声通道欠通畅;(5)合并其它系统恶性肿瘤、严重心、脑血管疾病者。按照随机数字表法将研究对象分为对照组、研究1组、研究2组,每组30例,分别给予不同治疗措施干预。对照组平均(38.0±8.5)岁,体重指数(Ibm)(21.5±3.6)kg/m2,VAS 评分(7.8±2.3)分,子宫体积(220.43±15.81)mm3;研究1 组平均(37.1±8.1)岁,Ibm(20.8±2.6)kg/m2,VAS 评分(7.5±3.4)分,子宫体积(219.63±18.11)mm3;研究2组平均(36.8±7.2)岁,Ibm(20.0±2.4)kg/m2,VAS 评分(7.8±1.4)分,子宫体积(213.43±25.01)mm3,3 组间年龄、Ibm、VAS 评分、治疗前子宫体积比较,差异均无统计学意义(均P>0.05)。
1.2 方法
1.2.1 临床资料采集 由研究人员与患者签署同意书后,采集其年龄、孕产史、Ibm、月经量、VAS 评分参数等指标,收集术前、术后超声、MRI等影像参数,彩色多普勒超声系统为深圳迈瑞生物医疗电子股份有限公司DC-8-Pro,三维容积探头,频率2.0~6.0 MHz。磁共振成像系统为德国西门子MAGNETOM Skyra 3.0T;增强磁共振对比剂采用钆双胺注射液0.5 mmol/mL(剂量15~20 mL 经肘静脉注射,注射流率2 mL/s,注射后即刻行矢状位和轴位动态增强扫描,观察至注射造影剂后120 s)TW2 像测量病灶三维直径;计算体积=0.5233×长径×前后径×横径。
1.2.2 分组处理 对照组使用高强度聚焦超声对病灶行消融治疗:高强度聚焦超声肿瘤消融系统为上海新地HIFU-2001,超声频率为1 MHz±50 kHz,超声消融区声强大于3 000 W/cm2,超声消融单点范围5 mm×5 mm×8 mm;超声消融区温度范围:65~100 ℃;患者术前2 d 进行少渣饮食及膀胱憋尿训练,治疗前1 d 禁食糖、蛋、奶制品减少肠道气体。采用连续3 d HIFU 治疗。治疗步骤:①会阴部备皮,确认患者治疗前排便排气及适量憋尿;②经腹超声定位子宫腺肌病病灶最大切面,再次确认膀胱充盈情况(如膀胱容量不理想或患者憋尿困难可放置膀胱导尿管并以常温生理盐水维持膀胱容量,等待10 min后开始治疗);③治疗时嘱患者俯卧,前腹壁与水槽内的脱气水充分接触;④仪器设置:超声换能器电功率60~80 V(声强2 800~3 200 W/cm2);点间隔距离:x 轴(左—右轴)7 mm、y轴(头—脚轴)7 mm、z轴(深—浅轴)8 mm;每点位发射时间200 ms;间隔时间150 ms;重复次数60次;⑤在机载超声探头定位子宫病灶最大切面后设计治疗范围,病灶边缘浅、头、两侧及脚象限内1 cm,及深象限内2 cm预留安全距离避免损伤正常组织;⑥开始治疗,并在治疗过程注意患者疼痛耐受情况、利用机载超声检测病灶位置是否偏离;⑦向病灶血流信号较丰富、两侧及靠近子宫肌层附着部分进行加强治疗,直至以上部分出现明显超声灰度变化,计算并记录靶区有灰度变化患者/无灰度变化患者比率。如治疗过程中患者疼痛难以耐受或出现其它不适终止治疗。
研究1组于HIFU治疗前,于月经来潮第一天予以皮下注射醋酸戈舍瑞林(AstraZeneca UK Limited,英国)3.6 mg,间隔28 d再次皮下注射诺雷德,共2次,28 d后予行HIFU治疗,治疗方式同对照组。
研究2 组于HIFU 治疗后第一次月经来潮第1 天皮下注射醋酸戈舍瑞林3.6 mg,间隔28 d 再次皮下注射1次,共2次。
1.3 疗效评估
于全部治疗结束3 个月、6 个月后,随访患者并进行疗效评估,随访指标包括治疗后经量变化、痛经VAS评分变化、术后并发症发生率及影像学指标等;比较治疗前后3个月、6 个月增强MRI评估子宫大小变化;子宫体积缩小率=(治疗前子宫体积-随访时子宫体积)/治疗前子宫体积×100%。疗效判定标准:(1)显著有效:3 个月病灶体积缩小>50%;(2)明显有效:病灶体积缩小20%~49%;(3)有效:病灶体积缩小10%~19%;(3)无效:病灶体积无变化或变化<10%[8]。月经量评估:为对每次月经周期使用的卫生巾血染面积进行评分,1 分为血染≤1/3面积,5 分为血染>1/3 面积,计算所有卫生巾得分为本周期月经量评分,计算3 个周期的平均月经得分。
1.4 统计学方法
采用SPSS 22.0 统计软件分析数据,计量资料以均数±标准差()表示。计量资料多组间比较采用单因素方差分析,两两比较采用SNK-q检验;计数资料以百分率(%)表示,率的比较采用χ²检验;以P<0.05为差异有统计学意义。
2 结果
2.1 子宫腺肌病患者接受HIFU治疗时间、靶区有灰度变化/无灰度变化比率和累积功率比较
3组间靶区有灰度变化/无灰度变化患者比率无明显差异(P>0.05),研究1组治疗时间较对照组及研究2 组明显缩短,累积功率较对照组及研究2 组明显下降,差异均有统计学差异(P<0.05),见表1。

表1 3组子宫腺肌病患者接受HIFU治疗时间、累积功率比较
2.2 痛经缓解情况比较
对照组、研究1组、研究2组治疗后痛经评分均较治疗前明显降低(P<0.05),但3 组间治疗前、后痛经评分比较差异无统计学差异(P>0.05),见表2。
表2 3组患者治疗前、后的痛经评分比较

表2 3组患者治疗前、后的痛经评分比较
与同组治疗前比较,aP<0.05。
2.3 治疗前后经量变化比较
3组患者接受治疗后经量均较治疗前减少(P<0.05),但3 组间治疗前、治疗后经量比较均无明显差异(P>0.05),见表3。
表3 3组患者治疗前、后的经量评分比较

表3 3组患者治疗前、后的经量评分比较
与同组治疗前比较,aP<0.05。
2.4 治疗前、后子宫体积变化比较 3 组患者经高强度聚焦超声治疗后,子宫体积均较治疗前明显缩小(P<0.05),其中研究组1、研究2组治疗后的子宫体明显小于对照组(均P<0.05),明显有效率均较对照组明显升高(P<0.05),而研究组1的明显有效率与研究组2比较无明显差异(P>0.05),见表4。
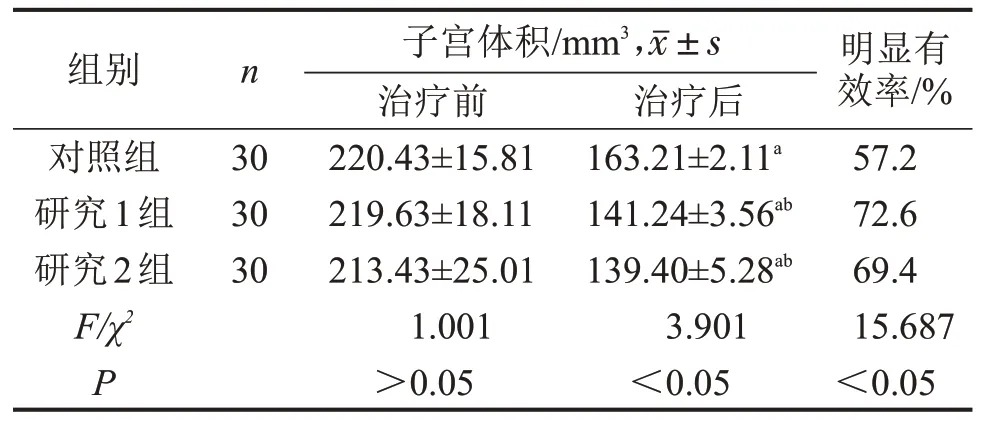
表4 3组子宫腺肌病患者治疗前、后子宫体积变化列表
2.5 典型病例
患者女,38 岁,因经痛3 年入院,B 超及MRI 提示子宫腺肌症,予GnRH-a 治疗3 次后行HIFU 治疗,患者治疗前后超声及磁共振影像学改变情况,见图1。
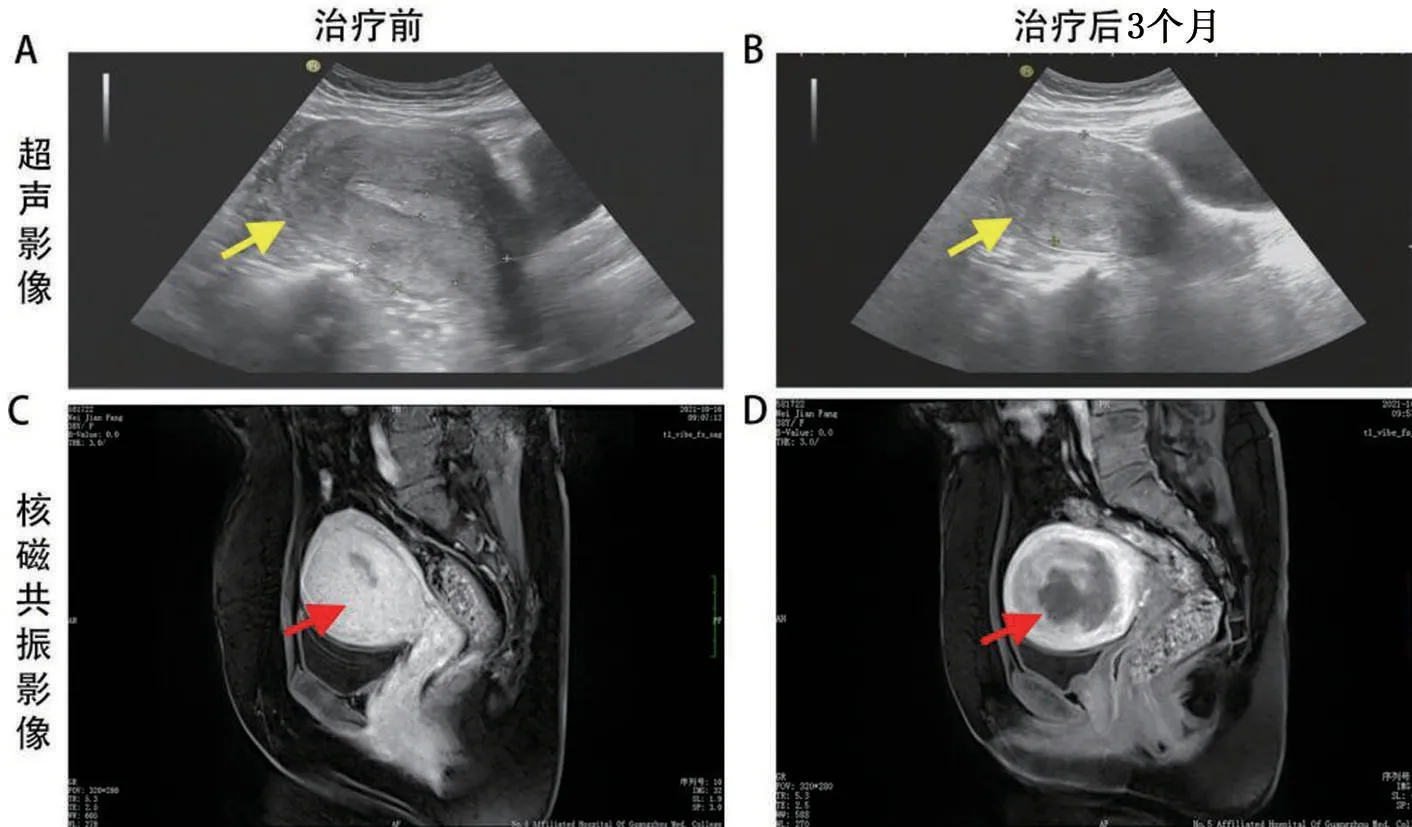
图1 患者经HIFU联合GnRH-a治疗前和治疗后3个月超声及磁共振影像学改变情况
3 讨论
根据2020年发布的“子宫腺肌病诊治中国专家共识”,子宫腺肌病的治疗策略包括药物治疗、手术治疗及介入治疗等方式。传统的保守手术方法为病灶切除,该方式对于局灶性子宫腺肌病的患者更为合适,但由于子宫腺肌病“弥漫性”分布的特点,使保守性手术治疗难以成为根治性的治疗方法。高强度聚焦超声(HIFU)利用超声波良好的组织穿透性和可聚焦性等物理特性,将体外发射的无数束低声强超声波准确聚焦于体内靶组织处,焦点声强得到数万倍放大,瞬间产生60~100 ℃高温,以及空化效应、机械效应和声化学效应等,使病灶发生凝固性坏死。HIFU 治疗子宫腺肌病是一种安全有效的治疗方式。Shui等[9]对224例HIFU治疗后的子宫腺肌病患者进行随访,结果提示HIFU 治疗后痛经及经量增多症状均明显改善,未出现明显并发症,认为HIFU 具有维持长期临床改善的能力,是一种安全有效的子宫腺肌病的治疗方法。荟萃分析结果显示,子宫腺肌病患者在结束HIFU 治疗后12 个月,痛经症状及经量仍有改善,提示HIFU治疗可使子宫腺肌病患者在结束治疗后持续获益[10]。但由于临床仍未就HIFU 消融子宫腺肌病剂量、治疗方式达成共识,故治疗疗效不一。本研究结果提示,高强度聚焦超声治疗子宫腺肌病患者,经量及VAS评分均明显下降,3个月复诊子宫体积较治疗前缩小,无一例发生治疗后并发症,表明HIFU 是治疗子宫腺肌病的安全有效的手段,经HIFU治疗后,患者痛经较前明显缓解,较大程度提高了子宫腺肌病患者的生活质量。
药物治疗可短时间内抑制子宫内膜异位灶的增长,为子宫腺肌病的治疗手段之一。有报道[11],子宫腺肌病患者在接受高强度聚焦超声治疗后联合使用GnRH-a,可增强HIFU 消融的疗效,治疗后半年随访子宫体积明显缩小,痛经程度改善,提示HIFU 消融联合GnRH-a 治疗,可明显提高临床效果。张楠等[12]在HIFU 消融子宫腺肌病后1 周内使用GnRH-a,1 年后随访结果显示,联合用药组复发率更低,症状改善优于单独使用HIFU 消融组及单独使用GnRH-a组。但由于以往国内外研究单方面侧重于在HIFU 前或HIFU 后单一时机使用GnRHa,缺乏将不同时机GnRH-a 横向比较的相关研究。本研究结果显示,单独使用HIFU 治疗、HIFU 治疗后使用GnRH-a、HIFU 治疗前使用GnRH-a 均能改善患者主观症状及缩小子宫体积。而HIFU治疗前使用GnRH-a 者,HIFU 使用功率更低,操作时间更短。
综上所述,HIFU 联合GnRH-a 治疗子宫腺肌病,疗效较好,且HIFU 治疗前接受预处理,可提高HIFU治疗效果,缩短治疗时间,一定程度上减少并发症的发生。经预处理后子宫体积减少,使HIFU治疗更具有高效性。HIFU治疗风险低、可重复、易普及,一方面可以让更多的患者得到早期治疗而免受疾病困扰;亦可以降低医疗诊治的负荷、缩短住院时间、减少输血及严重手术并发症的风险。
