高效液相色谱法测定氧化型染发产品中2-氨基-4-羟乙氨基茴香醚及其硫酸盐的含量
2022-01-19贾伯阳邬国庆
邸 铮,杨 玲,贾伯阳,杜 勇,左 雪,张 蓉,邬国庆
(北京市药品检验研究院,北京 102206)
2-氨基-4-羟乙氨基茴香醚是氧化型染发产品的常用成分,通常以硫酸盐的形式存在,结构式见图1。在染发产品的典型配方中,前体物质(如对苯二胺)被氧化剂(如过氧化氢)激活,形成有活性的亚氨基-亚胺离子前体,再与2-氨基-4-羟乙氨基茴香醚或其硫酸盐结合,形成新的化合物,进而改变头发的颜色,其中2-氨基-4-羟乙氨基茴香醚及其硫酸盐起到“偶联剂”的作用[1]。目前,2-氨基-4-羟乙氨基茴香醚及其硫酸盐在染发产品中应用广泛,是染发领域研究的热点。
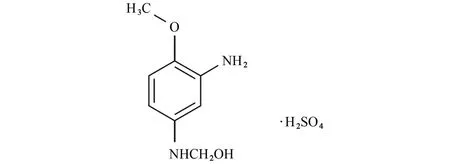
图1 2-氨基-4-羟乙氨基茴香醚硫酸盐的结构式Fig.1 Structure of 2-amino-4-hydroxyethylaminoanisole sulfate
美国食品药品监督管理局(FDA)公布的信息显示,2-氨基-4-羟乙氨基茴香醚硫酸盐在94种染发产品中的质量分数为0.008%~1.5%(稀释前最高为3%)[1];欧盟和我国《化妆品安全技术规范》(2015年版)中规定,该物质在用于氧化型染发剂时,其最大使用量为1.5%[2-3]。2-氨基-4-羟乙氨基茴香醚是一种仲胺,容易发生亚硝化反应,生成可能致癌的N-亚硝胺[1],并且有文献报道,2-氨基-4-羟乙氨基茴香醚硫酸盐是一种罕见的新型接触性过敏原[4]。因此,加强对氧化型染发产品中2-氨基-4-羟乙氨基茴香醚及其硫酸盐的监测十分必要。
测定染发产品中化合物的常见方法有高效液相色谱法(HPLC)[5-7]和液相色谱-串联质谱法[8-9],但是关于测定2-氨基-4-羟乙氨基茴香醚及其硫酸盐的报道较少,因此建立2-氨基-4-羟乙氨基茴香醚及其硫酸盐的测定方法,对于补充染发产品的监测种类具有重要意义。
2-氨基-4-羟乙氨基茴香醚及其硫酸盐在液相色谱上均以不含盐的游离态形式出峰,且具有明显的光谱吸收特征,但其水溶液的稳定性较差,在液相分析过程中,很容易随着分析时间的延长,氧化分解出大量杂质,影响定量结果的准确性。基于此,本工作通过研究不同抗氧化剂对2-氨基-4-羟乙氨基茴香醚分解速率的影响,建立了HPLC测定氧化型染发产品中2-氨基-4-羟乙氨基茴香醚及其硫酸盐含量的方法,并采用高效液相色谱-串联质谱法(HPLCMS/MS)对结果进行确证,为含此类化合物的染发产品的质量控制提供了依据。
1 试验部分
1.1 仪器与试剂
1260型高效液相色谱仪,配二极管阵列检测器;QTRAP 5500 型高效液相色谱-质谱联用仪;CP255D 型电子分析天平;KQ-500 型超声波清洗器;Milli-Q 型超纯水系统。
磷酸盐缓冲溶液:称取十二水合磷酸氢二钠3.6 g、磷酸二氢钾5.6 g,用水溶解并定容至1 L,充分混匀,用0.22μm 微孔滤膜过滤,备用。
L-半胱氨酸溶液:称取L-半胱氨酸0.25 g,用水溶解并定容至100 mL,配制成2.5 g·L-1L-半胱氨酸溶液。
提取剂:2.5 g·L-1半胱氨酸溶液与无水乙醇按体积比3∶7进行混合,备用。
2-氨基-4-羟乙氨基茴香醚标准储备溶液:称取2-氨基-4-羟乙氨基茴香醚25.31 mg,置于25 mL棕色容量瓶中,用提取剂溶解并稀释至刻度,摇匀,配制成0.992 2 g·L-12-氨基-4-羟乙氨基茴香醚标准储备溶液,于4℃保存。使用时,用提取剂稀释至所需质量浓度。
2-氨基-4-羟乙氨基茴香醚的纯度为98%;乙腈、乙酸铵为色谱纯;十二水合磷酸氢二钠、磷酸二氢钾、L(+)-抗坏血酸、L-半胱氨酸、亚硫酸氢钠均为分析纯;无水乙醇为优级纯;试验用水为超纯水。
样品均为市售氧化型染发产品,包含染发膏和氧化乳两种剂型。
1.2 仪器工作条件
1.2.1 HPLC
Waters Atlantis®T3 MV Kit色谱柱(250 mm×4.6 mm,5μm);柱温35 ℃;进样量5μL;流动相A 为含10%(体积分数,下同)乙腈的磷酸盐缓冲溶液,B 为乙腈;流量1.0 mL·min-1;检测波长304 nm。梯度洗脱程序:0~16.0 min时,A 为100%;16.0~16.1 min 时,A 由100%降 至25%,保持8.9 min;25.0~26.0 min时,A 由25%升至100%,保持14.0 min。
1.2.2 HPLC-MS/MS
1)色谱条件 Waters Atlantis®T3 色谱柱(100 mm×2.1 mm,3μm);柱温30 ℃;进样量2μL;流动相A 为10 mmol·L-1乙酸铵溶液,B为乙腈;流量0.5 mL·min-1。梯度洗脱程序:0~2.0 min时,A 为100%;2.0~8.0 min 时,A 由100%降至80%;8.0~12.0 min时,A 由80%降至5%,保持3.0 min。
2)质谱条件 电喷雾离子(ESI)源,正离子模式;离子源温度550℃;电离电压5 500 V;气帘气压力207 k Pa,碰撞气压力选择中等,雾化气压力379 k Pa,辅助气压力345 k Pa;多反应监测(MRM)模式。二级质谱参数见表1,其中“*”为定量离子。

表1 二级质谱参数Tab.1 MS/MS parameters
1.3 试验方法
称取染发膏0.5 g(精确至0.001 g)于比色管中,加入适量提取剂,涡旋30 s,超声15 min,冷却后再用提取剂定容至10 mL,充分混匀,经0.45μm微孔滤膜过滤,滤液供HPLC 分析,再用甲醇将其稀释至适当质量浓度后,采用HPLC-MS/MS进行分析确证。
2 结果与讨论
2.1 色谱行为
按照仪器工作条件对100 mg·L-12-氨基-4-羟乙氨基茴香醚标准溶液和供试品溶液分别进行测定,所得色谱图见图2。
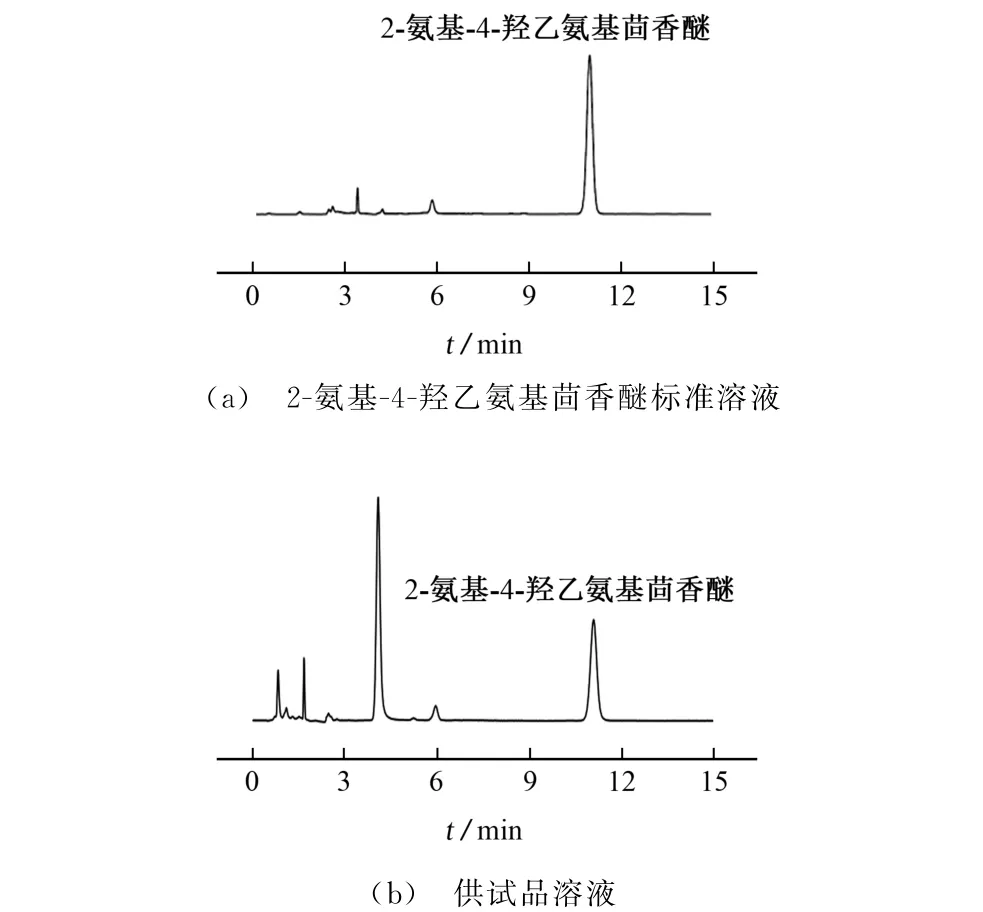
图2 色谱图Fig.2 Chromatograms
2.2 检测波长的选择
采用二极管阵列检测器,在检测波长为210~400 nm 时对100 mg·L-12-氨基-4-羟乙氨基茴香醚标准溶液进行扫描,结果见图3。
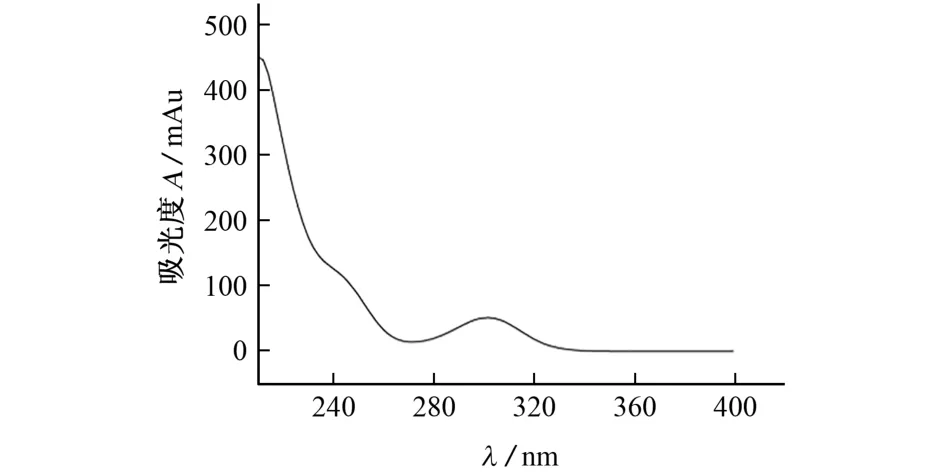
图3 2-氨基-4-羟乙氨基茴香醚的紫外吸收Fig.3 UV absorption of 2-amino-4-hydroxyethylaminoanisole
结果显示,2-氨基-4-羟乙氨基茴香醚在254,304 nm 处均有紫外吸收,考虑到大部分染发剂组分在210~280 nm 内有紫外吸收,为了避免其他杂质峰的干扰,试验选择检测波长为304 nm。
2.3 流动相的选择
在前期研究的基础上[6],参考文献[10],考察了不同流动相体系(乙腈-乙酸铵溶液、磷酸盐缓冲溶液-乙腈)对2-氨基-4-羟乙氨基茴香醚与其他30余种染发剂组分分离效果的影响。
结果显示:当以10%乙腈溶液-20 mmol·L-1乙酸铵溶液体系为流动相时,目标物与2-氨基-6-氯-4-硝基苯酚、2-硝基对苯二胺两种组分无法完全分离;增加乙酸铵溶液的比例,目标物出峰时间延长,并且2-氨基-4-羟乙氨基茴香醚的分解产物会影响对氨基苯酚和羟乙基对苯二胺两种组分的分离和定量;当以含10%乙腈的磷酸盐缓冲溶液-乙腈体系为流动相时,目标物仅与2-硝基对苯二胺无法分离。由于2-硝基对苯二胺是氧化型染发产品中的禁用成分,一般不会影响2-氨基-4-羟乙氨基茴香醚的定量,因此试验选择以含10%乙腈的磷酸盐缓冲溶液-乙腈体系为流动相,梯度洗脱程序见1.2.1节。
2.4 抗氧化剂的选择
2-氨基-4-羟乙氨基茴香醚水溶液的稳定性较差,测定时容易被氧化分解出大量杂质,影响测定结果的准确性。试验结果表明,添加抗氧化剂,可以改善2-氨基-4-羟乙氨基茴香醚的化学稳定性。常用的抗氧化剂有亚硫酸氢钠、抗坏血酸、巯基乙酸盐、半胱氨酸等,其原理都是在遇到空气时,上述抗氧化剂优先被氧化,消耗掉空气中的氧气,达到保护目标物免于被氧化的目的[11]。在100 mg·L-12-氨基-4-羟乙氨基茴香醚标准溶液中加入含有0.02 mol·L-1抗氧化剂的乙醇溶液,放置0,3,6,8,10,12,16,18,20,24 h进行测定,考察了L(+)-抗坏血酸、L-半胱氨酸、亚硫酸氢钠为抗氧化剂时对2-氨基-4-羟乙氨基茴香醚保留率(不同时段测定值占初始质量浓度的百分数)的影响。
结果表明:当不加抗氧化剂时,24 h 时目标物的保留率为92.8%;以L-半胱氨酸为抗氧化剂时,24 h时目标物的保留率为97.5%,说明L-半胱氨酸对目标物起到了保护作用;而以L(+)-抗坏血酸、亚硫酸氢钠为抗氧化剂时,8 h后目标物的保留率比不加抗氧化剂时的小,说明L(+)-抗坏血酸、亚硫酸氢钠加速了目标物的分解。这是由于L-半胱氨酸中含有活性较高的巯基,很容易与氧气发生反应[11-12],从而减缓了目标物的分解。因此,试验最终选择2.5 g·L-1(约0.02 mol·L-1)的L-半胱氨酸溶液为抗氧化剂。另外,在试验过程中发现,L-半胱氨酸被氧化后生成了不溶于乙醇的白色絮状沉淀L-胱氨酸,可能会堵塞进样系统,因此样品溶液经过滤后再进样分析。

图4 抗氧化剂对2-氨基-4-羟乙氨基茴香醚保留率的影响Fig.4 Effect of antioxidant on retention rate of 2-amino-4-hydroxyethylaminoanisole
2.5 提取剂的选择
试验考察了不同体积分数(5%,10%,30%,70%,90%)的乙醇-2.5 g·L-1L-半胱氨酸溶液的混合液为提取剂时对实际样品中2-氨基-4-羟乙氨基茴香醚测定值的影响。
结果显示:随着乙醇体积分数的增加,2-氨基-4-羟乙氨基茴香醚的测定值逐渐增大;当乙醇体积分数为70%,90%时,2-氨基-4-羟乙氨基茴香醚的测定值均较大,并且基本一致;另外,随着乙醇体积分数的增加,样品溶液的澄清度提高,过滤难度明显降低,可有效提高检测效率。因此,试验选择提取剂中乙醇的体积分数为70%。
2.6 工作曲线、检出限和测定下限
精密移取适量的2-氨基-4-羟乙氨基茴香醚标准储备溶液,用空白基质样品溶液配制成2-氨基-4-羟乙氨基茴香醚质量浓度为1.984,4.961,9.922,24.80,49.61,99.22,248.0,496.1 mg·L-1的基质匹配标准溶液系列。按照仪器工作条件对上述基质匹配标准溶液系列进行测定,以2-氨基-4-羟乙氨基茴香醚的质量浓度为横坐标,其对应的峰面积为纵坐标绘制工作曲线。结果显示,2-氨基-4-羟乙氨基茴香醚的质量浓度在1.984~496.1 mg·L-1内与其对应的峰面积呈线性关系,线性回归方程为y=3.765x+0.763 9,相关系数为0.999 9。
以3倍信噪比(S/N)计算检出限(3S/N),10倍信噪比计算测定下限(10S/N)。结果显示,2-氨基-4-羟乙氨基茴香醚的检出限为8μg·g-1,测定下限为26μg·g-1。以2-氨基-4-羟乙氨基茴香醚硫酸盐计,检出限为12μg·g-1,测定下限为40μg·g-1。
2.7 稳定性试验
按照仪器工作条件对4.961,99.22 mg·L-1基质匹配标准溶液分别于0,4,8,12,16,20,24 h时进行测定,计算峰面积的相对标准偏差(RSD)。
结果表明,4.961,99.22 mg·L-1基质匹配标准溶液在24 h内峰面积的RSD(n=7)分别为0.83%和0.62%,表明该方法稳定性良好。
2.8 精密度和回收试验
取6份空白基质供试品各0.5 g,分别加入质量浓度为1.5 mg·L-1的2-氨基-4-羟乙氨基茴香醚标准溶液1 mL,按照试验方法进行测定。结果显示,回收率为95.5%,测定值的RSD 为1.9%,说明在测定下限附近的加标回收率及精密度良好。
取18份2-氨基-4-羟乙氨基茴香醚质量分数为0.23%的供试品各0.2 g(精确至0.001 g),分别加入质量浓度为0.992 2 g·L-1的2-氨基-4-羟乙氨基茴香醚标准储备溶液0.4,0.5,0.6 mL,每个浓度水平平行制备6份溶液,按照试验方法进行测定,计算回收率和测定值的RSD,结果见表2。
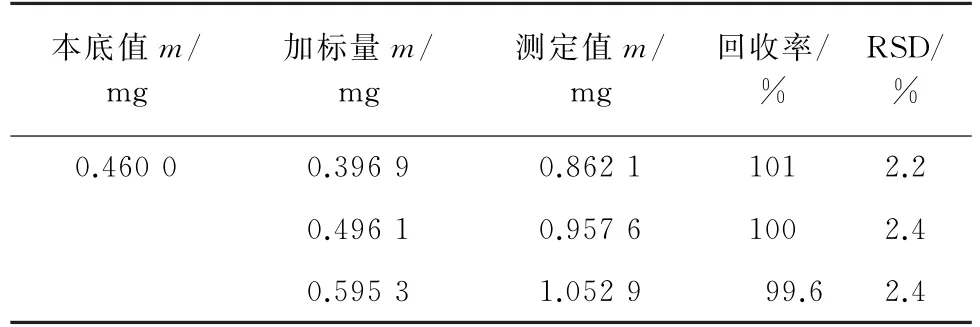
表2 回收试验结果(n=6)Tab.2 Results of test for recovery(n=6)
结果显示,回收率为99.6%~101%,测定值的RSD 为2.2%~2.4%,表明该方法的回收率和精密度较好。
2.9 HPLC-MS/MS的定性确证
为保证测定结果的准确性,试验采用HPLCMS/MS对样品进行进一步确认。目标化合物在电喷雾正离子源(ESI+)电离方式下可以获得响应值较高的母离子;在优化的二级质谱条件下,可生成m/z138.0,95.2,123.1等3个响应值较高的子离子,选择信号响应最强的m/z138.0 为定量离子。在1.2.2节确证条件下,若供试品中出现m/z183.0>138.0和m/z183.0>95.2两组离子对,且离子对间的相对丰度比在允许偏差±20%以内时,可以确认供试品中含有2-氨基-4-羟乙氨基茴香醚(硫酸盐)。按照1.2.2节对100 mg·L-12-氨基-4-羟乙氨基茴香醚标准溶液和供试品溶液进行测定,所得MRM 色谱图见图5。
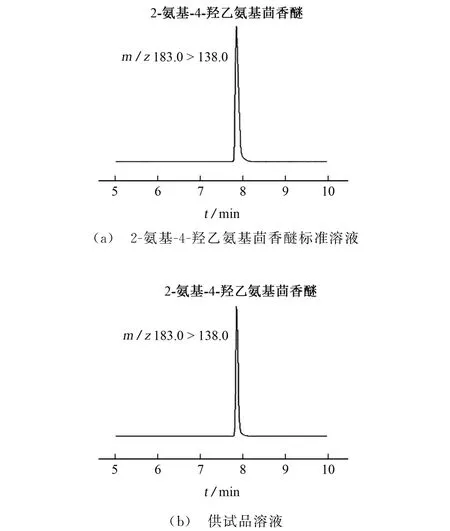
图5 MRM 色谱图Fig.5 MRM chromatograms
2.10 样品分析
按照试验方法对7个标签或产品配方中标示有2-氨基-4-羟乙氨基茴香醚硫酸盐的氧化型染发产品进行测定(以2-氨基-4-羟乙氨基茴香醚硫酸盐计),结果见表3。
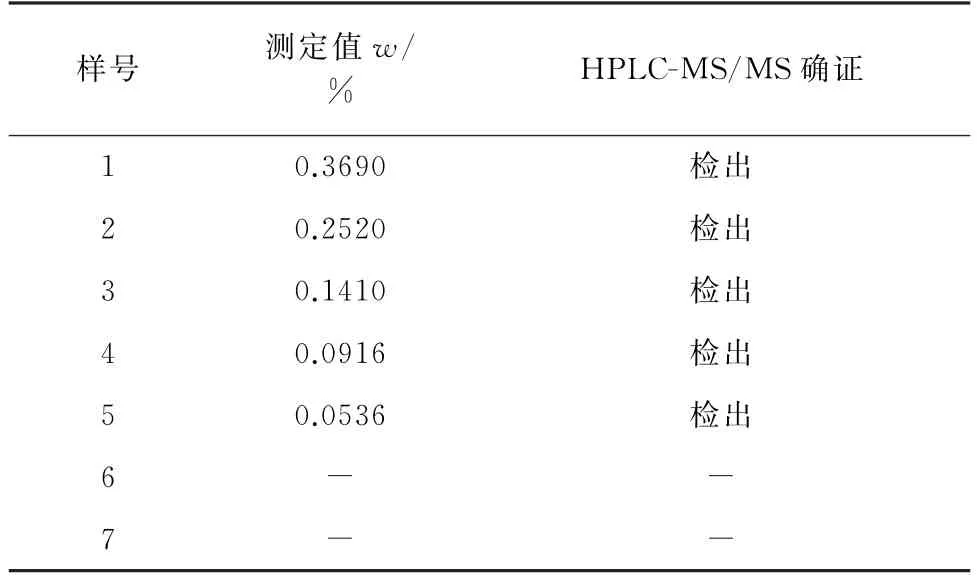
表3 样品分析结果Tab.3 Analytical results of samples
结果显示:HPLC 与HPLC-MS/MS的分析结果一致;5个产品中检出2-氨基-4-羟乙氨基茴香醚硫酸盐,检出量为0.053 6%~0.369 0%,而其余2个产品中未检出2-氨基-4-羟乙氨基茴香醚硫酸盐,与标示内容不相符。
在氧化型染发产品的安全监测中,除了要控制各成分含量在限值范围内,还要确定实际检出成分与产品配方及包装标示内容是否一致。本工作通过优化检测波长、流动相、抗氧化剂、提取剂等条件,建立了HPLC测定氧化型染发产品中2-氨基-4-羟乙氨基茴香醚及其硫酸盐含量的方法,并通过HPLCMS/MS对结果进行确证。该方法简单快速、准确度高、专属性强,为氧化型染发产品的质量监控提供了技术支持。
