磁性纳米颗粒的产热机制及在肿瘤热疗中的应用
2022-01-18解丽芹左喜瑞陈红丽张其清
解丽芹 左喜瑞 张 楠 陈红丽 张其清
1(新乡医学院生命科学技术学院,河南新乡 453003)
2(中国医学科学院生物医学工程研究所,天津 300192)
引言
磁感应热疗是Gilchrist 在1957年提出的[1],在对磁性材料产热破坏狗的淋巴癌组织进行研究的基础上,证明了磁性材料可以靶向性地移动并集聚到肿瘤组织,在交变磁场的作用下产热破坏肿瘤组织。磁感应热疗是利用肿瘤细胞与正常细胞对温度的耐受力不同,在肿瘤组织中引入磁性纳米颗粒,通过交变磁场的作用使磁纳米颗粒发生磁滞、弛豫现象而产热,造成组织区域内的温度升高[2-3]。当温度超过43℃时,对肿瘤细胞造成伤害,肿瘤细胞发生坏死或损伤,而正常细胞并不受到影响,以此达到杀死肿瘤细胞而不影响正常细胞的目的[4]。与传统的热疗方法相比,磁热疗的方法具有穿透深层组织、加热均匀、定位准确的特点,可以用于治疗深部肿瘤,并且对非肿瘤细胞的损伤比较小,安全性也更高。文中主要综述超顺磁性纳米颗粒在交变磁场中的产热机制、与细胞的作用机理、以及在肿瘤治疗中的应用。
1 磁性纳米颗粒产热的物理学机制
磁性材料的产热机制主要有涡流、磁滞和弛豫等3 种。涡流是磁性材料处于交变磁场中时,其磁通量和磁感应强度发生变化引起的环形感应电流。磁性材料在交变磁场中涡流效应产热的现象不够明显,通常发挥作用的是磁滞发热和弛豫发热[5]。
磁性纳米颗粒置于外加直流磁场中,磁化强度随着磁场强度的增加而增大(初始磁化曲线Oa),如图1(a)[6]。当磁场强度增大至Hs时,磁化强度增长趋于平缓至饱和,称为饱和磁化强度(Bs)。降低磁场强度至零并反方向增强时,磁化强度也在降为零后反方向增强(曲线abc′a′)。如此反复,磁性纳米颗粒的磁化曲线在磁场方向逆转过程中形成一个闭合的环(abc′a′b′c′a),即磁滞回线(直流磁滞回线或静态磁滞回线)。磁性物质磁矩的变化总是比磁场的变化慢,由此产生了磁滞(Br)和矫顽力(Hc),原子磁矩与晶格的耦合引起的磁滞损耗在磁化方向反转过程中转化为热能。由此可见,磁滞产热的效率正比于直流磁滞回线的面积,与材料的3个参数有关:饱和磁化强度Bs、剩磁Br和矫顽力[7]。当磁性纳米颗粒置于逐渐变大的交流磁场中,其呈现为一环套一环、面积逐渐增大的磁滞回线(交流磁滞回线或动态磁滞回线,如图1(b)),磁滞回线面积与交变磁场频率、温度等因素有关[8-10]。处于交流磁场的纳米颗粒的产热效率,不仅与磁滞回线面积有关,还与涡流产热和剩余损耗有关。磁性纳米颗粒的磁滞产热,主要取决于其本征特性,例如磁晶各向异性、磁致伸缩、内外应力、夹杂的体积分数、饱和磁化强度、几何形状等[11]。
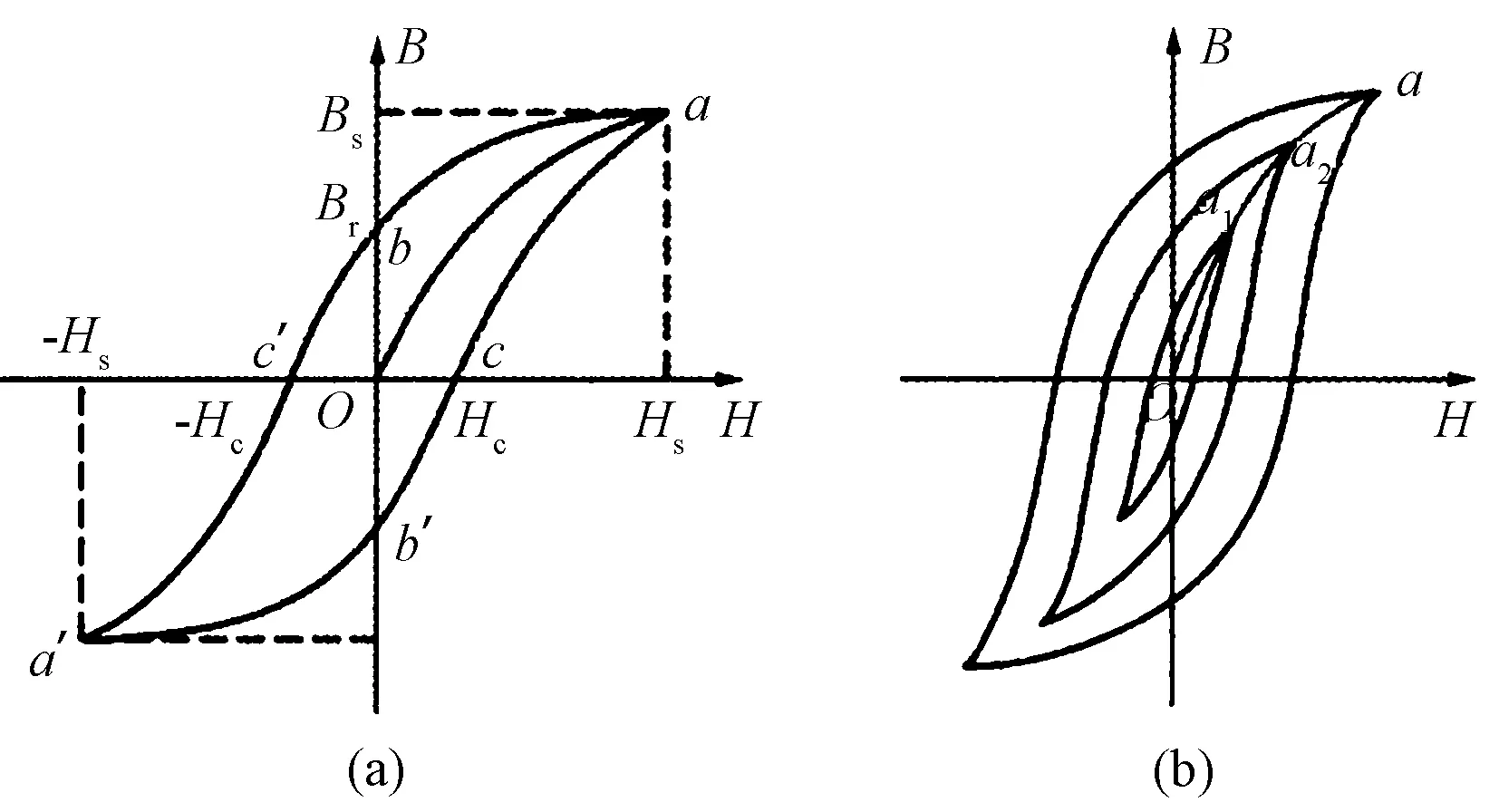
图1 磁性纳米颗粒的磁滞回线。(a)在直流磁场中[6];(b)在交流磁场中[10]Fig.1 Hysteresis loops of magnetic nanoparticles.(a) In a direct current magnetic field[6];(b) In an alternating current magnetic field[10]
磁性纳米颗粒的尺寸减小到某一数值时(粒径小于20 nm),其磁化曲线重合,没有剩磁和矫顽力,表现出超顺磁性(见图2(a))[12]。超顺磁性纳米颗粒的产热主要来自弛豫产热。弛豫产热主要是由于磁性物质的内耗产生的,有尼尔弛豫和布朗弛豫两种类型(见图2(b))[13]。尼尔弛豫是由于磁场方向的变化,导致磁性纳米颗粒的磁矩方向随之改变,但颗粒本身不转动。磁矩的改变需要充足的热能来克服磁晶各向异性能垒,即尼尔弛豫产热。布朗弛豫是磁性纳米颗粒在交变磁场作用下颗粒发生旋转,旋转中摩擦阻力产生的机械能以热能形式耗散,颗粒的磁矩固定在晶体轴上保持不变[14]。超顺磁性纳米颗粒是单畴颗粒集合体,产热机制以尼尔弛豫为主。Rovers 等[15]研究了12 nm 超顺磁性氧化铁纳米颗粒的尼尔弛豫和布朗弛豫,将其分散于水溶液或固定于聚甲基丙烯酸甲酯基质(限制其布朗运动)中,在3 种磁场强度(2 010、2 440、2 850 A/m)下,氧化铁纳米颗粒在两种介质中对应的比吸收率(specific absorption rates,SAR)相一致。据此得出结论,无论在低粘度介质或高粘度介质中,尼尔弛豫是主要产热机制。Jeun 等[16]用软磁Fe3O4和硬磁CoFe2O4证实,布朗弛豫强依赖于介质粘度,且粘度达到4×10-3Pa∙s(近似于细胞质或胞内环境的粘度)时,布朗弛豫严重衰减。而尼尔弛豫不受分散介质粘度的影响,且主导细胞内总产热比,因此肿瘤细胞的磁热疗应侧重于加强磁流体的尼尔弛豫。Deissler 等[17]和Dieckhoff 等[18]也通过实验证明,固定磁性纳米颗粒后只检测到尼尔弛豫,其弛豫时间与磁场强度有关。王煦漫等[19]也发现,油酸溶液中Fe3O4的SAR 与浓度无关,在不同粘度的分散介质(辛烷、甲苯、苯、苯乙烯、油酸)中Fe3O4的SAR 也相差无几,再次证明了超顺磁性纳米颗粒的产热机制主要是尼尔弛豫,SAR 正比于磁场强度的平方。无论是尼尔弛豫还是布朗弛豫,比产热率都依赖于磁性纳米颗粒的尺寸、形貌、组成等[16,20-21]。因此,研究者通过优化磁性材料的尺寸、形貌、组分和表面修饰等提高磁热性能[22]。
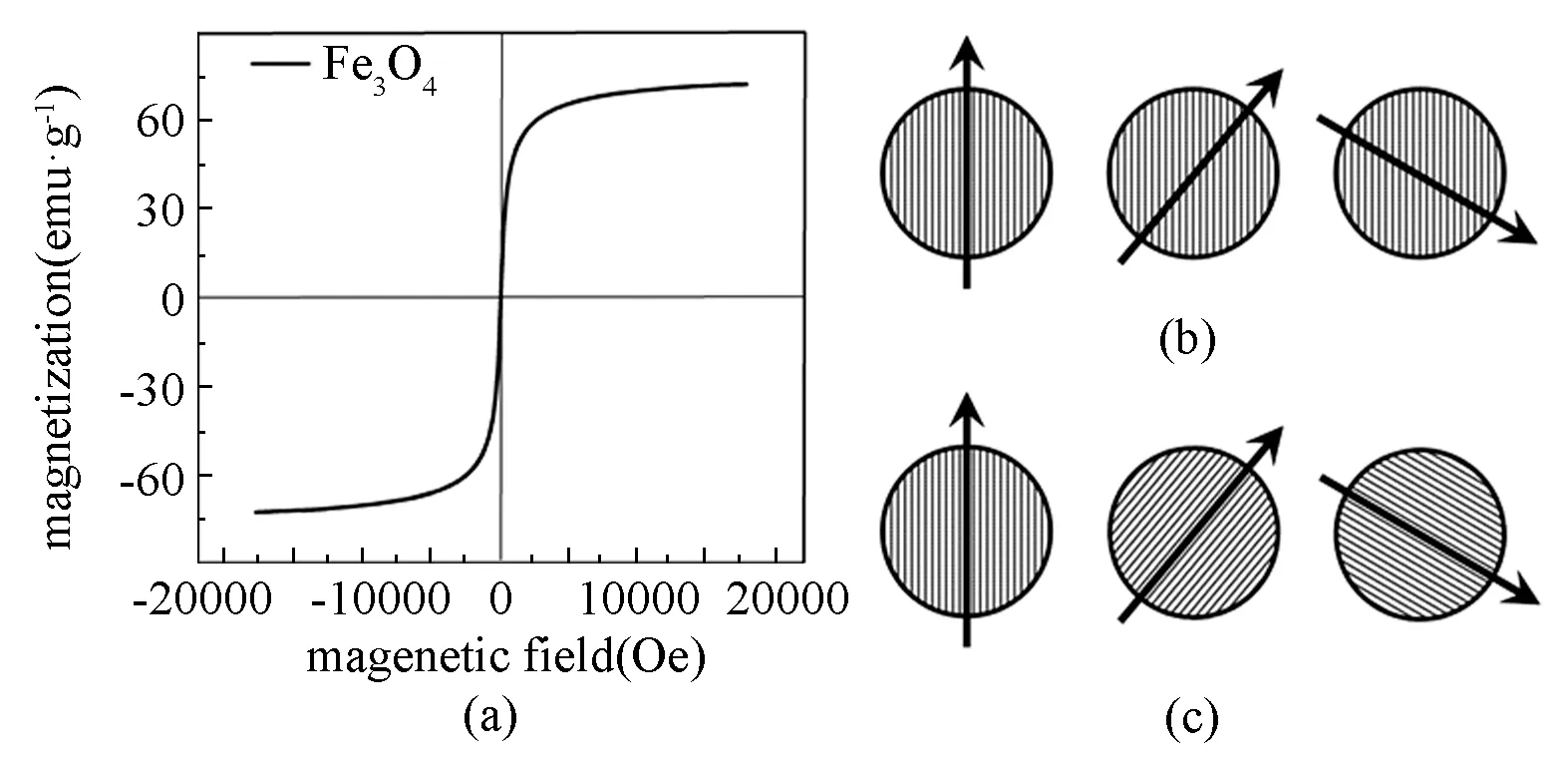
图2 超顺磁性纳米颗粒在外磁场下的磁化。(a)超顺磁性纳米颗粒的磁滞回线[12];(b) 尼尔弛豫[13];(c)布朗弛豫[13]Fig.2 Magnetization of superparamagnetic nanoparticles in an applied magnetic field.(a)Hysteresis loop of superparamagnetic nanoparticles[12];(b) Neel relaxation[13];(c)Brownian relaxation[13]
2 磁性纳米颗粒产热的影响因素
磁性纳米材料在交变磁场下通过磁滞或弛豫产热,产生的热量被广泛应用于肿瘤治疗或协同治疗。特别是超顺磁性材料,因为没有剩磁和矫顽力,被广泛用于肿瘤诊断和治疗[23]。提高磁性纳米材料的产热效率,赋予材料特定的结构和功能,是提高肿瘤治疗效果的基础[24]。
尺寸是影响磁性材料产热效率的首要因素。Bakoglidis 等[25]研究粒径对磁性纳米颗粒产热机制,结果发现,小于10 nm 的超顺磁性纳米颗粒,主要为尼尔弛豫升温;10~13 nm 的超顺磁-铁磁性过渡区的纳米颗粒和大于13 nm 的铁磁性纳米颗粒,主要为磁滞损耗产热。比损耗功率(specific loss power,SLP)结果表明,大粒径、高浓度的磁性纳米颗粒产热效率更高。韩栋等[26]采用多醇热解法制备了平均粒径分别为8.7、12.6、15.3 nm 的超顺磁性氧化铁纳米颗粒,磁饱和强度分别为31.4、50.3、60.6 A∙m2/kg。在交变磁场(425 kHz、5.3 kA/m)中,480 s 内,同一粒径的纳米颗粒水分散液升温速率随浓度的增大而增大,相同浓度(2 mg/ mL)的纳米颗粒水分散液温度随粒径的增大而增大。Nemati等[27]也比较了200 nm×25 nm 和12 nm×3 nm 磁盘的SLP,发现大粒径磁盘的加热效率远大于小粒径磁盘的加热效率,近似体积的磁性材料,盘状纳米颗粒的SLP 高于球状纳米颗粒的SLP。Lee 等[21]实验得出,9、12、15 nm 的Fe3O4纳米颗粒的SLP 分别为152、349、333 W/g;若组成为MnFe2O4(15 nm)或CoFe2O4(9 nm),SLP 分别为411 和443 W/g;通过交换耦合调节磁晶各向异性常数,具有核壳结构的CoFe2O4@ MnFe2O4、CoFe2O4@ Fe3O4、MnFe2O4@CoFe2O4、Fe3O4@ CoFe2O4等纳米颗粒的SLP 是单组分纳米颗粒SLP 的数倍或几十倍(见图3)。Kumar 等[28]总结为单畴单分散的Fe3O4纳米颗粒具有最大SLP 的尺寸在14~16 nm。由此可见,磁性纳米材料的产热能力依赖于尺寸,但是,形貌、组成等因素也极大地影响着材料的磁热性能。

图3 磁性纳米颗粒的SLP 对比[21]。(a)核壳结构的CoFe2O4@MnFe2O4(15 nm)与单组分CoFe2O4(9 nm)和MnFe2O4(15 nm)的SLP 对比;(b)单组分磁性纳米颗粒的SLP 对比;(c)核壳结构磁性纳米颗粒的SLP对比Fig.3 SLP comparison of magnetic nanoparticles[21].(a) SLP comparison of core-shell structured nanoparticles CoFe2O4@MnFe2O4(15 nm) and single-component nanoparticles CoFe2O4(9 nm) or MnFe2O4(15 nm);(b) SLP comparison of single-component magnetic nanoparticles;(c) SLP comparison of core-shell structured magnetic nanoparticles
形貌、组分、单分散性和表面修饰等均会影响磁性纳米颗粒的物理化学性质。Pradhan 等[29]对比了Fe3O4、MnFe2O4和CoFe2O4的产热能力,CoFe2O4的SAR 相对较低,Fe3O4和MnFe2O4可以优化尺寸达到最大SAR,但是CoFe2O4的磁晶各向异性能垒太高,即使优化尺寸也难以提高其SAR。Corato等[30]发现不同尺寸、组分、形貌的磁性纳米颗粒在细胞膜或细胞内的SLP,相对于水溶液中的SLP 严重衰减,如图4所示。对于单分散超顺磁性材料(γ-Fe2O3,Au-γ-Fe2O3)来说,尼尔弛豫是产热主导因素,在细胞膜和细胞内SLP 的下降只能通过缩短尼尔弛豫时间来调节;对于聚集态的超顺磁性材料,由于分子间的相互作用致使弛豫时间缩短,所以水溶液中其SLP 较单分散的纳米颗粒偏大;铁磁性材料(CoFe2O4)以布朗弛豫为主,所以CoFe2O4在细胞膜和细胞内的SLP 急剧衰减。由此可见,单纯通过调整磁晶各向异性常数和缩短弛豫时间来增强磁性纳米颗粒的产热能力,并不一定能提高细胞内的热疗效果。采用超顺磁性纳米颗粒[31],并将其进行表面修饰使之靶向于细胞膜表面,提高纳米颗粒在细胞表面的浓度,减小其与细胞直接的相互作用或许是提高肿瘤磁热疗的途径之一[32]。

图4 磁性纳米颗粒在水溶液(黑色)、细胞膜(棕红色)、细胞内(红色)的产热能力[30]。(A:γ-Fe2O3,10 nm;B:脂质体包裹的γ-Fe2O3,γ-Fe2O3 的粒径为10 nm;C:CoFe2O4,9.2 nm;D:Au-γ-Fe2O3 二聚体,14 nm;E:γ-Fe2O3 纳米立方体,18 nm;F:γ-Fe2O3 纳米花,22 nm)Fig.4 Heat-generating capacity of magnetic nanoparticles in water solutions,membranes,or cellular conditions[30](A:γ-Fe2O3,10 nm;B:γ-Fe2O3 in liposomes,diameter of γ-Fe2O3 is 10 nm;C:CoFe2O4,9.2 nm;D:Au-γ-Fe2O3 dimers,14 nm;E:γ-Fe2O3 nanocubes,18 nm;F;γ-Fe2O3 nanoflowers,22 nm)
采用表面修饰增强靶向性(见图5),等同于增加了病变组织的超顺磁性纳米颗粒浓度,提高病变组织的升温速率[33]。丁琪[34]构建了核壳型Fe3O4@Ag 和异聚体型Fe3O4-Ag 复合纳米颗粒,显著降低了纳米银的毒性,且二者有磁热和纳米银抗癌活性的协同作用,抑制肿瘤的生长。Albarqi 等[35]开发了掺杂钴和锰的六维氧化铁纳米颗粒,并将其封装在聚乙二醇-聚己内酯纳米载体中形成团簇。经静脉注射,团簇体可有效聚集在卵巢癌细胞中,且在安全可耐受的交变磁场中将瘤内温度提高至44℃,克服了目前磁热疗只能瘤内注射的局部治疗缺陷。赵印敏等[36]将靶向血管新生肽的RGD10 偶联至磁性纳米颗粒,局部热疗显示抑瘤率为54.8%。苏展[37]也将CD44 抗体偶联至磁性纳米颗粒,靶向肿瘤干细胞并在热疗作用下使其程序性死亡。Sadhukha 等[38]设计合成靶向表皮生长因子受体的可吸入磁性纳米颗粒,用于肺癌磁热疗。Ling等[39]综述了超小磁性纳米颗粒的合成和应用,比较了制备方法、粒径、形貌、自组装、表面修饰等因素对纳米颗粒性能的影响,粒径可控、形状规整、单分散、生物相容性好,是医学诊疗学对磁性纳米颗粒的要求和挑战。Li 等[40]详细讨论了基于聚合物的磁性纳米颗粒自组装体在医学诊疗中的应用。磁性纳米材料的磁学性能的优化、多功能的协同作用、生物相容性和靶向性的提高,仍是临床应用潜在的需求。
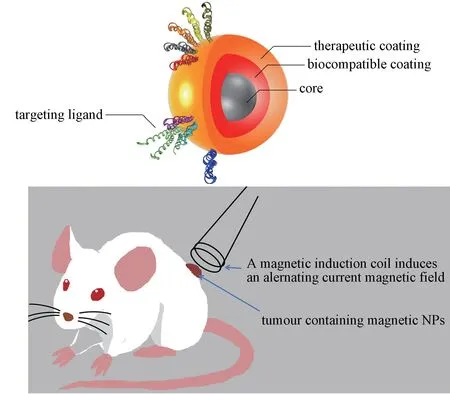
图5 表面修饰的磁性纳米颗粒及其在肿瘤中的磁热疗[33]Fig.5 Magnetic nanoparticles′surface modification and their application in tumor thermotherapy[33]
3 磁热的生物学效应
肿瘤组织内部的血管细、杂乱、容易扭曲扩张,并且血管壁薄、血流量少、血流阻力大、血管脆弱、容易破损。相比于正常组织来说,在温度升高的时候不能及时的将热量散发出去,导致热量聚集,温度升高比较快,并且容易引起磁滞留,使得肿瘤区域的温度高于其他区域温度。肿瘤细胞在高温下会发生一系列的变化,例如蛋白质变性导致细胞结构发生变化、核酸分子遭到破坏、免疫系统对肿瘤细胞杀伤力的增强等[41],使肿瘤细胞遭受损伤,进而导致其死亡。
3.1 磁热疗导致蛋白质变性
当肿瘤组织的温度达到43℃以上时,由于肿瘤组织对于温度的耐受力不强,导致肿瘤细胞的细胞膜结构发生变化,功能受到影响。细胞膜由磷脂双分子层构成,具有结构上的流动性和功能上的选择透过性。磁热疗使质膜蛋白发生变化,进而使细胞膜的通透性增强,流动性加快。若温度进一步升高,则会导致细胞膜表面的蛋白质脱落,细胞膜跨膜运输物质的功能丧失,最终引起细胞膜的永久性破损[42]。Sanz 等[43]研究了神经母细胞瘤细胞SHSY5Y 在高温水浴和交变磁场下的形态变化,如图6所示。在46℃水浴中,细胞器(线粒体和内质网)已完全空泡化,细胞膜有明显破裂;52℃时,细胞器坏死更加严重,细胞表面粗糙且塌陷明显(见图6(a))。在46℃交变磁场中,细胞有明显的凋亡,但是细胞核和细胞膜却完整无损(见图6(b))。通过实验对比得知,磁热疗在较低的温度下产生相同的细胞死亡率,这归因于附着于细胞膜的纳米颗粒产热,引起细胞膜的快速渗透和破坏而导致细胞凋亡。对比高温水浴和磁热处理小胶质瘤细胞BV2,验证了由磁热引起的细胞膜结构的破坏导致了细胞的死亡[44]。

图6 神经母细胞瘤细胞SH-SY5Y 的形态变化[43]。(a)SH-SY5Y 细胞在水浴中加热30 min 后的电镜图:对照组细胞结构的透射电镜图(A),46℃和52℃水浴中细胞结构的TEM(B,C),52℃水浴中单个细胞的扫描电镜图(SEM)(D,E,F);(b)SH-SY5Y 细胞在磁场中加热30 min 后的电镜图:对照组细胞结构的TEM(A),46℃和52℃磁场中细胞结构的TEM(B,C),52℃磁场中单个细胞的SEM(D,E,F)Fig.6 Morphological changes of human neuroblastoma SH-SY5Y cells[43].(a) Photographs of cells SH-SY5Y after heating in water bath for 30 min:Transmission electron microscopy (TEM) of the control cells (A);TEM of the cells in water bath 46℃ or 52℃ (B and C);Scanning electron microscope (SEM) of the cells in water bath 52℃(D,E,F);(b) Photographs of cells SH-SY5Y after heating under the alternating magnetic field (AMF)for 30 min:TEM of the control cells (A);TEM of the cells under the AMF at 46℃or 52℃(B and C);SEM of the cells under the AMF at 52℃(D,E,F)
磁热不仅破坏细胞膜的结构,进入到细胞内部的磁性纳米颗粒可导致细胞骨架的破坏。细胞骨架在细胞中起着支持细胞结构,形成稳定的细胞内空间。当温度升高,细胞膜出现空泡化,加速磁性纳米颗粒渗透到细胞内部,细胞膜及细胞质均有磁性纳米颗粒的聚集[44]。在磁场作用下,细胞骨架发生坍塌,细胞器等细胞内容物随之发生变化,影响细胞的正常生命活动。Prasad 等[45]将磁性纳米颗粒与细胞共孵育,在43℃磁场中作用30 min 后,细胞膜出现空泡化(见图7(a)中MF0)。将磁热疗后的细胞继续孵育0、4、8、12、24 h,荧光标记的微管蛋白和肌动蛋白骨架逐渐消失,由此也得出微管蛋白和肌动蛋白骨架的破坏导致了细胞的死亡。

图7 微管蛋白(a)和肌动蛋白(b)的荧光显影[45](微管:红色,肌动蛋白:绿色,细胞核:蓝色,标尺:1 μm)(C24:无磁性纳米颗粒,无磁场,孵育24 h;F24:无磁性纳米颗粒,磁场中作用30 min 后孵育24 h;M24:有磁性纳米颗粒,无磁场,孵育24 h;MF0:有磁性纳米颗粒,磁场中作用30 min;MF4:有磁性纳米颗粒,磁场中作用30 min 后孵育4 h;MF8:有磁性纳米颗粒,磁场中作用30 min 后孵育8 h;MF12:有磁性纳米颗粒,磁场中作用30 min 后孵育12 h;MF24:有磁性纳米颗粒,磁场中作用30 min 后孵育24 h)Fig.7 Fluorescence images of microtubules (a) and actin (b)[45] (Microtubules:red,actin:green,nucleus:blue,bar:1 μm) (C24:cells without AMF and without magnetic particles incubated for 24 h;F24:cells with AMF for 30 min but no particles incubated for 24 h;M24:cells with particles but without AMF incubated for 24 h;MF0:cells with particles and AMF for 30 min and immediately fixed;MF4:cells with particles and AMF for 30 min and incubated for 4 h;MF8:cells with particles and AMF for 30 min and incubated for 8 h;MF12:cells with particles and AMF for 30 min and incubated for 12 h;MF24:cells with particles and AMF for 30 min and incubated for 24 h)
3.2 磁热疗导致核酸分子损伤
脱氧核糖核酸(deoxyribo nucleic acid,DNA)作为细胞内的遗传物质,起到调控细胞生命活动的作用。当肿瘤细胞内温度升高时,会影响DNA 和核糖核酸(ribonucleic acid,RNA)的合成,DNA 的复制、转录和翻译等过程,细胞的生命活动也会随之受到影响。Hilger 等[46]将人乳腺癌细胞MX-1 和人成纤维细胞HTB-125 暴露在45℃~90℃的温度下4 min,经碱性单细胞凝胶电泳测定双链和单链DNA断裂比,结果表明随着磁热温度的升高,DNA 破损程度也随之加强。小鼠肿瘤模型实验得出,肿瘤细胞DNA 在55℃~60℃的断裂是不可修复的,在此阈值温度可消除肿瘤细胞。徐云钊等[47]研究了磁性顺铂微球对卵巢癌细胞skov-3 增殖、侵袭的抑制作用,得出细胞凋亡与基质金属蛋白酶2、CD44v6mRNA 的表达降低有关。顺铂用于癌症治疗,是因为与细胞内DNA 形成的加合物抑制了DNA 的转录和复制,导致细胞的坏死或凋亡。Petryk 等[48]也将顺铂和磁热共同作用于鼠乳腺癌细胞,联合治疗的效果是顺铂单独治疗的1.4 倍,是单独磁热疗的1.7 倍。
DNA 的损伤和修复过程会生成特定的生物标志物,通过检测生物标志物活性用以探究肿瘤磁热疗的作用机制[49]。M1dG 和8-oxodG 加合物是氧化应激和脂质过氧化的生物标志物,Cellai 等[50]通过检测其浓度来探究DNA 氧化损伤在肿瘤磁热疗中的作用机制,如图8所示。实验结果表明,DNA 氧化损伤有剂量依赖性,在Fe3O4纳米颗粒为60 μg/mL 时趋于平缓;暴露于交变磁场造成的DNA 氧化损伤量是未受磁热作用的20 倍,说明磁热引起的氧化应激损伤是肿瘤治疗的有效手段。Yang 等[51]以羟基磷灰石修饰磁性纳米颗粒提高其生物相容性,将其与肝癌细胞HepG2 共孵育,置于交变磁场30 min,细胞致死率达50%,乳酸脱氢酶浓度是对照组的3 倍。另外,p38 MAPK 的MKK3/MKK6 和ATF-2 受到抑制,导致ATM 和GADD45(DNA 损伤修复基因)下调。以上充分说明磁热增强了胞内活性氧水平,进而造成DNA 损伤且不易修复,最终导致癌细胞的死亡。

图8 磁热诱导的DNA 氧化应激损伤机制示意图[50]Fig.8 Potential mechanisms underlying the genotoxic effects caused by magnetic hyperthermia[50]
3.3 磁热疗导致免疫系统发生变化
热疗不仅可以直接杀死肿瘤细胞,还可以激活免疫细胞的免疫功能,其中包括抗原提呈细胞(antigen-presenting cell,APC)、T 细胞和自然杀伤细胞(natural killer cell,NK 细胞)等,以此增强免疫系统对于肿瘤的杀伤力。APC 的主要功能为摄取、加工和处理肿瘤抗原,随后提呈给T 淋巴细胞,使其对肿瘤细胞产生特异性免疫应答。Kobayashi等[52]综述了磁热疗引起的免疫原性细胞死亡的过程,如图9所示。磁热疗后,肿瘤细胞的坏死、凋亡和自噬过程会释放损伤相关的分子,即肿瘤相关抗原物质。这些物质可以在肿瘤部位招募单核细胞、巨噬细胞和树突状细胞(dendritic cell,DC)等免疫细胞,启动机体适应性免疫反应,进而杀死或清除肿瘤细胞,发挥抗肿瘤免疫效应。常见的损伤相关的分子有内质网蛋白、热休克蛋白(heat shock protein,HSP)、高迁移率族蛋白B1、终级降解产物(如三磷酸腺苷、DNA、RNA、尿酸等)、S100 蛋白和鞘氨醇等。
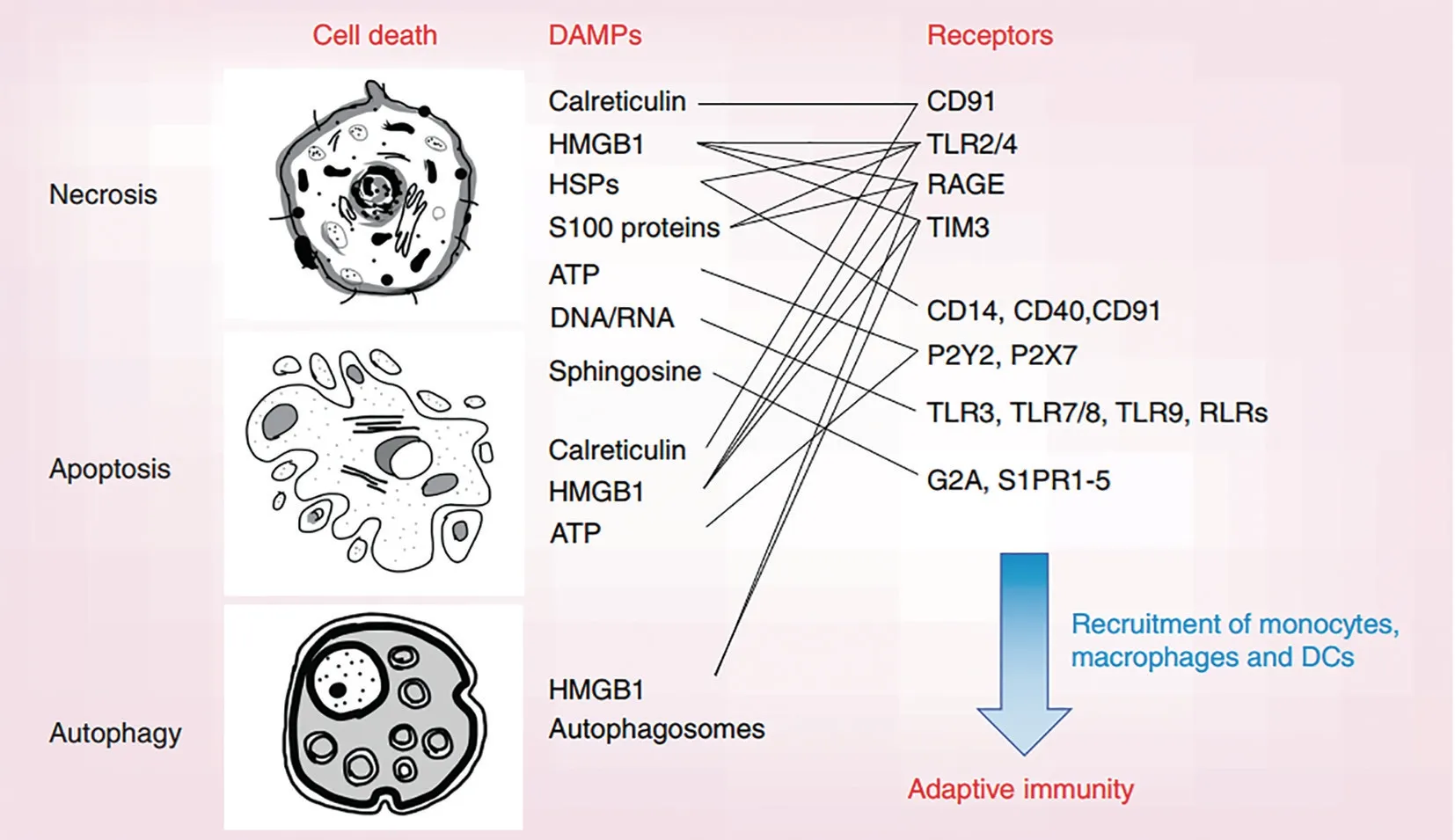
图9 免疫原性细胞死亡:将死细胞中释放的与损伤相关的分子模式可招募免疫细胞并诱导抗肿瘤免疫[52]Fig.9 Immunogenic cell death:damage-associated molecular patterns released from various forms of dying cells recruit immune cells and induce antitumor immunity[52]
HSP 在肿瘤细胞热疗过程中高表达,进而激活DC 达到抗肿瘤免疫反应[53-54]。然而,人脑膜瘤的磁热疗鲜有报道。王锐[55]结合氧化铁的磁热疗(42.5℃,30 min)和热休克RNA-1 反义转染基因治疗以抑制人脑膜瘤细胞热休克因子1 的蛋白活性,阻断HSP27、HSP70 和HSP90 的诱导表达,提高人脑膜瘤细胞热敏感性,达到抑制肿瘤细胞增殖和诱导细胞凋亡的治疗效果。黄芳玲[56]将非甲基化CpG 基序的寡聚脱氧核糖核苷酸与机体细胞内质网膜上的Toll 样受体9 作用,活化APC,促进DC 成熟,进而活化CD4+T 或CD8+T 细胞,或活化NK 细胞等,协同磁热疗,增强抗肿瘤细胞免疫。李凤武[57]将人表皮生长因子受体2(human epidermal growth factor receptor-2,HER2)核酸适配体修饰到铁纳米颗粒上,靶向攻击HER2 阳性乳腺癌细胞,以此提高其热疗效果。欧阳伟炜[58]也将甲氨蝶吟共价结合到多聚乙烯亚胺修饰的磁性纳米颗粒Fe3O4表面,联合磁热疗和化疗研究其对免疫功能的影响。经外周血检测,联合治疗组中γ-干扰素、白细胞介素-2(interleukin-2,IL-2)、IL-4 均有高表达,说明磁热疗和化疗不仅激活了机体细胞免疫功能,也激活了体液免疫功能。
磁热疗引发的免疫反应,不仅可以消除肿瘤,还可以防止肿瘤的转移和复发。Chao 等[59]将铁纳米颗粒局部注射到肿瘤,同时,聚乙二醇/多巴胺修饰的铁纳米颗粒静脉注射并聚集于肿瘤组织,在低功率磁热疗下将肿瘤消融。局部的磁热疗与系统给药的检查点阻断抗体(细胞毒性T 淋巴细胞抗原4 单克隆抗体,anti-cytotoxic T-lymphocyte antigen-4,anti-CTLA4)结合,引发了类似于疫苗的系统免疫反应,能够有效抑制肿瘤转移和防止肿瘤复发。Wang等[60]设计合成了肿瘤细胞膜修饰的Janus 结构的磁性纳米颗粒,并将其用于光动力和磁热的联合治疗,引发了肿瘤特异性的免疫反应。再结合anti-CTLA4,仿生且可生物降解的纳米颗粒彻底根除了原发性和深度转移性肿瘤。
4 磁热疗在肿瘤治疗中的应用
传统的肿瘤治疗技术以手术治疗、放射线治疗(放疗)、化学药物治疗(化疗)为主,因其对正常组织的损害导致患者承受程度不一的副作用。肿瘤磁热疗弥补了传统治疗方式的给药量大、给药次数多、无靶向性等不足,与化疗、放疗、光热治疗、免疫治疗等协同作用,提高肿瘤治疗的效果[61]。化疗与磁热疗是最常用的联合治疗方式,阿霉素(doxorubicin,DOX)是最常用的模型药物分子。王力[62]设计合成了高产热率的立方体纳米材料(Zn0.4Co0.6)Fe2O4@(Zn0.4Mn0.6)Fe2O4,表面修饰以PEG 增强单分散性,装载靶向分子透明质酸(【英文全称】HA)和药物分子DOX,此纳米复合材料可以靶向宫颈癌细胞Hela,且化疗和磁热疗有协同增强的治疗效果。Ferjaoui 等[63]报道了温度响应性的核壳结构的磁性纳米颗粒,负载DOX 后,磁热作用下可控释放DOX(见图10(a)),有效抑制了人卵巢癌细胞SKOV-3 的增殖。Cazares-Cortes 等[64]也设计了温敏性磁纳米凝胶,交变磁场下,磁热导致凝胶收缩释放药物DOX,还可以触发胞内DOX 释放(见图10(b)),增强DOX 的细胞毒性。Mai 等[65]在块状磁性纳米颗粒表面接枝温敏性聚合物,一方面防止粒子聚集,另一方面可以负载药物DOX。载药纳米颗粒在磁热作用下可控释放药物,实现荧光-磁共振双模态成像的检测和化疗-磁热疗的双模式治疗。顺铂、紫杉醇等也是常用的抗肿瘤药物,负载于磁性纳米颗粒用于肿瘤细胞的化疗和磁热疗的联合治疗[47,66-68]。

图10 磁热控制下的药物释放。(a)温敏性磁纳米颗粒[63];(b)温敏性磁纳米凝胶[64]Fig.10 The drug release under the AMF.(a) The thermosensitive magnetic nanoparticles[63];(b)Thermosensitive magnetic nanogel[64]
放射治疗是利用放射线如放射性同位素产生的α、β、γ 射线和各类X 射线治疗机或加速器产生的X 射线、电子线、质子束及其它粒子束等治疗恶性肿瘤的一种方法。随着医疗器械和治疗技术的发展,将微型放射源置于肿瘤内部,通过体内照射杀伤肿瘤组织,而正常组织不受到过量照射,避免了严重的并发症,成为放射治疗的一个焦点。将放射性同位素与磁性纳米颗粒结合,既可以磁热疗-放疗联合治疗,还可以多重成像示踪纳米颗粒在肿瘤内的分布。Ognjanovic′等[69]报道了用3 种同位素(锝(99mTc)、钇(90Y)和镥(177Lu))标记的磁性纳米颗粒,90Y 和177Lu 标记的纳米颗粒具有良好的磁致热-辐射效应,99mTc 标记的纳米颗粒有优异的成像能力。Ni 等[70]以锆(89Zr)标记磁性纳米颗粒和卟啉分子,将其用于切伦科夫辐射诱导的光动力治疗。89Zr 标记的纳米颗粒组织穿透能力强,不需要外部光激发,磁靶向聚集在肿瘤部位,是一种先进的磁增强切伦科夫辐射诱导的光动力治疗试剂。Spirou 等[71-72]综述了磁热疗和放疗的协同作用,分析了不同区域的细胞、细胞的不同时期、肿瘤微环境、热损耗、肿瘤部位热量浓度等因素对磁热疗和放疗的影响,为研究人员提供理论和实验依据。
光热疗以非侵入性、精准的特点受到研究者们的青睐,但是光的穿透深度有限,为解决这个局限性,近红外光热治疗成为研究热点[73]。产热效率一直是肿瘤治疗的关键环节,近红外光热疗与磁热疗的联合使用,致使产热效率倍增,治疗效果更佳。Espinosa 等[74]合成的块状氧化铁纳米粒,在交变磁场和近红外光(808 nm)的辐照下产热率是单独磁热的15 倍,双模态热疗致使细胞全部凋亡。Corato等[75]将光敏剂和磁性纳米颗粒包裹于脂质体中,将其用于光动力和磁热的双重治疗,致使实体瘤的彻底消融。Das 等[76]设计了多功能Ag/Fe3O4纳米花双热疗试剂,在外加磁场(200 Oe)和激光照射下,SAR 提高了一个数量级。例如加热温度需要40℃~44℃,单独磁热需要600 Oe 的磁场强度;若二者协同作用,需要400 Oe 的磁场强度和0.53 W/cm2的激光强度,或200 Oe 的磁场强度和0.93 W/cm2的激光强度。由此可见,光热和磁热的联合使用,显著降低了所需的磁场强度和激光强度,使其使用剂量在安全范围内。
免疫治疗是新兴的一种治疗方式,旨在激活人体免疫系统,依靠自身免疫机能杀死肿瘤细胞。磁热疗促使肿瘤细胞释放HSP,HSP 与胞内多肽物质形成复合物,激活APC,启动并促进T 细胞特异性免疫反应[77]。Pan 等[78]合成了单分散、超顺磁性CoFe2O4@MnFe2O4纳米颗粒,结合程序性死亡配体1(programmed death-ligand 1,α-PD-L1),联合磁热疗和检查点阻断免疫疗法用于原发性肿瘤的消融和转移瘤的抑制。Liu 等[79]也将磁热疗与免疫治疗结合,用于原发性肿瘤的根除和转移瘤的抑制,具体步骤为:氧化铁纳米环产生磁热,诱导乳腺癌细胞4T1 表达钙网蛋白(calreticulin,CRT),CRT 传递“吃掉我”信号,促使免疫系统吞噬癌细胞,导致免疫原性细胞有效死亡。Chao 等[32]联合聚乙二醇/多巴胺修饰的铁纳米颗粒和anti-CTLA4 消融原发性肿瘤和抑制转移瘤。程序性死亡受体-1(programmed cell death protein,PD-1)和CTLA4 具有负性免疫调节作用,抑制T 细胞的免疫应答,被称为免疫检查点。检查点阻断免疫疗法是解除抑制T 细胞的激活,现在研究最多的是靶向PD-1/PD-L1 和CTLA4的单克隆抗体,通过阻断PD-1 和CTLA4 的负调控通路以达到强化T 细胞免疫应答,进行肿瘤的治疗[80-81]。磁热疗有显著的免疫调节的作用,联合免疫治疗,二者协同增效,在肿瘤联合治疗中发挥着重要作用。
肿瘤细胞的磁热疗虽然在临床研究中得以广泛应用,但是磁性纳米颗粒的生物相容性、使用剂量、交变磁场频率、局域温度等是不容忽视的生物安全问题。一般认为治疗温度在42℃~45℃[82],超过50℃的热疗是有争议的;人体感受的磁场强度(H)和频率(ν)的临界值H.ν 为4.85×108A (m.s)-1。
磁性纳米颗粒在肿瘤治疗中一方面作为磁热疗的治疗试剂,一方面作为药物载体用作化疗试剂[83]。磁性纳米颗粒具有纳米材料的通病,比表面积大、穿透能力强,即便自身没有毒性,在体内运输至病变组织时也会产生不安全因素,所以深入研究材料与细胞的作用机制有助于优化材料结构和使用安全[84]。为了减小磁性纳米颗粒在体内的聚集或与蛋白等生物分子结合,常修饰以生物相容性的分子增强其分散性。Kim 等[85]以磁性纳米颗粒为核SiO2为壳,经荧光标记发现该纳米颗粒能穿过血脑屏障,4 周后仍在各组织器官(脑、肝、肾、睾丸、心脏、肺、脾、子宫) 中有存留,但没有明显毒性。Coricovac 等[86]采用非侵入法证实了油酸包裹的Fe3O4和Fe2O3接触人皮肤24 h 没有伤害。Agotegaray 等[87]采用壳聚糖包覆Fe3O4来研究其对血液、血管、神经和行为水平上的毒理学影响。纳米材料在100 μg/mL 时不影响内皮细胞的存活率,也不影响红细胞沉降率和完整性,血小板聚集也不受影响。对小鼠进行亚急性治疗后,行为和功能神经系统评估显示小鼠有肾炎和脾脏巨核细胞增多的迹象,但是未显示有神经系统毒性。以上研究证明,选择合适的表面修饰物能增强磁性纳米颗粒的生物相容性,但是细胞存活率不足以评价纳米材料的生物学毒性。
Häfeli 等[88]将磁性纳米颗粒修饰以聚氧乙烯封端的三嵌段聚合物,分子量高于2 kDa 显示较小的细胞毒性,分子量低于2 kDa 其细胞毒性明显。Wu 等[89]构建了柠檬酸或葡聚糖修饰的Fe3O4纳米颗粒,与人脐静脉内皮细胞共孵育24 h,在低浓度([Fe]:0.1 mM)时二者均为较高的细胞存活率(>80%),但是细胞骨架和细胞功能受到破坏。Sadeghi 等[90]采用肺吸入法研究了Fe2O3纳米颗粒对肺和肝的毒性,结果显示纳米颗粒引起大鼠的肺气肿、肺间质充血和肺部炎症。Kim 等[91]综述了作为药物载体的磁性纳米颗粒与蛋白和细胞的相互作用,分别阐述了其对组织器官、神经系统、心血管和血液系统、呼吸系统、免疫系统、泌尿系统和肝脏等潜在的生物毒性,并指出这些经典的毒理学分析并不足够反映其临床应用的效果,定量分析和结构性质测定新方法的开发能更好的指导研究人员在临床上的安全使用。磁性纳米颗粒的生物学毒性与其尺寸、表面官能团、结构等因素有关,也与给药方式、在体内的分布以及代谢途径有关,其研究涉猎范围较广[92]。
5 总结与展望
磁性纳米颗粒作为一类生物相容性好、表面易修饰的热疗载体,在肿瘤微创治疗中得到广泛应用。本文综述了磁性纳米颗粒的产热机制,在肿瘤治疗中与细胞的作用机制,以及与其他治疗方法的协同增效作用。目前,磁性纳米颗粒的研究还处于理论阶段,集中于优化材料的合成路线、结构、形貌等以提高产热率,对其进行表面修饰达到材料的单分散性、在体内的长循环、靶向性、生物相容性等。现在,已有研究利用仿生技术、生物矿化技术等设计合成生物相容性的磁性纳米颗粒,并将其用于疾病的诊断和治疗。磁性纳米颗粒不仅可以利用磁热杀伤肿瘤细胞,还可以充当纳米酶用于磁催化治疗。磁热与其他治疗方式的结合仍将是未来的发展方向,如何在安全范围内(磁场强度、局部温度、穿透深度、药物浓度、激光强度等)协同增效是需要解决的问题,磁性纳米颗粒在体内的生物学毒性和安全性评价仍需要大量的研究为临床应用提供必要的实验数据。另外,精准的医疗器械的开发也是一大挑战。
