Fe-Cr-Ni-Mn系黑色陶瓷颜料的制备及呈色性能分析
2022-01-17李治桥马国军刘孟珂
李治桥,张 翔,马国军,刘孟珂,王 强
(1.武汉科技大学钢铁冶金及资源利用省部共建教育部重点实验室,武汉 430081;2.武汉科技大学钢铁冶金新工艺湖北省重点实验室,武汉 430081)
0 引 言
黑色陶瓷颜料具有优异的耐候性、化学稳定性和热稳定性[1-2],已成为应用较为广泛的颜料之一,被大量应用于瓷砖、洁具、车漆和釉组合物等的起始原料中[3-5]。为了得到纯正的黑色陶瓷颜料,传统制备过程中通常需要加入氧化钴,而氧化钴的价格较高,严重制约了黑色陶瓷制品的发展[6-9]。因此,制备无钴黑色陶瓷颜料已成为研究热点。
Fe-Cr-Ni-Mn系无钴黑色陶瓷颜料的主要物相为尖晶石,结构式为AB2O4,其中A、B均可为+2、+3价金属元素,分别形成[AO4]四面体和[BO6]八面体。由于Fe、Cr、Ni和Mn均存在变价,因而均可能占据A和B位,形成混合尖晶石。Fe-Cr-Ni-Mn系黑色陶瓷颜料的烧结温度为1 000~1 300 ℃,保温时间为15~60 min[10-13]。李春文等[14]采用纯化工原料以固定配比在1 250 ℃下烧制合成该系颜料,分析结果表明该系颜料优先生成Ni[Cr2-yMny]O4和[Ni1-xFex]Fe2O4尖晶石,其次生成NiMn2O4和[Fe1-xCrx]Fe2O4尖晶石(0≤x≤1,0≤y≤2)。孙忱等[15]则认为该系颜料中,尖晶石B位由八面体的择位能而定,优先占据B位的顺序为Cr3+>Mn3+>Ni2+>Fe2+>Fe3+>Mn2+,对于占据A位的顺序并未进一步明确,因此该系颜料制备过程中尖晶石的形成机理有待进一步研究。此外,由于原料组分较复杂,任何化学计量偏差都可能导致杂质物相的形成,从而影响颜料的着色性[16-20],且现有研究均未考虑冷却方式对尖晶石形成过程中晶型构成产生的重要影响[14-17,21]。
本文以纯化学试剂为原料,在Fe-Cr-Ni-Mn系黑色陶瓷颜料的制备过程中,研究了该系颜料中着色尖晶石物相的晶型结构、组成、含量及颜料呈色性能随烧结温度、保温时间、冷却方式等条件变化时的演变规律,为制备该系无钴黑色陶瓷颜料提供指导。
1 实 验
1.1 原材料
原材料包括Fe2O3、Cr2O3、MnO和NiO四种化学试剂,均为分析纯。
1.2 试验方法
1.2.1 颜料制备
首先将化学试剂按特定比例混合,将混合物料置于翻转摇匀仪中以45 r/min混匀30 min,然后将30 g混匀物料置于马弗炉(SX2-10-13,武汉电庐实验电炉厂)中,以10 ℃/min的升温速率由室温升温至所需烧结温度并保温一定时间,随后以不同冷却方式将样品冷却至室温,得到黑色陶瓷颜料。相关工艺参数如表1所示,其中空冷与水淬分别为将保温结束后的样品从炉膛内取出,然后直接置于空气中或水中进行冷却。对于水淬后的颜料样品,将其在120 ℃下干燥24 h。

表1 制备黑色陶瓷颜料的工艺参数Table 1 Process parameters for the preparation of black ceramic pigments
1.2.2 陶瓷釉制备
为进一步研究所制备颜料的着色性能,将所制备颜料应用于陶瓷釉。首先将3.5 g坯泥(化学成分如表2所示)在15 MPa下压制成圆柱状(直径:15 mm,高:8 mm)试样,并在110 ℃下干燥3 h得到素坯。然后,将所制备颜料与透明生料釉(化学成分如表2所示)进行混合,混合物料中颜料所占比例分别为4%、7%、10%(质量分数)。采用湿法球混方法以m(混合体)∶m(球)∶m(水)=1 ∶2 ∶0.8将混合物料混匀10 h制备得到釉浆。通过浸施方式在素坯表面进行施釉,釉层厚度为0.3~0.5 mm,随后将施釉坯体在110 ℃下干燥3~4 h。最后,将干燥后的施釉坯体在马弗炉中以10 ℃/min的升温速率由室温加热至600 ℃后保温30 min,随后以相同升温速率加热至1 200 ℃保温30 min,保温结束后随炉冷却至室温,得到陶瓷釉。

表2 坯泥及透明生料釉的主要化学成分Table 2 Main chemical composition of ceramic base body and transparent raw glaze
1.2.3 颜料和陶瓷釉性能检测
对所制备的颜料与陶瓷釉面使用便携式色差仪(SC10 NR10QC,三恩时)测量L*、a*和b*值。L*表示颜色的明暗,为白色(L*=100)到黑色(L*=0)的标度;a*和b*分别表示绿色(-a*)到红色(+a*)、蓝色(-b*)到黄色(+b*)的标度。
利用X射线衍射仪(XPert PRO MPD,PANalytical)对颜料进行物相分析,测试条件为:Cu Κα辐射,管电压40 kV,管电流40 mA,2θ扫描范围10°~90°。使用场发射扫描电子显微镜(NanoSEM400,Philips)对颜料的微观形貌进行观测。采用紫外-可见分光光度计(UV-2600,岛津)测量颜料样品在200~900 nm范围内的漫反射光谱,并利用Kubelka-Munk公式(见式(1)、(2))推算出黑色颜料样品的禁带宽度。
R=1/10A
(1)
F(R)=(1-R)2/2R
(2)
式中:R为反射系数;A为吸收系数;F(R)为Kubelka-Munk函数。以E=1 240/λ为横坐标(其中:E为光子能量,eV;λ为对应波长,nm)、[F(R)·E]1/2为纵坐标作图,对所做图形作切线,切线在横坐标上的截距即为禁带宽度。
2 结果与讨论
2.1 原料配比对颜料呈色性能的影响
图1为Fe2O3的添加量对所制备颜料色度值与物相的影响,具体试验条件如图1(a)中所示。由图1(a)可知,随着Fe2O3添加量的增加,L*值呈先下降后升高的趋势。L*值从Fe2O3添加量为0 mol时的21.44降低至1.5 mol时的19.18,此后随着添加量增加L*值出现小幅上升。a*、b*值均在Fe2O3添加量为1.5 mol时出现转折。
不同Fe2O3含量下颜料的XRD谱如图1(b)所示。在无Fe2O3条件下,出现了NiMn2O4和NiCr2O4的特征衍射峰,物相中出现Mn3+表明MnO在加热过程中被氧化后参与反应。当原料中加入Fe2O3后,物相中立即出现的NiFe2O4黑色尖晶石,使颜料L*值大幅降低,如图1(a)所示。当Fe2O3的添加量介于0.5~1.5 mol时,原物相中NiMn2O4逐渐消失,并形成Ni[CrMn]O4,这是由于B位择位能Fe3+>Mn3+,随着Fe2O3添加量的增加,Fe3+也将占据更多B位形成NiFe2O4尖晶石,使颜料L*值降低,而原本位于B位的一部分Mn被Cr取代,形成[CrMn]6+固溶体。当Fe2O3的添加量超过1.5 mol时,Mn与Cr全部形成Ni[CrMn]O4,且此后颜料物相组成无变化。因此物相中仍保留[CrMn]6+,表明其B位择位能大于Fe3+。综上,B位择位能顺序为Cr3+>[CrMn]6+>Fe3+>Mn3+。
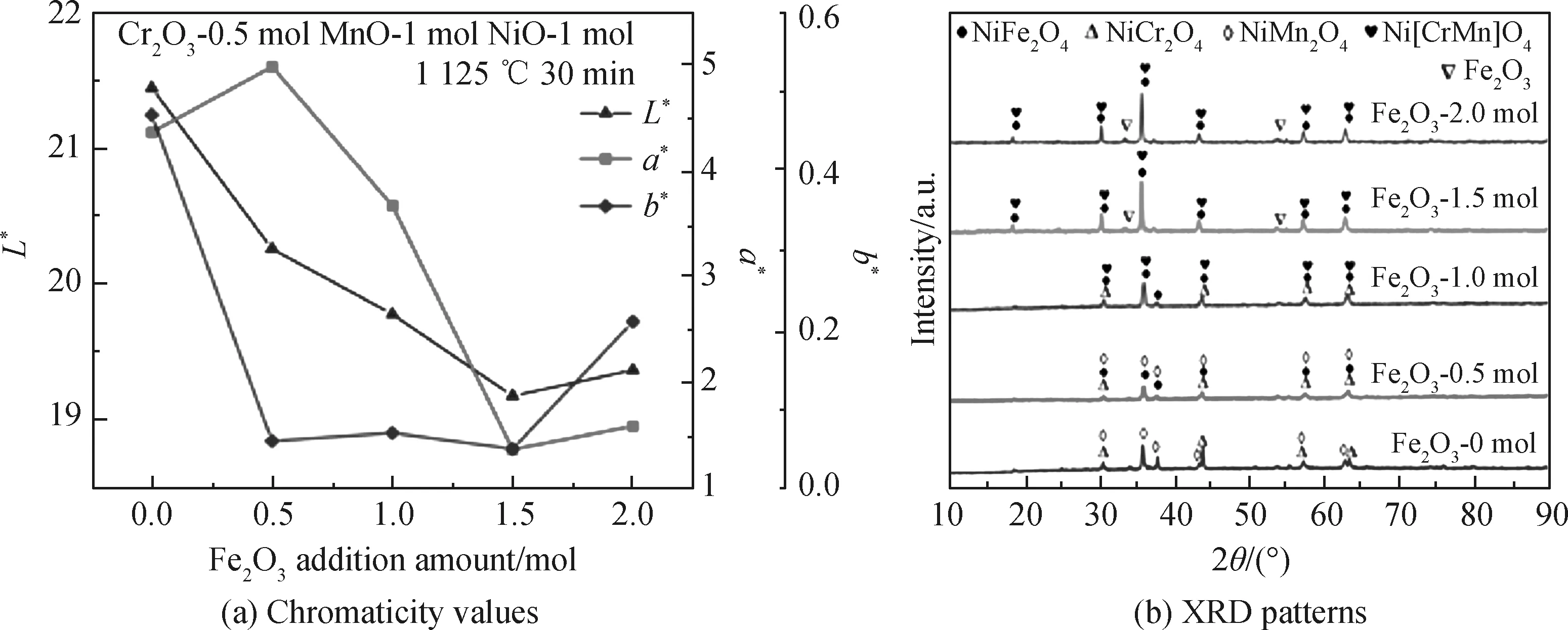
图1 不同Fe2O3添加量下颜料的色度值和XRD谱Fig.1 Chromaticity values and XRD patterns of pigments under different addition amounts of Fe2O3
图2为Cr2O3的添加量对颜料色度值与物相的影响。由图2(a)可知,随着Cr2O3添加量的增加,L*值呈现先下降后上升的趋势,在添加量为0 mol和0.25 mol时分别达到最大值(20.97)和最小值(20.05),同时a*与b*值变化趋势与L*相似,呈先小幅下降后显著上升的趋势。
在不添加Cr2O3的条件下,颜料中的物相主要为NiO、NiFe2O4、Ni6MnO8和NiMnO3,其中Fe与Ni形成尖晶石结构,而Ni与Mn仅形成氧化物。当加入Cr2O3后,物相中出现了NiMn2O4与NiCr2O4,表明Cr2O3能够促进Ni、Mn之间形成尖晶石结构。根据图2(b)中物相的变化可知,B位中Cr3+首先与Mn3+反应形成Ni[CrMn]O4,进而占据Fe3+所处的B位。
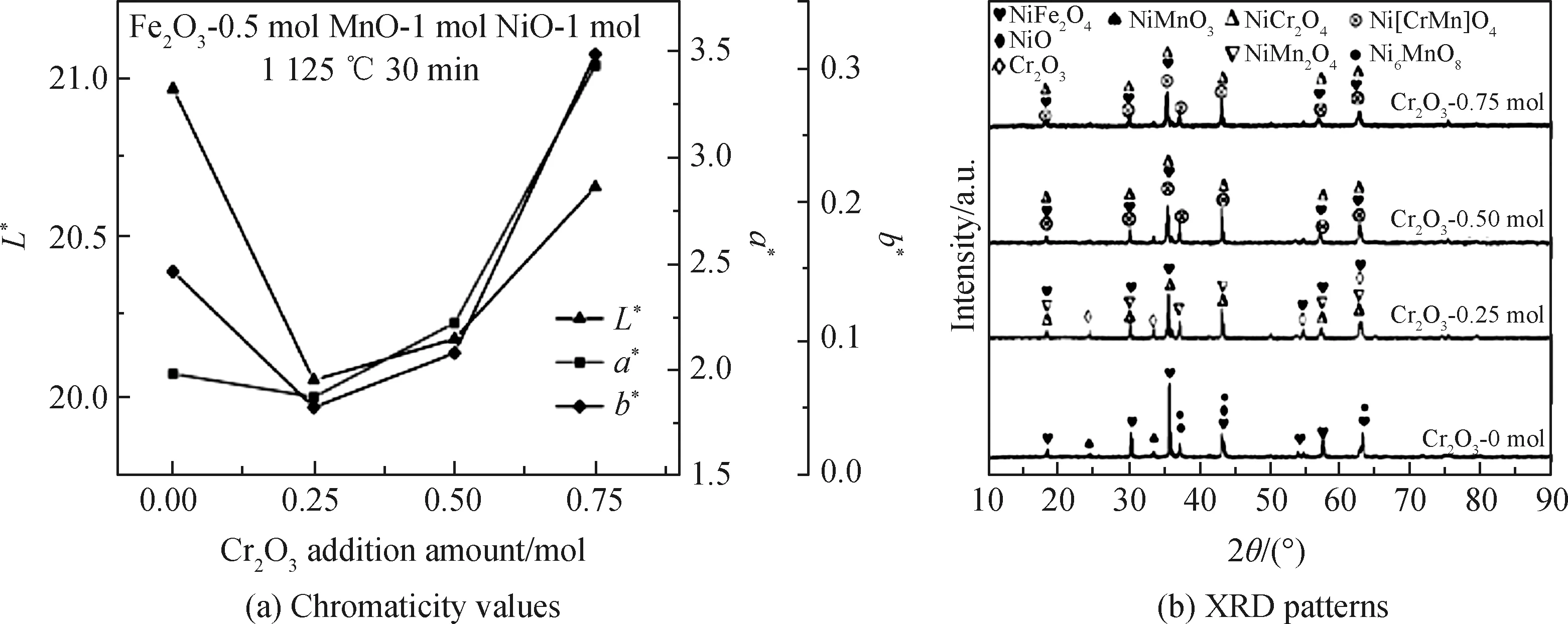
图2 不同Cr2O3添加量下颜料的色度值和XRD谱Fig.2 Chromaticity values and XRD patterns of pigments under different addition amounts of Cr2O3
MnO添加量对颜料色度值与物相的影响如图3所示。由图3(a)可知,所制备颜料L*、a*和b*值变化趋势一致。a*和b*值在MnO添加量达0.25 mol时快速上升,其中a*值由0.25 mol时的0.48攀升至0.75 mol时的6.16,颜料呈现出轻微红色。结合XRD数据分析(见图3(b)),随着MnO添加量的增加,物相组成中Ni[Mn0.5Cr1.5]O4逐渐减少直至消失,同时Ni[CrMn]O4不断生成,这是由原料中MnO含量增加使得Mn抢占更多B位所致。同时Mn3+较Cr3+的半径小,使晶格常数在一定程度上减小,从而增加了轨道杂化效应,使禁带宽度减小,因此Ni[CrMn]O4呈黑色性能远低于Ni[Mn0.5Cr1.5]O4。此外,由图3可知,当MnO与Cr2O3摩尔比≤1.5时生成[Mn0.5Cr1.5]6+,当MnO与Cr2O3摩尔比>1.5时则生成[CrMn]6+与[Mn2]6+。

图3 不同MnO添加量下颜料的色度值和XRD谱Fig.3 Chromaticity values and XRD patterns of pigments under different addition amounts of MnO
图4为NiO添加量对颜料色度值与物相的影响。由图4(a)可知,L*、a*和b*值变化趋势相同,且均在NiO添加量为0.25 mol时达到最小。如图4(b)所示:在无NiO添加的条件下,颜料中尖晶石物相为(Mn0.87Fe0.13)(Mn0.13Fe0.87Cr)O4,表明Mn2+与Fe2+将共同占据A位置,其中Mn2+比例远高于Fe2+;在原料中添加NiO后,颜料物相中有NiCr2O4生成,因此A位择位能顺序为Ni2+>Mn2+>Fe2+。
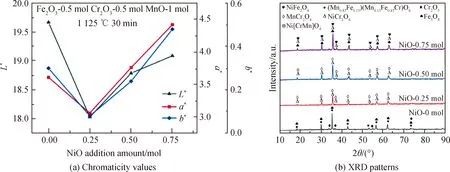
图4 不同NiO添加量下颜料的色度值和XRD谱Fig.4 Chromaticity values and XRD patterns of pigments under different addition amounts of NiO
上述结果表明,原料中各氧化物之间的摩尔比对颜料最终物相组成至关重要。所制备颜料物相组成中,NiFe2O4呈黑色偏红,NiCr2O4呈青绿色,而Fe2O3呈红色,通过复合呈色,使颜料呈黑色[22]。此外,原料中组分Cr2O3能促进Ni、Mn元素之间形成尖晶石相。当氧化物Fe2O3、Cr2O3、MnO和NiO的摩尔比为6 ∶1 ∶1 ∶1时,所制备的颜料呈色最佳,因此后续试验在该配比下进行。
2.2 制备工艺对颜料呈色性能的影响
图5为不同烧结温度下所制备颜料的色度值与XRD谱。由图5(a)可知,所制备颜料在1 150 ℃呈现出最佳色度值,当烧结温度高于或低于该温度时颜料L*、a*和b*值均明显升高。如图5(b)所示,在烧结温度为1 100 ℃时,原料不同组分间已发生反应,颜料所含尖晶石相为Ni[Mn0.5Cr1.5]O4。随着烧结温度的提高,各物相的反射峰越尖锐,表明混合物结晶度增加。当烧结温度为1 150 ℃时,颜料所含尖晶石相中还存在NiFe2O4与NiCr2O4,这表明NiFe2O4、NiCr2O4的生成温度高于1 100 ℃。当烧结温度高于1 200 ℃时,颜料中Ni[Mn0.5Cr1.5]O4消失,同时生成Ni[MnCr]O4,这是由于Ni[Mn0.5Cr1.5]O4在高温下会发生分解[23-24]。为获得稳定性良好的颜料,需对原料进行充分煅烧,从而提高结晶度并获得完整的尖晶石相,但温度过高会导致Ni[Mn0.5Cr1.5]O4分解,因此选择烧结温度为1 150 ℃进行后续试验。
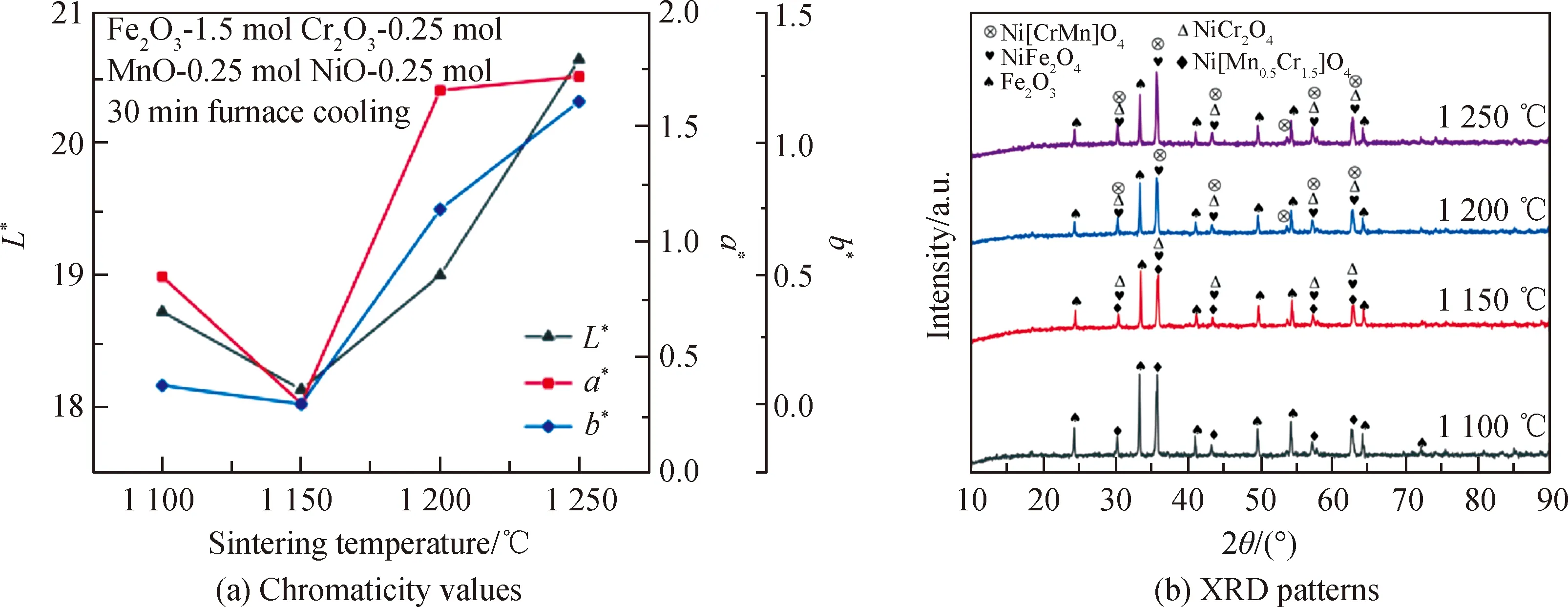
图5 不同烧结温度下颜料的色度值和XRD谱Fig.5 Chromaticity values and XRD patterns of pigments under different sintering temperatures
不同保温时间下颜料的色度值及物相组成如图6所示。由图6(a)可知,颜料的L*、a*和b*均随着保温时间的延长先减小后增大,并在45 min时颜料色度值达到最佳。由图6(b)可知:当保温时间为15 min时,颜料物相组成为NiFe2O4、Fe2O3、Ni[Mn0.5Cr1.5]O4、NiCr2O4和Cr2O3,由于Cr2O3呈绿色,当其残存于颜料中时势必会影响颜料呈色;当保温时间为45 min时Cr2O3消失;随着保温时间延长至60 min,颜料L*、a*和b*值均上升,且物相中出现[Fe0.6Cr0.4]2O3,这是因为Ni[Mn0.5Cr1.5]O4分解所产生的游离Cr3+与Fe3+的离子半径相近,二者之间产生固溶反应并形成[Fe0.6Cr0.4]3+。因此,在本试验条件下合理的保温时间为45 min。

图6 不同保温时间下颜料的色度值和XRD谱Fig.6 Chromaticity values and XRD patterns of pigments under different holding time
由于不同冷却方式会对尖晶石的富集度造成影响[25],因此有必要研究不同冷却方式对颜料物相变化及呈色的影响。图7为采用不同冷却方式所制备颜料的色度值和XRD谱。由图7(a)可知,不同冷却方式下颜料色度值之间差异较大,且在随炉冷却条件下所制备颜料的色度值最佳,其L*、a*与b*值分别为18.02、0.20和0。由图7(b)可知,在随炉冷却条件下,颜料的物相为NiFe2O4、Fe2O3、NiCr2O4和Ni[Mn0.5Cr1.5]O4。当冷却方式为空冷时,颜料主要的物相较随炉冷却未发生明显变化,但Fe2O3衍射峰强度有所增加,从而导致颜料a*值升高。当冷却方式为水淬时,颜料物相中存在的[Fe0.6Cr0.4]2O3会对颜料的呈色效果造成不利影响。因此,颜料制备过程中选择随炉冷却为宜。

图7 不同冷却方式下颜料的色度值和XRD谱Fig.7 Chromaticity values and XRD patterns of pigments under different cooling methods
2.3 颜料热力学分析
本研究所用原料Cr2O3为绿色,在加热过程中极难被氧化,而MnO在空气中加热至不同温度时可生成Mn3O4、Mn2O3或MnO2,如式(3)~(5)所示。此外NiO为绿黑色,加热时可被氧化为Ni2O3,但当温度超过600 ℃时将发生分解,如式(6)所示。由于Fe3+以不稳定的氧化态存在于尖晶石晶格中,易被还原,因此存在动态平衡关系Fe3+←→Fe2+[26]。
6MnO+O2=2Mn3O4
(3)
4MnO+O2=2Mn2O3
(4)
2MnO+O2=2MnO2
(5)

(6)
图8为反应式(3)~(5)的吉布斯自由能(ΔG)随反应温度的变化。由图8可知,在MnO与NiO被氧化的过程中,随着温度的升高,二者相关氧化反应的吉布斯自由能逐渐下降,因此氧化过程大多发生在较低温度(200~800 ℃)下,在该温度条件下生成尖晶石的反应尚未发生,由此可知颜料的制备过程可划分为两个阶段,首先为MnO和NiO的氧化以及Ni2O3的分解,随后为尖晶石的形成。如前所述,B位择位能顺序为Cr3+>[CrMn]6+或[Mn0.5Cr1.5]6+>Fe3+>Mn3+,因此尖晶石物相生成顺序依次为NiCr2O4、Ni[Mn0.5Cr1.5]O4或Ni[CrMn]O4、NiFe2O4和NiMn2O4,上述尖晶石物相的呈色不同,是由于Fe、Cr、Ni和Mn四种过渡金属元素最外层非球形对称结构的4d导带与价带(B位元素和O 2p组成的杂化轨道)之间电荷迁移所需能量不同。
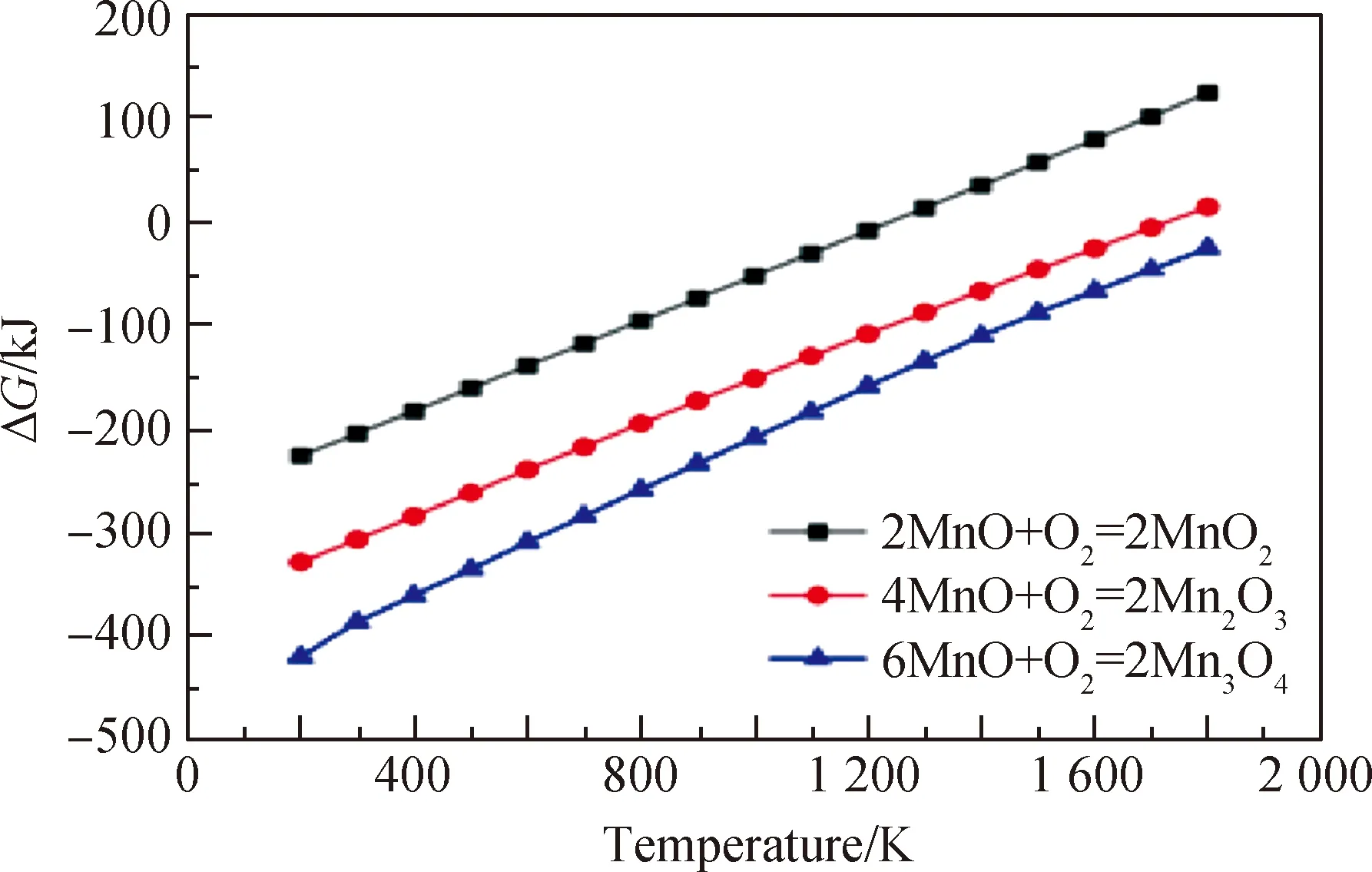
图8 各反应的吉布斯自由能随温度的变化规律Fig.8 Variation law of Gibbs free energy of each reaction with temperature
2.4 颜料表征与应用
在原料Fe2O3、Cr2O3、MnO和NiO四种组分摩尔比为6 ∶1 ∶1 ∶1,烧结温度为1 150 ℃,保温时间为45 min,采用随炉冷却条件下制备黑色陶瓷颜料并对其进行表征和着色性能检测。图9(a)、(b)为黑色陶瓷颜料的显微形貌图。由图9(a)可知,在该工艺条件下制备的颜料颗粒细小,且粒度分布均匀,但存在轻微聚集。对图9(b)中的颜料颗粒进行面扫描,结果如图9(c)所示,可知颜料所含主要元素Fe、Cr、O和Mn之间紧密聚集,且各元素分布均匀,这表明所制备颜料均质性较好,且颗粒内部结构较为紧密。

图9 颜料的SEM照片和面扫描图Fig.9 SEM images and mapping of pigments
图10(a)为所制备黑色颜料的紫外-可见光谱。由图10(a)可知,颜料在380~780 nm的可见光范围内反射率变化幅度不显著,这表明颜料对可见光各波段具有相同的吸收能力,使颜料呈黑色。但在700 nm附近的红光波段反射率略微下降,这是由于颜料中的NiCr2O4呈青色,与红色呈互补色。图10(b)为由紫外-可见光谱检测结果所推导出的颜料的禁带宽度。如图10(b)所示,颜料禁带宽度(Eg)为1.25 eV。根据能带理论,不同禁带宽度所对应颜料颜色不同,当Eg<1.7 eV时物质为黑色[27],因此颜料呈黑色。
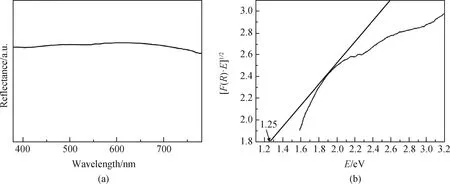
图10 所制备颜料的紫外-可见光反射光谱Fig.10 UV-Vis light reflection spectrum of prepared pigment
为进一步验证制备颜料黑色的纯正性,根据制备颜料的紫外-可见光谱检测结果,使用色度图对颜料颜色纯正度进行分析,结果如图11所示。图11中A点为消色点,对应CIE色度坐标为x=0.333 3、y=0.333 3,该点色饱和度为0,越接近该点,黑色越纯正。图11中B点为所制备颜料对应点,其色坐标为x=0.335 8、y=0.335 3。A、B两点色坐标接近,二者几乎重合,因此制备的颜料黑色纯正度高。
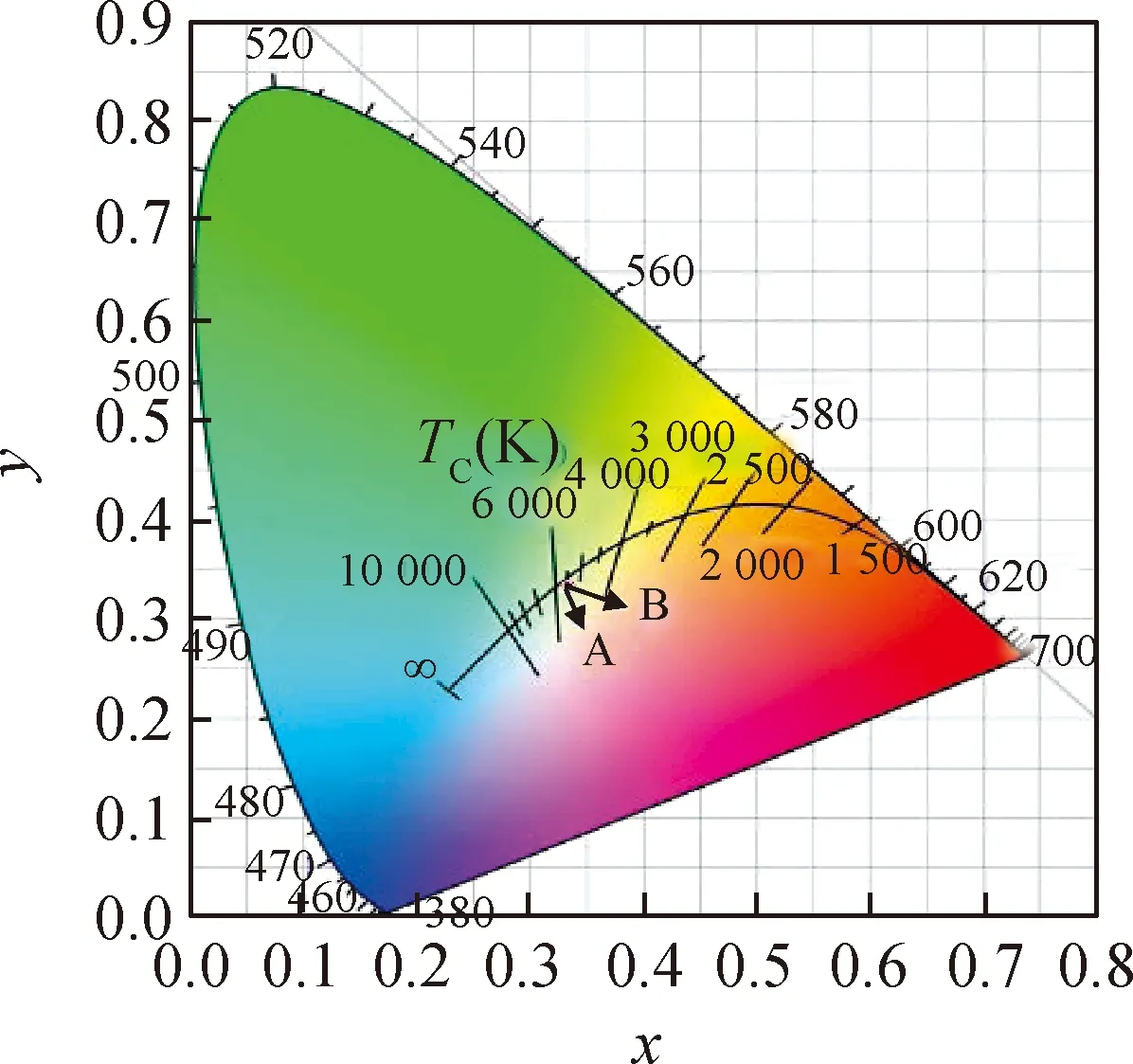
图11 所制备颜料色度图Fig.11 Chromaticity diagram of prepared pigment
图12为不同颜料添加量下陶瓷釉面的形貌图。如图12所示:未添加颜料的陶瓷釉面呈乳白色,质地紧密坚固;当添加颜料后,陶瓷釉面光滑致密,其L*值随着颜料添加量的增加有所增加,釉面黑色更为明亮,a*和b*值则呈显著下降趋势,黑色纯正度增加。上述结果表明该颜料具有优异的着色性能和应用潜力。

图12 不同颜料添加量(质量分数)下陶瓷釉面的形貌图Fig.12 Morphology of ceramic glaze surface with different prepared pigment addition amounts (mass fraction)
3 结 论
(1)在原料Fe2O3、Cr2O3、MnO和NiO四种组分摩尔比为6 ∶1 ∶1 ∶1,烧结温度为1 150 ℃,保温时间为45 min,冷却方式采用随炉冷却的条件下,所制备颜料的L*、a*与b*值分别为18.02、0.20和0,主要组成物相为NiFe2O4、NiCr2O4和Ni[Mn0.5Cr1.5]O4。
(2)在生成尖晶石的反应中A位择位能顺序为Ni2+>Mn2+>Fe2+,B位择位能顺序为Cr3+>[CrMn]6+或[Mn0.5Cr1.5]6+>Fe3+>Mn3+;热力学分析表明,该颜料的反应主要分为两个部分,首先为MnO和NiO的氧化以及Ni2O3的分解,随后为尖晶石的形成。
(3)所合成颜料颗粒细小,且粒度分布均匀,其禁带宽度为1.25 eV,呈纯正黑色。将颜料应用于陶瓷釉,陶瓷釉面光滑致密,随着颜料添加量的提高,L*值有所增加,釉面黑色更为明亮,而a*和b*值则呈显著下降趋势,黑色纯正度增加,因此颜料具备优异的着色性能和应用潜力。
