甲氟喹对急性癫痫小鼠认知功能的影响研究
2022-01-15倪红郑卜真王恩柯绍发王皖芬马传花罗莎
倪红 郑卜真 王恩 柯绍发 王皖芬 马传花 罗莎
癫痫是一种常见的神经系统慢性疾病。临床上30%~40%的癫痫患者存在认知功能障碍,这对其生活、工作等均有较大的影响。此外,临床常用的传统抗癫痫药物虽然能有效控制70%~80%的癫痫发作,但会加剧患者认知功能减退。N-甲基D-天冬氨酸(N-methyl-D-aspartic acid,NMDA)受体是中枢神经系统中主要的兴奋性氨基酸受体,其过度激活可导致癫痫,而癫痫发作后又可引起细胞膜内外离子失衡,激活神经毒性信号传导途径,产生神经毒性效应,导致神经元损伤或死亡,从而造成一系列神经元功能障碍。NMDA受体的适当激活与学习、记忆、认知过程的形成有关。Stafstrom等[1]利用致痫模型研究发现NMDA受体过度兴奋导致的发育期大鼠反复癫痫发作后,其成年期认知功能存在损伤,远期神经兴奋性发生改变。Thompson等[2]研究发现,NMDA受体激活后继发的内向电流系Pannx1通道开放所致,阻断Pannx1通道能抑制癫痫发作。甲氟喹是一种Pannx1通道阻滞剂,目前主要用于疟疾的治疗。Pinheiro等[3]研究发现,甲氟喹可抑制KA小鼠癫痫自发发作的频率和总时间。因此,本研究就甲氟喹对急性癫痫小鼠认知功能的影响作一探讨。
1 材料和方法
1.1 实验动物 健康黄色荧光蛋白转基因C57 Thy1-YFP小鼠30只,由蚌埠医学院实验动物中心提供。其中雄性16只,雌性14只;出生后15~17 d;体重(15.0±0.5)g。本实验通过动物伦理委员会伦理审查,全程遵守实验中心动物管理条例。
1.2 动物分组与处理 按随机数字表法分为癫痫组、甲氟喹组和对照组,每组10只。甲氟喹组在建模前1 h按20ml/kg的剂量腹腔注射甲氟喹注射液(规格:25mg/片,批号:53230-10-7,深圳海思安生物技术有限公司;将25 mg甲氟喹溶于25 ml 0.9%氯化钠溶液中配成1 g/L的甲氟喹注射液)[4];癫痫组、对照组按20 ml/kg的剂量腹腔注射0.9%氯化钠注射液。建模:癫痫组、甲氟喹组小鼠按3 ml/kg的剂量腹腔注射东莨菪碱注射液(规格:1 g/ml,批号:YRD059,成都仪睿生物科技有限公司;将2 mg东莨菪碱溶于10 ml的0.01 mol PBS中配成 0.2 g/L的东莨菪碱注射液),30 min后按15 ml/kg的剂量腹腔注射匹鲁卡品注射液(规格:5 g/瓶,批号:CAS 54-71-7,北京Med Chem Express生物科技公司;将0.57 g匹鲁卡品溶于20 ml 0.9%氯化钠溶液中配成28.5 g/L的匹鲁卡品注射液),诱发Ⅴ级癫痫发作持续1 h为建模成功。若注射后未诱发Ⅲ级以上癫痫发作,可重复给予原剂量匹鲁卡品注射液,以5次为最高限。癫痫发作分级标准:参照Racine分级标准。无惊厥为0级;面部阵挛为Ⅰ级;面部阵挛+节律点头为Ⅱ级;面部阵挛+节律点头+前肢阵挛为Ⅲ级;面部阵挛+节律点头+前肢阵挛+后肢站立为Ⅳ级;面部阵挛+节律点头+前肢阵挛+后肢站立+跌倒为Ⅴ级。
1.3 小鼠认知功能测定 使用Morris水迷宫系统(包括水迷宫、电脑摄像系统及配套软件分析系统;购自上海移码数字有限公司);水迷宫是一个直径96 cm、高 50 cm的圆柱形水池,池中水深 40 cm、水温(21.0±1.5)℃。(1)空间学习能力测定:采用定位航行试验。迷宫共分成4个象限,在距水面下1 cm处放置在一个固定的水下平台。所有小鼠接受连续5 d训练[5],每天进行4次空间习得实验,每次训练间隔时间60 min,记录其寻找到水下平台的时间,即逃避潜伏期。若60 s内找到水下平台,逃避潜伏期为小鼠找到水下平台的时间;若未在规定时间内找到平台,则将小鼠轻轻引导至水下平台停留10 s,逃避潜伏期为60 s。(2)记忆能力测定:采用空间探索试验。第6天撤走水下平台,任选一个入水点将小鼠放入水池中,使用水迷宫软件记录其在60 s内的游泳轨迹,记录小鼠穿越平台次数。
1.4 统计学处理 采用SPSS 20.0统计软件。计量资料符合正态分布的以 表示,多组间比较采用单因素方差分析,两两比较采用SNK-q检验;不符合正态分布的以 M(P25,P75)表示,多组间比较采用 Kruskal-Wallis H检验,两两比较采用Nemenyi检验。P<0.05为差异有统计学意义。
2 结果
2.1 3组小鼠5 d内逃避潜伏期比较 第1天癫痫组、甲氟喹组小鼠逃避潜伏期均明显长于对照组(均P<0.05),而癫痫组与甲氟喹组比较差异无统计学意义(P>0.05);第2~5天,癫痫组、甲氟喹组小鼠逃避潜伏期均明显长于对照组(均P<0.05),但甲氟喹组均短于癫痫组(均P<0.05),见表1。

表1 3组小鼠5 d内逃避潜伏期比较(s)
2.2 3组小鼠穿越平台次数比较 癫痫组、甲氟喹组小鼠第6天穿越平台次数均明显少于对照组(均P<0.05),但甲氟喹组多于癫痫组(P<0.05),见图1。
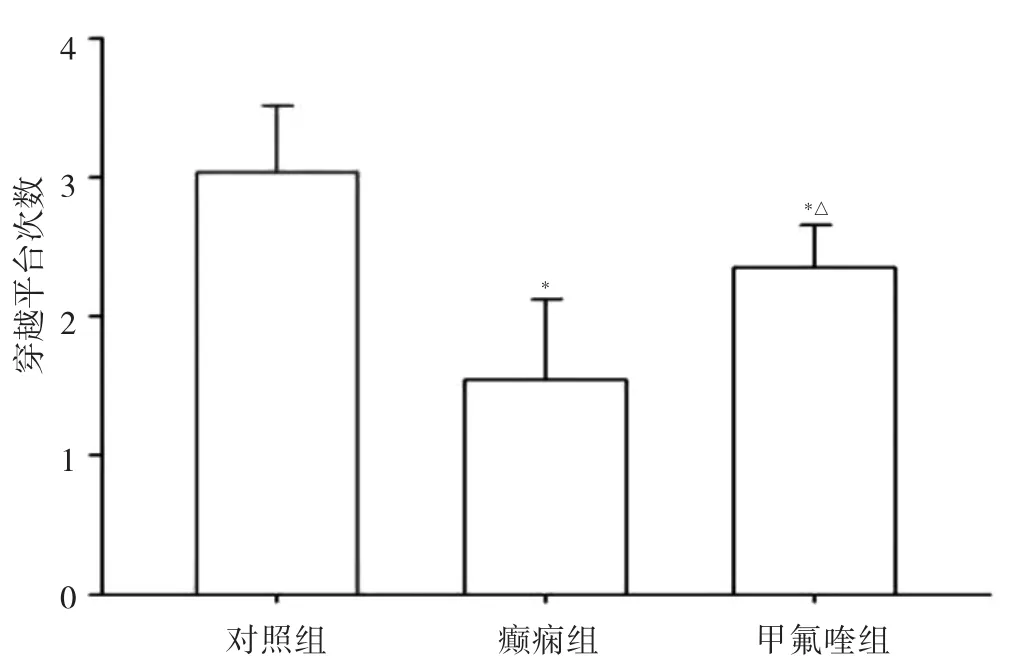
图1 3组小鼠穿越平台次数比较(与对照组比较,*P<0.05;与癫痫组比较,△P<0.05)
3 讨论
NMDA受体是中枢神经系统中主要的兴奋性氨基酸受体,在全脑都有分布,以海马、大脑皮质、纹状体、杏仁体中的含量最高[6]。NMDA参与学习、记忆、癫痫、药物依赖成瘾及神经系统退行性疾病等多种病理生理过程。NMDA是调节神经元兴奋性的关键,NMDA受体离子通道的超极化激活环磷酸腺苷门控通道,导致神经兴奋性增加,从而发生癫痫,甚至癫痫持续状态[7],而癫痫发作后又可导致NMDA受体过度激活,引起细胞膜内外离子失衡,激活神经毒性信号传导途径,产生神经毒性效应,使得神经元损伤或死亡,最终导致认知功能严重受损。Inostroza等[8]研究发现氯化锂-匹鲁卡品癫痫大鼠的空间学习及记忆获得及维持能力均明显受损。但NMDA受体的适当激活有助于提高学习及记忆能力。NMDA受体在重复或长时间激活产生的NMDA通道后存在一个继发的内向电流,即使洗脱NMDA,该内向电流依然存在。这一现象目前一直未得到合理解释。Thompson等[2]在急性分离的海马锥体神经元实验中发现,NMDAR受体激活后继发的内向电流系Panx1通道开放所致。Burma等[4]研究发现Pannx1通道抑制剂能产生类似抑制癫痫发作的作用。Silverman等[9]研究发现甲氟喹是Pannx1通道的良好阻滞剂。Velasquez等[10]研究发现甲氟喹能明显抑制癫痫发作。既往研究显示,NMDA受体在癫痫发作与学习、记忆等认知功能中均有重要作用,适当抑制NMDA受体活性也可以提高“致痫阈”,减少癫痫的发作频率;同时能保护神经元功能,也有利于防止癫痫患者认知功能的下降[11-12]。本实验使用甲氟喹阻断Panx1通道,以观察小鼠癫痫发作时谷氨酸能神经元的异常电活动对认知功能的影响,如影响变小或有改善作用,此通道或将成为抗癫痫药物治疗的重要靶点。
Morris水迷宫是英国心理学家Morris于1981年设计并应用于研究大脑学习记忆机制的一种实验手段[13],它主要用于评估空间学习和记忆能力[14-15]。随着实验的不断改良,Morris水迷宫被认为是一种稳健、可靠的测试[16]。经典的Morris水迷宫测试程序主要包括定位航行试验和空间探索试验两个部分,一般认为小鼠的标准训练周期为5 d[17-19]。最近一项研究报道,海马区胆碱能神经元活动在训练早期显著增加[20]。Stafstrom等[1]对NMDA致痫模型大鼠进行水迷宫试验,结果发现在出生后85 d的大鼠中,NMDA致痫组逃避潜伏期明显长于对照组,提示NMDA对大脑发育期的大鼠致痫后,会导致其成年期空间记忆能力下降。在前期研究中,笔者发现甲氟喹能抑制癫痫小鼠海马谷氨酸能神经元的兴奋性[21]。故本实验以甲氟喹阻断NMDA受体内向电流为切入点,采用Morris水迷宫实验来研究甲氟喹对急性癫痫发作小鼠空间学习及记忆能力的影响。本研究结果显示,定位航行试验第1天,癫痫组、甲氟喹组小鼠逃避潜伏期均明显长于对照组,而癫痫组与甲氟喹组比较差异无统计学意义;第2~5天,癫痫组、甲氟喹组小鼠逃避潜伏期均明显长于对照组,但甲氟喹组均短于癫痫组。第6天空间探索试验中,癫痫组、甲氟喹组小鼠穿越平台次数均明显少于对照组,但甲氟喹组多于癫痫组。这说明癫痫发作后小鼠空间学习及记忆能力较正常小鼠均有所下降;而甲氟喹干预能使急性癫痫发作小鼠的空间学习及记忆能力均有所改善。
综上所述,甲氟喹控制小鼠癫痫发作的同时,还能改善其空间学习及记忆能力,显著提高癫痫小鼠的认知功能。然而,亦有研究证实在少数疟疾患者中应用甲氟喹,可诱发癫痫发作[22-23]。由于甲氟喹作用于不同的靶点(如神经元、星形细胞、钠通道或内质网蛋白),可表现出多种不同的不良反应[24],这也导致其用于癫痫治疗仍存在明显的局限性。未来希望涌现出具有高选择性的Panx1通道阻滞剂,在做到控制急性癫痫的同时,又能减少对患者认知功能的影响。
