高效液相色谱-紫外光谱法测定醇胺溶液中4 种羧酸根离子
2022-01-11刘谋淋
李 沙,刘谋淋,张 静,黄 建
(1. 四川省德阳生态环境监测中心站,四川 德阳 618000;2. 四川蓝城检测技术有限公司,四川 成都 610000)
天然气工业中,常用以N-甲基二乙醇胺(MDEA)为主的醇胺溶液进行气体净化和脱硫脱碳[1-3]。在MDEA 的长期循环使用过程中,易产生热稳定性盐(HSS),当HSS 总量超过0.5%(w)时,易导致净化装置腐蚀、溶液发泡、效率降低。HSS 的来源包括:氧化降解产生的羧酸盐(以甲酸盐、乙酸盐为主,含少量草酸盐、乙醇酸盐、丙酸盐);天然气净化引入的无机盐(以氯化物、硫酸盐为主);脱硫过程中H2S 氧化形成的硫化物(如硫酸盐、硫代硫酸盐、硫氰酸盐)[4-6]。因此,及时准确掌握醇胺溶液中阴离子的含量,对监测和指导净化装置的实际运行具有重要作用。
现有测量HSS 的方法有滴定法和离子交换色谱法[7-9]。滴定法仅能获得HSS 的总量,渐已停用,目前多采用离子交换色谱法,该法主要解决了HSS 中无机阴离子(如氯离子、硫酸根、硫代硫酸根、草酸根、硫氰酸根等)的定量问题。HSS中的羧酸根离子(如乙酸根、甲酸根、丙酸根、乙醇酸根等)因化学结构相似难以有效分离,因此难以准确定量[10-11]。寻找一种简便、准确定量HSS 中羧酸盐的方法,具有重要意义。现有分析有机羧酸盐的方法有离子排斥色谱法和高效液相色谱法。牟世芬等[12]研究了36 种有机羧酸根离子的排斥色谱分离行为。
本工作采用高效液相色谱-紫外光谱法建立了定量醇胺溶液中乙醇酸根、甲酸根、乙酸根、丙酸根的方法,对色谱柱、色谱分离条件等进行了选择和优化,并考察了该方法的精密度和准确性。
1 实验部分
1.1 主要仪器与试剂
LC-20AD 型液相色谱仪(配有紫外吸收检测器)、Intersil ODS-3 型色谱柱(4.6 mm×250 mm×5 μm):日本Shimadzu 公司;Kromasil 100-5-C18 型色谱柱(4.6 mm×250 mm×5 μm):瑞典 AkzoNobel公司;InfinityLab Poroshell 120 EC-18 型色谱柱(4.6 mm×100 mm×2.7 μm):美国Agilent 公司;PC HILIC 型色谱柱(2.0 mm×100 mm×3 μm):日本Shiseido 公司;Thermo Dionex Acclaim Mixed-Mode WAX-1 型色谱柱(4.6 mm×250 mm×5 μm):美国Thermofisher 公司。
磷酸氢二铵、磷酸:分析纯,成都市科隆化学品有限公司;乙腈:色谱纯,西陇科学股份有限公司;乙醇酸盐标准溶液:乙醇酸根质量浓度为1 000 μg/mL,北京北方伟业计量技术研究院;丙酸盐标准溶液:丙酸根质量浓度为1 000 μg/mL,天津阿尔塔科技有限公司;乙酸盐标准溶液(乙酸根质量浓度为1 000 μg/mL)、甲酸盐标准溶液(甲酸根质量浓度为1 000 μg/mL):美国Inorganic Ventures 公司。5 份醇胺溶液试样来源于新疆、广西等地。
1.2 标准工作溶液配制
分别准确移取乙醇酸盐、乙酸盐、甲酸盐、丙酸盐标准溶液5.00,2.50,1.25,0.50,0.25 mL 至25 mL 容量瓶中,用去离子水定容,得到质量浓度依次为200,100,50,20,10 μg/mL 的5 种羧酸根混合标准工作溶液,记作标准工作溶液1#~ 5#。
1.3 试样前处理
准确移取0.5 mL 待测醇胺溶液至10 mL 容量瓶中,用去离子水定容,经过0.22 μm 滤膜过滤后,作为供试液备用。
1.4 液相色谱分析条件
Thermo Dionex Acclaim Mixed-Mode WAX-1型色谱柱,柱温25 ℃;流动相为7.5%(φ)乙腈+92.5%(φ)磷酸氢二铵水溶液(用磷酸调节pH 至6.0,浓度为20 mmol/L),流量1.0 mL/min,等度洗脱;检测器为紫外检测器,波长为210 nm;进样体积10 μL。
2 结果与讨论
2.1 液相色谱分析条件的优化与确定
2.1.1 基本操作条件的确定
实验所分析的乙醇酸根、甲酸根、乙酸根和丙酸根,仅具有一个羧酸根,缺少其他助色基团,导致紫外吸收较弱,它们的紫外吸收最大波长(λmax)通常小于200 nm。在液相色谱分析过程中,为使待测羧酸根离子有足够的灵敏度,需采用溶剂截止波长(λUV)远小于200 nm 的流动相体系。液相色谱分析中最常用的3 种溶剂乙腈、甲醇和水的λUV分别是190,205,180 nm,磷酸盐溶液通常无紫外吸收[13],因此,选择乙腈、水及磷酸盐缓冲溶液作为流动相的主体。
尽管羧酸根离子的λmax小于200 nm,但此波长已属于近紫外区范围,多数化合物在200 nm 附近均有吸收,为了避免相互干扰,选择210 nm 作为检测波长[14-15]。
2.1.2 色谱柱的选择
采用Intersil ODS-3,Kromasil 100-5-C18,InfinityLab Poroshell 120 EC-18 等常用反相C18 型色谱柱对乙醇酸根、乙酸根、甲酸根、丙酸根进行分离[12],发现这些羧酸根离子由于亲水性太强,在C18 型色谱柱上保留值较低,无法有效分离。在反相色谱模式无法分离小分子羧酸化合物的情况下,尝试采用亲水作用色谱模式和混合模式(阴离子交换、反相色谱)进行有效分离。初步实验结果表明,采用PC HILIC 型色谱柱,基于亲水作用色谱模式,用10%(φ)甲醇-水等度洗脱,小分子羧酸化合物无法有效分离;而在混合分离模式下,4 种羧酸根离子在Thermo Dionex Acclaim Mixed-Mode WAX-1 型色谱柱上的分离度明显提高,分离效果明显改善。因此,选择Thermo Dionex Acclaim Mixed-Mode WAX-1 型色谱柱。
2.1.3 色谱柱分离条件的优化
参考Thermo Dionex Acclaim Mixed-Mode WAX-1 型色谱柱的使用手册及混合分离模式的特点[16],主要从流动相离子强度、有机改性剂浓度、流动相pH、色谱柱温度等方面进行优化。
首先考察了色谱柱温度为25 ℃时,浓度为20,30,40 mmol/L 的磷酸氢二铵水溶液(pH=6.0)流动相对4 种羧酸根保留行为的影响。流动相离子强度(即磷酸氢二铵的浓度)对4 种羧酸根离子色谱的影响见图1。由图1 可知,随着流动相离子强度的增加,4 种羧酸根的保留时间缩短,乙酸根与甲酸根之间的分离度由1.08 降至共同洗脱。从有效分离和延长色谱柱寿命的角度考虑,选择20 mmol/L 的磷酸氢二铵水溶液作为流动相主体。
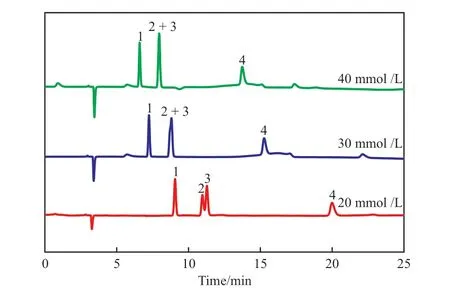
图1 流动相离子强度对4 种羧酸根离子色谱的影响Fig.1 Effect of ionic strength of mobile phase on the chromatography of four types of carboxylate ions.
为了考察有机改性剂(乙腈)对色谱分离行为的改善效果,向20 mmol/L 的磷酸氢二铵水溶液(pH=6.0)中添加体积分数分别为2.5%,5.0%,7.5%,10.0%的乙腈作为流动相,并在色谱柱温度为25 ℃条件下进行测试。有机改性剂添加量对4种羧酸根离子色谱的影响见图2。由图2 可知,随着有机改性剂用量的增加,4 种羧酸根的保留时间均缩短,乙酸根和甲酸根之间的分离效果逐渐变好(分离度从1.08 变成完全分离)。在不影响分离效果的前提下,考虑到待测主体是含有一定有机物的醇胺溶液,为保持流动相主体对有机物的洗脱能力,控制有机改性剂的体积分数为7.5%。
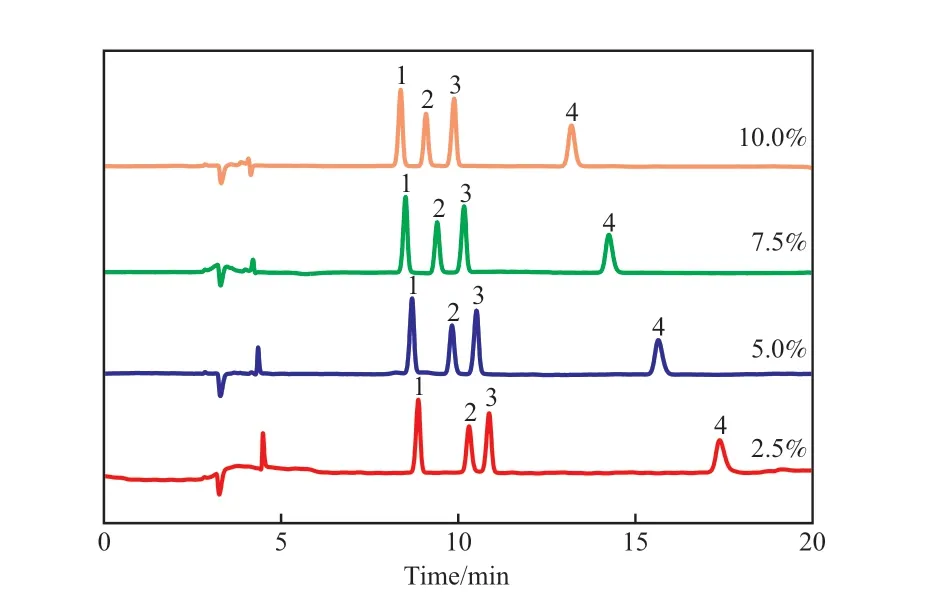
图2 有机改性剂添加量对4 种羧酸根离子色谱的影响Fig.2 Effect of the additional amount of organic modifier on the chromatography of four types of carboxylate ions.
采用10%(φ)的磷酸溶液调节流动相(20 mmol/L的磷酸氢二铵水溶液)的pH分别至4.0,5.0,6.0,并在色谱柱温度为25 ℃条件下进行测试,流动相pH 对4 种羧酸根离子色谱的影响见图3。
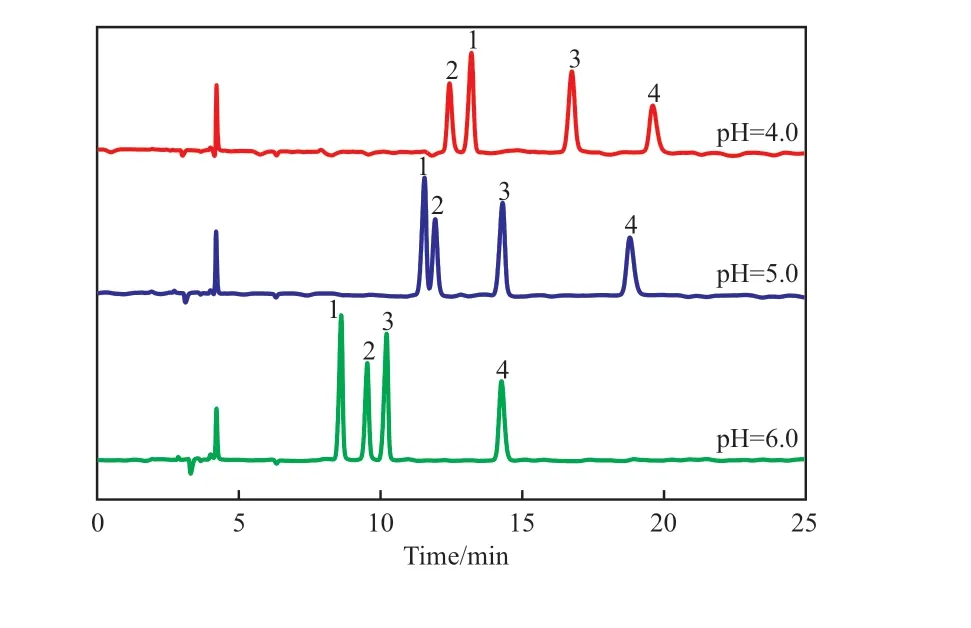
图3 流动相pH 对4 种羧酸根离子色谱的影响Fig.3 Effect of the pH of mobile phase on the chromatography of four types of carboxylate ions.
由图3 可知,随着流动相pH 的降低,4 种羧酸根离子的解离受到抑制,亲水性降低,导致保留时间延长;同时pH 的降低明显改变了乙醇酸根和乙酸根的保留行为,在pH 为4.0 时,乙酸根的出峰时间移至乙醇酸根之前。pH 为6.0 时,乙醇酸根、乙酸根、甲酸根、丙酸根的保留时间分别为8.611,9.532,10.217,14.282 min。从单次分析时长的角度考虑,选择流动相的pH 为6.0。
在流动相离子强度为20 mmol/L、pH 为6.0、有机改性剂乙腈体积分数为7.5%的条件下,进一步考察色谱柱温度分别为20,25,30,35 ℃时对分离结果的影响。实验结果表明,在考察的温度范围内,4 种羧酸根的保留行为无明显差异。
综合色谱分离要素的优化情况,从实际取得的分离效果、色谱柱的寿命、单次分析时长等方面考虑,选择含7.5%(φ)乙腈的磷酸氢二铵水溶液(20 mmol/L,pH=6.0)作为流动相、色谱柱温度为25 ℃以及等度洗脱,作为分析醇胺溶液中乙醇酸根、乙酸根、甲酸根和丙酸根含量的测试条件。2.1.4 试样初步测试情况
在选定的测试条件下,对实际醇胺溶液试样进行初步测试,实验结果表明,溶液中待测的4 种羧酸根离子均能有效分离和定量,无干扰。
2.2 分析方法学研究
2.2.1 精密度实验
仪器精密度实验:取标准工作溶液2#,在优化后的测试条件下平行测试6 次。实验结果为:4 种羧酸根离子色谱峰面积的相对标准偏差为1.21%~2.07%,表明仪器的精密度好。
方法精密度实验:取实际醇胺溶液试样,平行测试6 次。实验结果为:4 种羧酸根离子色谱峰面积的相对标准偏差为1.49%~3.31%,表明该方法性能稳定,精密度好。
2.2.2 标准工作曲线取标准工作溶液1#~5#进行分析,以相应组分的色谱峰面积为纵坐标(y)、离子质量浓度为横坐标(x)进行线性回归,拟合得到标准工作曲线及线性相关系数(r)。乙醇酸根:y=1 710x-1 997,r=0.999 8;乙酸根:y=1 263x-1 407,r=0.999 9;甲酸根:y=1 706x+1,r=0.999 3;丙酸根:y=1 505x-1 131,r=0.999 8。该结果表明,4 种羧酸根离子在质量浓度为10 ~ 200 μg/mL 时,标准曲线的r均大于0.999 0,线性关系良好,可用于定量分析。
2.2.3 回收率实验
取1.3 节中的供试液3 份,分别加入质量浓度为200 μg/mL 的标准工作溶液1#0.5,1.0,2.0mL,用去离子水定容后进样分析,计算回收率,结果见表1。由表1 可知,3 个质量浓度水平下的回收率为94%~104%,表明该方法测试结果可靠。
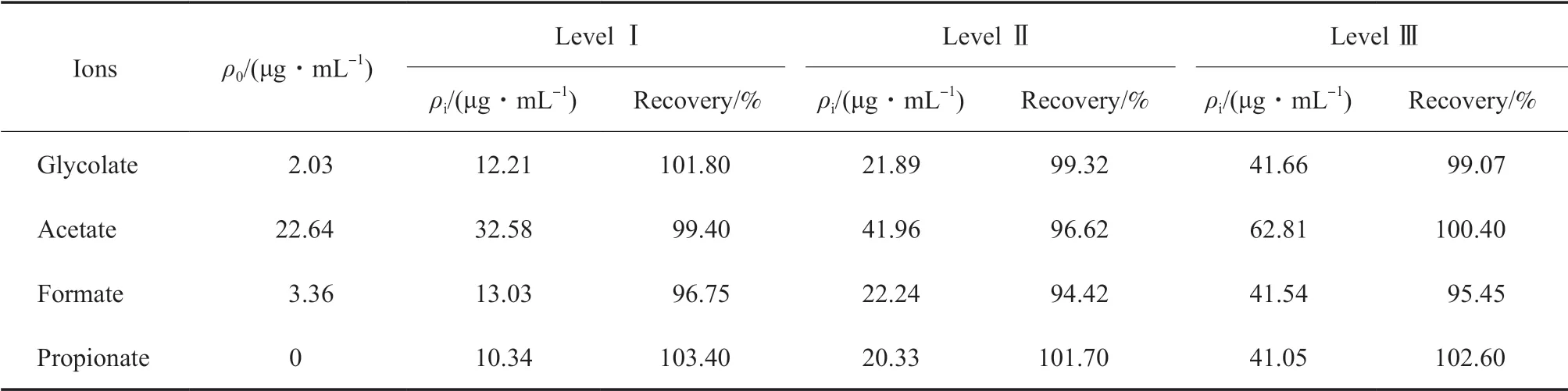
表1 回收率实验结果Table 1 Recovery of the determination method
2.2.4 方法的检出限和定量限
依据基线噪声的3 倍作为检出限、10 倍作为定量限的原则,以各离子色谱峰的峰高计算对应离子的检出限和定量限,结果见表2。由表2 可知,该方法的检测灵敏度低于离子交换色谱法,但依然能够满足实际检测需求。
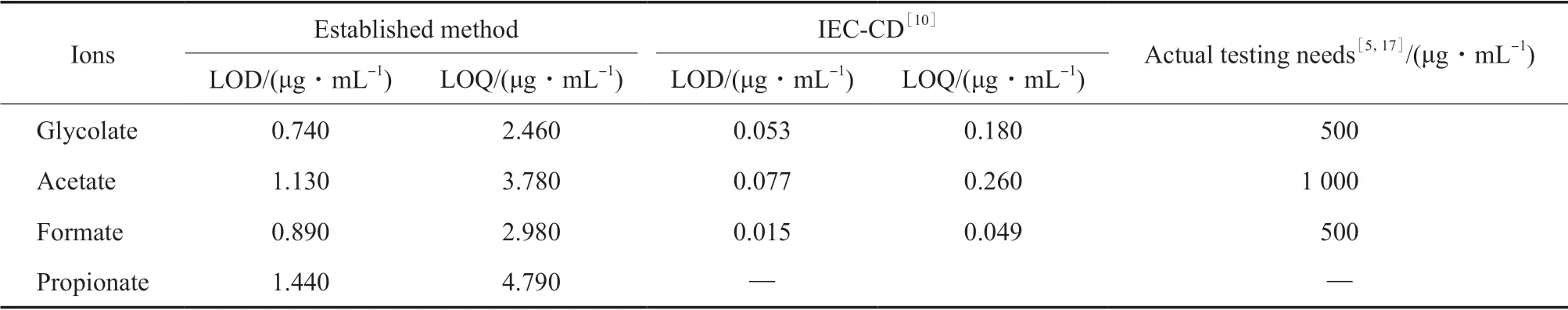
表2 本方法与离子交换色谱法测定4 种羧酸根离子的检出限、定量限及各离子的检测需求Table 2 Comparison of LOD and LOQ between the established method and ion exchange chromatography for the determination of four types of carboxylate ions and the actual testing needs
2.3 实际试样分析结果
测定了5 份不同来源的醇胺溶液中4 种羧酸根离子的含量,结果见表3。由表3 可知,5 份试样中的羧酸盐主要为乙酸盐和甲酸盐,含少量乙醇酸盐,均未检测到丙酸盐。这表明该检测方法能够有效定量不同来源的醇胺溶液中有机羧酸盐的含量,可作为离子交换色谱法测定HSS 含量的补充,同时能够为探究不同使用条件下醇胺溶液中羧酸盐的形成原因及影响因素提供参考。

表3 5 份醇胺溶液中4 种羧酸根离子的含量测定结果Table 3 Results of four types of carboxylate ions in five alcohol amine solution samples
3 结论
1)建立了基于高效液相色谱-紫外光谱法测定醇胺溶液中乙醇酸根、乙酸根、甲酸根、丙酸根含量的分析方法,并对影响色谱分离效果的主要因素(如色谱柱、分离模式、流动相)进行了考察和优化。
2)在优化的分离条件下进行了分析方法研究,结果显示,建立的测试方法具有良好的精密度、重复性和准确度,能够用于实际醇胺溶液的分析,具有良好的使用价值。
3)与常用的离子色谱分析法相比,该方法选择性更好,分离性能更佳,不足之处是检测灵敏度较离子交换色谱法有所降低。
