ERAS策略在腹腔镜保留脾脏的胰体尾切除术中的应用
2022-01-09钱建平朱碧娟张起帆王恺孙世波朱碧丽李加付霞张思云李欢娱谭清周杰
钱建平,朱碧娟,张起帆,王恺,孙世波,朱碧丽,李加,付霞,张思云,李欢娱,谭清,周杰
(南方医科大学南方医院,广东 广州 510515,1.普通外科学肝胆胰外科,2.惠侨医疗中心)
随着对脾脏免疫、造血、抗肿瘤及抗感染等相关功能的深入研究与认识,以及在尽量保留健康器官功能的要求下,越来越多的学者选择保留脾脏的胰体尾切除术(spleen-preserving distal pancreatectomy,SPDP)来治疗胰体尾良性或低度恶性肿瘤。保留脾脏并不影响肿瘤根治性,且可避免脾切除术后相关并发症,对于患者远期预后有益,能改善其生活质量[1]。SPDP可以分为两种术式,即Kimura法和Warshaw法。Kimura法在切除胰体尾的同时全程解剖出脾动脉、脾静脉并予以保留,Warshaw法则将脾动静脉主干与胰体尾一并切除,但需保留胃网膜左血管和胃短、胃后血管以维持脾脏血供。近年来,随着腹腔镜技术的进展,腹腔镜保留脾脏的胰体尾切除术(laparoscopic spleen-preserving distal pancreatectomy,LSPDP)逐渐成为治疗胰体尾良性和低度恶性肿瘤的标准术式[2],其在保证肿瘤根治的基础上,兼具微创、术野清晰、操作精准等特点,患者术后创伤应激小、疼痛轻、感染率低、恢复快,术后并发症和远期生存率与开腹手术无统计学差异[3-4]。从解剖学层面来看,LSPDP操作相对困难,术中大出血等风险较高,对手术团队要求更高[5]。目前开展LSPDP的中心越来越多,不少文献肯定了LSPDP的安全性和可行性,部分研究结果显示,相对于腹腔镜胰体尾联合脾切除术(laproscopic distal pancreatectomy with splenectomy,LDPS),LSPDP不增加手术时间及术中出血量,并可缩短住院时间,保留脾脏的患者术后生活质量要优于联合脾脏切除的患者[6-9]。国内也有不少采用Kimura法实施LSPDP的成功报道[10-11]。本研究回顾性分析南方医科大学南方医院近年收治的胰体尾良性病变和低度恶性肿瘤行腹腔镜胰体尾切除术的患者临床资料,现报道如下。
1 资料和方法
1.1 一般资料
收集2018年6月至2020年12月本中心收治的38例胰体尾良性病变和低度恶性肿瘤行腹腔镜胰体尾切除术的病例资料。根据手术是否保留脾脏分为保脾组和切脾组,保脾组23 例(实施Kimura法20 例,Warshaw法3例),切脾组15例。术前常规行腹部彩超、增强CT和(或)MRI检查,查血CA199、CEA、AFP等肿瘤标志物,术后病理均证实为胰体尾良性或低度恶性肿瘤。保脾组中胰腺单纯囊肿1 例,浆液性囊腺瘤10 例,黏液性囊腺瘤4 例,导管内乳头状黏液肿瘤(intraductal papillary mucinous neoplasm,IPMN)1例,实性假乳头状瘤1例,胰腺神经内分泌肿瘤(pancreatic neuroendocrine tumor,PNET)5例(G1 2例,G2 3例),囊性淋巴管瘤1例;切脾组中浆液性囊腺瘤3例,黏液性囊腺瘤5例,IPMN 1例,实性假乳头状瘤2例,PNET 4例(G1 2例,G2 2例)。
1.2 手术方法
Kimura法LSPDP:采用“V”字型5孔法。超声刀打开胃结肠韧带,暴露胰腺,确定病灶位置、大小及毗邻关系,决定手术方式。在胰腺上缘解剖分离脾动脉主干,必要时悬吊;在胰腺下缘打开胰后间隙,寻找脾静脉并适当游离;避开脾动静脉,在病灶右侧1~2 cm处离断胰腺;牵拉远端胰腺,沿脾动静脉与胰腺之间的疏松组织向胰尾侧解剖,将脾动静脉从胰腺实质内分离出来,妥善处理脾动静分支(结扎或缝扎)(图1A~B)。接近脾门时打开脾结肠韧带及部分脾胃韧带,辨认脾动静脉分支走行,离断细小穿支血管,解剖分离胰尾周围间隙(图1C),最终切除胰体尾。胰腺断端使用3-0 Prolene线缝合(图1D),检查无出血,于胰腺断端处放置双腔引流管。
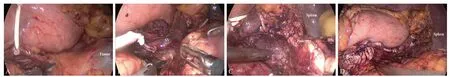
图1 腹腔镜保留脾脏的胰体尾切除术中操作图(Kimura法)
Warshaw法LSPDP:前面步骤同Kimura法,当发现脾动静脉难以分离时,在病灶右侧1~2 cm处结扎脾动静脉主干并离断;然后向胰尾方向分离,将脾血管连同胰体尾一并游离切除,保护好胃后血管、胃网膜左血管和胃短血管。注意观察脾脏血运。
LDPS手术方法参照Warshaw法,在此基础上游离脾周韧带,一并切除脾脏。
1.3 围术期ERAS策略
参考《加速康复外科中国专家共识及路径管理指南(2018版)》[12]中的胰十二指肠切除术章节实施。入院后行ERAS宣教,术前禁食2 h、禁水6 h,不留置胃管;术后鼓励患者早期下床活动,尿管一般在术后24 h内拔除,术后第1天进全流食,如无胰瘘,尽早恢复半流质饮食。围术期实施“术前超前镇痛+多模式镇痛”方案。常规放置腹腔引流管,术后结合引流液性状、流量及淀粉酶水平,决定拔管时机。对于术后第1、3天引流液淀粉酶均<5 000 U/L者,如引流液量不多,早期拔管;对于胰瘘高风险的病例(引流液淀粉酶>5 000 U/L),经引流管做冲洗处理,酌情延缓进食时间并延长生长抑素使用时间,并结合引流液量及淀粉酶水平的变化决定具体拔管时机。
1.4 术后处理及随访
动态监测腹腔引流液淀粉酶水平,胰瘘的诊断标准参照国际胰瘘研究小组(International Study Group on Pancreatic Fistula,ISGPF)2016版的诊断与分级标准[13]。出院前复查腹部CT,出院后患者均于门诊随访,内容包括上腹部B超或CT、血常规、肝功能、肿瘤标志物等。
1.5 统计学分析
采用SPSS 28.0统计软件,计量资料符合正态分布的以()表示,两组之间比较采用独立样本t检验;偏态分布数据以M(P25~P75)表示,两组之间比较采用秩和检验(Mann-WhitneyU检验);计数资料组间比较采用χ2检验或Fisher确切概率法;以P<0.05为差异有统计学意义。
2 结果
2.1 两组术前资料和手术情况比较
两组在性别、年龄、肿瘤大小方面差异均无统计学意义(P>0.05),具有可比性。保脾组与切脾组相比较,手术时间、术中失血量、术后引流管拔除时间及术后住院时间差异均无统计学意义(P>0.05),详见表1。全组中位引流管拔除时间为6(5~7)d,保脾组为7(4~7)d,切脾组为6(5~7)d。

表1 保脾组和切脾组的术前资料和手术情况
2.2 术后并发症及处理
两组围术期无死亡,保脾组有1 例腹腔出血,2例B级胰瘘,其余患者无严重并发症;术后并发症方面两组之间差异无统计学意义(P>0.05),详见表2。1例LSPDP患者,术后第2天发现腹腔出血,再次手术探查止血,发现是脾静脉分支出血,缝扎止血并行脾切除。2例B级胰瘘患者,均予冲洗引流等处理,待引流量减少后再拔管;其中1例于术后22 d拔除腹腔引流管(上述二次手术患者),另1例术后15 d带引流管出院,前期仍予间断冲洗,后期无冲洗,术后45 d复查时行造影检查显示引流管周围已包裹,予适当冲洗后即拔除引流管。

表2 保脾组和切脾组的术后并发症发生率比较[例(%)]
2.3 随访
患者出院后均进行门诊随访,随访时间3~18个月,均无肿瘤复发、转移,保脾组无脾梗死发生。3例Warshaw法LSPDP者,术后随访期间未发现有食管胃底静脉曲张破裂出血。
3 讨论
3.1 LSPDP手术安全性
对于胰腺体尾良性和低度恶性肿瘤患者目前多主张行腹腔镜保留脾脏的胰体尾切除术,不但体现了微创优势,还可避免无辜脾脏的切除以及脾切除术后的相关并发症[4,7,14]。已有不少文献证实了LSPDP手术的安全性,本中心数据也显示腹腔镜保脾胰体尾切除手术是可行的,保脾组与切脾组相比,手术时间、术中失血量、术后腹腔引流管拔除时间、术后严重并发症发生率、术后住院时间等没有统计学差异。因此,从保留器官功能的角度来讲,更推荐对于胰腺体尾良性和低度恶性肿瘤患者实施LSPDP。本组20例Kimura法完成者中有8例病灶最大径超过5 cm,尽管肿瘤偏大,但良性病灶尤其是囊性病变与脾血管之间往往存在间隙,大部分情况下可以解剖分离,提示对于肿瘤偏大者仍可考虑实施Kimura法LSPDP。
3.2 LSPDP手术操作经验
Kimura法LSPDP技术难点是如何将脾动、静脉全程安全游离以及发生出血时的控制、处理,这是手术成败关键,也是保障患者术中安全的要点。我们的体会是:脾动脉往往有鞘外层次可供分离,脾静脉壁薄易撕裂,因此解剖分离时更要小心。对于部分胰尾处相对容易解剖的病例,可以事先解剖肿瘤远处的脾静脉,术中万一出现脾静脉出血可以从容控制;可以用腔镜下血管阻断夹来控制出血并解放术者器械。此外,为了减少术后出血的发生,术中尤其应警惕血管断端回缩、结扎夹脱落等风险,额外缝扎脾血管分支断端更为确切。研究组有1 例Kimura法行LSPDP的患者,术后第2天发现腹腔出血,探查发现是脾静脉分支出血所致。
3.3 ERAS策略的具体实施
大部分ERAS措施在胰腺手术中实施没有异议,胰体尾切除术ERAS实施的关键和争议点在于能否早期拔除腹腔引流管。2012年欧洲《胰十二指肠切除围术期ERAS指南》及2019 更新版[15]建议,对于胰瘘低风险患者(术后第3 天腹腔引流液淀粉酶<5 000 U/L),可于术后早期(72 h)拔除腹腔引流管;《加速康复外科中国专家共识及路径管理指南(2018版)》在胰十二指肠切除术章节中,也有类似阐述[12]。本中心对于腹腔引流液淀粉酶>5 000 U/L的胰瘘高风险者,进行冲洗引流,再动态监测腹腔引流液量及淀粉酶水平变化,待引流液淀粉酶<5000 U/L且引流量不多时,再适时拔管,大部分病例可在术后7 d左右拔管;胰瘘低风险者则自然引流。待引流液量不多时即予拔管。对于引流液量较多(>100 mL/d)或引流液淀粉酶水平居高不下者,则加强引流,延缓拔管时间。以往文献显示胰体尾切除术后胰瘘发生率约10%~30%[16],本研究中共有2 例B级胰瘘,发生率为5.26%,后期均不需要再穿刺引流,全组中位引流管拔除时间为6(5~7)d,保脾组为7(4~7)d,除去2例B级胰瘘患者,保脾组中位拔管时间为5(4~7)d。由此可见,这种处理策略安全可行,腹腔镜胰体尾切除术后可以按照ERAS理念实施早期拔除腹腔引流管。
综上所述,对于胰体尾良性和低度恶性肿瘤,保留脾脏的胰体尾切除术可作为首选,提倡在大型胰腺外科中心由具备丰富腹腔镜手术经验的医师实施LSPDP,娴熟的腔镜下血管缝合技术及默契的团队配合往往是手术成败的关键。LSPDP围术期实施ERAS策略,是安全可行的,尤其是术后针对腹腔引流管的评估和处理,可以按照ERSA模式下的早期拔管理念实施。
