具有甜味抑制作用的2-(4-甲氧基苯氧基)丙酸衍生物的构效关系
2022-01-06邓雯婷李加兴郑建仙
邓雯婷,李加兴,郑建仙,*
(1.华南理工大学食品科学与工程学院,广东 广州 510640;2.湖南省井矿盐工程技术研究中心,湖南 长沙 410004)
甜味是人们偏爱的基本味。然而,以蔗糖为代表的甜味剂在发挥提供能量、改善质地、提升风味、抑菌防腐等重要作用时,容易产生令人不愉悦的甜腻口感,影响其他风味的释放[1]。甜味抑制剂正是解决食品“过甜”问题的一类化合物[2],在保持甜味剂有益功能特性的同时,降低它们对味蕾的甜味刺激。
2-(4-甲氧基苯氧基)丙酸(2-(4-methoxyphenoxy)propionic acid,HPMP,图1)是目前应用最为广泛的甜味抑制剂,在我国已经使用15 年之久。HPMP对于多种甜味物质均有显著的甜味抑制作用[3],不仅解决月饼、果酱、巧克力等传统高糖食品甜度太高的实际难题,推动食品工业发展,还能有效改善高能食品和运动食品的食用品质,促进我国体育强国战略的实现。HPMP作用迅速,持续时间短暂,并且在作用后的一段时间内,喝纯水会有微甜的感觉[4]。但是,它也存在明显的缺陷,在实际使用时可能影响某些食品的原有风味,在高添加量时也会伴随异味刺激。
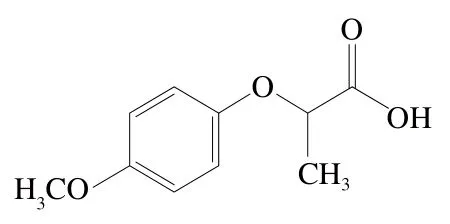
图1 HPMP的结构图Fig. 1 Structure of HPMP
因此,深入探究HPMP的构效关系,对于开发高强度、兼具更少异味的新型甜味抑制化合物,扩展其在食品工业生产的应用具有重要意义。但国内外目前对于HPMP的研究多集中于它的制备[5-6]和应用[7],其构效关系有待阐明。有报道称HPMP的对位取代对活性的影响颇为明显[8],对位基团的疏水性是其发挥甜味抑制作用的重要因素[9]。然而,其他疏水基团修饰对位后是否同样具有甜味抑制作用,以及对位疏水基团的变化对抑制效果影响的相关研究却比较空白。
甜味评价手段主要包括人群感官评价、钙离子成像技术和电子舌味觉分析技术[10]。人群感官评价是最常用的味觉评价方法,却极易受到参与者生理、心理等主观因素的影响,不适用于安全性未知的物质。钙离子成像技术通过甜味感应细胞中钙离子的浓度变化来反映甜度,但如何构建稳定表达甜味受体蛋白的细胞株是一大挑战[11]。电子舌具有灵敏度高、准确性高和重复性好等优势,对样品安全性要求不高,在甜味评价方面应用潜力巨大。杨阳等[12]利用电子舌准确区分5 种不同组成的甜菊糖,并且甜度识别结果与感官评定结果基本吻合。黄嘉丽等[13]研究显示电子舌能够实现蔗糖、安赛蜜、糖精钠、新橙皮苷二氢查耳酮、柚苷二氢查耳酮多种甜味剂的甜度预测。另外,电子舌在掩味效果评价方面也有良好的应用,电子舌用于医药品的苦味遮蔽研究屡见不鲜[14-16],但有关甜味抑制效果的电子舌评价方法鲜有报道。
本研究针对HPMP苯环对位进行修饰,合成HPMP及其衍生物(A1~A4),通过傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FTIR)、核磁共振波谱(nuclear magnetic resonance,NMR)进行结构表征,建立甜味抑制效果的电子舌评价方法,分析HPMP及其衍生物的甜味抑制效果和自身呈味特征,探索HPMP的构效关系,以期为新型甜味抑制剂的开发和甜味抑制机理的完善提供可靠的理论指导。
1 材料与方法
1.1 材料与试剂
蔗糖 河南万邦实业有限公司;木糖醇、果糖、山梨糖醇 深圳鸿海食品科技有限公司;所有甜味剂均为食品级。
对甲酚、2-氯丙酸、对氯苯酚、4-丙氧基苯酚上海麦克林生化科技有限公司;4-甲氧基苯酚、4-乙氧基苯酚 上海阿拉丁生化科技有限公司;硫酸 广州化学试剂厂;氢氧化钠、碳酸氢钠 福晨化学试剂有限公司;乙醇 天津富宇精细化工有限公司。以上试剂均为分析纯。
1.2 仪器与设备
DT500A电子天平 常熟市意欧仪器仪表有限公司;SHA-C恒温水浴振荡器 江苏省金坛市农仪器厂;pH-25 pH计 上海精密科学仪器有限公司;AVANCE III HD超导核磁共振波谱仪、VERTEX 33 FTIR仪 德国Bruker公司;SA402B电子舌 日本Insent公司。
1.3 方法
1.3.1 HPMP及其衍生物的合成
HPMP及其衍生物A1~A4的合成路线如图2所示。具体操作参照文献[6,17]并稍作修改,在250 mL圆底烧瓶中加入20 mmol 4-甲氧基苯酚和40 mmol氢氧化钠,用30 mL无水乙醇溶解,随后缓慢滴加22 mmol 2-氯丙酸,85 ℃回流反应5 h。反应结束后,50 ℃旋蒸除去乙醇。将产物倒入70 mL蒸馏水中,滴加6 mol/L硫酸溶液,调节溶液pH值为2,析出固形物。将所得固形物溶于饱和碳酸氢钠溶液,过滤除去不溶性杂质,用6 mol/L硫酸溶液再次酸化滤液,调节溶液pH值为2,收集析出的结晶并用体积分数20%乙醇溶液重结晶,过滤并在50 ℃干燥后得到目标产物HPMP。HPMP衍生物A1~A4的合成方法同上。
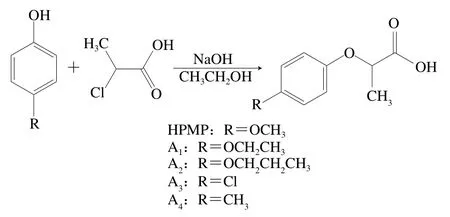
图2 HPMP及其衍生物A1~A4的合成路线Fig. 2 Synthetic routes of HPMP and its derivatives A1-A4
1.3.2 FTIR分析
称取5 mg目标化合物,经溴化钾压片处理后,进行FTIR扫描,扫描范围为4 000~500 cm-1。
1.3.3 NMR分析
称取20 mg目标化合物,用0.6 mL氘代氯仿充分溶解,于室温条件下进行1H-NMR、13C-NMR分析。1H-NMR、13C-NMR共振频率分别为600、151 MHz。
1.3.4 感官评价
参考文献[18]稍作修改,将甜味划分为5 级,配制不同质量浓度的蔗糖溶液作为参比样品,每个等级对应的甜度值和蔗糖溶液质量浓度见表1。从本课题组所在学院的研究生中招募15 名志愿者(6 名男性、9 名女性)组成感官评价小组,所有志愿者在实验前1 h不得进食。取10 mL待口尝样品溶液于透明口尝杯。实验前,志愿者将参比样品溶液含于口中10 s,期间做漱口动作,使舌头充分感受甜味,记下该参比样品溶液对应的甜度值,吐出,用蒸馏水漱口至少4 次,休息30 s后口尝下一个参比样品溶液。志愿者按照上述方法对待测样品进行口尝,根据口尝感受,结合参比样品液的甜度值,给出待测样品的口尝甜度。

表1 甜度值与对应的蔗糖溶液质量浓度Table 1 Sweetness scores and corresponding concentrations of sucrose solutions
1.3.5 电子舌分析
本研究所用的SA402B型电子舌传感器阵列由6个味觉传感器和3 根玻璃管参比电极构成[19],各传感器代表的味觉信息见表2。正式测试前,传感器需进行活化、自检以确保数据的可靠性和稳定性。甜味和酸味、苦味、涩味、鲜味、咸味分开测试。测试甜味时,所有样品重复测试5 次。测试其他味觉时,所有样品重复测试4 次。根据韦伯-费希纳定律,电子舌系统将测得的电势信号转化为对应的味觉值。

表2 各味觉传感器代表的味觉信息Table 2 Taste information represented by various taste sensors
1.3.5.1 电子舌甜味抑制效果评价方法的建立与验证
以蔗糖为研究载体,配制质量浓度15 g/100 mL蔗糖溶液,分别添加终质量浓度分别为0、50、75、100、125、150、200、250 mg/L的HPMP,进行电子舌甜味测定和感官评价,建立甜味抑制效果的电子舌评价方法。
以木糖醇为研究载体,配制质量浓度15 g/100 mL木糖醇溶液,分别添加终质量浓度0、50、75、100、125、150、200、250 mg/L的HPMP,进行电子舌甜味测定和感官评价,验证电子舌甜味抑制效果评价方法的合理性。
1.3.5.2 HPMP及其衍生物的甜味抑制效果评价
选取4 种常用甜味剂蔗糖、果糖、木糖醇、山梨糖醇,评估HPMP及其衍生物A1~A4的甜味抑制效果。分别配制质量浓度15 g/100 mL蔗糖溶液、果糖溶液、木糖醇溶液、山梨糖醇溶液,依次添加终质量浓度分别为0、100、200 mg/L的HPMP和衍生物A1~A4,进行电子舌甜味测定。
1.3.5.3 其他味觉指标测定
配制质量浓度为200 mg/L的HPMP、化合物A1~A4溶液,使用电子舌对HPMP及其衍生物A1~A4的酸味、苦味、涩味、鲜味、咸味5个味觉指标进行测定。
配制质量浓度15 g/100 mL蔗糖溶液各6 份,其中1 份作为空白处理组,另外5 份分别添加终质量浓度为200 mg/L的HPMP、衍生物A1~A4,测定上述5个味觉指标。
1.3.6 甜味抑制效果评价指标测定
感官评价以口尝甜度抑制率为评价指标,考察HPMP及其衍生物A1~A4对甜味剂口尝甜度的抑制作用,口尝甜度抑制率的计算如式(1)所示。将甜味传感器输出的味觉值称为电子舌甜度,电子舌分析以电子舌甜度抑制率为评价指标,考察HPMP及其衍生物A1~A4对甜味剂电子舌甜度的抑制作用,电子舌甜度抑制率的计算如式(2)所示。

式中:Ia为未添加甜味抑制化合物的口尝甜度;Ib为添加甜味抑制化合物的口尝甜度。
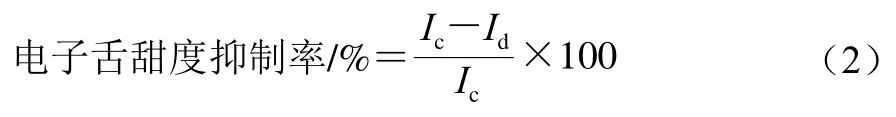
式中:Ic为未添加甜味抑制化合物的电子舌甜度;Id为添加甜味抑制化合物的电子舌甜度。
1.4 数据处理与分析
采用MestReNova 12.0软件进行NMR谱图解析。采用SPSS 22.0软件进行统计分析,使用Ducan检验进行多重比较,P<0.05表示差异显著。采用Origin 2018软件进行绘图。
2 结果与分析
2.1 目标化合物的结构表征
HPMP:白色晶体,FTIR(KBr)v/cm-1:2 950、1 715、1 222、1 043、822。1H NMR(600 MHz,CDCl3):δ6.88~6.81(m,4H,-Ar-H)、4.70(q,1H,J=6.8 Hz,-CH)、3.77(s,3H,-OCH3)、1.63(d,3H,J=6.9 Hz,-CH3)。13C NMR(151 MHz,CDCl3):δ177.55(C=O)、154.77(Ar)、151.22(Ar)、116.72(Ar)、114.80(Ar)、73.25(CH)、55.69(OCH3)、18.45(CH3)。
2-(4-乙氧基苯氧基)丙酸(衍生物A1),白色晶体,FTIR(KBr)v/cm-1:2 975、1 715、1 220、1 045、819。1H NMR(600 MHz,CDCl3):δ6.87~6.80(m,4H,-Ar-H)、4.70(q,1H,J=6.9 Hz,-CH)、3.98(q,2H,J=7.0 Hz,-OCH2)、1.63(d,3H,J=6.9 Hz,-CH3)、1.39(t,3H,J=7.0 Hz,-CH2CH3)。13C NMR(151 MHz,CDCl3):δ177.20(C=O)、154.15(Ar)、151.08(Ar)、116.73(Ar)、115.48(Ar)、73.29(CH)、63.95(OCH2)、18.43(CH3)、14.89(CH3)。
2-(4-丙氧基苯氧基)丙酸(衍生物A2),白色晶体,FTIR(KBr)v/cm-1:2 966、1 717、1 221、1 045、825。1H NMR(600 MHz,CDCl3):δ6.87~6.80(m,4H,-Ar-H)、4.70(q,1H,J=6.8 Hz,-CH)、3.87(t,2H,J=6.6 Hz,-OCH2)、1.82~1.75(m,2H,-OCH2CH2)、1.63(d,3H,J=6.9 Hz,-CH3)、1.02(t,3H,J=7.4 Hz,-CH2CH3)。13C NMR(151 MHz,CDCl3):δ177.42(C=O)、154.36(Ar)、151.06(Ar)、116.72(Ar)、115.49(Ar)、73.29(CH)、70.07(OCH2)、22.64(CH2)、18.44(CH3)、10.52(CH3)。
2-(4-氯苯氧基)丙酸(衍生物A3),白色晶体,FTIR(KBr)v/cm-1:2 993、1 715、1 225、1 043、825。1H NMR(600 MHz、CDCl3):δ7.26~7.22(m,2H,-Ar-H)、6.84~6.80(m,2H,-Ar-H)、4.75(q,1H,J=6.9 Hz,-CH)、1.66(d,3H,J=6.9 Hz,-CH3)。13C NMR(151 MHz,CDCl3):δ177.81(C=O)、155.81(Ar)、129.58(Ar)、126.90(Ar)、116.48(Ar)、72.31(CH)、18.38(CH3)。
2-(4-甲基苯氧基)丙酸(衍生物A4),白色晶体,FTIR(KBr)v/cm-1:2 996、1 712、1 224、1 043、807。1H NMR(600 MHz,CDCl3):δ7.10~7.05(m,2H,-Ar-H)、6.82~6.76(m,2H,-Ar-H)、4.75(q,1H,J=6.9 Hz,-CH)、2.28(s,3H,-CH3)、1.64(d,3H,J=6.9 Hz,-CH3)。13C NMR(151 MHz,CDCl3):δ178.06(C=O)、155.04(Ar)、131.33(Ar)、130.11(Ar)、115.08(Ar)、72.24(CH)、20.50(CH3)、18.44(CH3)。
2.2 基于电子舌的甜味抑制效果评价方法的建立与验证
基于人工脂膜技术,电子舌可以模拟人的口腔味蕾对不同类型甜味物质的感知[20]。利用电子舌法和口尝法分析不同质量浓度的HPMP对蔗糖甜度的影响,结果见图3A。由图3A可知,随着HPMP质量浓度的增加,HPMP对蔗糖的电子舌甜度和口尝甜度的抑制作用逐渐增强,这一发现与HPMP竞争性抑制的机制[21]相符,电子舌在一定程度上可以反映HPMP的甜味抑制规律。为进一步验证甜味抑制效果的电子舌评价方法的可行性,选取与蔗糖甜度相当的木糖醇作为甜味载体,测定不同质量浓度HPMP的电子舌甜度抑制率和口尝甜度抑制率,结果如图3B所示。在实验质量浓度范围内,HPMP同样抑制了木糖醇溶液的电子舌甜度,抑制作用呈现浓度依赖性,并且电子舌甜度抑制率和口尝甜度抑制率的变化趋势相对一致。在电子舌抑制苦味效果评价研究中,甜味剂类苦味抑制剂会通过占据苦味物质在传感膜上的结合位点,导致电子舌对苦味物质的不敏感[22],推测HPMP以相同的原理降低甜味剂的电子舌甜度。对于2 种甜味剂,感官评价的测定值误差明显偏大,提示电子舌用于甜味抑制效果评价具有更高的精确度。对电子舌甜度抑制率和口尝甜度抑制率进行相关性分析,二者具有良好的线性相关性(P<0.01),对于蔗糖和木糖醇,电子舌结果和口尝结果的决定系数分别为0.969、0.983。综上,电子舌法和感官评价法对HPMP的甜味抑制效果的评价基本等效。电子舌有望代替人工感官成为科学、客观的甜味抑制效果评价手段,可为后续甜味抑制研究提供重要借鉴。
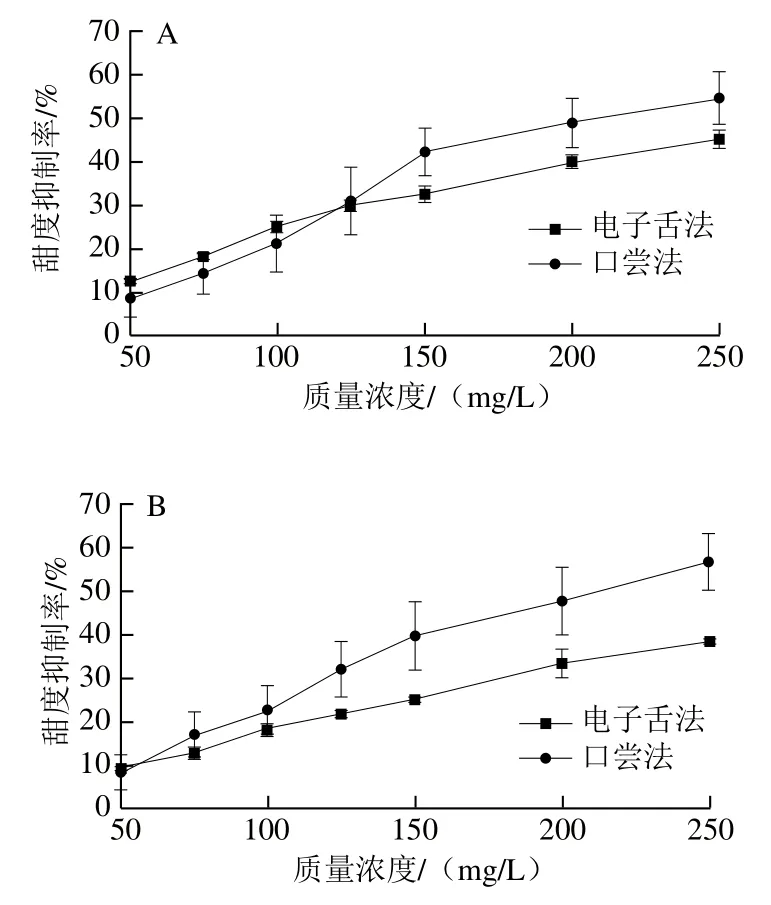
图3 不同质量浓度的HPMP对蔗糖(A)和木糖醇(B)的甜味抑制作用Fig. 3 Sweetness inhibitory activities of HPMP at different concentrations on sucrose (A) and xylitol (B)
2.3 HPMP及其衍生物对甜度的影响
图4A~D分别为HPMP及其衍生物对蔗糖、果糖、木糖醇、山梨糖醇电子舌甜度的影响。如图4所示,针对HPMP苯环对位进行不同的疏水性基团修饰后,其衍生物对4 种甜味剂仍展现出一定的甜味抑制作用,而且随着添加量的增加,各化合物的甜味抑制效果愈加明显。衍生物A1~A4对果糖、木糖醇、山梨糖醇的电子舌甜度抑制率相对较低,可能是电子舌对甜味物质的敏感程度不同所致。黄嘉丽等[13]研究显示等甜度不同类型甜味剂的电子舌甜味值会存在较大差异。因此,目前无法通过电子舌甜度抑制率直接比较同一甜度抑制化合物对多种甜味剂的抑制作用。
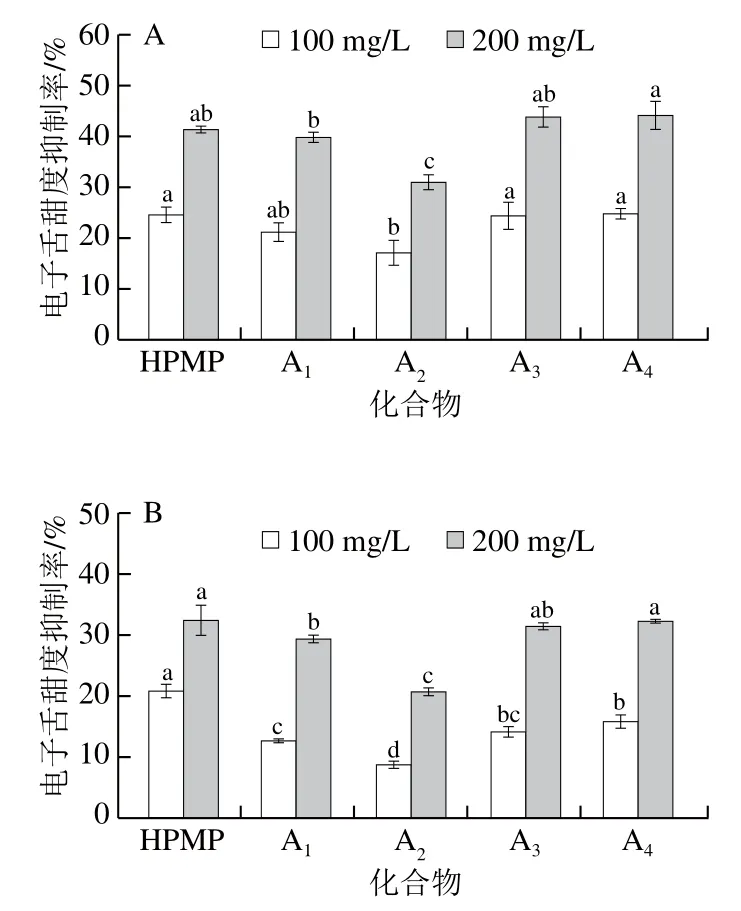
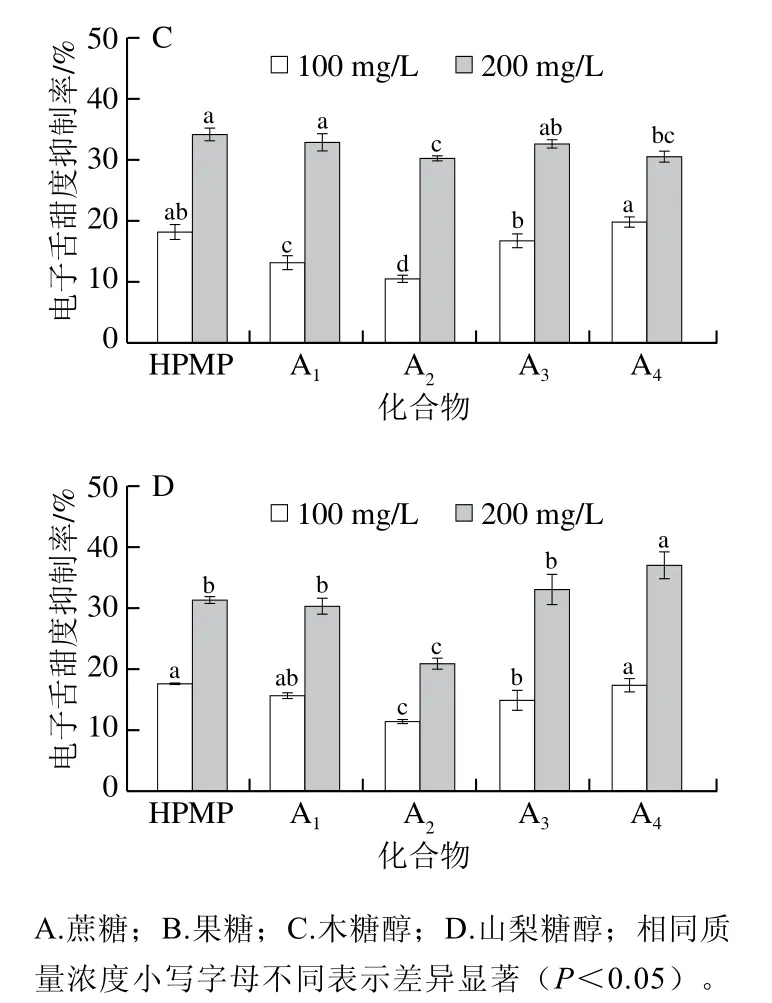
图4 HPMP及其衍生物A1~A4对4 种甜味剂的电子舌甜度的影响Fig. 4 Effects of HPMP and its derivatives A1-A4 on electronic tongue sweetness intensity of four sweeteners
研究表明HPMP的疏水性会阻碍甜味受体对甜味物质的识别,进而达到降低甜度的目的[23]。尝试以疏水性更强的基团替代对位的甲氧基,当不同的烷氧基修饰苯环对位时,在实验质量浓度下,对于4 种甜味剂的甜味抑制程度均为:甲氧基>乙氧基>丙氧基,甜味抑制作用随对位基团疏水性的增强反而减弱,丙氧基的修饰对甜味抑制作用的不利影响尤为明显,这一发现与Acree等的研究结论[24]相符。以其他疏水性更强的基团修饰对位时,甲基修饰的A4和氯原子修饰的A3的甜味抑制效果与HPMP相近。对于蔗糖,在实验质量浓度下,A3、A4的甜味抑制率均高于HPMP,但在抑制效果方面无显著性差异;对于果糖,在低添加量时,HPMP的甜味抑制效果显著强于A3、A42 种衍生物(P<0.05),抑制作用程度为:HPMP>A4>A3,但随着添加量的提高,三者的甜味抑制作用差异不显著;对于木糖醇,在高添加量时,A4的抑制作用显著低于HPMP(P<0.05),但在相同质量浓度下,A4对于山梨糖醇甜度的抑制作用显著高于HPMP(P<0.05)。可见,HPMP及其衍生物A1~A4在甜味抑制效果的差异无法用简单的疏水性强弱来解释。Xia Yi[9]认为HPMP对位的甲氧基增加了芳香环的疏水性和体积,对甜味抑制活性有积极影响。Nakagita等[25]对一些与HPMP碳骨架相似的非甾体消炎药物的甜味抑制活性进行分析,发现甜味受体的结合口袋可以容纳不同体积大小的甜味抑制化合物,适当大小的疏水空间可能对保持高甜味抑制活性至关重要。由HPMP和甜味受体的分子对接结果可知[26-27],HPMP的苯环与多种氨基酸残基组成的结合口袋存在疏水相互作用,苯环对位的甲氧基正好朝向疏水性口袋内部。通过对比各疏水性基团的体积参数(丙氧基>乙氧基>甲氧基>甲基>氯原子),提示对位取代基体积大小对甜味抑制效果有一定影响。在甜味抑制识别过程中,芳香环和对位疏水取代基可能共同构成一个疏水性实体,进入甜味受体的疏水结合空腔,对位基团以甲氧基或与甲氧基体积相近的甲基、氯原子为佳,乙氧基、丙氧基等大体积疏水基团由于空间障碍可能不易于进入疏水口袋,会导致抑制活性的下降。
2.4 HPMP及其衍生物的滋味分析
利用电子舌评估HPMP及其衍生物A1~A4自身除甜味外的其他味觉指标,结果见图5。HPMP及其衍生物A1~A4在酸味、苦味、涩味方面比较突出,但鲜味和咸味不明显。在酸味方面,HPMP的酸味最强,接下来依次为A4、A1、A3、A2,说明将苯环的甲氧基修饰为其他疏水性更强的基团,对于HPMP自身酸味有一定的改善作用,可能与各甜味抑制化合物的质子化有机酸浓度和氢离子浓度有关[28]。据报道,苦涩味与疏水性存在一定的相关性,疏水性越强,苦涩味越明显[29]。各甜味抑制化合物在涩味方面比较接近,HPMP的涩味最弱;在苦味方面差异较大,HPMP苦味最弱,乙氧基修饰的A1和甲基修饰的A4具有中等强度的苦味,丙氧基、氯原子等强疏水性基团的修饰使得A2、A3的苦味最强。由于苦味传感器基于疏水作用和电荷吸附作用检测苦味物质,相比于其他传感器,会产生更显著的响应[30],各衍生物与HPMP之间实际的苦味差异仍有待进一步探讨。
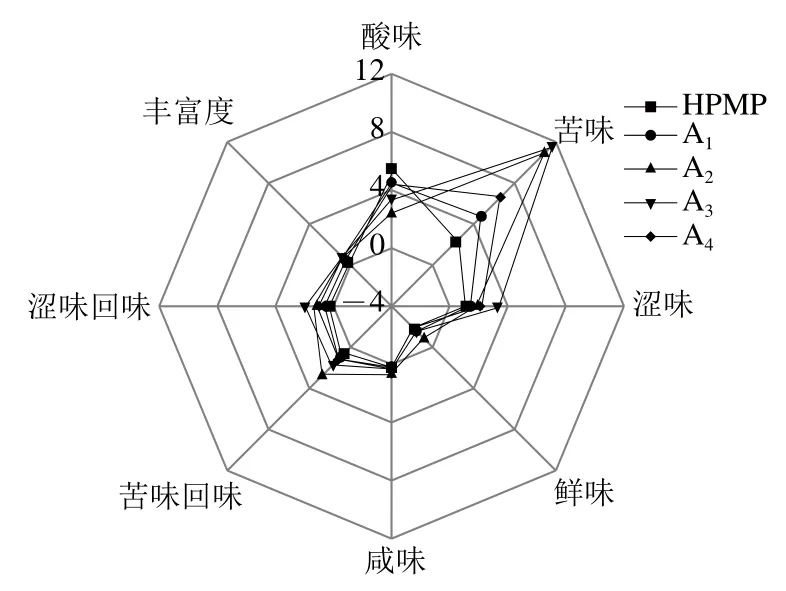
图5 HPMP及其衍生物A1~A4的电子舌雷达图Fig. 5 Radar map of electronic tongue responses to HPMP and its derivatives A1-A4
为考察各化合物在使用时是否引入上述不良滋味,进一步测定了含有不同甜味抑制化合物的蔗糖溶液除甜味外的其他味觉指标,结果见图6。添加有HPMP及其衍生物A1~A4的蔗糖溶液相比于纯蔗糖溶液,都具有更明显的酸味、苦味、涩味和苦味回味。潘露云[31]、武雯[23]研究也显示HPMP加入蔗糖溶液后,会引入一定的酸味和苦味,容易使蔗糖丧失正常的风味,钠盐化或锌盐化对这些不良滋味有明显的改良作用。在前期口尝含有HPMP的蔗糖溶液时,感评人员感受到的异味以酸涩味为主,对苦味的感知并不明显,一方面可能是口尝过程中,苦味被酸味所抑制;另一方面可能是本研究中的苦味传感器C00主要针对食品中酸性物质的苦味[22],不排除人们在感评过程将酸涩味和苦味混淆。此外,先前有文献报道HPMP是潜在的鲜味抑制剂[32],本研究中HPMP及其衍生物的添加都使蔗糖溶液的鲜味值降低,说明与HPMP一致,衍生物A1~A4也是潜在的鲜味抑制剂。
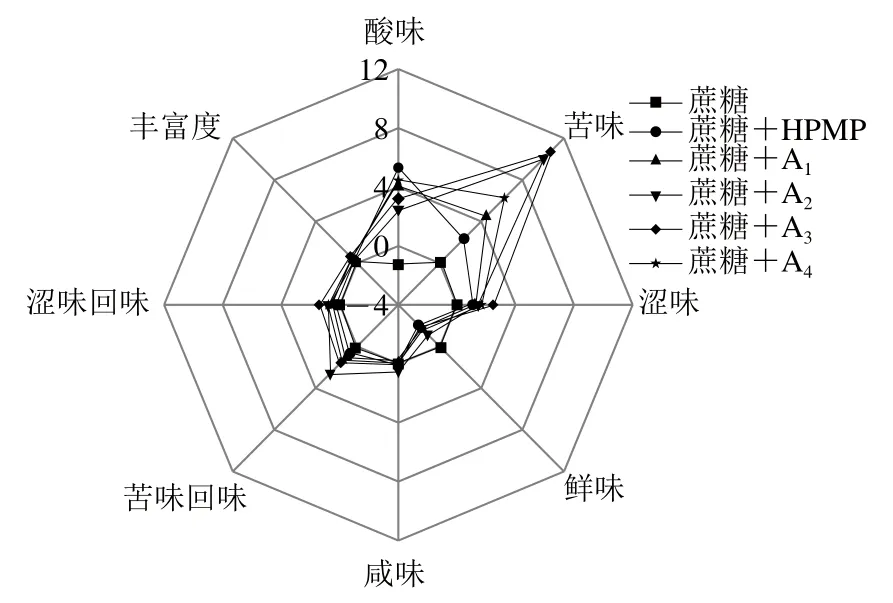
图6 含有不同甜味抑制化合物的蔗糖溶液的电子舌雷达图Fig. 6 Radar map of electronic tongue responses to sucrose solutions containing different sweetness inhibitors
3 结 论
本研究以电子舌甜度抑制率为评价指标,分析了不同质量浓度的HPMP对蔗糖甜度的抑制作用,初步构建了基于电子舌的甜味抑制效果评价方法,并选择与蔗糖甜度相当的木糖醇作为甜味载体进行验证。结果表明,电子舌可以客观反映HPMP对蔗糖、木糖醇的甜味抑制规律,并且电子舌甜度抑制率与口尝甜度抑制率具有较好的一致性。
基于建立的电子舌甜味抑制效果评价方法,考察HPMP及其衍生物A1~A4对蔗糖、果糖、木糖醇、山梨糖醇甜度的影响。结果表明,以不同的疏水性基团修饰苯环对位,衍生物A1~A4同样能够抑制4 种甜味剂的电子舌甜度,一定程度上说明对位基团疏水性对于甜味抑制的重要性,但初步推测疏水性基团体积大小而非疏水性强弱是影响甜味抑制效果的关键因素。当不同的烷氧基修饰苯环对位,甜味抑制活性随着疏水基团体积的增大有所下降。氯原子修饰的衍生物A3和甲基修饰的衍生物A4在甜味抑制效果方面与HPMP相近,可改善HPMP自身酸味,但苦味有所增强,添加到甜味剂中也会带来上述异味刺激。因此,如何合理优化衍生物结构,使其在发挥高强度甜味抑制作用的同时,平衡酸味、苦涩味等异味刺激,是今后甜味抑制研究的一个关键性问题。本研究对于新型甜味抑制剂的开发和甜味抑制机理的完善提供了重要参考。
