LTZ 联合Hp- HMG 低剂量方案治疗耐药PCOS 患者对SHBG、DHEAS 的影响及其意义
2022-01-06许艳华单远媛路云
许艳华,单远媛,路云
(鹤壁煤业(集团)有限责任公司总医院(鹤壁市第二人民医院)妇产科,河南 鹤壁 458000)
多囊卵巢综合征(Polycystic ovary syndrome,PC OS) 是一种以慢性无排卵及高雄激素血症为特征的育龄女性常见疾病[1]。 患者临床表现以月经周期不规律、不孕、多毛等为主,本病严重影响患者生活质量[2]。 来曲唑(Letrozole,LTZ)是芳香化酶抑制剂的一种,具有抑制雌激素水平,降低雌激素对女性内分泌的影响等功能[3]。 尿促性素(human tropin,HMG)是一种促性腺激素,具有促卵泡生成素表达等功能,对女性卵泡发育及成熟具有重要作用。 高纯度尿促性素(High purity human tropin,Hp -HMG)则是排除常规HMG 内的无关蛋白,并降低了HMG 促黄体生成素活性后的一种药物[4]。 为分析LTZ 联合Hp-HMG 在PCOS 中的临床价值,并探究其对患者血清指标的影响,本文选取114 例PCOS 不孕患者进行了如下研究。
1 资料与方法
1.1 一般资料 选取2017年1月-2019年6月在我院就诊的耐克罗米芬的PCOS 不孕患者114 例,纳入标准: ⑴PCOS 诊断符合2003年美国生殖医学会及欧洲人类生殖与胚胎学会在鹿特丹会议上推荐的标准,耐克罗米芬标准为至少6 个克罗米芬治疗周期有1 个周期克罗米芬剂量为150mg,均无优势卵泡发育;⑵均为初次治疗;⑶患者及家属知情同意。 排除标准:⑴有泌尿生殖系统感染、性传播疾病等;⑵合并有恶性肿瘤、内分泌疾病、肝肾功能障碍等其他疾病。 根据治疗方案的不同分为观察组(n=55)和对照组(n=59),两组患者一般资料比较,差异无统计学意义(P>0.05),见表1。
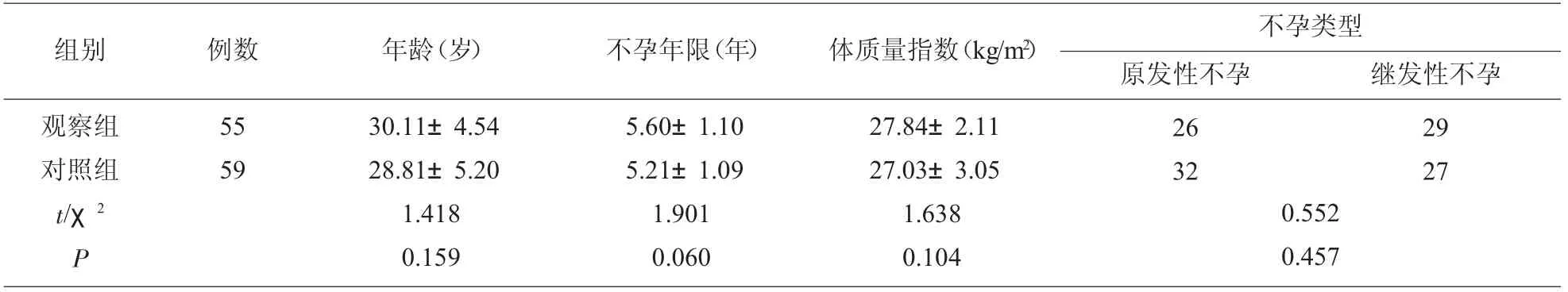
表1 两组一般资料比较
1.2 治疗及随访方法 对照组给予Hp-HMG 低剂量方案治疗:于月经第8d 开始给予患者肌肉注射75IU Hp-HMG (马鞍山丰原制药有限公司),1 次/d,持续3d。 随后选用东芝Aplio 500 彩色多普勒超声诊断仪对患者进行阴道超声检测,分析患者卵泡发育情况,根据患者卵泡数量、大小以及子宫内膜状态调整Hp-HMG 给药剂量,最大剂量为140IU/d。观察组给予LTZ 联合Hp-HMG 低剂量方案治疗,LTZ 给药方案为:于月经第3d 开始给予患者5mg LTZ(江苏恒瑞医药股份有限公司)口服,1次/d,持续5d;月经第8d 进行Hp-HMG 给药,方案参照对照组。 当患者主导卵泡直径( follicle diameter,FD)高于18mm 或存在两个及以上卵泡FD 高于16mm,且患者尿促黄体生成激素>40~50IU/L 时给予患者皮注0.1L GnRH-a(法国博福益普生制药有限公司),并嘱咐患者GnRH-a 注射24d 后同房。 GnRH-a 注射48d 后嘱患者来院再次行阴道超声检测,观察是否排卵,并给予患者20mg 地屈孕酮口服,1 次/d,持续20d。 超声显示患者存在4 个及以上卵泡FD 高于14mm,或者存在3 个及以上卵泡FD 高于18mm,且卵巢直径高于5cm,并存在恶心、呕吐、腹胀等症状者,则需取消治疗,同时嘱咐患者做好避孕措施。 治疗20d 后卵巢依然无反应的患者,则终止治疗。
1.3 检测方法 抽取两组患者入院和治疗后次日清晨外周静脉血4ml,5000r/min,6cm 半径,离心14min,收集上清后选用电化学发光法检测两组患者FSH、LH、T 和E2 等激素表达水平,试剂盒由上海凯创生物技术公司提供; 选用ELISA 法检测患者性激素结合球蛋白( SHBG) 及硫酸脱氢表雄酮( DHEAS)表达水平,试剂盒由北京博迈斯科技发展有限公司提供,操作根据相应说明书进行。 所有指标检测仪器UniCel DxI800 全自动免疫分析系统(美国贝克曼库尔特有限公司)
1.4 统计学处理 数据分析采用SPSS22.0 软件,计量资料采用(±s)表示,两组间比较使用独立样本t检验,计数资料比较使用χ2检验。 检验水准α=0.05。
2 结果
2.1 两组促排卵及妊娠情况比较 观察组hCG 日内膜厚度、 优势卵泡数及临床妊娠率明显高于对照组(P<0.05),见表2。

表2 两组促排卵及妊娠情况比较
2.2 两组治疗前后性激素比较 观察组和对照组治疗后FSH、LH、T 和E2 均较治疗前改善(P<0.05);观察组治疗后LH 和T 明显低于对照组(P<0.05),而E2 明显高于对照组(P<0.05)。 见表3。

表3 两组治疗前后性激素比较
2.3 两组治疗前后血清TG、TC、HDL-C、LDL-C 比较 观察组和对照组治疗后TC 和LDL-C 较治疗前降低(P<0.05),而HDL-C 均较治疗前提供(P<0.05);观察组治疗后HDL-C 明显高于对照组(P<0.05),而LDL-C 明显低于对照组(P<0.05)。 见表4。

表4 两组治疗前后血脂比较
2.4 两组治疗前后血清SHBG、DHEAS 比较 观察组和对照组治疗后血清SHBG 较治疗前升高(P<0.05),而DHEAS 较治疗前升高(P<0.05);观察组治疗后血清SHBG 明显高于对照组(P<0.05),而DHEAS 明显低于对照组(P<0.05)。 见表5。

表5 两组治疗前后血清SHBG、DHEAS 比较
3 讨论
PCOS 患者伴长期的卵泡选择障碍现象,募集的卵泡往往停滞在小窦卵泡阶段,虽然对FSH 刺激具有一定反应,但难以无法形成优势卵泡[5]。 不同卵泡的FSH 阈值也各不相同,只有FSH 达到一定阈值卵泡才可以继续发育,而PCOS 患者卵泡FSH 阈值较健康女性更大,并且与患者卵巢敏感度有关[6]。 因此,临床往往通过药物来增加患者卵巢内小卵泡的募集,并促进优势卵泡形成。 但需要注意的是,药物干预一旦超过某个阈值,患者将可能出现多卵泡共同发育情况,并且体内雌激素也将异常表达,进而引发卵巢过度刺激综合征,导致多胎妊娠或宫内外同时妊娠等不良现象[7]。 本研究选取的LTZ+Hp-HMG 低剂量方案的一种安全且刺激较小的促排卵方案。
LTZ 是苄三唑类衍生物的一种,可抑制中枢系统内的芳香化酶的功能,并降低人体雌激素水平,抑制雌激素对促性腺激素合成的负反馈效应,进而增强促性腺激素表达,刺激卵泡发育[8]。LTZ 不与雌激素受体结合,因此本品对人体子宫内膜生长及子宫黏液无影响,这对提高精子穿透率及受精卵着床率具有重要意义[9]。 LTZ 还可阻止雄激素的雌激素向转化,并诱使卵巢内雄激素出现一过性高表达,进而增强FSH 基因受体表达,提升卵泡的FSH 敏感性。 Hp-HMG 是促性腺激素不足的女性不孕症常用药物,本品含有大量的FSH 及hCG。 其中hCG 是滋养层分泌的一种蛋白,具有类似于LH α 亚单位的功能,可与LH 受体结合并生成与LH相似的功能。 Hp-HMG 具有纯度高,蛋白质杂质含量少,批间稳定等优势[10]。 本组研究中,观察组hCG日内膜厚度、 优势卵泡数及临床妊娠率明显高于对照组,表明LTZ 联合Hp-HMG 低剂量方案在促排卵及提升妊娠率上具有显著优势。 有研究发现[11],LTZ+小剂量Hp-HMG 给药后,PCOS 患者卵泡率及单卵泡发育率显著上升,并且子宫内膜厚度及周期妊娠率也大幅上升,这与本组研究结果相似。 相较其他促排卵方案,LTZ 联合Hp-HMG 低剂量方案还具有用药时间短,剂量小,相关医疗支出少,患者接受度高等优势。
LH 是子宫排卵及黄体生成的重要介质,近几年的研究发现[12],LH 可抑制小卵泡数量,并增强优势卵泡形成率,降低多胎及卵巢过度刺激综合征发生率;T 高表达是PCOS 患者重要病理表现;E2是卵泡颗粒细胞合成的一种雌激素,具有促细胞合成DNA、RNA 及蛋白等功能[13]。 本组研究中,观察组治疗后LH 和T 水平明显低于对照组,而E2明显高于对照组,表明联合给药方案可有效改善PCOS 患者内分泌水平,降低患者雄激素表达水平。 SHBG 是性激素运输载体之一,多毛症及男性化女性SHBG 表达水平仅为健康女性的50%左右,提示SHBG 低表达与PCOS 密切相关[14]。DHEAS 则是雄激素的一种,主要由肾上腺皮质合成,DHEAS 高表达与PCOS、肾上腺肿瘤等疾病有关[15]。 本组研究中,观察组治疗后血清SHBG 为明显高于对照组,而DHEAS 明显低于对照组,表明联合给药方案可有效改善患者SHBG、DHEAS 水平来抑制高雄激素血症,并增强性激素功能,进而提高患者排卵率及妊娠率。
本研究通过对比实验发现,LTZ 联合Hp-HMG 低剂量方案具有较高促排卵疗效,可显著提高PCOS 排卵率及妊娠率。 但由于本研究属于回顾性分析,研究基础资料总量及完整度可能还存在一定缺陷,这有待我们随后的研究完善。
综上所述,LTZ 联合Hp-HMG 低剂量方案治疗PCOS 患者有较好的效果,且药物剂量小,费用少,患者依从性高,值得临床使用。
