CNTs/Bi 12O17Cl 2光催化剂的制备及其光降解罗丹明B性能
2022-01-04李杰方可欣姚丽珠
李杰,方可欣,姚丽珠
(辽宁石油化工大学石油化工学院,辽宁抚顺 113001)
在经济高速发展的今天,环境污染也日趋严重,环境治理已经成为当前社会研究的热点问题。然而,传统的物化法和生物处理技术存在易产生二次污染和降解效率低的问题[1]。在这样的背景下,光催化技术应运而生。继1972年日本学者A.Fujishima等[2]发现可以用TiO2光解水制氢后,光催化技术得到了迅猛的发展。随着对光催化技术研究的不断深入,各种替代传统TiO2系列光催化剂的新型光催化材料也不断涌现,例如LaFeO3[3]、Bi2MO6(M=W、Mo)[4-5]、BiOX(X=Cl、Br、I)[6-8]等。其中,具有特殊层状结构、光电性能优异的BiOX(X=Cl、Br、I)光 催 化 材 料 更 是 研 究 中 的 热点。通过富集铋来提高BiOX(X=Cl、Br、I)的光催 化活性效 果显著,例 如Bi24O31Br10[9]、Bi5O7I[10]、Bi4O5Br2[11]和Bi12O17Cl2[12]等,除了具备卤氧化铋系光催化剂的优点外,还具有更强的氧化还原能力[13]。Bi12O17Cl2具有优异的光学性能、较窄的禁带宽度(2.4 eV左右)[14-15],使其在光催化选择性氧化、降解污染物等方面展现出卓越的性能。常用的纳米片状Bi12O17Cl2的制备方法有水热法[16]和化学沉积法[17]。近些年,相继出现了不同形貌和维度的Bi12O17Cl2光催化材料[18-19]。然而,改变形貌和维度并没有使其光生电子-空穴分离效率低的问题得到根本改善,这也大大限制了其在社会经济生活和工业生产中的应用[20]。为此,国内外的学者围绕Bi12O17Cl2改性开展了大量研究,包括贵金属沉积Bi12O17Cl2以及Bi12O17Cl2基复合材料的制备等[21-22],这使Bi12O17Cl2各方面的光催化性能得到了极大的改善。但贵金属的改性成本高等问题成为了另一个制约这项技术广泛应用的因素。为了增强Bi12O17Cl2的光生电子-空穴的分离效率以及可见光响应能力,纳米碳材料因其相对低的成本、较高的比表面积以及较好的导电性[23],成功引起了人们的关注。纳米碳经常用作光催化剂的载体[24],增强材料所需要的光催化活性,当纳米碳和半导体复合时,可作为电子受体,加速电子-空穴的分离。当碳材料与半导体界面接触,光生电子可以迅速转移到碳材料上,进而达到电子-空穴对分离效果。其次,纳米碳材料具有很大的比表面积和规则的孔结构[25],能够提供更多的活性位,加快反应速率。
本文采用化学沉淀法制备CNTs/Bi12O17Cl2复合材料,以氙灯为模拟光源、罗丹明B为模拟污染物,通过紫外可见分光光度计来测试罗丹明B(RhB)的最大吸收波长判断其被降解的情况。对合成的CNTs/Bi12O17Cl2复合材料的化学结构、组成、形貌和光学性能进行了表征,并用有机降解反应评价了其光催化活性。最后,根据捕获实验推断起主要作用的活性物种和可能的光催化降解机理。
1 实验部分
1.1 试剂与仪器
试剂:氢氧化钠(NaOH)、氯化铋(BiCl3)、无水乙醇、罗丹明B(RhB)、硫脲(CH4N2S),分析纯,国药集团化学试剂有限公司;碳纳米管(CNTs,纯度95%),山东大厂纳米材料有限公司;TiO2,阿拉丁试剂(上海)有限公司。
仪器:D8 Advance型X射线粉末衍射仪,布鲁克公司;SU8010型场发射扫描电镜,日立公司;Cary 5000型紫外可见近红外分光光度计、Cary Eclipse型号荧光分光光度计,安捷伦公司。
1.2 光催化剂的制备
Bi12O17Cl2及其复合材料的制备:称取0.004 mol BiCl3和一定量的CNTs,分散于20 mL无水乙醇中,磁力搅拌20 min,形成均一悬浊液。将20 mL 1.2 mol/L的NaOH溶液缓慢滴入上述混合液中,继续搅拌3.5 h。将目标产物抽滤,依次用去离子水和无水乙醇洗涤3次,并在60℃的烘箱中干燥5.0 h得到CNTs/Bi12O17Cl2复合光催化剂。其中,基于不同CNTs负载量(2.8、6.6 mg和11.0 mg)的样品分别命名为CNTs/Bi12O17Cl2-1、CNTs/Bi12O17Cl2-2和CNTs/Bi12O17Cl2-3。单一相Bi12O17Cl2样品的制备过程不添加CNTs,其余过程与复合材料制备相同。
g-C3N4的制备:称取10 g硫脲置于坩埚中,使用马弗炉在550℃下煅烧2.0 h,马弗炉升温速率为5℃/min,即得到g-C3N4。
1.3 光催化性能测试
称取0.03 g样品置于250 mL烧杯中,量取50 mL质量浓度为10 mg/L的RhB溶液与其混合后避光搅拌1.0 h,达到吸附-脱附平衡。300 W氙灯为模拟光源照明。在实验过程中,每5 min取4 mL溶液,共4次。将溶液离心(10 000 r/min、5 min)2次以除去催化剂,然后用紫外-可见分光光度计在入射波长为553 nm的条件下测不同降解时间下溶液的吸光度。
2 结果与讨论
2.1 催化剂XRD表征分析
图1为样品的XRD图谱。
从图1可以看出,Bi12O17Cl2的衍射峰为四方晶系(JCPDS No.37-0702)[26],将Bi12O17Cl2样 品 的XRD衍射峰与标准卡片对比,其峰位与标准卡对应完好,但是在30°左右出现两晶面叠加的情况((117)和(0012)晶面),这可能是因制备方法所导致的结晶度不完全,文献[21]也报道过类似现象;负载CNTs后,Bi12O17Cl2的特征峰并没有发生变化,谱图中很难看出CNTs的特征峰,这可能是由其含量太低造成的[27]。
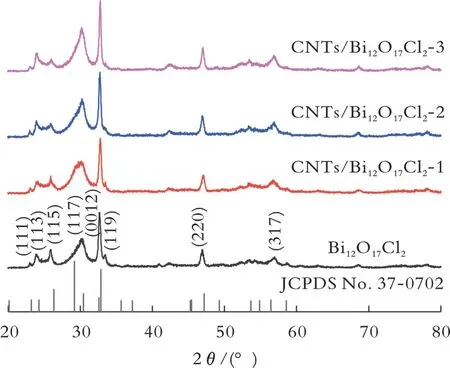
图1 样品的XRD图谱
2.2 催化剂的SEM表征分析
图2为样品的SEM图谱。从图2(a)可以看出,Bi12O17Cl2样品为不规则纳米薄片状,表面光滑。从图2(b)可以看出,CNTs呈现出细长而又杂乱的管状 形 貌;从 图2(c)-(e)可 以 看 出,在 光 滑 的Bi12O17Cl2表面分布着碳纳米管,随着CNTs负载量的增加,在Bi12O17Cl2表面出现了小范围CNTs聚集的情况,并覆盖在Bi12O17Cl2表面,这会阻止光催化剂对光的吸收,使光催化效率降低[38]。

图2 样品的SEM图谱
2.3 催化剂的UV-vis DRS表征分析
图3为样品的UV-vis DRS图谱。从图3可以看出,单一相Bi12O17Cl2在紫外-可见光区有一定程度的光响应吸收能力,它的吸收边带为510 nm(Eg=2.43 eV);经过与不同负载量的CNTs复合后,CNTs/Bi12O17Cl2复合材料在紫外光区域(λ<400 nm)表现出相似的吸收能力,但是在可见光区域,CNTs/Bi12O17Cl2复合材料展现出更强的光响应能力,且随着CNTs负载量的增加,复合材料在可见光区域(450~800 nm)的吸光度逐渐增强。
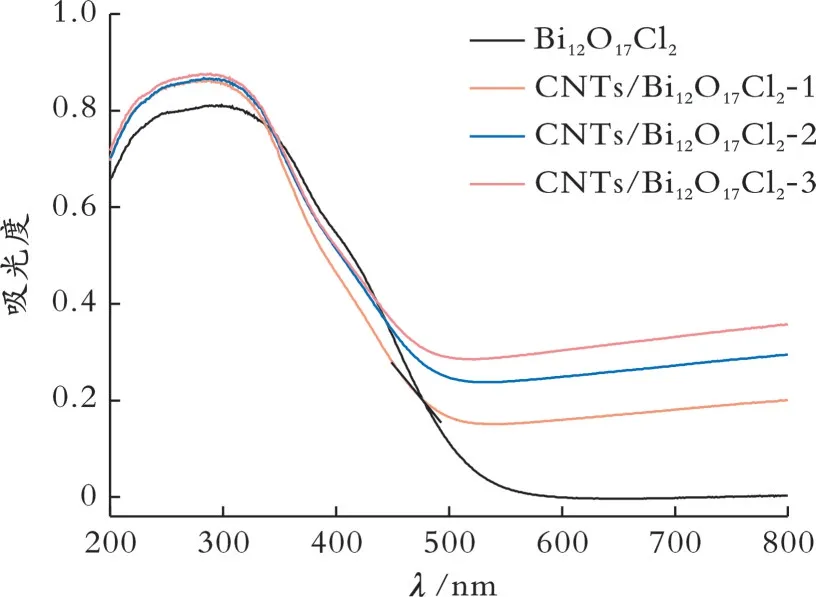
图3 样品的UV-vis DRS图谱
2.4 催化剂的光致发光光谱分析
光致发光光谱(PL)可以很好地反映半导体光催化材料中光生电子与空穴的复合与迁移情况。一般来说,荧光强度越高,光生电子与空穴的复合率越高。图4为Bi12O17Cl2和CNTs/Bi12O17Cl2-2的PL图谱。从图4可以看出,CNTs/Bi12O17Cl2-2复合材料的荧光强度明显弱于Bi12O17Cl2,说明CNTs的引入可以有效降低光生电子与空穴的复合率,提高光生载流子的分离效率,进而提高样品的光催化性能。

图4 Bi12O17Cl2和CNTs/Bi12O17Cl2-2的PL图谱
2.5 催化剂的光催化活性分析
RhB是一种化学性质稳定的偶氮类染料,以RhB为污染物模型进行光催化降解测试。图5为样品光催化降解RhB的曲线。
从图5可以看出,CNTs/Bi12O17Cl2复合材料对RhB的降解能力明显高于Bi12O17Cl2、TiO2和g-C3N4光催化材料。其中,CNTs/Bi12O17Cl2-2展现出最佳的降解活性,这说明在降解RhB有机染料方面,CNTs/Bi12O17Cl2复合材料不但表现出优于Bi12O17Cl2的降解活性,更展现出了优于传统光催化剂的光催化性能。因此,制备的CNTs/Bi12O17Cl2是一种性能卓越的新型Bi系复合光催化材料。
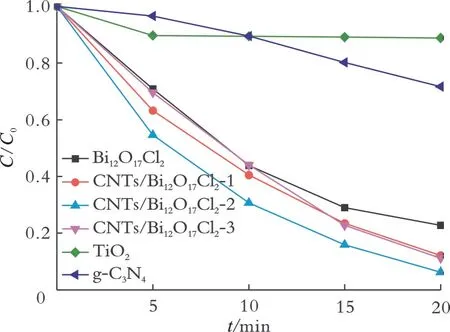
图5 样品光催化降解RhB的曲线
有机污染物的光催化降解符合准一级反应动力学,为了对比单一相Bi12O17Cl2及所制备的CNTs/Bi12O17Cl2复合材料对RhB降解速率,利用ln(C0/C)与光照时间t作图,结果见图6。从图6可以看出,所有曲线的相关系数R均大于0.99,证明RhB光催化降解符合准一级反应动力学。
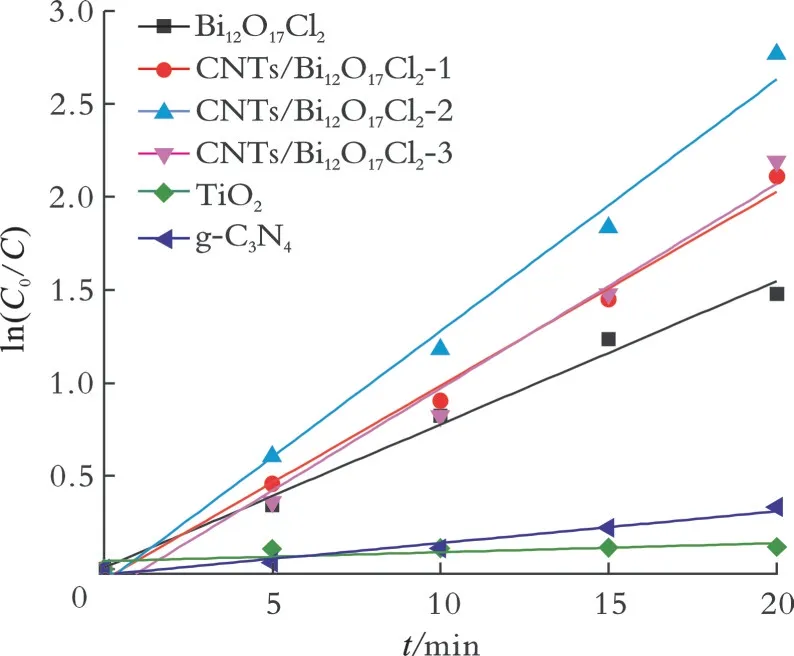
图6 样品降解RhB的ln(C0/C)~t曲线
图7为不同催化剂的降解速率常数。从图7可以 看 出,CNTs/Bi12O17Cl2-1、CNTs/Bi12O17Cl2-2和CNTs/Bi12O17Cl2-3复合材料的降解速率分别是单一 相Bi12O17Cl2降解速率的1.29倍、1.68倍 和1.30倍。CNTs/Bi12O17Cl2-2复合材料展现了最佳的光催化降解RhB的能力,这可能归功于CNTs和片状Bi12O17Cl2之间的异质结,负载在Bi12O17Cl2表面的CNTs可以作为电子传递轨道,促进电子的有效转移,增强可见光吸收,同时具有较高的光生电子与空穴的分离效率,最终促进其催化活性的提高。
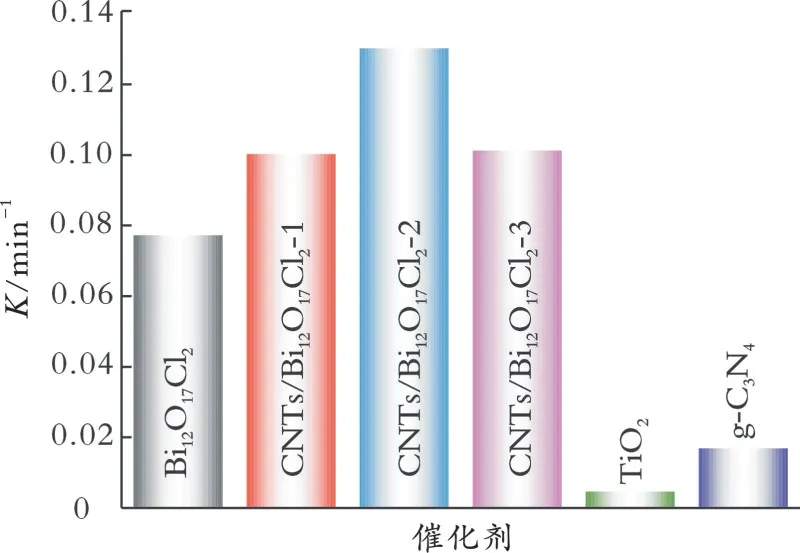
图7 不同催化剂的降解速率常数
2.6 催化剂的稳定性分析
为了测试CNTs/Bi12O17Cl2-2复合材料的光催化稳定性能,对其进行了光催化循环测试,结果见图8。从图8可以看出,经过3次光催化降解循环实验,CNTs/Bi12O17Cl2-2复合材料的降解速率略微降低。由此可见,该复合催化剂具有良好的稳定性和循环使用性能。
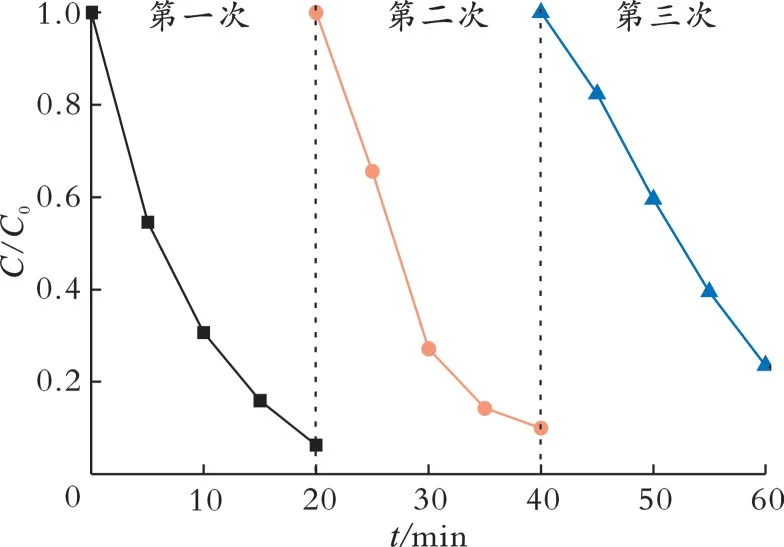
图8 CNTs/Bi12O17Cl2-2降解RhB的循环稳定性
2.7 催化剂活性组分分析
为了进一步探究光催化降解过程中起主要作用的活性组分,推测可能的光催化反应机理,通过在光催化反应体系中添加不同种类的捕获剂进行了捕获实验,结果见图9。其中,乙二胺四乙酸、抗坏血酸和甲醇分别为h+、·O-2和·OH的捕获剂[29-31]。从图9可以看出,加入甲醇后,反应体系的降解活性基本未发生改变,这表示·OH不是起主要作用的活性物种。当加入乙二胺四乙酸和抗坏血酸后,CNTs/Bi12O17Cl2-2复合材料的降解活性几乎完全被抑制,说明h+和·O-2在降解RhB染料过程中起主要作用,是主要的活性物种。

图9 不同捕获剂对CNTs/Bi12O17Cl2-2复合材料降解RhB活性的影响
2.8 催化剂光催化反应机理
图10为CNTs/Bi12O17Cl2复合材料催化降解有机污染物的可能机理。Bi12O17Cl2的价带和导带分别 为0.69 eV和-1.74 eV[26]。
从图10可以看出,分散在Bi12O17Cl2表面的CNTs与Bi12O17Cl2具有良好的接触界面。因此,在可见光照射下,Bi12O17Cl2被激发,产生光生电子(e-)与空穴(h+)。由于CNTs具有良好的导电性,Bi12O17Cl2导带(CB)上的电子(e-)高效且迅速地转移到CNTs上,而聚集在CNTs上的电子(e-)进一步与氧气(O2)发生反应,生成超氧自由基(·O-2)。由于Bi12O17Cl2的VB的电位弱于·OH/H2O(2.68 eV vs.SHE)[32],因此留在Bi12O17Cl2价带(VB)上的空穴会直接降解RhB。在CNTs/Bi12O17Cl2体系中,染料的降解由超氧自由基(·O-2)与留在Bi12O17Cl2的价带(VB)上的空穴(h+)共同完成,CNTs可以促进光诱导电荷的分离,从而提高样品的光催化活性。

图10 CNTs/Bi12O17Cl2复合材料催化降解有机污染物的可能机理
3 结论
采用化学沉淀法制备了CNTs/Bi12O17Cl2复合光催化材料。研究发现CNTs的负载能够有效促进Bi12O17Cl2光生载流子的分离,当它被用于光催化降解RhB染料时,CNTs/Bi12O17Cl2复合光催化材料表现出更好的降解RhB染料的光催化活性,CNTs/Bi12O17Cl2复合材料还在光催化降解过程中表现出了良好的稳定性和循环使用性。本文提供了一种简单有效的合成高效光催化剂的方法,这在环境保护和绿色化学领域具有潜在的应用前景。
