高效液相色谱法测定鸡蛋中氟喹诺酮类药物残留量前处理方法的优化
2021-12-31达列亚阿合买提张崇威司慧民宋志超
陈 蔷,达列亚·阿合买提,张崇威,司慧民,张 磊,宋志超*
(1.河南省兽药饲料监察所,郑州 450008;2.新疆兽药饲料监察所,乌鲁木齐 830063)
氟喹诺酮类药物(Fluoroquinolones)是一类人工合成的广谱杀菌性抗菌药物,因其具有广谱、高效、低毒以及与其它抗菌药物无交叉耐药性等特点,已广泛应用于兽医临床。但人们若长期使用含较低浓度氟喹诺酮类药物的动物食品后,易诱导耐药性的产生[1-2]。目前,鸡蛋中氟喹诺酮类药物残留的检测方法有液质联用法[3-5]、液相色谱法[6-8]、酶联免疫法[9]等,其中一些是现行的检测标准[5-7]。在日常检测中,采用国内农业部781号公告-6-2006和NY 5039-2005的方法对鸡蛋中4种氟喹诺酮类药物检测时发现回收率较低且平行性较差。本实验结合几种常见的氟喹诺酮类药物检测标准,优化了样品提取净化条件,建立了鸡蛋中环丙沙星、达氟沙星、恩诺沙星和沙拉沙星4种氟喹诺酮类药物多残留的液相色谱-荧光检测器分析方法。本方法检测结果灵敏度高、准确度好,适用鸡蛋中氟喹诺酮类药物残留的分析检测。
1 材料和方法
1.1 仪器和材料 高效液相色谱仪Waters2695(配荧光检测器2475),美国Waters公司;分析天平(感量0.00001 g),METTLE TOLEDO XP205;天平(感量0.01 g),ALC-1100;涡旋混合器,IKA MS2;振荡器,江苏金坛市正基仪器有限公司HZ-82;离心机, Sigma公司3-30 K;C18固相萃取柱,美国Agilent公司,规格100 mg,3 mL。
1.2 试剂 乙腈、甲醇均为色谱纯;氢氧化钠、磷酸、三乙胺、磷酸二氢钾、正己烷为分析纯; 实验用水为高纯水;盐酸环丙沙星、甲磺酸达氟沙星、恩诺沙星、沙拉沙星对照品(中国兽医药品监察所,纯度≥99%)。
1.3 试剂的配制 5.0 mol/L氢氧化钠溶液, 取氢氧化钠20 g或饱和溶液28 mL,加水稀释至100 mL;0.03 mol/L氢氧化钠溶液,取5.0 mol/L氢氧化钠溶液0.6 mL,加水稀释至100 mL;磷酸盐缓冲液,取磷酸二氢钾6.8 g,加水使溶解并稀释至500 mL(pH≈4.4),用5.0 mol/L氢氧化钠溶液调节pH值至7.0;0.05 mol/L磷酸/三乙胺溶液,取85%磷酸3.4 mL,用水稀释至1000 mL(pH≈1.7),用三乙胺调节pH值至2.4)。
1.4 试验方法
1.4.1 色谱条件 色谱柱:XBridgeTMC18(5 μm,4.6×150 mm);柱温:30 ℃;流动相:0.05 mol/L磷酸溶液/三乙胺-乙腈(87+13);流速:1.0 mL/min;进样量:20 μL;检测波长:激发波长280 nm;发射波长450 nm。
1.4.2 标准曲线绘制 分别称取4种氟喹诺酮类药物对照品,用0.03 mol/L氢氧化钠溶液配制成浓度分别为1 mg/mL(环丙沙星、恩诺沙星、沙拉沙星)和0.2 mg/mL(达氟沙星)的标准贮备液; 用流动相稀释成浓度分别为2、5、10、20、50、100、200 ng/mL(环丙沙星、恩诺沙星、沙拉沙星)和0.4、1、2、4、10、40 ng/mL(达氟沙星)的系列标准工作液。
1.4.3 样品前处理 鸡蛋去壳,混合均匀。-20 ℃以下贮存备用。称取新鲜或解冻的试料2±0.02 g置50 mL离心管中,加入磷酸盐缓冲液10 mL,涡旋混合,中速振荡10 min,10000 r/min离心10 min,转移上清液于25 mL容量瓶中。用磷酸盐缓冲液10 mL重复提取一次。合并两次上清液,定容,混匀,转移到50 mL离心管中。加入正己烷10 mL,涡旋混合,中速振荡5 min。10000 r/min离心10 min,吸取下层清液备用。C18固相萃取柱依次用甲醇2 mL,磷酸盐缓冲液2 mL预洗。取上述备用液10.0 mL以1 mL/min的速度过柱。用水2 mL洗柱,挤干。用洗脱液2.0 mL以1 mL/min的速度将样品洗脱入10 mL离心管中,挤干,涡旋混合,过0.22 μm微孔滤膜,供高效液相色谱-荧光检测器测定。
1.4.4 样品回收率与精密度 取空白样品,分别添加5、10、20、50 μg/kg(环丙沙星、恩诺沙星、沙拉沙星)和1、2、4、10 μg/kg(达氟沙星)4个浓度,按1.4.3项进行测定。每个浓度分别测定6次,连续测定4 d,计算回收率及批内批间相对标准偏差。
1.4.5 检测限 取20个空白样品进行适当浓度的添加,按上述步骤操作,测得噪音信号的平均值,按信噪比≥3为检测限。
2 结果与分析
2.1 色谱分离与测定 图1 为混合标准溶液色谱图,4种氟喹诺酮类药物的保留时间依次为环丙沙星5.5 min、达氟沙星6.6 min、恩诺沙星7.7 min、沙拉沙星12.1 min。图2、图3分别为鸡蛋空白样品、空白添加样品的色谱图。

图1 2 ng/mL标准溶液中氟喹诺酮类药物色谱图Fig 1 Chromatogram of standard solution of fluoroquinolones

图2 空白鸡蛋中氟喹诺酮类药物色谱图Fig 2 Chromatogram of fluoroquinolones in blank egg
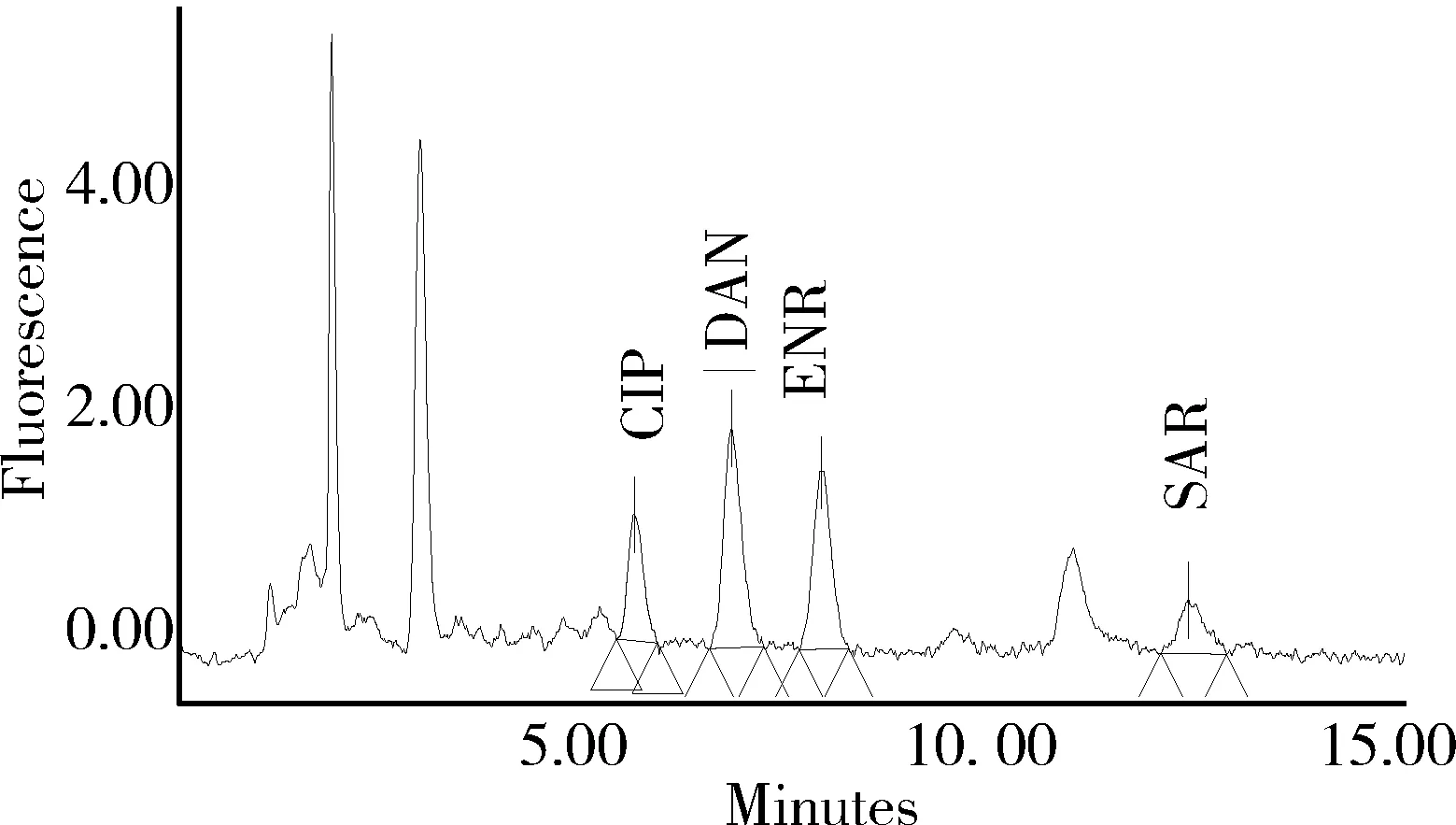
图3 5 μg/kg空白鸡蛋添加试样中氟喹诺酮类药物色谱图Fig 3 Chromatogram of fluoroquinolones with 5 μg/kg added to blank egg
2.2 标准曲线 在选定的色谱条件下,配制系列标准工作液(1.4.3项)进行色谱分析,4种氟喹诺酮类药物的回归方程及相关系数见表1,标准曲线见图4。

表1 4种氟喹诺酮类药物测定的工作曲线Tab 1 Standard curves of 4 fluoroquinolones

图4 4种氟喹诺酮类药物标准曲线Fig 4 Standard curves of 4 fluoroquinolones
2.3 回收率与精密度 用空白鸡蛋添加后进行方法回收率试验,结果见表2。由表2可见4种氟喹诺酮类药物均具有良好的回收率和重现性。

表2 鸡蛋中氟喹诺酮类药物残留回收率试验及批内批间相对标准偏差Tab 2 Recoveries of fluoroquinolone Remained in Eggs and the Intra-batch and Inter-batch RSDs

化合物Compound添加浓度Add concentration/(μg·kg-1)测定次数Number of determinations平均回收率/%Average recovery批内相对标准偏差Intra-assay coefficientof variation/%(n=6)批间相对标准偏差Inter-assay coefficient ofvariation/%(n=4)恩诺沙星Enrofloxacin5102050123412341234123492.090.194.484.992.893.394.392.091.691.694.590.988.488.493.986.02.35.54.54.62.63.53.51.91.21.62.34.11.12.82.83.54.51.01.73.8沙拉沙星Sarafloxacin5102050123412341234123494.092.395.285.196.095.895.589.196.996.797.793.494.092.894.089.33.95.73.64.82.71.83.74.61.41.41.52.42.62.13.83.25.03.52.02.4
2.4 检测限 本方法的检测限为环丙沙星、恩诺沙星、沙拉沙星5 μg/kg,达氟沙星1 μg/kg。
3 讨论与结论
3.1 提取条件的选择 目前,鸡蛋中氟喹诺酮类药物的提取液有乙腈[3]、甲酸乙腈溶液[8]、EDTA-Mcllvaine缓冲溶液[5]、磷酸盐缓冲溶液[6-7]等。采用乙腈或酸化乙腈提取均需要增加浓缩步骤,较为繁琐,而EDTA-Mcllvaine缓冲溶液的配制也较为复杂,故本实验借鉴文献[6-7]的提取方法,采用磷酸盐缓冲溶液(pH 7.0)对鸡蛋中氟喹诺酮类药物进行提取。本实验对振荡时间、提取次数进行了考察,结果发现,样品提取的振荡时间大于10 min,4种氟喹诺酮类药物的回收率无明显变化。用磷酸盐缓冲溶液(pH 7.0)提取2次比提取1次回收率提高9.8% ~15.6%,提取3次后,回收率无明显增加。此外,由于鸡蛋中含有大量水分,提取时与提取液混合在一起,用加入的提取液体积来计算结果会引起较大偏差,所以本实验采用用磷酸盐缓冲溶液(pH 7.0)提取2次,合并后定容的方法准确定量提取液体积。
3.2 脱脂条件的选择 由于鸡蛋中含有大量的脂肪、蛋白质及氨基酸等组分,样品的提取液呈浑浊状,高速离心无法使其澄清。所以,在固相萃取前应先进行脱脂。本实验考察了不同体积、不同次数的正己烷脱脂效果,结果发现,用10 mL正己烷脱脂1次即能达到脱脂效果。需要注意的是,加入正己烷振荡离心后正己烷和提取液会产生乳化,形成凝絮状物质,低速离心往往使正己烷、乳化层、提取液层分层不明晰,采用高速(10000 r/min)离心10 min可改善分层现象。然而,用吸管不易吸取凝絮状物质,所以,可用吸管小心吸取下层清液备用。
3.3 固相萃取条件的选择 本实验采用3 mL C18固相萃取柱净化,比1 mL C18固相萃取柱能有效减少堵塞现象发生。首先用2 mL甲醇活化柱子,尽可能除去填料中存在的杂质,使填料溶剂化,提高固相萃取的重现性。再用2 mL磷酸盐缓冲溶液平衡,为上样创造一致的溶剂环境。本实验比较了5、10、15、20 mL4种上样体积的回收率,结果发现,5 mL和10 mL上样量的回收率无明显差异,但对于的低残留样品,采用5 mL上样净化时最终上机测试溶液的浓度较低,灵敏度不能满足需要;而当上样体积增加到15 mL以上后会出现不同程度的过柱缓慢甚至堵塞现象,回收率有所降低。所以,最终选择取备用液10 mL进行净化。之后用2 mL水淋洗固相萃取柱,除去其中的干扰物。淋洗完后,挤干固相萃取柱,尽可能除去柱中的残留液体,再用2 mL 0.05 mol/L磷酸溶液/三乙胺(pH 2.4)-乙腈(82+18)即可完全洗脱。本实验比较了不同体积、不同洗脱液组成比例的洗脱效果,结果发现,1 mL 0.05 mol/L磷酸溶液/三乙胺(pH 2.4)-乙腈(82+18)洗脱不完全,若增大乙腈比例,虽然可以提高洗脱效率但会引起色谱峰展宽。
3.4 方法比较 在空白鸡蛋中添加环丙沙星、恩诺沙星、沙拉沙星20 μg/kg和达氟沙星4 μg/kg,采用该方法与常用标准进行比较,实验结果见表3。

表3 不同方法测定鸡蛋中氟喹诺酮类药物残留的比较Tab 3 Comparison of Different Methods for Testing of Fluoroquinolone Drugs Residues in Eggs
结果显示:采用农业部781号公告-6-2006的检测方法平均回收率低,原因在于合并提取液后脱脂时正己烷和提取液形成凝絮状沉淀,除去沉淀后损失部分提取液,致使净化液体积减少。按照公式A·Cs·V/As/m计算,净化液与提取液体积不相等,样品最终的稀释体积产生偏差。而且,对于不同的样品,视其脂肪等杂质含量的高低,形成的凝絮状沉淀量不同,损失的提取液体积也不尽相同,其回收率的相对标准偏差也较大。
采用NY 5039-2005附录A的方法回收率较低的主要原因是2次提取合并后鸡蛋中本身的水分进入提取液,影响提取液的体积,且不同的样品水分有所差别,致使提取液体积无法准确计量,按照公式A·Cs·V提取·V洗脱/As/m/V净化计算,样品提取液体积V1应为20 mL,实际值一般有24 mL左右,所以按加入的提取液体积计算的回收率结果会较低,且对于水分不同的样品,它们之间的回收率的相对标准偏差也较大。
采用本实验方法,平均回收率和相对标准偏差均满意,提取后定容可以视为提取液体积为25 mL,脱脂后虽然提取液有损失,但取部分脱脂后的提取液净化,其提取液、净化液和定容液的体积均准确,按照公式A·Cs·V提取·V洗脱/As/m/V净化计算,结果准确,回收率稳定,相对标准偏差小。将称样量增大至5 g时,平均回收率和相对标准偏差也均较满意,但由于增加样品的称样量,其脂肪等杂质的含量也相应提高,一般需要进行2次脱脂,增加了实验步骤,故舍去该方法。
本研究通过优化前处理方法,建立起了液相色谱-荧光法同时检测鸡蛋中4种氟喹诺酮类药物的方法,该方法线性范围宽,灵敏度高,重复性好,可满足日常样品的检测需求,完全适合鸡蛋中氟喹诺酮类药物残留的检测。
