利拉鲁肽联合胰岛素对2型糖尿病患者内皮素-1、瘦素和胰岛素抵抗的影响
2021-12-30陈正刘开渊朱榕峰郭岚岚
陈正 刘开渊 朱榕峰 郭岚岚
2型糖尿病(T2DM)属于常见内分泌疾病,其以血糖慢性升高为特征,可引起患者多尿、多食、多饮等症状,若血糖长期控制不佳,可导致体内血管、神经等受高血糖刺激而病变,增加心肝肾等多器官损害[1]。胰岛素是临床治疗T2DM的重要方式,通过皮下注射可迅速补充内源性胰岛素,缓解胰岛β细胞压力,以快速降低机体血糖水平,减轻临床症状[2]。但胰岛素长期使用易增加患者体质量,使得外周组织对胰岛素敏感性下降,加重胰岛素抵抗现象。利拉鲁肽属于新型降糖药物,其是胰高血糖素样-1(GLP-1)类似物,具有与天然GLP-1相似活性,可改善胰岛细胞功能,促进胰岛素分泌,以稳定血糖水平,且该药可增加饱腹感,减轻患者体质量[3]。鉴于此,本研究旨在分析利拉鲁肽联合胰岛素治疗T2DM的临床效果,报道如下。
1 资料与方法
1.1 一般资料
选取2018年6月-2020年6月于本院就诊的86例T2DM患者,纳入标准:符合文献[4]《中国2型糖尿病防治指南(2017年版)》中相关诊断;空腹血糖≥7.0 mmol/L,餐后 2 h 血糖≥11.1 mmol/L;临床资料完整;可正常沟通。排除标准:伴随其他严重内分泌系统疾病;肝肾功能障碍;对本研究用药过敏;中途失联。按随机数字表法分为两组,各43例。对照组男26例,女17例;年龄42~68岁,平均(54.63±4.78)岁;体质量指数22~29 kg/m2,平均(26.34±1.52)kg/m2;病程 2~9年,平均(5.32±1.05)年;腰围99~122 cm,平均(106.85±3.78)cm;文化程度:大专及以上3例,高中21例,初中及以下19例。观察组男24例,女19例;年龄43~69岁,平均(54.65±4.81)岁;体质量指数 22~29 kg/m2,平均(26.36±1.54)kg/m2;病程 2~9 年,平均(5.34±1.07)年;腰围 98~124 cm,平均(106.88±3.81)cm;文化程度:大专及以上3例,高中22例,初中及以下18例。两组一般资料对比,差异无统计学意义(P>0.05)。本研究经医学伦理委员会批准。患者及家属知情同意。
1.2 方法
两组均制定饮食及运动计划,进行糖尿病知识宣教。对照组予以胰岛素治疗,选用门冬胰岛素30注射液(Novo Nordisk A/S,国药准字 S20140060),初始每日皮下注射0.2 U/kg,之后依据空腹血糖调整,直至血糖达标。观察组加用利拉鲁肽注射液(Novo Nordisk A/S,国药准字 J20160037)治疗,初始睡前注射0.6 mg/d,之后依据空腹血糖调整,1~2周后增至1.2 mg/d。两组均持续治疗16周。
1.3 观察指标及评价标准
(1)血糖水平及体质量指数(BMI):治疗前和治疗16周后,以血糖分析仪测定两组空腹血糖(FPG)、糖化血红蛋白(HbA1c)和餐后2 h血糖(2 h PG)变化,并计算两组 BMI,BMI= 体重(kg)/身高2(m)2。(2)内皮素 -1(ET-1)、瘦素(Lp)和胰岛素抵抗指数(HOMA-IR)变化:治疗前和治疗16周后,空腹采集两组3 ml静脉血,分离血清后,以放射免疫法测定ET-1、Lp变化,并以免疫发光仪测定空腹胰岛素水平,计算HOMA-IR。(3)不良反应:头晕、低血糖、胃肠不适。
1.4 统计学处理
2 结果
2.1 血糖水平及BMI
治疗前两组 FPG、HbA1c、2 h PG 和 BMI比较,差异无统计学意义(P>0.05),治疗后,观察组FPG、HbA1c、2 h PG和 BMI低于对照组,差异有统计学意义(P<0.05),见表1。
表1 两组血糖水平及BMI对比(±s)

表1 两组血糖水平及BMI对比(±s)
组别 FPG(mmol/L)HbA1c(%)2 h PG(mmol/L)BMI(kg/m2)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组(n=43) 10.15±2.13 6.16±1.25 9.48±1.69 5.23±1.08 14.68±2.53 8.31±1.32 26.36±1.54 23.05±1.24对照组(n=43) 10.07±2.08 7.15±1.31 9.52±1.71 6.75±1.23 14.72±2.55 10.36±1.45 26.34±1.52 24.56±1.33 t值 0.176 3.585 0.109 6.089 0.073 6.856 0.061 5.445 P值 0.861 0.001 0.913 0.000 0.942 0.000 0.952 0.000
2.2 ET-1、Lp和HOMA-IR变化
治疗前,两组ET-1、Lp、HOMA-IR比较,差异无统计学意义(P>0.05),治疗后,观察组ET-1、Lp、HOMA-IR低于对照组,差异有统计学意义(P<0.05),见表 2。
表2 两组ET-1、Lp和HOMA-IR变化对比(±s)
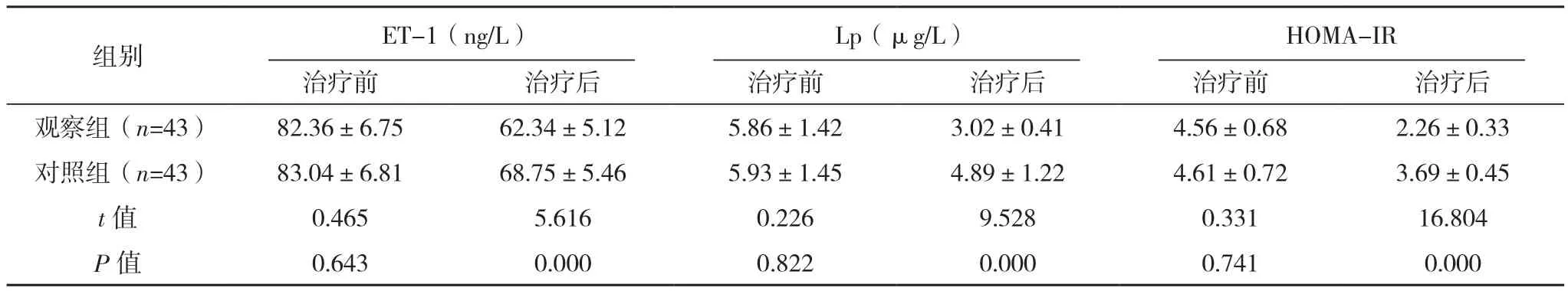
表2 两组ET-1、Lp和HOMA-IR变化对比(±s)
组别 ET-1(ng/L)Lp(μg/L)HOMA-IR治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组(n=43) 82.36±6.75 62.34±5.12 5.86±1.42 3.02±0.41 4.56±0.68 2.26±0.33对照组(n=43) 83.04±6.81 68.75±5.46 5.93±1.45 4.89±1.22 4.61±0.72 3.69±0.45 t值 0.465 5.616 0.226 9.528 0.331 16.804 P值 0.643 0.000 0.822 0.000 0.741 0.000
2.3 不良反应
对照组出现1例头晕,1例低血糖,2例胃肠不适,不良反应发生率为9.30%(4/43);观察组出现2例胃肠不适,不良反应发生率为4.65%(2/43)。两组不良反应发生率相比,差异无统计学意义(χ2=0.179,P=0.397)。
3 讨论
T2DM发病较为复杂,临床认为胰岛素抵抗和胰岛素分泌不足是诱发本病的重要因素,可促使胰岛素相关信号传递受阻,大脑对葡萄糖的利用率下降,导致血糖水平异常升高[5-6]。门冬胰岛素30是T2DM常用治疗药物,其是由30%的可溶性门冬胰岛素和70%精蛋白门冬胰岛素组成,皮下注射10~20 min即快速起效,与肌肉和脂肪细胞上胰岛素受体相结合,促进细胞对葡萄糖吸收利用,并能抑制肝糖输出,从而稳定控制血糖水平[7-8]。但该药配比相对固定,且中效胰岛素覆盖时间短,清晨易出现血糖波动,加之胰岛素单用可增加肥胖风险,进一步加重胰岛素抵抗。
ET-1是调节心血管功能的重要因子,在高血糖持续刺激下,血管内皮可出现损伤,导致ET-1水平升高,增强血管收缩能力,引起血管痉挛;Lp是由脂肪组织分泌的蛋白质类激素,是参与糖、脂肪和能量代谢的重要物质,可加重胰岛素抵抗;HOMA-IR是反映胰岛素抵抗的重要指标,当其升高时,提示胰岛素抵抗加重,血糖难以稳定控制[9-10]。本研究结果显示,观察组FPG、HbA1c、2 h PG和BMI低于对照组,ET-1、Lp、HOMA-IR低于对照组,两组均无严重不良反应发生,表明利拉鲁肽联合胰岛素可增强T2DM治疗效果,加快血糖水平恢复正常,减轻体质量及胰岛素抵抗,降低ET-1和Lp水平,且不良反应少。利拉鲁肽属于GLP-1激动剂,经皮下注射后可补充内源性GLP-1不足,且该药结构更为稳定,不易被DPP-4降解,利于保持体内GLP-1生理学浓度。而GLP-1具有葡萄糖浓度依赖性促进胰岛β细胞分泌胰岛素和抑制胰高血糖素分泌双重作用,利于提高胰岛β细胞活性,加快β细胞增殖,以改善胰岛功能,减轻胰岛负担,稳定机体血糖水平[11-12]。利拉鲁肽还可作用于稳定性自然杀伤T细胞,加快白色脂肪产热,以抑制内脏脂肪表达,减少脂肪素和Lp沉积,且能作用于中枢神经产生饱腹感,减少食物摄取,延长胃排空时间,从而降低患者体质量,减轻胰岛素抵抗现象。
综上所述,利拉鲁肽联合胰岛素可降低T2DM患者ET-1和Lp水平,减轻胰岛素抵抗现象,促进体质量下降,增强血糖控制效果,且安全性高。
