基于HPLC-Q-TOF-MS技术鉴定热毒宁注射液中活性成分
2021-12-23徐玉琴刘娟欧阳婷卿志星刘红宇
徐玉琴 刘娟 欧阳婷 卿志星 刘红宇

〔摘要〕 目的 利用高效液相色谱-四级杆飞行时间串联质谱(HPLC-Q-TOF-MS)技术快速鉴定热毒宁注射液中主要活性成分,阐明热毒宁注射液的物质基础及微量成分。方法 采用HPLC-Q-TOF-MS技术首先研究绿原酸类、多酚类化合物的质谱裂解规律,同时结合文献,利用已知的质谱裂解规律推测热毒宁注射液中主要活性成分的结构。结果 共鉴定热毒宁注射液中40个化合物,包括14个绿原酸类化合物、13个环烯醚萜类化合物、13个有机酸类化合物,其中24个化合物首次在热毒宁注射液中报道。结论 热毒宁注射液中主要活性成分为绿原酸、环烯醚萜和有机酸类化合物。
〔关键词〕 热毒宁注射液;高效液相色谱-四级杆飞行时间串联质谱;活性成分;质谱裂解规律;结构解析
〔中图分类号〕R284.1 〔文献标志码〕A 〔文章编号〕doi:10.3969/j.issn.1674-070X.2021.12.010
Identification of Active Components in Reduning Injection Based on HPLC-Q-TOF-MS Technology
XU Yuqin1, LIU Juan1, OUYANG Ting1, QING Zhixing2, LIU Hongyu1*
(1. The First Affiliated Hospital of Hunan University of Chinese Medicine, Changsha, Hunan 410007, China;
2. Hunan Agricultural University, Changsha, Hunan 410128, China)
〔Abstract〕 Objective To identify the main active ingredients quickly in Reduning injection by high performance liquid chromatography quadrupole time of flight tandem mass spectrometry (HPLC-Q-TOF-MS) technology, and to clarify the material basis and trace components of Reduning injection. Methods The HPLC-Q-TOF-MS technique was first employed to investigation the fragmentation pathways of chlorogenic acids and polyphenols. And then, the structures of the main active ingredients in Reduning injection were speculated using the well-investigated fragmentation pathways of standards combined with the literatures. Results A total of 40 compounds, which including 14 chlorogenic acid, 13 iridoid, and 13 organic acid type compounds were identified from Reduning injection. Among them, 24 compounds were reported for the first time in Reduning injection. Conclusion The chlorogenic acids, iridoids and organic acid compounds were the main active ingredients of Reduning injection.
〔Keywords〕 Reduning injection; HPLC-Q-TOF-MS; active components; fragmentation pathways; structural identification
热毒宁注射液是由青蒿、金银花、栀子三味中药材组方制成的复方制剂,1 mL热毒宁注射液由1.25 g青蒿、0.75 g金银花和0.6 g栀子提取加工而成[1-2]。热毒宁注射液具有清热、疏风、解毒之功效,临床上主要用于外感风热所引起的高热畏寒、头身疼痛、咳嗽咳痰等上呼吸道感染[3-4]。热毒宁注射液的主要活性成分为有机酚酸类和环烯醚萜类,包括绿原酸、隐绿原酸、异绿原酸A、异绿原酸B、栀子苷、京尼平苷酸、京尼平龙胆双糖苷等[5-6],除了这些主要的活性成分,热毒宁注射液中还存在一系列含量较低的化学成分,这些化学成分需要进一步研究。
在2020年第七版《新型冠状病毒肺炎诊疗方案》[7]中,热毒宁注射液被推荐用于新型冠状病毒肺炎的治疗。同时,其被列入《甲型H1N1流感诊疗方案》《登革热诊疗指南》《人感染H7N9禽流感診疗方案》中[8-10]。但是,在临床使用热毒宁注射液的过程中,出现了多种不良反应,主要表现为过敏、皮肤损伤,严重时出现过敏性休克[11-12]。热毒宁注射液除了主要活性成分,还有很多低含量的化合物没有被报道,而这些物质可能导致热毒宁注射液出现不良反应。因此,本文拟采用高灵敏度的质谱技术对热毒宁注射液中化学成分进行系统研究不仅有利于其质量控制,而且可对过敏原的筛查奠定物质基础。
1 材料
1.1 主要仪器
高效液相色谱-四极杆飞行时间串联质谱(HPLC-Q-TOF-MS)(美国Agilent公司);Milli-Q Advantage A10系统(美国MILLPORE公司);ML204/02型精密天平[梅特勒-托利多(上海)仪器有限公司];KQ5200DE型超声波清洗器(昆山超声仪器有限公司)。
1.2 主要试剂与药物
新绿原酸(批号DST180130-015,纯度为99%)、异绿原酸B(批号DST180130-037,纯度为98%)、异绿原酸C(批号DST180210-038,纯度为98%)、咖啡酸(批号 MUST-18040102,纯度为98%)均购自成都曼思特生物技术有限公司;绿原酸(批号110753-201415,纯度为98%)、异绿原酸A(批号111782-201706,纯度为98%)均购自中国食品药品检定研究院;甲醇和乙腈(色谱纯,德国Merck公司);甲酸(色谱纯,瑞士Fluka-Sigma-Aldrich公司);热毒宁注射液(江苏康缘药业股份有限公司,批号Z200707)。
2 方法与结果
2.1 色谱与质谱条件
色谱条件:XAqua C18 (150 mm×2.1 mm,2.8 μm)色谱柱;乙腈(A)-0.1%甲酸水(B)为流动相,梯度洗脱(0~5 min,1%~29% A,5~15 min,29%~50% A,15~30 min,50%~95% A);柱温 30 ℃;检测波长 280 nm;体积流量0.3 mL/min;进样量2 μL。
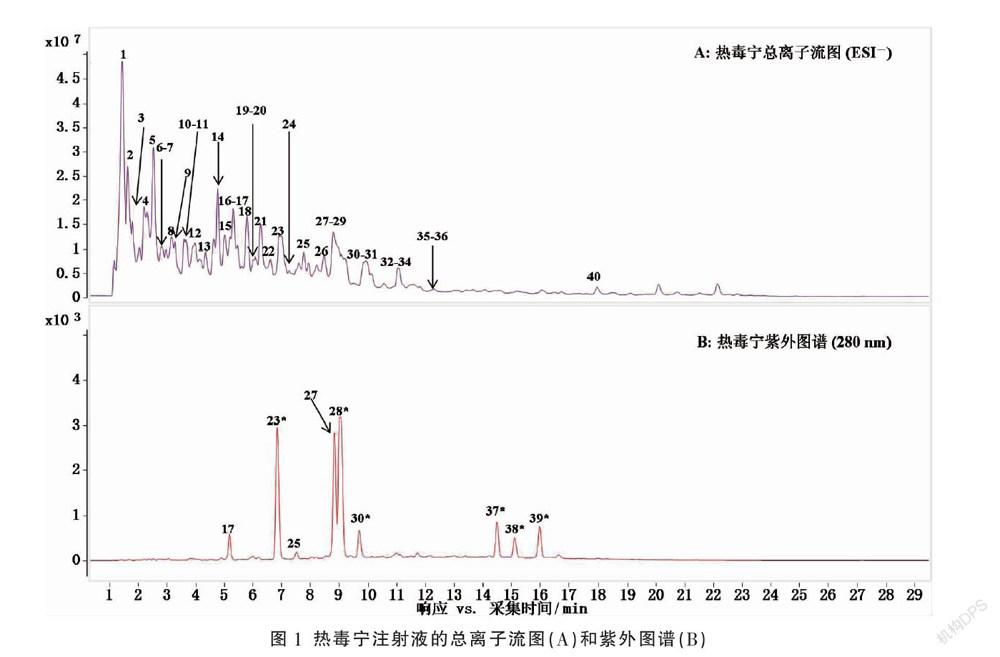
质谱条件:ESI离子源,負离子模式(ESI-)检测;干燥气体积流量:10 L/min;干燥气温度:350 ℃; 鞘气温度:350 ℃;鞘气体积流量:11 L/min;毛细管电压:3500 V;锥孔电压:100 V;化合物质核比扫描范围为m/z 100~1700;化合物二级裂解电压为10~30 eV。热毒宁注射液的总离子流图和色谱图分别见图1A和1B。
2.2 对照品及供试品溶液制备
称取对照品新绿原酸、绿原酸、咖啡酸、异绿原酸A、异绿原酸B、异绿原酸C各10 mg左右,溶解在5 mL的甲醇溶液中,取1.5 mL标准品溶液过0.22 μM的微孔滤膜,装入液相小瓶中待用。直接吸取1.5 mL热毒宁注射液过0.22 μM的微孔滤膜,装入液相小瓶中待用。
2.3 对照品质谱裂解规律的研究
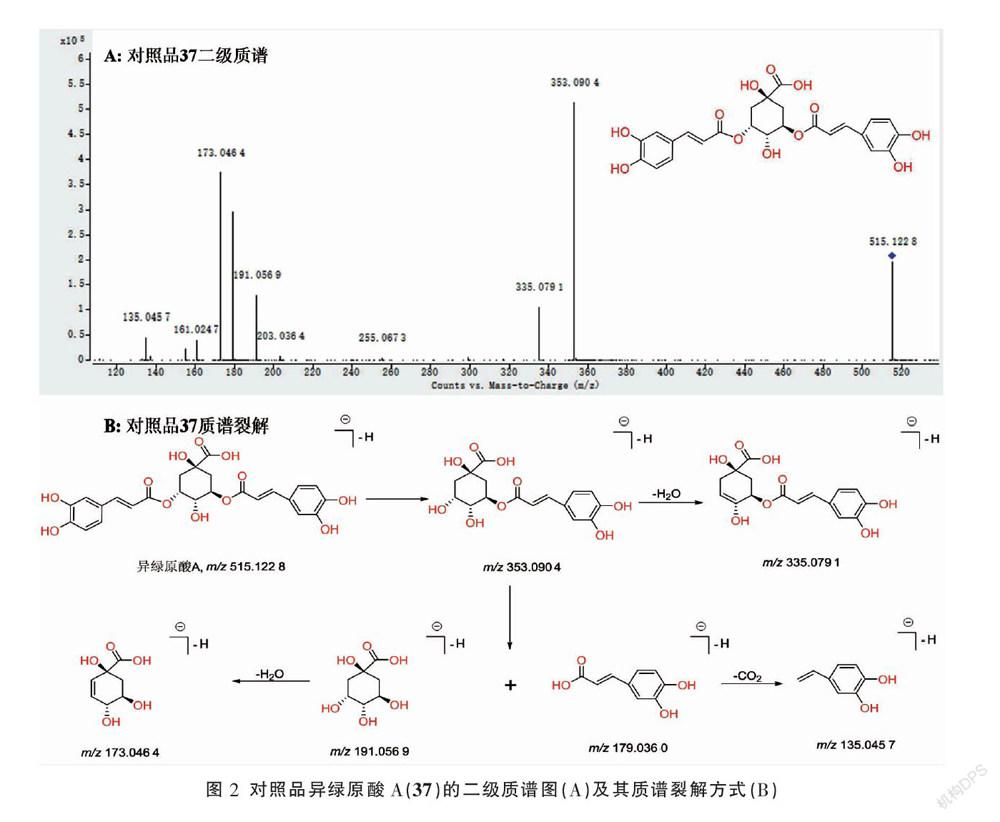
热毒宁注射液中主要成分为绿原酸类、环烯醚萜类、有机酸类等化合物。因此,购买6个对照品进行质谱裂解规律的研究,相同类型的化合物在质谱中存在相同的裂解规律。研究已知化合物的质谱裂解规律,从而推测未知类似物的结构。新绿原酸(23)、绿原酸(28)、异绿原酸A(37)、异绿原酸B(38)和异绿原酸C(39)属于绿原酸类化合物,这种类型的化合物质谱裂解有两个明显的特征:(1)因绿原酸类化合物结构中存在酯基,在质谱中酯基容易断裂而形成的质核比较小而丰度高的碎片离子(相对于母离子);(2)因化合物结构中存在羟基以及羧基,因此,在二级质谱中会出现[M-H2O]-以及[M-CO2]-的碎片离子。以化合物37为例(图2),因其结构中存在酯基,在质谱中酯基容易断裂而形成高丰度的m/z 353.090 4、191.056 9和179.036 0碎片离子。碎片离子m/z 353.090 4和191.056 9会继续失去一分子H2O而形成m/z 335.079 1和173.046 4的碎片离子。因碎片离子m/z 179.036 0结构中含有羧基,容易失去一分子CO2而形成m/z 135.045 7的碎片离子。
咖啡酸(30,m/z 179.040 7[M-H]-)属于有机酸类化合物,其质谱裂解有如下特征:因其结构中存在大-π共轭系统,因此其骨架很难裂解,主要出现取代基的丢失。因其结构中存在羧基,会失去一分子CO2而形成m/z 135.044 6的碎片离子;因其结构中存在邻二酚羟基,容易失去一分子H2O而形成m/z 161.026 8的碎片离子。环烯醚萜类化合物因未购买相关标准品,没有对其二级质谱裂解规律进行研究,其质谱裂解主要有如下特征:(1)会失去所有的糖基从而形成基本的母核离子;(2)因环烯醚萜类化合物结构中不存在大-π共轭系统,因此会发生骨架的裂解,如RDA裂解等[13-14]。
2.4 热毒宁注射液中化学成分的结构鉴定
基于上述质谱裂解规律结合HPLC-Q-TOF-MS对热毒宁注射液中主要活性成分进行结构鉴定,共鉴定化合物40个,包括14个绿原酸类化合物、13环烯醚萜类化合物、13有机酸类等化合物,其中24个化合物首次在热毒宁注射液报道。具体结构解析过程如下。
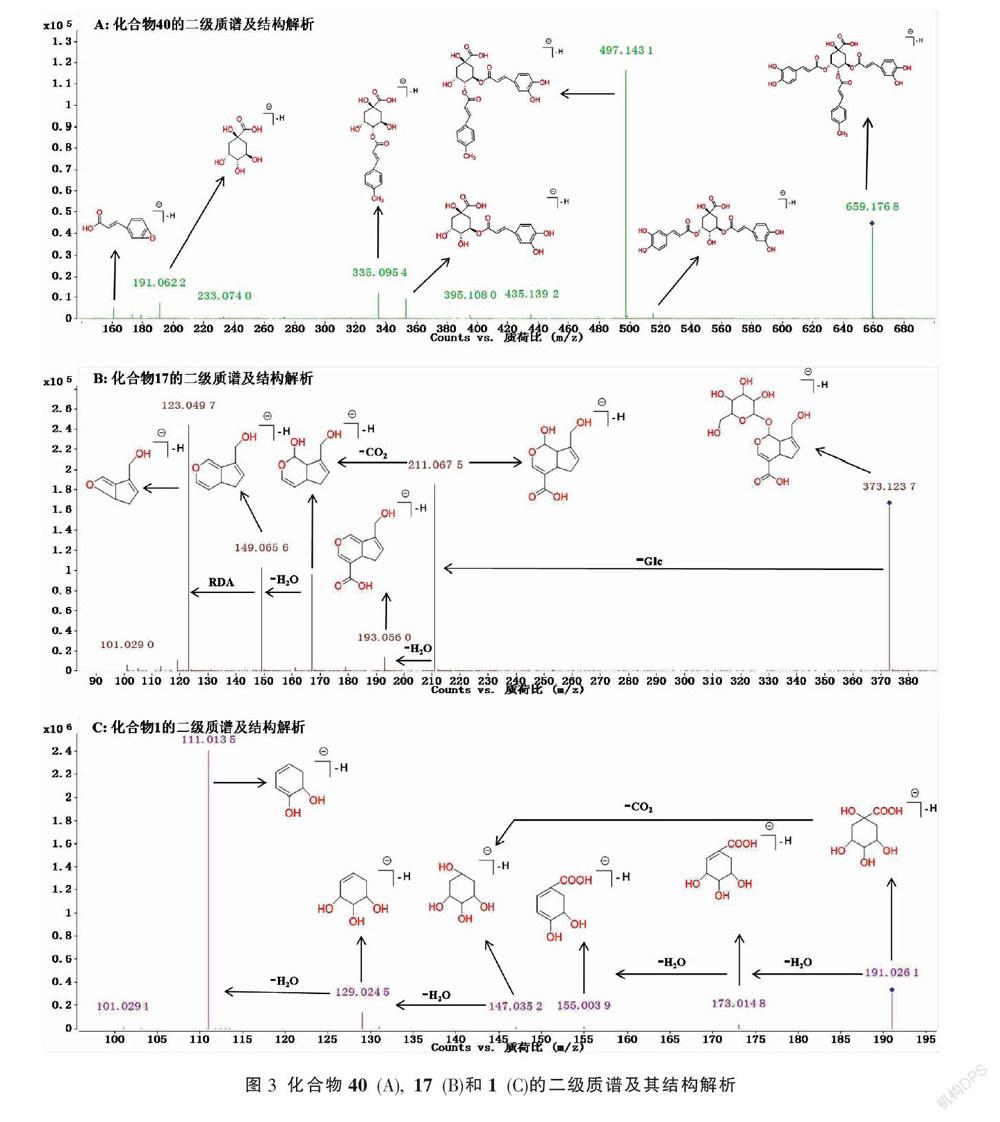
2.4.1 绿原酸类化合物的结构鉴定 根据绿原酸类化合物质谱裂解规律与化合物的二级质谱,化合物14-16、23、28、29、32、33、35-40被鉴定为绿原酸类化合物(表1)。以化合物40的结构解析为例,化合物40的质核比为m/z 659.176 8,推测其分子式为C35H32O13,从化合物40的二级质谱可知(图3A),其存在m/z 515.131 8、353.098 0、191.062 2和161.050 4的碎片离子,说明其结构中的一部分为异绿原酸。化合物40的母离子(m/z 659.176 8)会失去一分子对甲基苯乙酸基团从而形成m/z 515.131 8的碎片离子,说明化合物40是由异绿原酸和对甲基苯乙酸组合而成,因此,化合物40被鉴定为异绿原酸E(图3A)。在化合物40的二级质谱,其母离子(m/z 659.176 8)会失去一分子咖啡酸基团从而形成m/z 497.143 1的分子离子,说明化合物40结构推测的正确性。通过相同的方法,其他13个绿原酸类化合物被初步鉴定(表1),化合物23、28、30、37-39通过与标准品保留时间、一级质谱与二级质谱的比对,分别准确鉴定为新绿原酸、绿原酸、隐绿原酸、异绿原酸B、异绿原酸A和异绿原酸C。化合物14-16、32、33、35、36和40首次在热毒宁注射液中报道。
2.4.2 环烯醚萜类化合物的结构鉴定 根据环烯醚萜类化合物质谱裂解规律与化合物的二级质谱,化合物8、10、17-22、24、26、27、31和34被鉴定为环烯醚萜类化合物(表1)。以化合物17的结构解析为例,化合物17的质核比为m/z 373.123 7,推测其分子式为C16H22O10,从化合物17的二级质谱可知(图3B),化合物17的母离子(m/z 373.123 7)会失去一分子葡萄糖基团从而形成m/z 211.067 5的骨架碎片离子,说明化合物17中含有一分子葡萄糖基。质核比为m/z 211.067 5的碎片离子会继续丢失一分子H2O或者一分子CO2从而形成m/z 193.056 0或167.076 5的碎片离子,m/z 167.076 5的碎片离子会继续丢失一分子H2O,以上质谱裂解特征说明化合物17中含有羟基以及羧基。分子离子峰m/z 123.049 7则来源于的m/z 149.065 6的碎片离子发生RDA裂解。通过化合物17的质谱裂解特征、环烯醚萜类化合物的质谱裂解规律以及参考相关文献[13,15], 化合物17被初步鉴定为京尼平酸苷。通过相同的方法,其他12个环烯醚萜类化合物被初步鉴定(表1),其中化合物10、21、22、26和31首次在热毒宁注射液报道。
2.4.3 有机酸类化合物的结构鉴定 化合物1-7、9、11-13、25和30被鉴定为有机酸类化合物(表1)。以化合物1的结构解析为例,化合物1的质核比为m/z 191.026 1,推测其分子式为C7H12O6,从化合物1的二级质谱可知(圖3C),化合物1的母离子(m/z 191.026 1)会失去一分子H2O或者一分子CO2从而形成m/z 173.014 8或147.035 2的碎片离子,说明化合物1中含有羟基和羧基。质核比为m/z 147.035 2的碎片离子会继续丢失两分子H2O从而形成m/z 111.013 5的分子离子峰,说明化合物1的结构中至少存在两个羟基。化合物1的母离子(m/z
191.026 1)会连续失去两分子H2O也验证了上述结论。通过化合物1的质谱裂解特征及参考相关文献[15],化合物1被初步鉴定为喹啉酸。通过相同的方法,其他12个有机酸类化合物被初步鉴定(表1),化合物30通过与标准品保留时间、一级质谱与二级质谱的比对,准确鉴定为咖啡酸。其中化合物2-7、9、11-13和25首次在热毒宁注射液报道。
3 讨论
HPLC-Q-TOF-MS因其检测限低、灵敏度高、重复性好而广泛应用于中药材、中成药、中药注射剂中主要活性成分的定性研究[16-18]。特别是对于一些含量很低、极性较大、无紫外吸收的化合物结构鉴定具有优势。在本研究中,利用HPLC-Q-TOF-MS共鉴定了热毒宁注射液40个化合物,其中大部分属于极性较大和无紫外吸收的化合物,这些化合物使用传统植物化学分离难度较大,难以被分离纯化。HPLC-Q-TOF-MS技术能够确定化合物的骨架和取代基,但是却无法确定骨架与取代基的连接位点[19-20]。因此,除了新绿原酸(23)、绿原酸(28)、咖啡酸(30)、异绿原酸A(37)、异绿原酸B(38)和异绿原酸C(39)被准确鉴定外,其他化合物均为初步鉴定。
中药注射剂作为现代中药新剂型,具有起效迅速、生物利用度高等优点,为中药在防治危急重症疾病中开辟了新途径[21]。但是,中药注射剂的不良反应严重阻碍了其快速发展,主要原因是中药注射剂成分过于复杂,对于引起不良反应的物质难以鉴定。在临床上,热毒宁注射液的主要不良反应为速发型的皮肤过敏,表现为皮肤瘙痒和斑丘疹等,但是过敏源却鲜有报道[11-12]。在本研究中,从热毒宁注射液中共鉴定了40个化合物,除了京尼平酸苷(17)、新绿原酸(23)、断马钱子酸(27)绿原酸(28)、咖啡酸(30)、异绿原酸A(37)、异绿原酸B(38)和异绿原酸C(39)等高含量的化合物以外,其他化合物含量相对较低,而这一些化合物均有可能为热毒宁注射液致敏因子,本研究为热毒宁注射液致敏因子的发现奠定物质基础。同时,也可以考虑将京尼平酸苷、新绿原酸、断马钱子酸、绿原酸、咖啡酸、异绿原酸A、异绿原酸B和异绿原酸C等热毒宁注射液中的主要成分与热毒宁注射液进行等效性研究,以期排除热毒宁注射液中的致敏因子,为热毒宁注射液的快速发展奠定基础。
参考文献
[1] 王 璨,王保和,黄宇虹,等.UPLC-MS/MS同时测定大鼠血浆中热毒宁注射液13个潜在质量标志物及其药动学研究[J].中草药,2021, 52(9):2653-2664.
[2] 葛 雯,李海波,于 洋,等.热毒宁注射液化学成分研究(Ⅳ)[J].中草药,2017,48(15):3042-3050.
[3] 吴 莎,王 雪,吴亚男,等.UPLC用于热毒宁注射液中11种成分测定及其指纹图谱研究[J].中国中药杂志,2014,39(24):4804-4810.
[4] 范震宇,蔡亮亮,王亚格,等.热毒宁注射液解热作用与化学质控成分相关性研究[J].南京中医药大学学报,2021,37(1):126-130.
[5] WANG Z, CHEN W, LI Y Y, et al. Reduning injection and its effective constituent luteoloside protect against Sepsis partly via inhibition of HMGB1/TLR4/NF-κB/MAPKs signaling pathways[J]. Journal of Ethnopharmacology, 2021, 270: 113783.
[6] 葛 雯,李海波,于 洋,等.热毒宁注射液化学成分、药理作用及临床应用研究进展[J].中草药,2017,48(5):1027-1036.
[7] 国家卫生健康委员会.新型冠状病毒肺炎诊疗方案(试行第七版)[EB/OL].(2020-03-03)[2020-03-04].http://www.nhc.gov.cn/yzygj/s7653p/202003/46c9294a7dfe-4cef80dc7f5912eb1989.shtml.
[8] 秦素红.基于治疗新型冠状病毒肺炎的清热解毒中成药应用研究[J].中药与临床,2020,11(6):1-4, 12.
[9] MA Q H, XIE Y Q, WANG Z L, et al. Efficacy and safety of ReDuNing injection as a treatment for COVID-19 and its inhibitory effect against SARS-CoV-2[J]. Journal of Ethnopharmacology, 2021, 279: 114367.
[10] 陈元堃,曾 奥,罗振辉,等.热毒宁注射液治疗新型冠状病毒肺炎的活性成分与潜在作用机制初探[J].广东药科大学学报,2020, 36(3):381-387.
[11] 汪敏慧.34例热毒宁注射液不良反应报告分析[J].世界复合医学,2020,6(12):186-188.
[12] 刘力亨,裴东根.59例热毒宁注射液致儿童皮肤系统不良反应报告分析[J].儿科药学杂志,2021,27(4):52-54.
[13] 雷 磊,王 玉,霍志鹏,等.LCMS-IT-TOF分析栀子炒焦前后化学成分的变化[J].中国实验方剂学杂志,2019,25(17):88-97.
[14] 龚兴成,刘文静,曹丽波,等.DI-MS/MSALL法快速定性分析金银花的化学成分[J].中国中药杂志,2021,46(9):2220-2228.
[15] CHENG C, DU F F, YU K, et al. Pharmacokinetics and disposition of circulating iridoids and organic acids in rats intravenously receiving ReDuNing injection[J]. Drug Metabolism and Disposition: the Biological Fate of Chemicals, 2016, 44(11): 1853-1858.
[16] YU L Y, CHEN M F, LIU J H, et al. Systematic detection and identification of bioactive ingredients from Citrus aurantium L. var. Amara using HPLC-Q-TOF-MS combined with a screening method[J]. Molecules, 2020, 25(2): 357.
[17] 赵 权,张 优,陈 影,等.HPLC-VWD-Q-TOF-MS/MS 法定性与定量分析枳实栀子豉汤成分[J].中成药,2021,11:3067-3075.
[18] 刘红宇,徐玉琴,欧阳婷,等.HPLC-Q-TOF-MS鉴定注射用益气复脉冻干粉中皂苷类成分[J].中国实验方剂学杂志,2018,24(5):7-12.
[19] QING Z X, ZHAO H, TANG Q, et al. Systematic identification of flavonols, flavonol glycosides, triterpene and siraitic acid glycosides from Siraitia grosvenorii using high-performance liquid chromatography/quadrupole-time-of-flight mass spectrometry combined with a screening strategy[J]. Journal of Pharmaceutical and Biomedical Analysis, 2017, 138: 240-248.
[20] QING Z X, CHENG P, LIU X B, et al. Systematic identification of alkaloids in Macleaya microcarpa fruits by liquid chromatography tandem mass spectrometry combined with the isoquinoline alkaloids biosynthetic pathway[J]. Journal of Pharmaceutical and Biomedical Analysis, 2015, 103: 26-34.
[21] 葉爱军,邵 晖,李 怡,等.2015年至2017年我国老年医保患者中药注射剂临床使用现状分析[J].中华中医药杂志,2021,36(4): 2345-2349.
〔收稿日期〕2021-09-01
〔基金项目〕国家自然科学基金面上项目(82174069);湖南省教育厅科学研究重点项目(18A216);湖南中医药大学药学一流学科开放基金重点项目(2021YX02)。
〔作者简介〕徐玉琴,女,硕士,研究方向:中药及复方制剂中药化学成分鉴定。
〔通信作者〕*刘红宇,女,博士,主任药师,硕士研究生导师,E-mail:lhy9544@163.com。
