电厂运营初期温排水口沉积物中多环芳烃的监测和来源分析
2021-12-23王智锋梁诗梅赵利容谭文韬姚栋才赵子科
王智锋,梁诗梅,赵利容,谭文韬,姚栋才,赵子科
(广东海洋大学化学与环境学院,广东 湛江 524088)
0 引言
当海水作为电厂冷却水并排放回海域时,温排水可能对邻近海域产生影响。海水作为电厂冷却水时,浮游生物在高温或防止其附着而投入的试剂影响下大量死亡,并在高温作用下加速分解成有机颗粒,对亲脂性的有机污染物具有很强的吸附富集作用,会增加悬浮物中有机污染物的含量。目前有关电厂温排水对海水pH、温度、COD、叶绿素、重金属等的影响已进行了大量研究,但在有机污染方面比较缺乏[1-6]。多环芳烃(PAHs)是典型的持久性的有机污染物,具有“三致”作用和环境激素效应,已被国内外列入优先控制污染物名单。本研究在湛江湾某电厂运行初期对温排水口沉积物中的PAHs含量进行监测和来源分析,为进一步探讨研究区域PAHs的变化及其趋势,分析海水冷却水对海洋环境PAHs污染的影响提供基础数据和资料。
1 材料与方法
1.1 样品采集
本研究中电厂为火电厂,采用海水冷却,2015年开始试运行,温排水口位于湛江湾的东南部。图1为采样站位分布图,18个站位以温排水口(S9)为中心呈放射状分布,采样时间在2016年3月。样品经冷冻干燥、研磨和过筛后置于棕色玻璃瓶中保存。
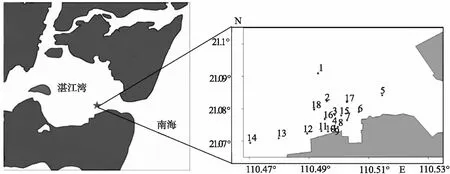
图1 采样站位分布图
1.2 样品预处理
样品前处理方法采用索氏提取法:称取约10 g样品于滤纸筒内,量取180mL二氯甲烷于蒸馏瓶,加入一定量铜片,索氏提取48h;提取液经旋转蒸发仪蒸发至约3mL,用正己烷置换2次,再浓缩至约0.5mL,转移至样品瓶,挥发定容至约0.5mL,加入内标物,待测。
1.3 分析测定条件和质量保证
样品测试采用气相色谱/串联质谱法(Trace GC Ultra &TSQ Quantum XLS, Thermo Fisher, USA)进行测试,HP-5ms色谱柱,进样口温度290℃,初始温度70℃保持2min,以5℃/min程序升温至290℃,保持10min;离子源为EI源,温度250℃;采用SCAN模式定性,SRM模式定量分析。
本研究中15种PAHs分别为苊烯(Acenaphthylene,Acy)、苊(Acenaphthene,Ace)、芴(Fluorene,Flu)、菲(Phenanthrene,Phe)、蒽(Anthracene,Ant)、荧蒽(Fluoranthene,Fla)、芘(Pyrene,Pyr)、苯并[a]蒽(Benzo(a)anthracene,BaA)、(Chrysene,Chr)、苯并[b]荧蒽(Benzo(b)fluoranthene,BbF)、苯并[k]荧蒽(Benzo(k)fluoranthene,BkF)、苯并[a]芘(Benzo(a)pyrene,BaP)、茚并[1,2,3-cd]芘(Indeno(1,2,3-cd)pyrene,IcdP)、二苯并[a,h]蒽(Dibenzo(a,h)anthracene,DahA)、苯并[g,h,i]苝(Benzo(ghi)perylene,BghiP)。测试结果以内标法定量,最终结果经回收率校正,数据分析采用统计分析SPSS软件。
2 结果与讨论
2.1 沉积物中PAHs的含量和组成特征
本研究对18个站位沉积物的15种PAHs单体进行了分析测试,除Acy、BaA、BaP、DahA外,其它化合物的检出率均达到100%,图2(a)为18个站位ΣPAHs的含量。ΣPAHs的含量范围在43.18~133.06ng/g,均值为80.53ng/g,相对标准偏差为30.5%,其中站4和站8含量最高,分别是132.38ng/g和133.06ng/g;若不讨论站4和站8,其它站位ΣPAHs含量的相对标准偏差为22.2%,表明研究区域PAHs含量的差异较小。
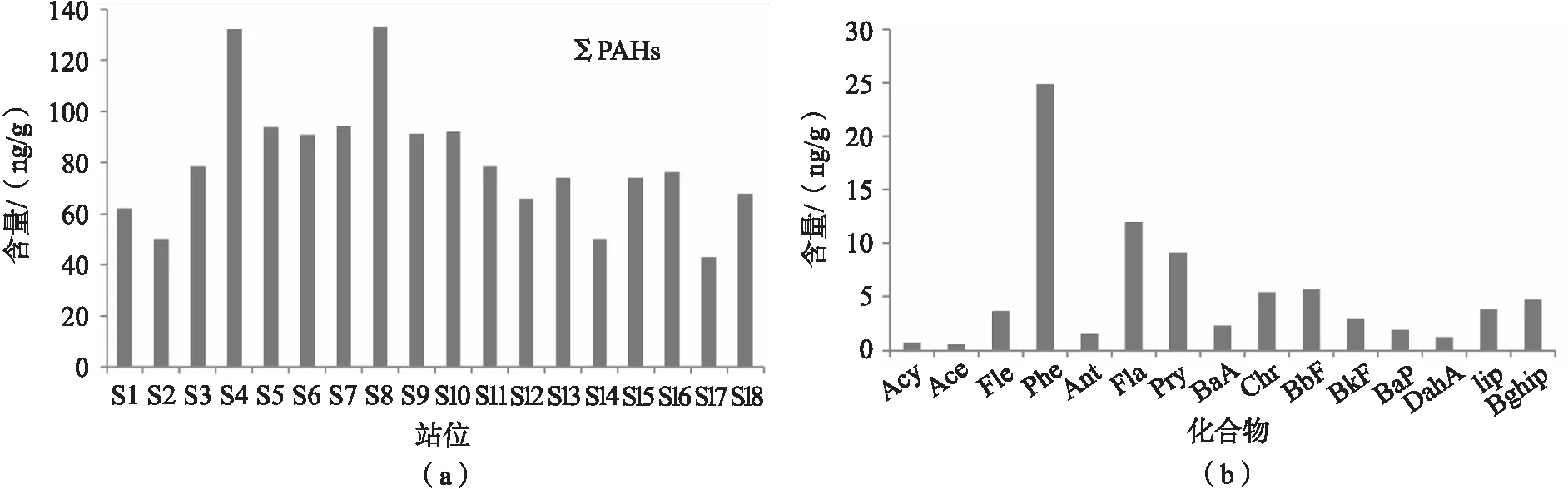
图2 18个站位的ΣPAHs含量(a)和15种PAH单体的含量(b)
图2(b)显示15种PAHs单体的含量,其中Phe含量最高,含量范围为13.62~32.11ng/g,均值为24.83ng/g,其次为Fla、Pyr和BbF。陈志强等[7]研究表明,湛江湾柱状沉积物∑PAHs含量均值为132.72ng/g,以Phe、Fla、Pyr和BbF为主,与本研究结果一致。表1中列出了南海[8]、南黄海中部[9]、台州湾[10]、大亚湾[11]、Daliao River Estuary[12]、Pearl River Esruary[13]沉积物中PAHs的含量。与其它海域相比,本研究区域沉积物的PAHs含量处于较低水平。
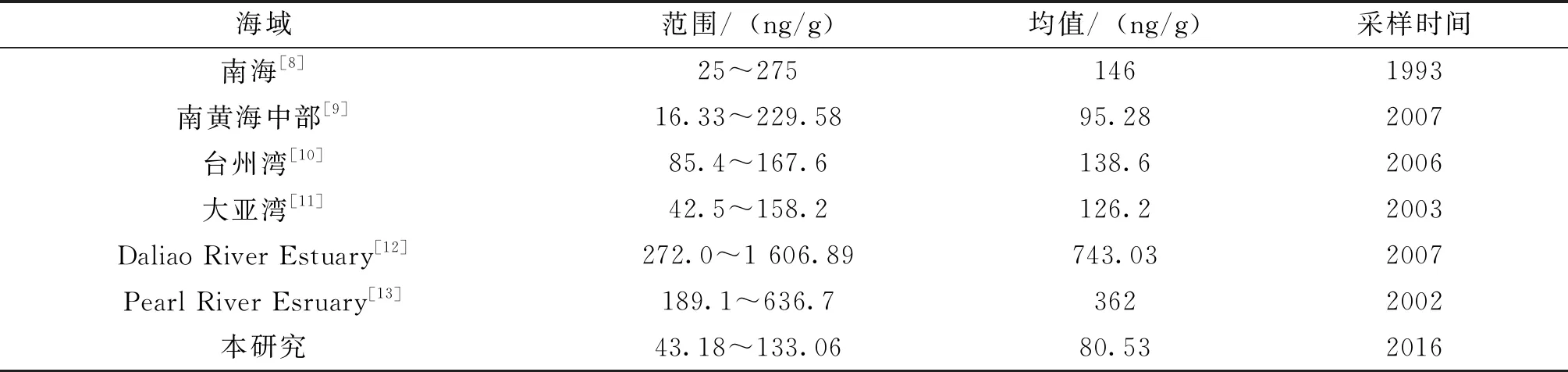
表1 本研究与其它海域沉积物ΣPAHs的含量比较
2.2 沉积物中PAHs的来源分析
2.2.1 PAHs成分构成对其来源的指示意义
PAHs的轻重组分常用于探讨PAHs可能的来源,一般情况下,2~3环低分子量的PAHs来自石油源,4~6环高分子量的PAHs来自燃烧源。因此,PAHs的低环/高环比值用以判别石油源和燃烧源,当低环/高环>1时表征石油源,反之则表征燃烧源[14-16]。图3为18个站位3环~6环PAHs的含量百分比构成和LMW/HMW比值,体现出如下特征:
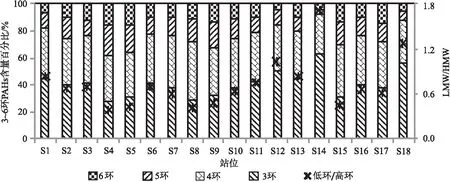
图3 沉积物中3环~6环PAHs含量百分比和低环/高环PAHs比值
(1)在站位S12、S14和S18,3环PAHs占有绝对优势,占ΣPAHs的50.9%、63.0%和56.0%,低环/高环比值分别为1.04、1.71和1.27,表征这些站位沉积物中的PAHs来自石油源;S1和S13的3环均占ΣPAHs的45.4%,低环/高环之比均为0.83,说明石油源占优势,但同时也有燃烧源的贡献;
(2)在站位S4、S5、S8、S9和S15,4环PAHs占有明显优势,含量百分比在33%~43%,是主要的PAHs化合物,4~5环PAHs占∑PAHs的54%~60%,低环/高环比值低于0.5,表征PAHs主要来自燃烧源;
(3)除上述站位外,低环/高环比值为0.6~0.8,表征石油源占优势,同时也有燃烧源的贡献。
2.2.2 PAHs特征比值对其来源的指示意义
同分异构体比值法是目前判断PAHs来源最常用的方法,当Ant/(Ant+Phe)<0.1时表明PAHs来自石油源,反之则是燃烧源;Fla/(Fla+Pyr)<0.4、IcdP/(IcdP+BghiP)<0.2指示石油源,Fla/(Fla+Pyr)>0.5、IcdP/(IcdP+BghiP)>0.5指示煤和生物质燃烧源,中间比值则指示石化燃料燃烧源;BaA/(BaA+Chr)<0.2为石油源,BaA/(BaA+Chr)>0.35为燃烧源,中间值则为石油和燃烧源的混合源[14-16]。图4为18个站位PAHs异构体的特征比值图,显示18个站位的Fla/(Fla+Pyr)比值均>0.5,均值0.57,除站位S4外其它站位的Ant/(Ant+Phe)比值均<0.1,均值为0.06,表明PAHs来自石油源和煤、生物质燃烧。BaA/(BaA+Chr)比值在0~0.40,均值为0.27,IiP/(IiP+BghiP)比值在0.36~0.72,均值为0.45,表征PAHs主要来自石油源和石化燃料燃烧源。
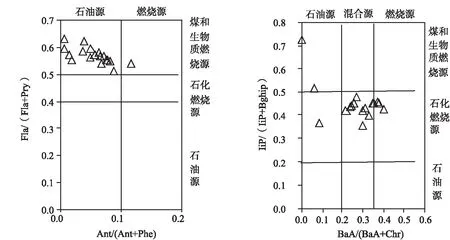
图4 PAHs异构体特征比值分布图
本研究中PAHs来自石油源、煤和生物质燃烧和石化燃料燃烧混合源,与湛江湾和湛江湾陆源入海排污口沉积物中PAHs沉积物中PAHs来源特征相同[7, 17]。本研究中石油源的特征明显,原因可能是冷却所用的海水直接取自湛江湾,沉积物PAHs受海水PAHs的影响;由于电厂周边存在着大面积的农耕区,使得沉积物高环数PAHs占ΣPAHs的比例增加,煤、生物质燃烧源具有重要贡献;由于研究区域具有多个码头,石油源的特征较明显。
2.2.3 主成分分析
通过SPSS统计分析软件,采用主成分分析法对研究区域沉积物中PAHs的来源进行解析。经过主成分提取和最大方差旋转法提取到两个主成分因子,总方差解释率为75.1%,表2为旋转后的各因子载荷表。第一主成分的解释率为46.3%,在高环PAHs具有较高载荷,表示石化燃料的高温燃烧[18];第二主成分的解释率为28.8%,主要是3环和4环PAHs有较大负荷值,可产生于木材、煤在低至中等温度范围内的燃烧[19],同时低环PAHs由石油和油类有关物质产生[20],因此该主成分表示煤、生物质燃烧源和石油源的贡献。
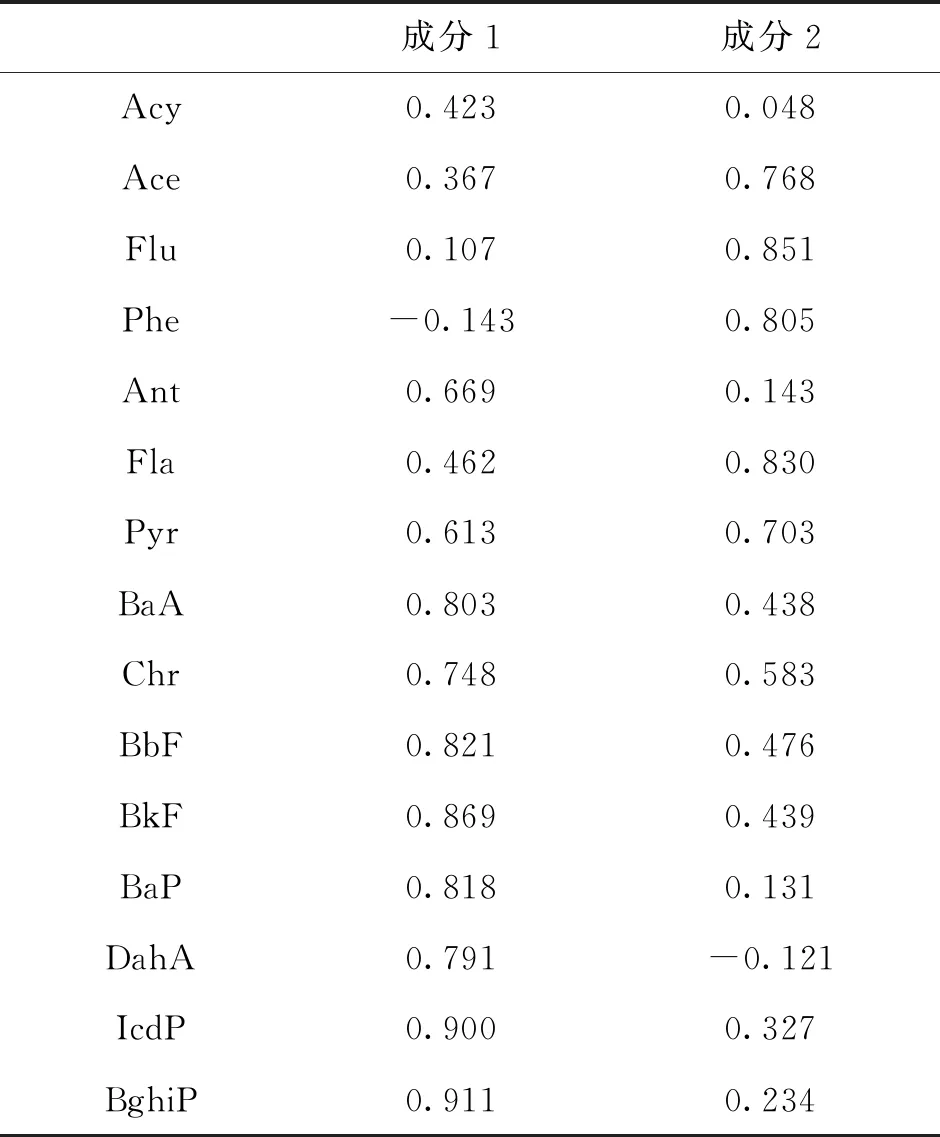
表2 各因子载荷表
2.3 沉积物中PAHs的生态风险评价
沉积物质量基准法(SQGs)常用于评估河口、海湾和湖泊沉积物中PAHs的生态风险,当检测值小于ERL(effects range-low, ERL)时,PAHs对生物有毒害作用的概率<10%,很少产生负面的生态影响;检测值大于ERM(effects range-median, ERM)时,PAHs对生物有毒害作用的概率高于50%,生物毒性效应将频繁发生;若介于两者之间,PAHs将偶尔产生生物毒性效应。根据Long等[21]建议的生态风险评价标准,本研究区域PAHs含量的最大值均小于ERL值,表明研究区域PAHs的生态风险低(见表3)。
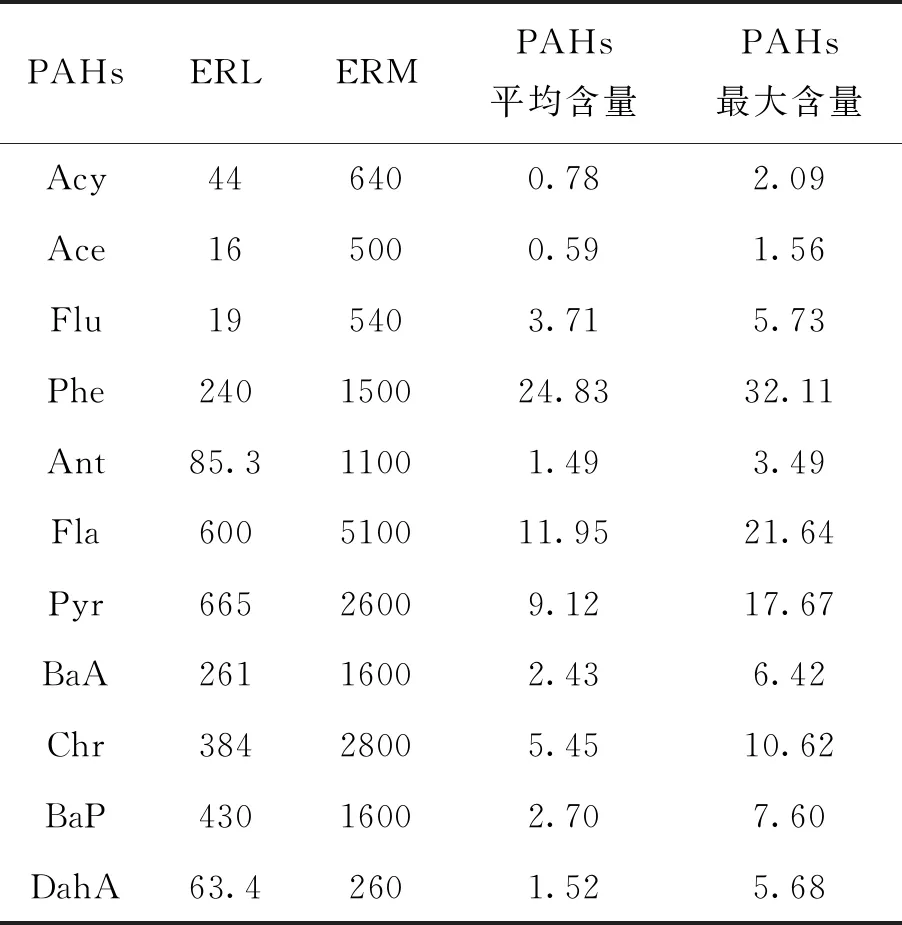
表3 沉积物中PAHs含量与ERL和ERM值比较/(ng/g)
3 结论
本研究对湛江湾某电厂营运初期温排水口沉积物中的PAHs特征进行研究,以此获得该区域PAHs的基本资料。相对于其它海域,研究区域PAHs的含量水平低,空间分布差异小,生态风险低,来源主要为石化燃料、煤和生物质燃烧等燃烧源和石油源混合源。本研究中PAHs的含量和来源特征与湛江湾及陆源入海排污口研究结果具有较好的一致性,可为进一步探讨海水冷却水对邻近局部海域的影响提供基础资料和数据。
