艾迪注射液联合培美曲塞及铂类药物一线治疗非小细胞肺癌(肺腺癌)的临床观察Δ
2021-12-22毛国富李松花倪国华丰奕恒
毛国富,李松花,倪国华,刘 敏,丰奕恒
(1.丹阳市人民医院临床药学科,江苏 丹阳 212300; 2.丹阳市人民医院肿瘤科,江苏 丹阳 212300)
肺癌是呼吸道常见恶性肿瘤,随着环境污染、不良生活习惯、精神压力和基因遗传等因素的影响,肺癌的发病率逐年升高,2020年全球预计新发肺癌患者超过200万例[1]。肺癌早期因为缺乏特异性表现,患者在明确诊断时病情多已进展至中晚期[2]。治疗后的高复发率导致肺癌的病死率仍居高不下。目前,临床上主要以手术为主,放疗、化疗、靶向治疗和免疫治疗等多种手段联合的综合治疗方法,以期延长肺癌患者的生存期和改善其生活质量。以铂类为基础的双药联合方案是中晚期非小细胞肺癌(non-small cell lung cancer,NSCLC)标准的化疗方案,但因为肿瘤的复发性和抗肿瘤药作用的选择性低,导致治疗疗程长、不良反应发生率高,患者依从性降低,从而中断治疗[3-4]。抗肿瘤中药注射剂是我国独创的中药现代化新剂型,因其具有多组分、多靶点和双向调节等独特药理作用,目前已成为我国抗肿瘤治疗的特色之一。肺癌属于中医理论中“肺积”“咳嗽”和“痰饮”等范畴,临床上常用的艾迪注射液、康莱特注射液等中药可有效提高机体免疫功能,减轻骨髓抑制,进而改善患者的生活质量,延长生存期,对放化疗有增敏减毒等功效[5-6]。本研究旨在探讨艾迪注射液辅助治疗中晚期NSCLC(肺腺癌)的疗效,为临床用药提供参考依据。
1 资料与方法
1.1 资料来源
选取2019年4月至2020年3月丹阳市人民医院收治的NSCLC(肺腺癌)患者122例。纳入标准:(1)符合《原发性肺癌诊疗规范》中晚期肺癌的诊断标准[7];(2)经过病理学结果证实为Ⅲ—Ⅳ期NSCLC(肺腺癌),同时基因突变检测排除表皮生长因子受体突变;(3)具有至少1个影像学可测量病灶;(4)患者自愿签署知情同意书,年龄18~70岁,美国东部肿瘤合作组(Eastern cooperative group,ECOG)评分<2分;(5)初次确诊NSCLC,既往未接受过化疗、靶向治疗和免疫治疗等。同时满足以下排除标准:(1)合并其他部位恶性肿瘤者;(2)合并血液系统疾病、机体严重感染、肿瘤已脑转移者;(3)合并严重并发症或合并心肝肾脏器功能不全、自身免疫疾病者,妊娠期、哺乳期妇女;(4)既往接受过针对NSCLC的治疗或预计生存期<3个月者;(5)对研究中的药物过敏、正在参与其他研究和依从性差无法遵循研究程序者。采用随机数字法将所有入组患者平均分为研究组61例和对照组61例。两组患者的性别、年龄、疾病分期和体力状态等基线资料比较的均衡性较高,见表1。对照组患者采用培美曲塞+顺铂治疗,研究组患者采用艾迪注射液联合培美曲塞+顺铂治疗,本研究通过医院伦理委员会备案审批。

表1 两组患者基线资料比较
1.2 方法
研究组患者采用艾迪注射液联合培美曲塞+顺铂治疗:给予艾迪注射液(规格:每支10 ml)100 ml,以0.9%氯化钠注射液400 ml稀释后静脉滴注,1日1次,10 d为1个疗程。同时给予注射用培美曲塞二钠(规格:100 mg)500 mg/m2,静脉滴注10 min,第1日;培美曲塞治疗前后7 d内肌内注射维生素B121次,1 000 μg,培美曲塞给药前1 d、当日和给药后3 d内,每日给予地塞米松1次4 mg,1日2次,口服,此外给药前7 d内开始给予叶酸,1次400 μg,1日1次,口服,服用至最后1次给药后21 d。给予注射用顺铂(规格:10 mg)75 mg/m2,静脉滴注2 h以上,第1—3日。治疗21 d为1个周期,共治疗2~4个周期,期间严密监测患者的不良反应,根据患者的耐受性及时停药。
对照组患者采用培美曲塞+顺铂治疗,治疗方法、给药剂量和预处理等均与研究组保持一致。
1.3 观察指标
观察对比两组患者治疗后的近期疗效和1年生存率,观察记录两组患者肿瘤标志物水平变化,包括神经元特异性烯醇化酶(NSE)、癌胚抗原(CEA)、细胞角蛋白19可溶性片(Cyfra21-1)和糖类抗原199(CA199)等。观察对比两组患者治疗期间的不良反应,采用世界卫生组织抗癌药物急性和亚急性毒性反应分度标准对不良反应进行分级,分为0—Ⅳ级,对比两组患者的不良反应发生情况及严重的(Ⅲ—Ⅳ级)不良反应发生情况。
1.4 疗效评定标准
采用实体瘤临床疗效评价标准(response evaluation criteria in solid tumor,RECIST)1.1对近期疗效进行评价,分为完全缓解(complete response,CR):所有靶病灶消失且无新病灶,肿瘤标志物水平正常,至少维持4周;部分缓解(partial response,PR):靶病灶的最大直径之和减少>30%,至少维持4周;疾病稳定(stable disease,SD):靶病灶最大直径之和缩小未达到PR,或增加未达到疾病进展;疾病进展(progressive disease,PD):靶病灶的最大直径之和增加>20%,或出现了新的病灶。疗效评估主要包括:客观缓解率(objective response rate,ORR),指肿瘤缩小达到一定程度且维持一定时间的患者比例,包括CR+PR的患者;疾病控制率(disease control rate,DCR),指肿瘤缩小或肿瘤稳定且维持一定时间的患者比例,包括CR+PR+SD的患者。
1.5 统计学方法
采用SPSS 22.0统计软件对本研究中获得的所有数据进行分析处理,计数资料采用χ2检验;计量资料采用t检验;设定检验水准为α=0.05,P<0.05时差异有统计学意义。
2 结果
2.1 两组患者治疗前后肿瘤标志物水平比较
两组患者治疗前CEA、NSE、CA199和Cyfra21-1水平比较,差异均无统计学意义(P>0.05);治疗后,两组患者各肿瘤标志物水平显著降低,且研究组患者治疗后的CEA、CA199和Cyfra21-1水平显著低于对照组患者,差异均有统计学意义(P<0.05),见表2。

表2 两组患者治疗前后肿瘤标志物水平比较
2.2 两组患者治疗后近期疗效及生存情况比较
治疗后,两组患者的ORR和1年生存率比较,差异无统计学意义(P>0.05);研究组患者治疗后的DCR显著高于对照组患者,差异有统计学意义(P<0.05),见表3。

表3 两组患者治疗后近期疗效及生存情况比较[例(%)]
2.3 两组患者不良反应发生情况比较
研究组患者的恶心呕吐、白细胞减少和血红蛋白减少等不良反应所有级别的发生率均显著低于对照组,差异均有统计学意义(恶心呕吐发生率:Z=15.168,P=0.000;白细胞减少发生率:Z=11.084,P=0.000;血红蛋白减少发生率:Z=7.846,P=0.011)。本研究中,两组患者其他所有级别不良反应发生率比较,差异均无统计学意义(P>0.05),见表4。
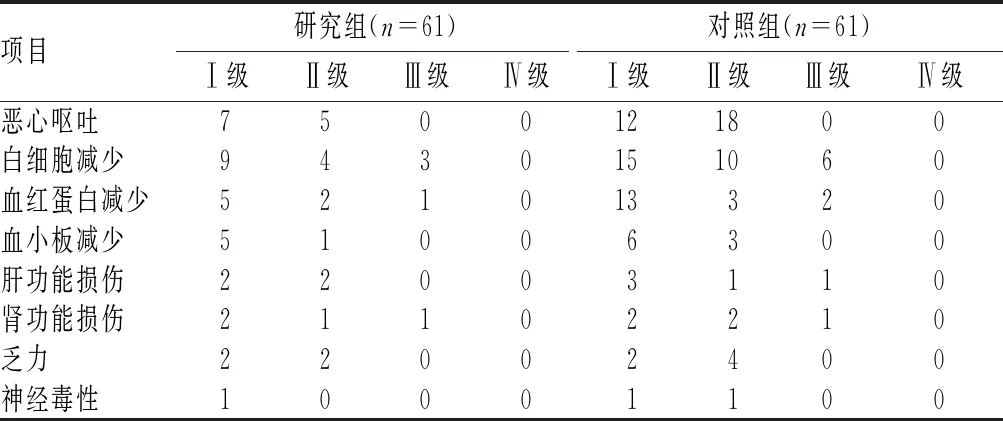
表4 两组患者不良反应发生情况比较(例)
3 讨论
艾迪注射液的主要成分为斑蝥、人参、黄芪和刺五加,目前多被用于肺癌、肝癌、肠癌和妇科恶性肿瘤等疾病的治疗,大量基础和临床研究结果表明,艾迪注射液具有抗肿瘤、提高机体免疫功能、促进骨髓造血功能和改善神经内分泌等功能[7-8]。其作用机制主要包括:(1)去甲斑蝥素可以直接干扰肿瘤细胞核酸代谢,抑制肿瘤细胞蛋白质合成,从而诱导细胞凋亡;可以直接抑制肿瘤新生血管生成[9];同时,可促进骨髓造血干细胞分化、成熟,增加外周血白细胞和血小板数量[10]。(2)人参皂苷可以阻止恶性肿瘤细胞于G1期,进而诱导肿瘤细胞分化;同时,可增强T细胞、淋巴因子激活的杀伤细胞和自然杀伤细胞功能,诱导干扰素、白细胞介素产生[11-12]。(3)黄芪多糖能提高网状内皮系统功能,增强T细胞、淋巴因子激活的杀伤细胞、自然杀伤细胞和白细胞介素11等的抗恶性肿瘤活性[13]。(4)刺五加多糖可干扰或抑制磷脂酰肌醇转换,增强体液免疫,增强B细胞、淋巴因子激活的杀伤细胞和自然杀伤细胞等的活性,还可以通过改变单胺氧化酶及其同工酶的活性,从而影响单胺类神经递质水平,改善神经系统功能,具有明显镇静、改善癌性抑郁综合征等功效[8,14-15]。艾迪注射液通过多环节、多渠道和多靶点的协同药理作用,构成了“减毒、增效”的鲜明治疗特色。
本研究采用艾迪注射液联合顺铂+培美曲塞一线用于中晚期NSCLC(肺腺癌)患者的治疗,结果显示,两组患者治疗后的ORR及1年生存率比较,差异无统计学意义(P>0.05),而研究组患者治疗后的DCR显著高于对照组,差异有统计学意义(P<0.05),与伍家鸣等[16]的结果一致。提示通过艾迪注射液能够保持疾病的稳定,对瘤体缩小的作用不明显。此外,一项Meta分析结果表明,艾迪注射液联合化疗较单纯化疗对瘤体改变的作用更有效[17]。
本研究观察了两组患者治疗前后肿瘤标志物水平变化情况,结果显示,两组患者治疗后的CEA、NSE、CA199和Cyfra21-1水平均显著降低,而研究组患者CEA、CA199和Cyfra21-1水平的降低程度更显著。CEA在许多上皮来源的恶性肿瘤中均为高表达状态,且相关研究结果表明,CEA水平高低与肿瘤大小及转移情况呈正线性相关[18];CA199是消化道肿瘤中常见的标志物,在正常人体内表达水平极低,在肺癌患者体内会处于高表达状态;Cyfra21-1是一种新型的肺癌标志物,尤其是对于NSCLC具有较高的诊断价值。尽管艾迪注射液对肿瘤标志物水平影响的机制尚未明确,但本研究结果提示,艾迪注射液能够增强化疗的抗肿瘤效应,降低肿瘤标志物水平。
此外,本研究对两组患者不良反应发生情况进行观察,结果表明,通过艾迪注射液的联合治疗,患者的恶心呕吐、白细胞减少和血红蛋白减少等不良反应发生率显著降低,与对照组的差异有统计学意义(P<0.05)。整体上,两组患者的不良反应多为轻度,且Ⅲ—Ⅳ级不良反应发生率低,而艾迪注射液对患者不会造成新的不良反应,反而能够改善恶心呕吐及骨髓抑制等不良反应。相关研究结果表明,中药注射剂主要通过改善机体免疫功能对血液系统发挥保护作用,部分中药成分能够通过调节胃肠激素和神经递质改善胃肠道功能[19]。
综上所述,培美曲塞联合顺铂是中晚期NSCLC(肺腺癌)患者的重要治疗手段,通过联合应用艾迪注射液,能够进一步提高疾病控制率,降低肿瘤标志物水平,改善胃肠道及血液系统的不良反应。但本研究入组病例数较少,周期较短,尚未分析联合用药对患者长期生存情况的影响,因此需要进一步扩大样本量进行深入研究。
