EB/g-C3N4/Fe3O4复合光催化剂的制备及其在铬污染土壤中的应用
2021-12-17尚荣刚廖辉伟周艳娜黄晓枫
尚荣刚 廖辉伟 周艳娜 周 宇 黄晓枫
(1. 西南科技大学环境友好能源材料国家重点实验室 四川绵阳 621010; 2. 西南科技大学材料科学与工程学院 四川绵阳 621010)
随着工业的发展,环境污染成为当今社会的热门话题。在此背景下,土壤污染成为研究的前沿领域[1]。制革、铬盐等行业的大力发展,导致土壤中Cr(VI)含量超标。Cr(VI) 具有迁移性强、活性较高、毒性大、不易被土壤吸附等特性,使其对环境和动植物造成极大威胁[2-3]。因此,土壤中重金属Cr(VI)的处理成为污染土壤修复的一个重要课题。
目前,光催化还原法、化学清洗法、生物修复法等技术能将Cr(Ⅵ) 还原为Cr(III),从而达到降低Cr(Ⅵ)的生物可利用性和毒性的目的[4]。其中,光催化技术由于反应条件温和、低成本和可持续利用,被认为是高效、绿色治理铬污染土壤的最有效方法之一。
自Hiroshi[5]用TiO2光催化还原Cr(VI)以来,因其光学性能优异、结构稳定等优点,成为大家所熟悉和性能较好的一种常用光催化剂[6-7]。但TiO2不具备可见光响应活性,从而使其应用受到一定限制[8]。g-C3N4光催化剂因具有经济、对可见光响应以及环境友好等优点而受到广泛关注。Liu[9]等将g-C3N4用于处理含Cr(VI)废水,结果表明g-C3N4可将Cr(VI)还原为Cr(III),但其光生电子和空穴复合率较高,严重阻碍其光催化活性,同时粉体易团聚且回收难。
膨润土由于具有孔隙率高、经济及吸附性好等优点被作为良好的光催化剂载体,但因其多层结构导致层间透光性差而使光催化剂效率降低。将其剥离后,比表面积增加且更易受到光照,从而使其负载催化剂的光化学转化效率提高,还可避免粉体g-C3N4的团聚[10]。Fe3O4由于易得、易分离和循环利用的特性,在能够实现催化剂快速回收的同时还能提升g-C3N4的光催化活性。因此,利用剥离膨润土(EB)和Fe3O4可克服g-C3N4的团聚并有利于催化剂的回收再利用。
基于此,本文以剥离膨润土为载体,将g-C3N4与Fe3O4负载于其上,形成具有较高光催化活性的磁性EB/g-C3N4/Fe3O4复合光催化材料。通过研究不同因素对土壤中Cr(VI)光还原率的影响,优化了催化剂使用条件,为磁性复合催化剂处理铬污染土壤提供依据。
1 实验部分
1.1 材料和仪器
试剂:三聚氰胺、六水合氯化铁、乙醇、盐酸、氢氧化钠、膨润土,均为分析纯,成都科龙化工试剂厂。二苯基碳酰二肼、醋酸钠、聚乙二醇、乙二醇,均为分析纯,成都金山化学试剂有限公司。
722S型紫外-可见光分光光度计,上海尤尼科公司;X' Pert PRO型X射线衍射仪:荷兰帕纳科公司);ZeissNTS Ultra55型扫描电子显微镜,德国蔡司仪器公司; KSL-1750型马弗炉,上海苏达实验仪器有限公司;HS-25型pH计,上海仪电科学仪器股份有限公司; KH-1型反应釜,上海岐耀仪器设备有限公司;NOVA 3000型比表面积分析仪,美国康塔公司。
1.2 供试土壤
采集某地的铬污染土壤,采样深度0~30 cm,去除碎石等杂物后,经自然风干,磨碎过10目筛后装袋备用。供试土壤的Cr(VI)含量测定为20 mg/kg,pH值为6.15。土壤pH值通过加入1.0 mol/L HNO3和1.0 mol/L NaOH调节。土壤Cr(VI)含量调节:将K2Cr2O7溶液与风干的土壤混合后风干至恒定重量,测定Cr(VI)直到满足所需含量范围要求。
1.3 EB/g-C3N4材料的制备
参考文献[11]报道的方法制备剥离膨润土(EB)后,取10 mL EB样品与5 g三聚氰胺混合,超声60 min,接着放入烘箱中烘干,干燥后的粉末倒入坩埚并移入马弗炉中,煅烧至550 ℃,保持180 min(升温速率5 ℃/min)。最后,待冷却至20 ℃时取出研磨得到的黄色粉末即为EB/g-C3N4样品。参考文献[12]报道的方法制备g-C3N4。
1.4 EB/g-C3N4/Fe3O4材料的制备
取3.15 g本文1.3节中制备的EB/g-C3N4加入不同质量(0.35,0.79,1.35,2.10 g)氯化铁、4.0 g醋酸钠、2.0 g聚二醇和10 mL乙二醇后,超声30 min,分散后转入20 mL聚四氟乙烯内衬的不锈钢高压釜中,随后于200 ℃下保温反应8 h。最后冷却至室温,用乙醇和去离子水洗涤、过滤,于70 ℃下干燥 6 h,即得样品。根据Fe3O4质量分数记为EB/g-C3N4/Fe3O4-10%,EB/g-C3N4/Fe3O4-20%,EB/g-C3N4/Fe3O4-30%,EB/g-C3N4/Fe3O4-40%。
1.5 修复实验与分析方法
以1.2中的供试土壤为目标污染物来研究催化剂光催化性能对其修复的影响。分别称不同pH值、Cr(VI)含量的供试土壤500 g于若干500 mL塑料盘中与各催化剂均匀混合,在吸附-脱附平衡后,开启350 W氙灯(用滤光片过滤λ<540 nm的紫外光),每间隔30 min取出土壤,根据HJ 491—2009[13]标准测定土壤中总铬含量,按照US EPA Method 3060A[14]和GB/T 15555.4—1995[15]标准测量Cr(VI)含量。土壤的pH值按《土壤 pH值的测定电位法》(HJ 962—2018)[16]测量。Cr(VI)还原率(%)由式(1)计算:
(1)
式中,C0,Ct分别为反应前后 Cr(VI)的含量 (mg/kg)。
1.6 催化剂的再生利用实验
在实验效果最佳的条件下,利用磁铁将进行过光催化实验的EB/g-C3N4/Fe3O4和土壤分离,然后将收集的光催化剂洗涤干燥,在相同的条件下,再次使用干燥后的EB/g-C3N4/Fe3O4进行光还原实验,重复进行这3个步骤,测得复合光催化剂EB/g-C3N4/Fe3O4的循环再生情况。
1.7 材料表征及土壤中Cr(VI)含量测定
采用X' Pert PRO型多用途粉末衍射仪对光催化剂晶体结构进行XRD表征(光源CuKα,2θ=3°~80°,扫描速率 5°/min)。采用NOVA 3000型比表面积分析仪测定催化剂的比表面积(BET)。催化剂的微观形貌利用ZeissNTS Ultra55型扫描电子显微镜(SEM)观察。光反应后,将定时取的样,用722S型紫外-可见光分光光度计测量土壤中Cr(VI)含量。
2 结果与讨论
2.1 样品表征
EB,Fe3O4,g-C3N4和EB/g-C3N4/Fe3O4的XRD图谱如图1所示。纯g-C3N4两个明显的特征峰位于2θ=13.2° 和27.6°[17],它们分别对应g-C3N4的(100)晶面和(002)晶面的特征衍射峰。Fe3O4在5°~80° 之间的明显特征峰有:18.0°,30.1°,35.5°,43.9°,52.9°,57.7°,63.4°,这些数据与标准卡片(PDF#65-3107)中的描述大致相当[18]。宽化、弱化的EB峰表明,液相法破坏了膨润土层状结构,证明膨润土被成功剥离为基本结构单元的片状。EB/g-C3N4/Fe3O4上同时具备EB,g-C3N4和Fe3O4的特征峰,表明g-C3N4和Fe3O4成功负载于EB上。而EB/g-C3N4/Fe3O4上的Fe3O4特征峰非常尖锐,表明Fe3O4晶体结构完好。
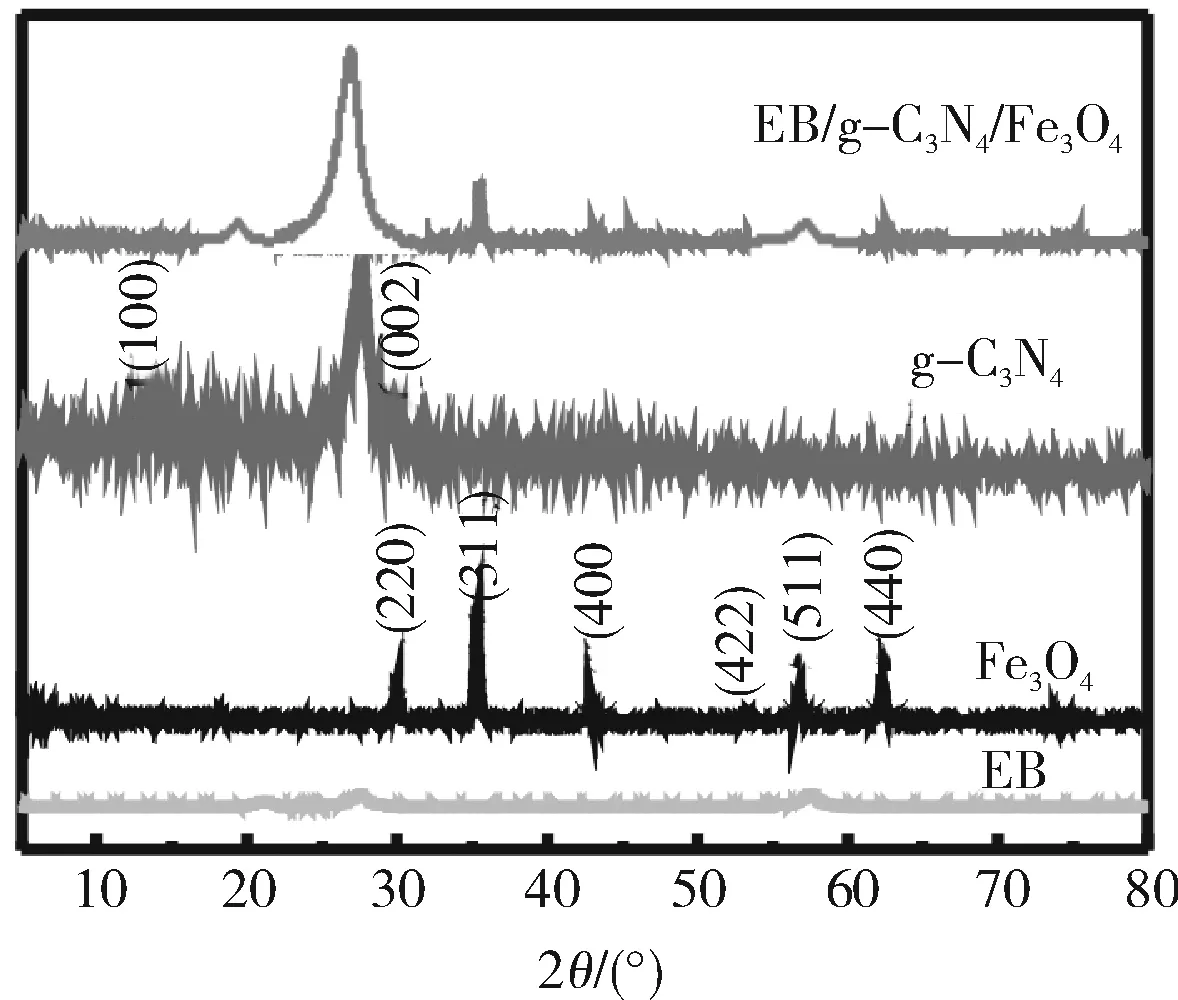
图1 样品的XRD图谱Fig.1 XRD pattern of the samples
比表面积对光催化剂的催化性能起着重要作用。g-C3N4,EB和EB/g-C3N4/Fe3O4-30%的比表面积分别为25.19,67.35,55.99 m2/g。相对于单一的EB,比表面积较大的EB/g-C3N4/Fe3O4复合物在光催化反应中不仅能提供较多的活性位点,还可减少g-C3N4粉体的团聚,让g-C3N4和Fe3O4尽可能地负载在其上,使EB/g-C3N4/Fe3O4复合物同时具备较大的比表面积和优良的光催化性能。与此同时,高比表面积有利于电子的传输,加速光催化反应进行,从而提升EB/g-C3N4/Fe3O4复合催化剂的光催化活性,这一结果与图8的描述一致。
EB,Fe3O4,g-C3N4和EB/g-C3N4/Fe3O4的SEM图片如图2所示。图2(a)表明水热法合成的Fe3O4颗粒呈现较为规律的球形。图2(b)表明合成的g-C3N4整体呈现不规则、大小不一的片状堆叠结构,其比表面积较大且堆积严重。图2(c)显示,膨润土经过剥离后,其结构如薄片状,且存在卷曲现象,这是由基本结构单元组成的超薄片。由图2(d)可明显看出,大量 Fe3O4微球与g-C3N4附着在EB片层上,形成了EB/g-C3N4/Fe3O4复合材料。

图2 样品的SEM图Fig.2 SEM images of the samples
2.2 EB/g-C3N4/Fe3O4处理铬污染土壤的工艺条件优化
2.2.1 Fe3O4含量对Cr(VI)还原率的影响
在EB/g-C3N4/Fe3O4复合材料中,Fe3O4不仅作为磁性组分,还能提升EB/g-C3N4/Fe3O4对Cr(VI)的还原率。研究4种不同Fe3O4含量的EB/g-C3N4/Fe3O4对Cr(Ⅵ)的还原情况,结果如图3所示。由于g-C3N4的光生电子-空穴复合率较高,Fe3O4易团聚,纯Fe3O4和纯g-C3N4对土壤中Cr(VI)的还原率并不高,在20%~50%之间。相比于EB,g-C3N4的加入显著提升了EB/g-C3N4对Cr(VI)的还原率。在EB/g-C3N4/Fe3O4复合材料中,当Fe3O4含量增加到30% 时,Cr(VI)的还原率都在80%以上,但当Fe3O4含量增加到40% 时,Cr(VI)还原率反而降低。这是由于EB/g-C3N4/Fe3O4的较大比表面积增加了可见光吸收,促进了光生电子-空穴对的分离,从而提升了光催化性能。Fe3O4的导带高于O2/·O2-(-0.33 eV)电位,复合材料表面的O2不能被还原为·O2-,而光生电子会迁移到Fe3O4的导带,故Fe3O4过量时,光生电子会移动到Fe3O4,导致光催化性能下降。所以,EB/g-C3N4/Fe3O4体系中Fe3O4的最佳含量为30%[19]。

图3 不同Fe3O4含量下Cr(VI) 的还原率Fig.3 Reduction rates of Cr(VI) at different Fe3O4 contents
图4为不同EB/g-C3N4/Fe3O4-30%投加量下Cr(VI)的还原率。250 min时,投加量在0.5,1.0,1.5,2.0 g下的Cr(VI) 还原率依次是35.6%,45.0%,69.0%和47.0%。从图4可以看出,投加量在1.5 g时,Cr(VI) 还原率达到最佳。继续增加催化剂含量时,来不及反应的催化剂会与土壤中的其他离子反应,产生竞争而降低还原率。在当前实验条件下,1.5 g剂量时Cr(VI)的还原率达到最大值,继续增加催化剂的剂量反而不能使还原率再度增加。因此,从提高还原率和经济性角度考虑,EB/g-C3N4/Fe3O4复合催化剂的最优投加量为1.5 g。

图4 不同EB/g-C3N4/Fe3O4-30%投加量下Cr(VI) 的还原率Fig.4 Reduction rates of Cr(VI) at different EB/g-C3N4/Fe3O4-30% dosing rates
2.2.2 初始Cr(VI)含量对还原率的影响
为考察EB/g-C3N4/Fe3O4-30%对土壤中不同Cr(VI)含量的光还原能力,研究了5~100 mg/kg范围内 Cr(Ⅵ)污染土壤的光催化还原情况,结果如图5所示。土壤中Cr(VI)含量在 0~60 mg/kg范围时,Cr(VI)含量对还原率有极大影响。其中Cr(VI)含量为20 mg/kg时,Cr(VI)还原率达到峰值,这一结果与表1一致,此时速率常数最大。当土壤中Cr(VI)含量超过60 mg/kg时,由于过量的Cr(VI)会富集在催化剂的表面,造成活性位点被占据,致Cr(VI)含量对其还原率影响较小。综上所述,最佳初始Cr(VI)含量约为20 mg/kg。

图5 不同初始Cr(VI)含量的还原率Fig.5 Reduction rates of different initial Cr(VI) contents
2.2.3 土壤pH值对Cr(VI)还原率的影响
在不同土壤pH值(4.41~10.16)下,投加1.5 g EB/g-C3N4/Fe3O4-30%于Cr(VI)含量为20 mg/kg土壤中,其Cr(VI)光还原率如图6所示。土壤pH值为6.15时,Cr(VI)还原率最高时可达到97%,在250 min 后依然可保持在80%附近。土壤pH值在6.15时,在催化剂的表面质子化较高,增加的表面电荷对Cr(VI) 静电引力更强,不仅利于光还原,正负电荷的静电吸引也提高了EB/g-C3N4/Fe3O4对 Cr(Ⅵ)的吸附能力。在强酸性土壤中,H+会与Fe3O4发生反应破坏复合材料的结构;强碱性土壤中,不利于g-C3N4,Fe3O4间的电子传递。因此,适用土壤的最佳pH值约为 6.15。

图6 不同土壤pH值下Cr(VI)的还原率Fig.6 Reduction rates of Cr(VI) at different soil pH
2.2.4 EB/g-C3N4/Fe3O4的循环利用
光催化剂的循环利用也是评价催化剂性能和经济性的重要参数。将反应后的EB/g-C3N4/Fe3O4-30%进行磁分离收集,干燥后进行循环实验。如图7、图8所示。在初始Cr(VI)含量为20 mg/kg,土壤pH值6.15,催化剂投加量为1.5 g情况下(即在实验条件最佳时),将其重复使用3次后,EB/g-C3N4/Fe3O4的还原率仍达95.3%。磁回收率仍然高达90%。但经过两次回收以后,其光还原率略有下降,这是由于在催化中部分活性位点阻塞和损失所造成的。总体而言, EB/g-C3N4/Fe3O4对土壤中Cr(VI)具有高效的还原活性,且具有良好的重复使用性能。

图7 EB/g-C3N4/ Fe3O4-30% 的磁回收率Fig.7 Magnetic recovery of EB/g-C3N4/ Fe3O4-30%

图8 催化剂还原土壤中Cr(VI) 的活性图Fig.8 Activity diagrams of the catalyst for the reduction of Cr(VI) in soil
2.2.5 动力学研究
在Cr(VI)光还原率最佳条件下进行了动力学研究。如图9所示,ln(C0/Ct)与光照时间具有明显的线性关系。EB/g-C3N4/Fe3O4-30%对Cr(VI)的还原可通过Langmuir-Hinshelwood(L-H)模型评估[21-22],计算如式(2)所示:
(2)
其中:r0是初始光催化还原率(mg·kg-1min-1);C0为Cr(VI)初始含量(mg/kg);KLH是吸附平衡常数(mg/kg)。式(2)可以简化为式(3):
(3)
其中:Ct为时间t时的Cr(VI)的含量;线性回归的斜率是伪一阶速率常数Kapp,Kapp=KrKLH。一般情况下,初始还原率可推导如式(4):
r0=KappC0
(4)
如图9所示,ln(C0/Ct)与时间的斜率表示表观伪初阶速率常数Kapp。在不同的初始浓度下所获得的值列于表1。按式(3)进行线性化时,可得到式(5)所示关系式:

图9 Cr(VI)还原的ln(C0/Ct)对光照时间的线性变换Fig.9 Linear transformation of Cr(VI)-reduced ln(C0/Ct) on photoperiod
(5)
根据表1中的数据绘制的图10可知,1/r0与1/C0的相关性很好。因此L-H是Cr(VI)还原的最佳动力学模型,其动力学公式(5)满足于图10,获得截距为1/Kr、斜率为1/KrKLH的直线,其中,Kr和KLH的值分别为3.9 mg·kg-1·min-1和 0.021 8 mg·kg-1。回归线的相关系数(R2)为0.997。Kr>KLH,表明Cr(VI)被吸附的表面反应是该过程的控制步骤。

图10 不同Cr( Ⅵ)含量下1/r0和1/C0间的相关性Fig.10 Correlation between 1/r0 and 1/C0 at different Cr(VI) contents

表1 Cr(VI)还原的伪一阶表观常数Table 1 Pseudo-first-order apparent constants of Cr(VI) reduction
2.2.6 EB/g-C3N4/Fe3O4的光催化机理
EB/g-C3N4/Fe3O4的光催化机理如图11所示。可见光照在EB/g-C3N4/Fe3O4上时,g-C3N4价带(VB)上的电子(e-)经光激发跃迁到导带(CB)时,由于g-C3N4的CB位置比Fe3O4更高,所以g-C3N4产生的光生电子会向Fe3O4的CB位置转移。由于高电导率的Fe3O4传输e-速度快,抑制EB/g-C3N4/Fe3O4复合体系中e-和h+的直接重组,因此Fe3O4是g-C3N4光诱导电子的接受体。此外,EB中自带的e-和Na+也会与g-C3N4中e-和h+反应,进一步抑制e-和h+的重组。最后,EB/g-C3N4/Fe3O4界面的存在,更进一步抑制e-和h+的重组。这也是EB/g-C3N4/Fe3O4比EB/g-C3N4光催化性能更优的原因。
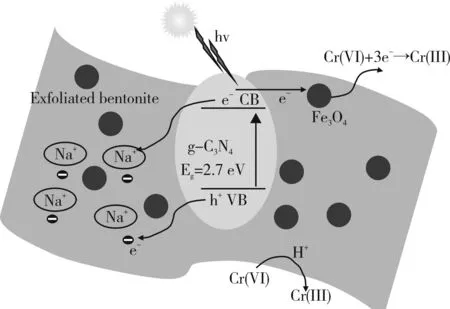
图11 EB/g-C3N4/Fe3O4催化还原机理示意图Fig.11 Schematic diagrams of EB/g-C3N4/Fe3O4 catalytic reduction mechanism
Fe3O4和g-C3N4产生的e-是良好的还原剂,可以有效地将吸附在EB/g-C3N4/Fe3O4附近的Cr(VI)还原为Cr(III)[20]。此外,酸性和碱性土壤中的H+和OH-也将会与Cr(Ⅵ)反应(如式(6)、式(7)),从而达到提升光催化性能的目的。
Cr( Ⅵ) 在酸性土壤条件下的反应为:
2Cr2O72-+16H+→ 4Cr3++8H2O+3O2
(6)
Cr( Ⅵ) 在碱性土壤条件下的反应为:
4CrO42-+2OH-→ 4Cr3++10H2O +3O2
(7)
3 结论
(1)采用EB/g-C3N4/Fe3O4处理铬污染土壤,在EB/g-C3N4/Fe3O4投加量1.5 g,土壤pH值6.15,Cr(Ⅵ)含量20 mg/kg,Fe3O4含量为30%,光照250 min的最优条件下,土壤中Cr( Ⅵ)的光还原率可达97%。循环使用3次后光还原能力及磁回收率仍保持较高水平。Cr(VI)还原的最佳动力学符合Langmuir-Hinshelwood模型。
(2)EB/g-C3N4/Fe3O4复合材料光催化性能的提升,为铬污染土壤的实际处理提供了实验参考及理论依据。基于EB/g-C3N4/Fe3O4回收容易及光还原能力强的特性,EB/g-C3N4/Fe3O4在重金属污染处理方面有广阔的应用前景。
