外周血Cyp A、NF-κB及VEGF水平与CHD患者术后再狭窄的相关性
2021-12-16李洪朱强石梦然刘福元
李洪 朱强 石梦然 刘福元
作者单位:湖北医药学院附属襄阳市第一人民医院心血管内科,湖北,襄阳441000
冠心病(coronary atherosclerotic heart disease,CHD)是由于血管狭窄或闭塞,导致心肌缺血、缺氧而引起的心脏病,以突发性心前区疼痛为主要症状[1]。经皮冠状动脉介入术(percutaneous coronary intervention,PCI)是治疗CHD 的首要方法,具有显著疗效,但可损伤冠脉血管,导致支架内再狭窄发生,而支架内再狭窄是影响患者预后的主要因素之一[2]。据报道显示,支架再狭窄的发生率为20%[3],对CHD患者预后产生严重影响。中亲环素A(Cyclophilin A,Cyp A)是氧化应激引起组织损伤的介质,可通过促进单核细胞粘附和创造氧化环境来促进炎症,在动脉粥样硬化的几个阶段中发挥重要作用[4]。核因子-κB(nuclear factor-κB,NF-κB)是炎症和免疫调节的关键核转录因子,可通过调节细胞因子和炎症分子的表达,参与冠心病过程[5]。血管内皮生长因子(vascular endothelial growth factor,VEGF)是一种特异的内皮细胞促分裂剂,能特异性促进血管内皮细胞的增殖和分裂,促进细胞转移,促进血管生成[6]。本研究将分析外周血Cyp A、NF-κB及VEGF水平与CHD患者PCI术后再狭窄的关系,以期为临床降低再狭窄发生率提供参考。现报道如下。
1 资料与方法
1.1 一般资料
选取2018年8月至2019年8月本院收治的200 例行PCI术治疗的CHD患者为研究对象。纳入标准:①符合《临床冠心病诊断与治疗指南》[7]中诊断,冠脉造影示左主干管腔狭窄程度≥50%,分支血管管腔狭窄程度≥75%,成功置入支架,无支架贴壁不良;且均于6~12 个月内行CAG 复查;②年龄40~80 岁;③知情同意并经医院伦理委员会批准。排除标准:①脏器功能不全;②合并恶性肿瘤者;③认知障碍者;④急性脑血管疾病、急性心肌梗死、风湿性心脏病及肝功能损害者。随访1年,根据冠脉造影结果分为血管再狭窄组(n=40)和血管未再狭窄组(n=160)。
1.2 研究方法
记录两组患者临床资料,包括性别、年龄、吸烟史、高血压病史及支架长度、直径及数量。术后12 个月后采集3.0 mL 患者外周静脉血,离心10 min 分离血浆,采用雅培越捷型血糖仪(雅培贸易上海有限公司,批准文号:2404047)检测空腹血糖(fasting plasma glucose,FPG);采用全自动生化分析仪(日立7600 系列全自动生化分析仪)测定总胆固醇(totalcholesterol,TC)、甘油三酯(triglycerides,TG)、纤维蛋白原(Fibrinoge,FIB)、低密度脂蛋白(low-density lipoprotein cholesterol,LDL-C)、高密度脂蛋白(high-density lipoprotein cholesterol HDL-C)、红细胞计数(Red blood cells,RBC)、D-二聚体(D-Dimer,DD)、中性粒细胞、白细胞计数(White Blood Count,WBC)及淋巴细胞表达水平;采用酶联免疫吸附法(山东风途物联网科技有限公司FT-SY96A 型)检测血清Cyp A、NF-κB、VEGF水平。
1.3 统计学处理
采用SPSS 20.0 软件进行统计分析,计数资料采用n(%)表示,行χ2检验,计量资料采用()表示,行t检验,多因素采用logistic 回归分析,以P<0.05 为差异有统计学意义。
2 结果
2.1 CHD患者PCI术后再狭窄的单因素分析
两组FPG、LDL-C、TC、FIB、Cyp A、NF-κB、VEGF及支架直径比较差异有统计学意义(P<0.05),两组性别、年龄、吸烟史、高血压病史、TG、LDL-C、HDL-C、RBC、DD、中性粒细胞、WBC、淋巴细胞、支架长度及支架数量比较差异无统计学意义(P>0.05)。见表1。
表1 CHD患者PCI术后再狭窄的单因素分析[n(%),(±s)]Table 1 single factor analysis on restenosis of CHD patients after PCI[n(%),(±s)]
项目年龄(岁)性别 男女吸烟史高血压病史FPG(mmol/L)TG(mmol/L)TC(mmol/L)LDL-C(mmol/L)HDL-C(mmol/L)FIB(g/L)RBC(×1012/L)DD(ug/L)中性粒细胞(×109/L)WBC(×109/L)淋巴细胞(×109/L)Cyp A(ng/mL)NF-κB(pg/mL)VEGF(ng/L)支架长度(mm)支架直径(mm)支架数量(个)血管再狭窄组(n=40)62.56±7.80 30(75.00)10(25.00)22(55.00)26(65.00)6.25±2.05 1.62±0.14 5.04±2.33 3.45±0.30 1.05±0.23 4.34±0.51 4.35±1.28 261.52±20.36 4.71±1.22 7.02±2.16 1.58±0.19 17.82±5.69 52.65±7.03 313.28±50.36 22.80±6.53 2.84±0.70 1.85±0.23血管未再狭窄组(n=160)61.82±7.76 128(80.00)32(20.00)85(53.13)87(54.38)5.40±1.63 1.65±0.19 4.21±1.56 2.61±0.35 1.12±0.26 3.22±0.40 4.41±1.36 255.60±18.77 4.67±1.20 6.97±2.13 1.63±0.21 13.71±3.90 35.59±5.23 259.41±40.26 23.04±6.58 3.15±0.98 1.80±0.17 t/χ2值0.539 0.482 0.045 1.470 2.794 0.936 2.700 13.946 1.557 14.945 0.252 1.754 0.188 0.132 1.372 5.392 17.141 7.180 0.207 1.883 1.542 P 值0.591 0.487 0.832 0.225 0.006 0.350 0.008<0.001 0.121<0.001 0.801 0.081 0.851 0.895 0.172<0.001<0.001<0.001 0.837 0.061 0.125
2.2 CHD患者PCI术后再狭窄的多因素Logistic回归分析
Logistic 回归分析,结果显示,FPG、LDL-C、TC、FIB、Cyp A、NF-κB、VEGF及支架直径为CHD患者PCI术后再狭窄的独立危险因素(P<0.05)。见表2。2.3 外周血Cyp A、NF-κB及VEGF水平预测CHD患者PCI术后再狭窄的ROC 曲线分析
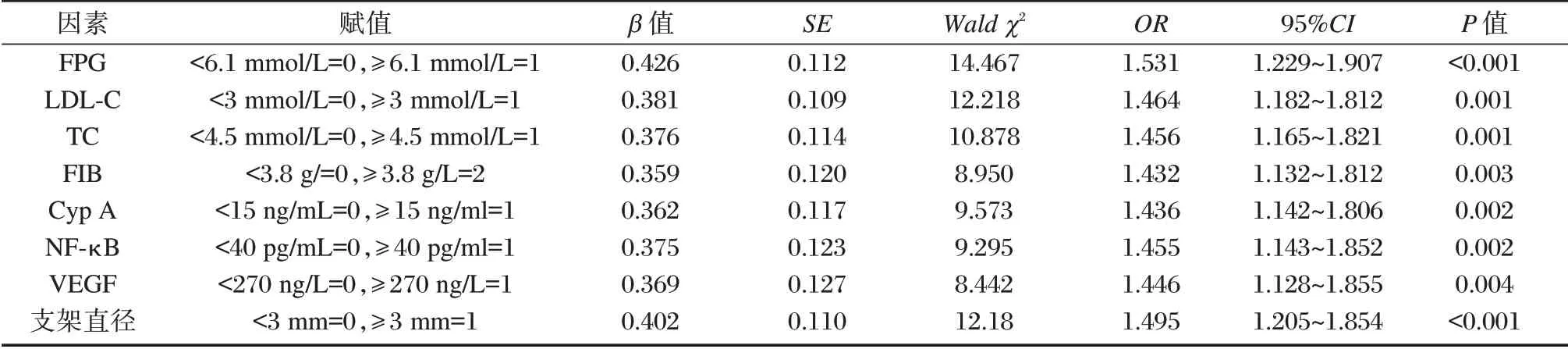
表2 CHD患者PCI术后再狭窄的影响因素赋值表Table 2 evaluation table of influencing factors of restenosis in CHD patients after PCI
ROC 曲线分析显示,外周血Cyp A、NF-κB及VEGF水平联合预测CHD患者PCI术后再狭窄的敏感度为94.00%,AUC 为0.951,高于单独检测(P<0.05)。见表3 和图1。
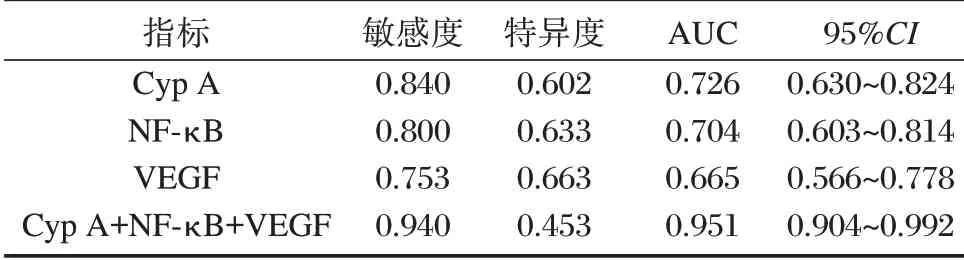
表3 外周血Cyp A、NF-κB及VEGF水平预测CHD患者PCI术后再狭窄的ROC 曲线分析Table 3 CYP in peripheral blood A、NF-κ ROC curve analysis of B and VEGF levels in predicting restenosis after PCI in patients with CHD
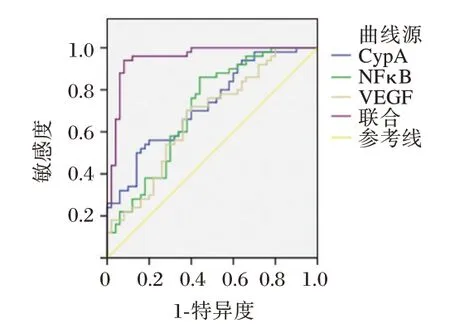
图1 ROC曲线Figure 1 ROC curve
3 讨论
近年来,随着生活水平的提高和饮食结构的改变及工作压力的增加,CHD 发病率逐年上升。PCI 是治疗有效手段,但术后再狭窄发生率较高。目前认为,PCI术后再狭窄的原因是:血管内膜过度增生和平滑肌细胞迁移,支架置入后新生内膜增生,导致再狭窄发生,进而影响疗效[8]。因此对再狭窄进行诊断并进行干预至关重要。
相关研究显示,FPG、TC、LDL-C、支架直径为CHD患者PCI术后再狭窄的危险因素[9]。本研究显示,FPG、LDL-C、TC、FIB及支架直径为CHD患者PCI术后再狭窄的独立危险因素。分析其可能机制为:较高浓度的血糖可影响支架置入后的冠脉内皮修复,促进冠脉内血栓形成、平滑肌迁移和新生内膜增殖,从而导致再狭窄发生。LDL-C 和TC可评估血脂水平,高水平的血脂会引起过多脂质和斑块,从而损伤血管内皮细胞,促进动脉粥样硬化,导致再狭窄发生。FIB 可促使平滑肌细胞迁移,引起冠脉内膜增生,最终引起再狭窄[10]。同时相关研究显示,支架直径、长度及数量是CHD患者PCI术后再狭窄的危险因素[11]。本研究显示,支架直径是CHD患者PCI术后再狭窄的独立危险因素,由于支架直径较小对于狭窄部位无功能性作用,并对血管损伤更为严重,进而增加血管狭窄发生率。
CypA 是受体蛋白,具有肽基脯氨酰顺反异构酶活性,在蛋白质折叠、细胞外信号调节激酶和细胞凋亡诱导因子中起重要作用;CypA 还可作为氧化应激诱导的分泌因子。此外CyPA 的分泌受Rho激酶激活的调节,对血管平滑肌细胞的收缩和动脉粥样硬化具有重要作用[12]。研究证实,CyPA 可使内膜增厚,形成腹主动脉瘤、动脉粥样硬化和心肌肥厚[13]。活化的NF-κB 能与DNA 链特定的κB 序列结合,启动和调节与免疫和炎症反应有关的基因转录,在机体的免疫应答、炎症反应及细胞的生长调控中具有重要作用[14]。VEGF 主要分布于血管内皮细胞,能促进缺血组织血管内皮细胞增殖和血管生成及多种血管活性物质的合成,并抑制平滑肌细胞增殖。VEGF 可反映心肌缺血的程度,与冠心病的程度密切相关[15]。本研究结果提示Cyp A、NF-κB、VEGF 可能参与血管再狭窄发生发展。分析原因可能为:PCI术可导致冠状动脉斑块破裂出血,并可损伤内膜,释放炎症介质,诱导Cyp A、NF-κB、VEGF表达;同时缺血再灌注损伤可激活外周血单核和T 淋巴细胞,浸润内皮细胞下层,释放大量炎症介质,从而导致外周Cyp A、NF-κB、VEGF 升高。多因素Logistic 回归分析结果显示,Cyp A、NF-κB、VEGF 为CHD患者PCI术后再狭窄的独立危险因素。高水平的Cyp A、NF-κB、VEGF 可损伤血管并刺激血小板,致使平滑肌细胞堆积、血管内膜增生,从而导致再狭窄发生。ROC 曲线分析显示,Cyp A、NF-κB及VEGF水平联合预测CHD患者PCI术后再狭窄的敏感度和AUC 高于单独检测,提示外周血Cyp A、NF-κB及VEGF水平联合预测CHD患者PCI术后再狭窄的价值较高。
综上,FPG、LDL-C、TC、LDL-C、Cyp A、NF-κB、VEGF及支架直径是CHD患者PCI术后再狭窄发生的独立危险因素,其中外周血Cyp A、NF-κB及VEGF水平联合检测可提高对其诊断价值。
