脑小血管病总负荷对急性缺血性脑卒中合并慢性肾病的血液透析患者预后的影响
2021-12-14杨湘燕卢振产党辉
杨湘燕 卢振产 党辉
我国是脑血管病高发国家,其中缺血性脑卒中占74%[1],20%~35%的急性缺血性脑卒中患者合并慢性肾病(chronic kidney disease,CKD),CKD 与急性缺血性脑卒中患者不良预后密切相关,其可增加急性缺血性脑卒中患者死亡风险[2]。有研究证实,脑白质疾病、脑微出血等脑小血管病(cerebral small vessel disease,CSVD)可能在CKD早期就已存在[3],然而,CSVD是否会影响急性缺血性脑卒中合并CKD的血液透析患者的预后,目前鲜有研究。本研究观察CSVD总负荷对于急性缺血性脑卒中合并CKD的血液透析患者的疗效和预后的影响,现将结果报道如下。
1 对象和方法
1.1 对象 选择2017年1月至2020年12月在湖州市中心医院及新疆维吾尔自治区人民医院神经内科住院治疗的急性缺血性脑卒中合并CKD的血液透析患者93例,其中湖州市中心医院54例,新疆维吾尔自治区人民医院39例,根据Staals等[4]的CSVD总负荷评分量表,将CSVD总负荷评分≤2分患者作为轻度组,>2分患者作为重度组。轻度组55例,男30例,女25例,年龄 45~77(60.4±8.2)岁;重度组 38 例,男 21 例,女 17例,年龄 43~78(61.6±8.9)岁。两组患者性别、年龄比较,差异均无统计学意义(均P>0.05)。纳入标准:(1)年龄18~80 岁;(2)发病 24 h 内入院;(3)急性缺血性脑卒中符合2018年中华医学会神经病学分会制定的《中国急性缺血性脑卒中诊治指南》[5]的诊断标准;(4)终末期肾病符合2012年改善全球肾脏病预后组织(Kidney Disease:Improving Global Outcomes,KDIGO)颁布的CKD指南的诊断标准[6];(5)发病1周内完成头颅MRI检查。排除标准:(1)超早期进行静脉溶栓和(或)动脉介入取栓;(2)美国国立卫生研究院卒中量表(National Institute of Health Stroke Scale,NIHSS)评分>25 分,失语或意识不清;(3)明显遗传性脑血管病、遗传性痴呆等;(4)合并严重呼吸、循环、消化等多器官功能衰竭或严重系统性感染、恶性肿瘤;(5)合并颅内、消化道、泌尿系统出血情况;(6)存在严重自身免疫性疾病;(7)患者及家属不能配合。本研究经医院医学伦理委员会审核批准(批准文号:2017-07047),两组患者均签署知情同意书。
1.2 方法
1.2.1 一般资料收集 收集两组患者的一般资料,包括透析病程、高血压、冠心病、糖尿病、吸烟史、BMI、收缩压、舒张压、FPG、同型半胱氨酸、TC、LDL-C、HDLC、肌酐、超敏 CRP(hs-CRP)。
1.2.2 CSVD总负荷评分 采用美国GE Discovery 750,3.0T超导型MRI扫描系统和8通道相控阵头线圈,完成头颅MRI检查,包括T1WI、T2WI、液体衰减反转恢复(fluid attenuated inversion recovery,FLAIR)、弥散加权成像(diffusion weighted imaging,DWI)、磁敏感加权成像(susceptibility-weighted imaging,SWI)序列。参数设定:视野 240 mm×240 mm,矩阵 512×512,层厚5 mm,T1WI(回波时间 24 ms,重复时间 3 077 ms),T2WI(回波时间 94 ms,重复时间 4 500 ms),FLAIR(回波时间 145 ms,重复时间 8 000 ms),DWI(回波时间65 ms,重复时间 2 000 ms,b 值取 0 和 1 000 s·mm-2),SWI(回波时间 45 ms,重复时间 52 ms,翻转角 15°)。按照Staals等[4]的CSVD总负荷评分量表进行评分:(1)腔隙性脑梗死,≥1个病灶计1分;(2)脑白质病变,按Fazekas量表[7]评分评估,脑室旁不规则高信号延伸到白质,和(或)深部白质高信号融合,计1分。(3)脑微出血,≥1个微出血计1分。(4)扩大的血管周围间隙,取单侧基底节区病灶数量最多的层面,存在>10个扩大的血管周围间隙计1分[8]。
1.2.3 治疗方法 常规药物治疗包括:阿司匹林肠溶片100 mg/d(拜阿司匹林,拜耳医药保健有限公司,规格:100 mg/片,国药准字:J20171021)口服,阿托伐他汀钙片20 mg/d(立普妥,辉瑞制药有限公司,规格:20 mg/片,国药准字:H20051408)口服,如有其它合并症则常规对症治疗。血液透析使用Fresenius公司4008B透析机,联机在线配置碳酸氢盐透析液,透析液流速500 ml/min,血流速为 200~300 ml/min,每周透析 3 次,4 h/次。
1.2.4 神经功能的评价 记录两组患者入院时、治疗后72 h、1周、4周的NIHSS评分,记录入院时和发病3个月的改良 Rankin量表(modified Rankin scale,mRS)评分,评价神经功能。
1.2.5 认知功能的评价 记录两组患者入院时和发病3个月的简易精神状态检查量表(mini-mental state examination,MMSE)评分,评价认知功能。
1.3 统计学处理 应用SPSS 20.0统计软件,符合正态分布的计量资料以表示,组间比较采用两独立样本t检验,组内比较采用配对t检验,偏态分布的计量资料以 M(Q1,Q3)表示,组间比较采用 Wilcoxon秩和检验;计数资料组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者一般资料的比较 见表1。
由表1可见,重度组透析病程长于轻度组,肌酐、hs-CRP高于轻度组,差异均有统计学意义(均P<0.05)。两组患者高血压、冠心病、糖尿病、吸烟史、BMI、收缩压、舒张压、FPG、同型半胱氨酸、TC、LDL-C、HDL-C 比较,差异均无统计学意义(均P>0.05)。
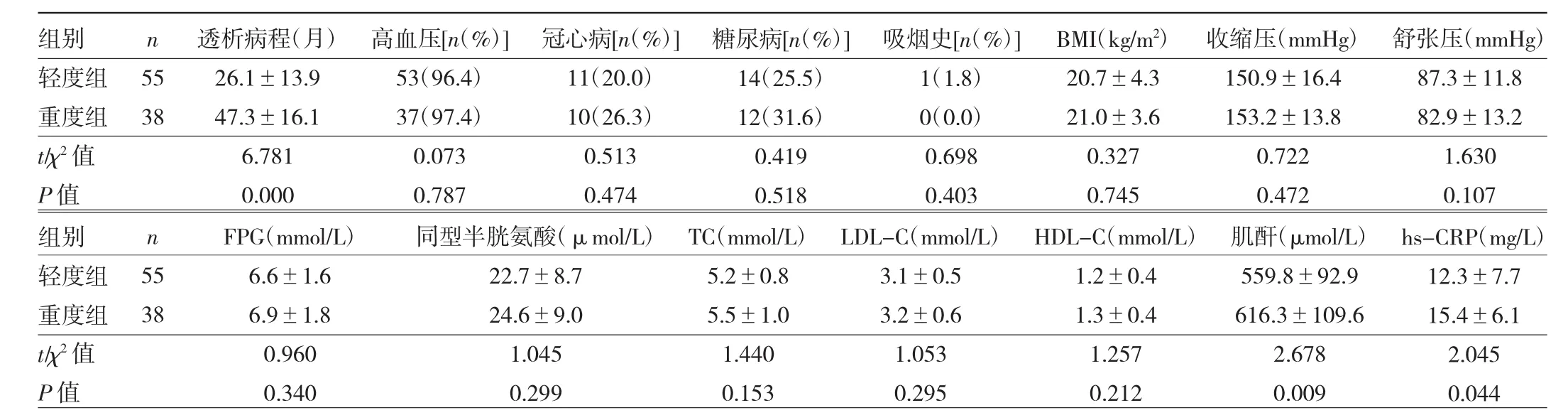
表1 两组患者一般资料的比较
2.2 两组患者神经功能比较 见表2。
由表2可见,重度组治疗后4周的NIHSS评分高于轻度组,差异有统计学意义(P<0.05)。两组患者入院时、治疗后72 h、1周的NIHSS评分比较,差异均无统计学意义(均P>0.05)。两组患者入院时mRS评分比较,差异无统计学意义(P>0.05),重度组发病3个月mRS评分高于轻度组,差异有统计学意义(P<0.05)。轻度组发病3个月mRS评分较入院时下降,差异有统计学意义(P<0.05),重度组发病3个月mRS评分和入院时比较,差异无统计学意义(P>0.05)。

表2 两组患者神经功能比较
2.3 两组患者认知功能比较 见表3。

表3 两组患者认知功能比较
由表3可见,两组患者入院时MMSE评分比较,差异无统计学意义(P>0.05),重度组发病3个月MMSE评分低于轻度组,差异有统计学意义(P<0.05)。轻度组发病3个月MMSE评分较入院时升高,差异有统计学意义(t=3.117,P<0.05),重度组发病 3个月MMSE评分和入院时比较,差异无统计学意义(t=0.793,P>0.05)。
3 讨论
脑卒中是危害人类健康的重大疾病之一,CKD增加了脑卒中的患病风险及致残率。Masson等[9]基于83项研究,共2 253 741例参与者的Meta分析发现,当估算的肾小球滤过率(estimated glomerular filtration rate,eGFR)<90 ml·min-1·1.73 m-2时,脑卒中风险开始增加,eGFR 每降低 10 ml·min-1·1.73 m-2,脑卒中风险增加7%。与肾功能正常者相比,终末期肾病患者发生脑卒中的风险增加10倍多,且致残、致死率更高[10-14]。
本研究发现,在急性缺血性脑卒中合并CKD的血液透析患者中,重度组较轻度组有更高的肌酐值,透析病程更长,与既往研究一致[3,15-16]。CSVD是脑血管病的一个重要亚型,是指颅内小血管病变所致临床、影像学和病理综合征[17],主要累及颅内小动脉、微动脉、毛细血管、微静脉及小静脉。CSVD总负荷是将白质高信号、扩大的血管周围间隙、腔隙和微出血纳入评估标准,以评分的方式综合评估CSVD的累积效应,是目前比较认可的一种综合评估CSVD的方法[4]。由于肾脏和大脑的微血管在结构、功能、微循环调节上相似,有研究发现,CKD的肾小球硬化与CSVD有相似的病理机制:内皮功能障碍、缺血性动脉硬化、低灌注、小血管渗漏[18],因此CKD与CSVD关系密切,eGFR不仅有助于CKD患者肾功能的评价,还可能提示潜在的脑血管损伤[16]。而血液透析可显著降低老年患者的脑血流量,可能造成终末期肾病患者脑白质损伤的加重[15]。
CSVD总负荷可能影响急性缺血性脑卒中合并CKD的血液透析患者神经功能恢复。Sutherland等[2]发现,CKD是接受血管内血栓切除术治疗的脑卒中患者mRS评分较高和死亡率增加的的显著预测因子。Gensicke等[19]发现,在接受静脉溶栓治疗的脑卒中患者中,较低的eGFR与不良预后、症状性脑出血和死亡的风险增加有关。本研究发现,在急性缺血性脑卒中合并CKD的血液透析患者中,重度组有更高肌酐值,神经功能恢复情况更差,治疗后4周NIHSS评分及发病3个月mRS评分均高于轻度组,发病3个月mRS评分较入院时无明显改善。本研究认为,CKD进程中的氧化应激、炎症、神经激素失衡、尿毒症毒素累积导致的CSVD病变,可能损害大脑从急性缺血性损害中恢复的能力,影响神经功能恢复。
CSVD总负荷可能影响急性缺血性脑卒中合并CKD的血液透析患者认知功能恢复。CKD是认知功能下降的独立危险因素[20],在所有CKD导致患者认知功能障碍的机制中,CSVD可能发挥重要的作用,CSVD可导致患者语言、记忆力、视空间能力等认知功能损害[21]。2008年一项REGARDS研究证实,在全美范围的成年人中,认知功能损害在CKD早期即已存在,且在eGFR<60 ml·min-1·1.73 m-2的 CKD 患者中,eGFR 每降低 10 ml·min-1·1.73 m-2,损伤发生率增加 11%[22]。一项包含54 779例参与者的横断面和纵向研究的Meta分析表明,接受血液透析的老年患者中,认知功能障碍的发病率高达60%[15]。本研究发现,急性缺血性脑卒中合并CKD的血液透析患者MMSE评分均偏低,重度组MMSE 评分(23.0±3.3)分,轻度组(23.9±3.3)分,两组比较差异无统计学意义,这可能与MMSE评分灵敏度偏低有关。重度组发病3个月MMSE评分低于轻度组,且与入院时比较无明显改善。由此推测,CKD进程中的CSVD改变不仅导致认知功能下降,而且损害脑功能储备和代偿能力,影响了脑卒中后的认知功能恢复。
综上所述,在急性缺血性脑卒中合并CKD的血液透析患者中,CSVD总负荷可能影响神经功能及认知功能的恢复,而CSVD总负荷与肾功能、透析病程相关,因此对CKD患者尽早实施肾功能保护措施,尽早筛查CSVD并积极干预,有利于更好的康复,降低致残率,提高生存质量。本研究也存在一定不足,如样本量少,观察时间较短,因此在未来工作中需进行更大规模的研究来验证,以指导临床实践。
