硫酸铵处理下茶园土壤氮素转化和交换态金属离子含量的动态变化
2021-12-13蔡秋亮方显瑞张传芳
蔡秋亮,钟 宁,方显瑞,陈 玲,张传芳
(1.百色学院,广西 百色 533000;2.闽南师范大学,福建 漳州 363000;3.中国科学院 宁波城市环境观测研究站,浙江 宁波 315830)
0 引言
随着工业、农业发展和人民生活水平提高,人们对优质蔬菜、水果、粮食产品的需求日益增加,同时化肥、农药的使用量也不断增加。而化肥施用不合理会对土壤酸碱性产生较大的影响,也会导致土壤中重金属含量发生较大变化,从而对农作物生长和农产品品质造成一定危害[1-2]。研究表明Cu、Pb、Se等金属是普遍存在的土壤污染金属,也受土壤酸碱性的影响[3-4]。因此,施肥对不同耕作时间的土壤的理化性质影响,已成为关注的热点。关于施入氮、磷肥对土壤酸碱性,以及土壤重金属形态和有效性的影响研究[5-9]较多。硫酸铵主要用作氮肥,长期施用会导致土壤的酸性增强和重金属活性增强等,已受到越来越多研究者的关注[10-11]。已有研究表明,施用硫酸铵、尿素能增加土壤中水溶性和交换性的 Mn、Zn、Pb 和Cd等的含量[12-13]。王一志等[14]通过盆栽试验研究发现随着土壤 pH值升高,土壤弱酸提取态 Cd 含量逐渐降低。彭晓春等[15]的研究表明随着土壤pH值升高至中性,土壤提取态重金属含量显著提高。钟宁等[16]通过室内土壤培养发现:随着硫酸铵或尿素施入土壤中,pH值升高后下降,而土壤中铵态氮含量呈现先升高后下降的趋势,硝态氮含量呈现先稍微下降后上升的趋势。有关施肥不当导致土壤酸性增强和土壤中金属离子含量增加等的研究报道已经有很多,但针对不同耕作年限的土壤pH值和金属成分变化规律受施氮肥影响的研究尚少。鉴于此,本试验通过静态和动态试验研究了施用硫酸铵对新、老茶园土壤pH值、金属离子(Al、Mn、Cu、Se、Ca、Mg、Pb、Fe等)含量和氮转化的影响。
1 材料与方法
1.1 供试茶园及其土壤
两种供试土壤均采自福建省漳州市漳浦县天福石雕园附近(N24°07′,E117°44′),其中一种土壤采自当年种植茶园(后面称为新茶园),另一种土壤采自已经种植5年的茶园(后面称为老茶园)。两种茶园均属于山地茶园,无灌溉系统,施用肥料以散施为主,主要采春茶、秋茶;土壤为砂壤土。以1个取土点为中心,在10 m半径内取5个点,在各点采集0~20 cm土层的土壤,然后将5个点的土样混合成1个土壤样品。剔除土壤样品中的植物残体,经四分法取其中1份(1.0 kg左右),带回实验室,置于干燥阴凉处风干,磨碎过20目筛,备用。供试土壤的基本理化性质见表1,测定方法参照文献[17]。
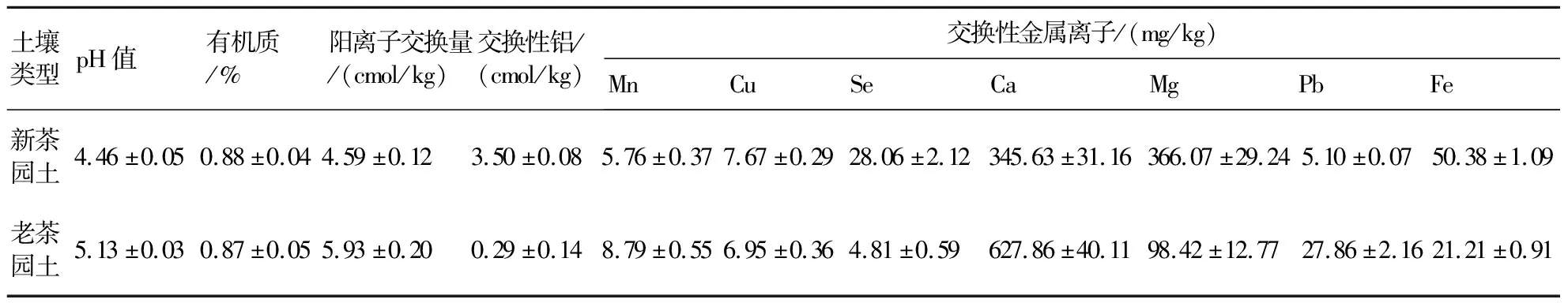
表1 两种供试土壤的基本理化性质
1.2 试验设计
静态试验:称取20 g土样置于相应编号的250 mL锥形瓶中,分别加入浓度为0、25、75、125、200、300 mmol/L的硫酸铵溶液4 mL,使硫酸铵在土样中的浓度分别为0、5、15、25、40、60 mmol/kg(土),每个处理均重复3次,在(25±1)℃条件下放置7 d,测定各土样的pH值、Al3+含量。
长期动态周变化试验:称取20 g土样置于相应编号的250 mL锥形瓶中,向土样中均匀滴加200 mmol/L的硫酸铵溶液4 mL,使土样中的硫酸铵浓度为40 mmol/kg,各处理均重复3次;分别在第0、7、14、20、27、34、41、47天的固定时间测定各处理土样的pH值,以及NH4+、NO3-、Al3+、Mn2+、Cu2+、Se4+、Ca2+、Mg2+含量。
短期动态日变化试验:试验方法和测定指标均与长期动态周变化试验一样,测定时间分别为第0、1、3、5、7、9、11、13天。
1.3 样品分析及数据处理方法
pH值测定:加100 mL水(水土质量比5∶1),用玻璃棒搅拌3 min,静置30 min,然后用酸度仪测定pH值[18]。
1 mol/L氯化钾浸提液的配制:称取74.6 g氯化钾(化学纯)溶于800 mL水中,用稀氢氧化钾和稀盐酸调节溶液的pH值为5.5~6.0,稀释至1 L。
浸提液的制备:称取20 g供试土壤,置于250 mL锥形瓶中,加入100 mL浓度为1 mol/L的氯化钾溶液(液土质量比5∶1),放在振荡器上震荡2 h,然后用滤纸过滤,并将滤液收集于100 mL的聚乙烯瓶中,滴加硝酸保存,备用。
NH4+含量的测定:向50 mL容量瓶中加入2 mL 浓度为1 mol/L的氯化钾浸提液,加蒸馏水定容;转入100 mL三角瓶中,加入次溴酸钠溶液5 mL,摇匀;在氧化30 min后,加入5 mL磺胺溶液,摇匀;再加入1 mL盐酸萘乙二胺,形成紫红色溶液,摇匀,发色,以蒸馏水作参比,在波长540 nm下测定吸光度[18]。同时也测定不同浓度标准溶液的吸光度,获得NH4+-N浓度与吸光度的曲线,并把样品的吸光度代入标准曲线,从而获得样品的浓度值。
NO3-含量的测定:向25 mL容量瓶中加入2 mL浓度为1 mol/L的氯化钾浸提液,加入0.2 mL氨基磺酸溶液,再加入2 mL浓度为0.5 mol/L的盐酸,加入蒸馏水定容,摇匀;以蒸馏水作参比,分别在220和275 nm波长下测定吸光度,吸收值差值△A=A220-A275[18]。同时也测定不同浓度标准溶液的吸光值,获得NO3--N浓度与吸收值ΔA的曲线,并把样品的吸收值ΔA代入标准曲线,从而获得样品的浓度值。
Al3+含量的测定:向10 mL比色管中加入2 mL浓度为1 mol/L的氯化钾浸提液,加入2 mL现配的0.5%抗坏血酸,再加入2 mL蒸馏水,置于80~90 ℃水浴锅中水浴加热30 min,冷却后加入2 mL铝试剂,最后加入蒸馏水,定容至刻度并摇匀;形成桃红色溶液显示2 h后,在波长530 nm下测定吸光度[18]。同时也测定不同浓度标准溶液的吸光值,获得Al3+浓度与吸光度的曲线,并把样品的吸光度代入标准曲线,从而获得样品的浓度值。
Mn2+、Cu2+、Se4+、Ca2+、Mg2+含量的测定:将20 g供试土样放入消解罐中,加入6 mL硝酸、3 mL氢氟酸和2 mL高氯酸,混匀;将消解罐放入消解仪中,启动消解程序,消解20 min;取出消解罐,放在风机上,待完全冷却后,将溶液移入25 mL容量瓶中定容并摇匀,过滤到25 mL比色管中,同时做空白消解。采用火焰原子吸收分光光度法[19],用GBC932B原子吸收分光光度计测定各离子的浓度。
1.4 数据处理方法
采用Excel 2010软件进行数据计算,用SPSS 12.0统计软件进行数据分析,显著性水平设定为α=0.05。
2 结果与分析
2.1 施用硫酸铵对茶园土壤pH值的影响
2.1.1 不同浓度硫酸铵对新、老茶园土壤pH值的影响 土壤pH值是土壤的酸碱度的表征,影响土壤溶液的离子组成和各种化学反应,从而影响土壤重金属的生物有效性、土壤-植物系统的迁移和钝化污染的修复效果。从图1可看出,经过硫酸铵处理7 d后,新、老茶园土壤pH值均随硫酸铵浓度的增大而减小,新、老茶园土壤的pH值经处理后分别从4.46、5.13降至4.16、5.00;从线性拟合效果上看,老茶园土壤的斜率(-0.0047)绝对值高于新茶园土壤的(-0.0018),可看出经硫酸铵溶液处理7 d后老茶园土壤的pH值变化幅度比新茶园土壤的变化幅度大。

图1 新、老茶园土壤pH值随施用硫酸铵浓度的变化
2.1.2 施加硫酸铵后新、老茶园土壤pH值的短期日变化和长期周变化 硫酸铵处理新、老茶园土壤短期和长期培养的土壤pH值变化结果见图2,施加硫酸铵后,新茶园土壤pH值先降低至4.1,后升高到峰值4.4,再降低并在5 d趋于稳定,随着时间延长新茶园土壤的pH值略有降低。而对于老茶园,施入硫酸铵后5 d土壤pH值降低至最低值(4.5),经7周处理后土壤pH值略有上升。
从图2也可看出,施用硫酸铵7 d后,新、老茶园土壤pH值都先略有下降,接着缓慢上升;新茶园土壤经49 d处理后pH值小于其初始值,而经49 d处理后老茶园土壤pH值则大于其初始值。但总体看两者与对应初始值差别不大,表明经过硫酸铵长时间处理后新、老茶园土壤的pH值变化不显著。从新、老茶园土壤pH值的变化规律还看出,施入硫酸铵处理新茶园土壤pH值的变化幅度稍微大于老茶园土壤。

图2 施加硫酸铵后短期和长期时间内新、老茶园土壤pH值的变化
2.2 硫酸铵在土壤中的氮素转化
2.2.1 NH4+-N含量的动态变化 两种茶园土壤中NH4+-N含量的短期和长期动态变化结果如图3所示,在短期动态中土壤中NH4+-N含量随着培养时间延长呈现下降趋势,并在第5天降至最小值,分别为:24.42 mg/kg(新茶园土壤)、20.80 mg/kg(老茶园土壤);然后迅速上升,最后趋于平稳。在长期动态变化中NH4+-N含量先升高后下降,在第28天时达到最大值,分别为:44.85 mg/kg(新茶园土壤)、44.65 mg/kg(老茶园土壤)。
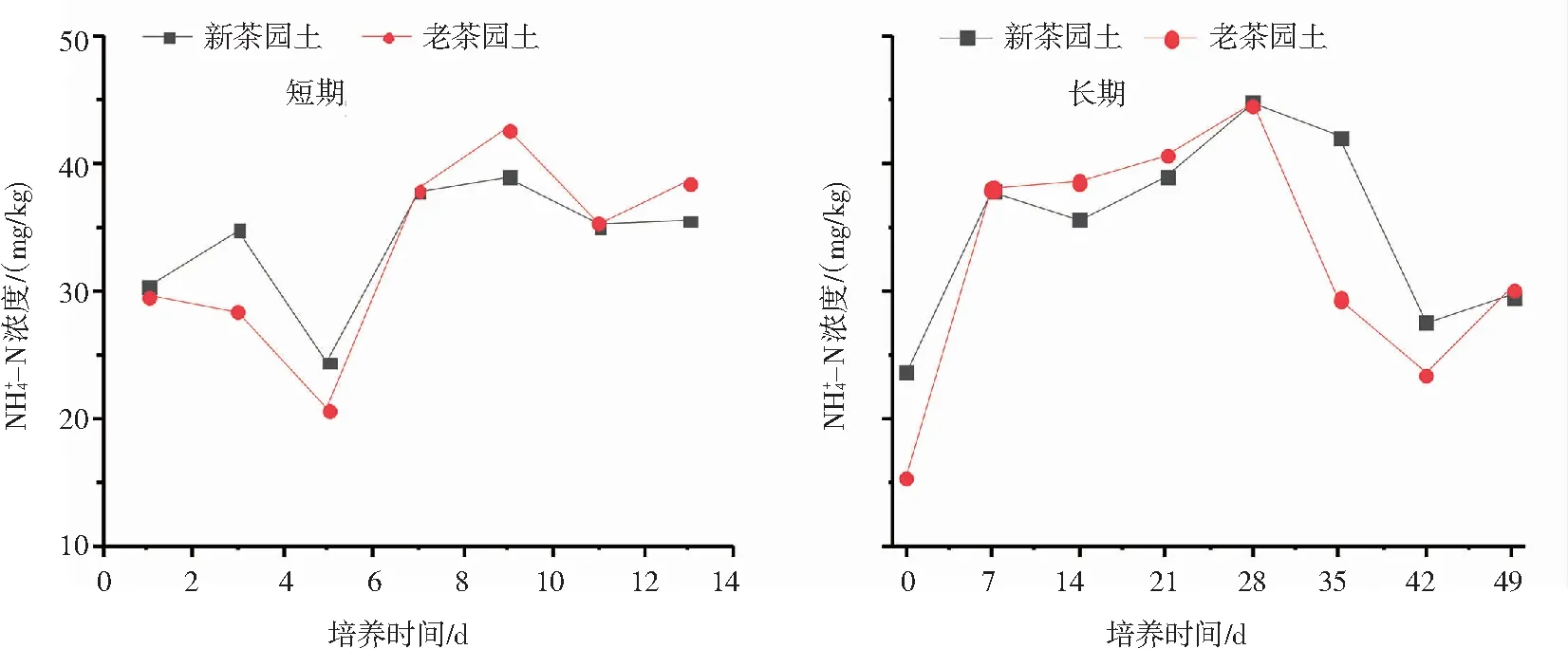
图3 施用硫酸铵后短期和长期时间内新、老茶园土壤铵态氮含量的动态变化
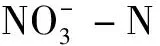
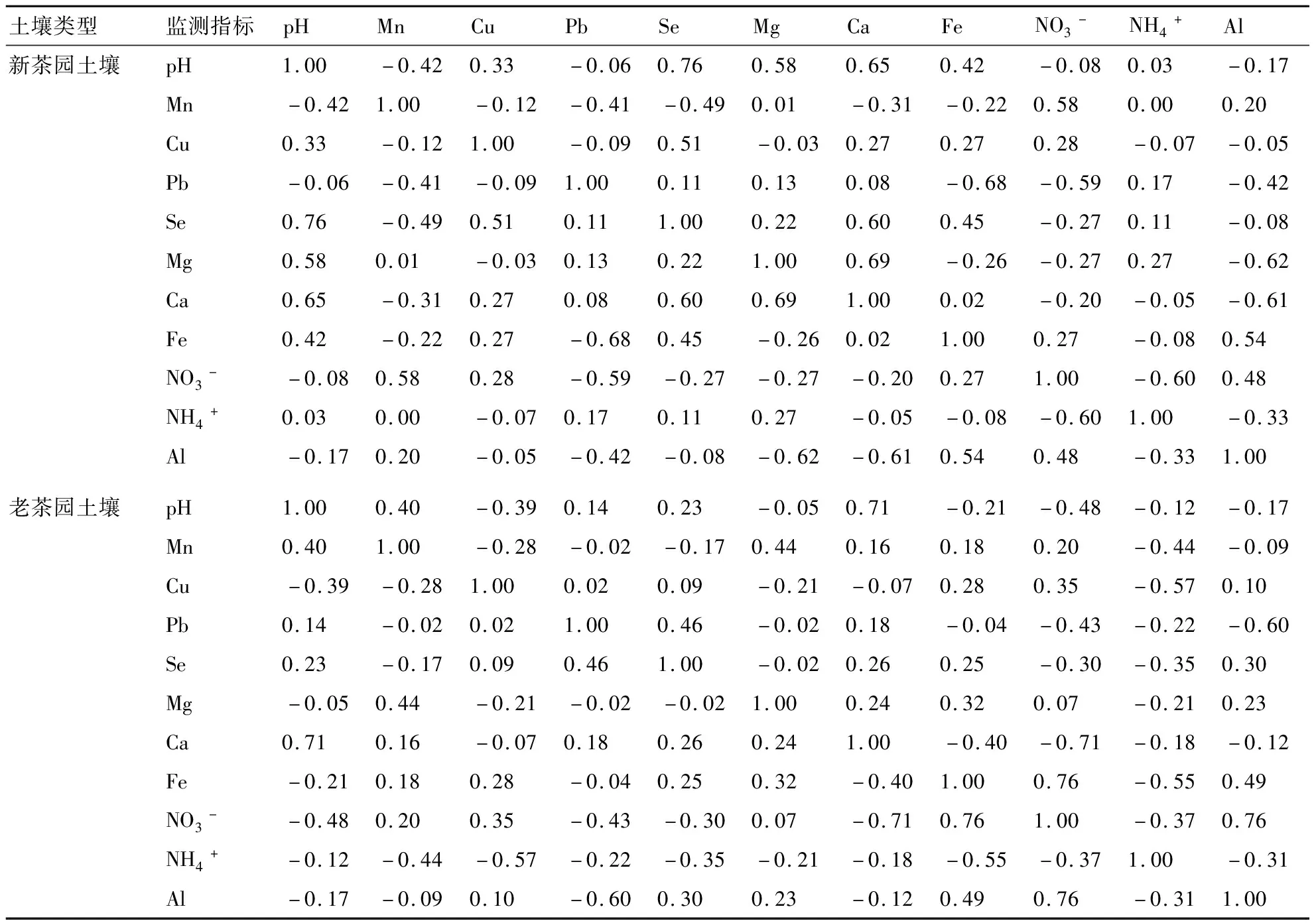
表2 施入硫酸铵后2种茶园土壤各指标相关性分析结果

图4 施加硫酸铵后短期和长期时间内新、老茶园土壤硝态氮含量的动态变化
2.3 施用硫酸铵对土壤中Al、Mn、Cu、Se、Ca、Mg、Pb、Fe含量的影响
2.3.1 土壤中交换性铝含量的动态变化 土壤中铝主要以交换性铝、吸附态羟基铝、有机络合态铝等形态存在,并且在土壤中铝的形态与土壤pH值有直接关系[20]。经不同浓度硫酸铵处理后新、老茶园土壤交换性铝含量的变化结果见图5,从中可看出随着硫酸铵浓度增高,新、老茶园土壤交换性铝含量总体呈现下降趋势,结合图2可知经硫酸铵处理后,土壤交换性铝含量与土壤pH值呈负相关[20]。对比两个拟合斜率可知,新茶园土壤交换性铝含量曲线的斜率绝对值大于老茶园土壤,分别为0.260和0.078,表明硫酸铵处理对新茶园土壤交换性铝含量的影响大于老茶园,也说明新茶园土壤对铝的缓冲性弱于老茶园。
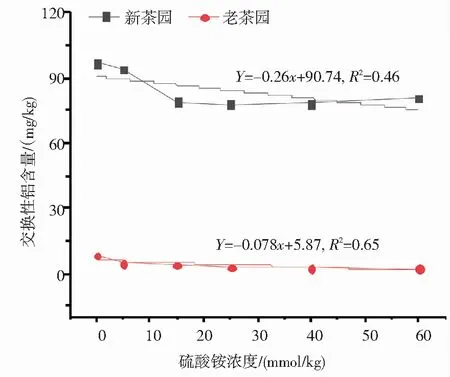
图5 新、老茶园土壤交换性铝含量随硫酸铵浓度的变化
从不同处理茶园土壤交换性铝含量的短期动态和长期动态变化(图6)可以看出,新茶园土壤交换性铝含量先升高,于第3天出现峰值,在第14天时交换性铝含量出现最低值,分别为:58.36 mg/kg(新茶园土壤)、2.94 mg/kg(老茶园土壤);之后变化不明显。而老茶园土壤交换性铝含量随着培养时间延长而逐渐下降(短期处理),在第14天后趋于稳定。结合图2和图6可看出,施用硫酸铵处理后,新茶园土壤交换性铝含量与pH值呈负相关。老茶园土壤中交换性铝含量总体随时间延长而下降,说明硫酸铵长期处理对老茶园土壤交换性铝含量影响不明显。
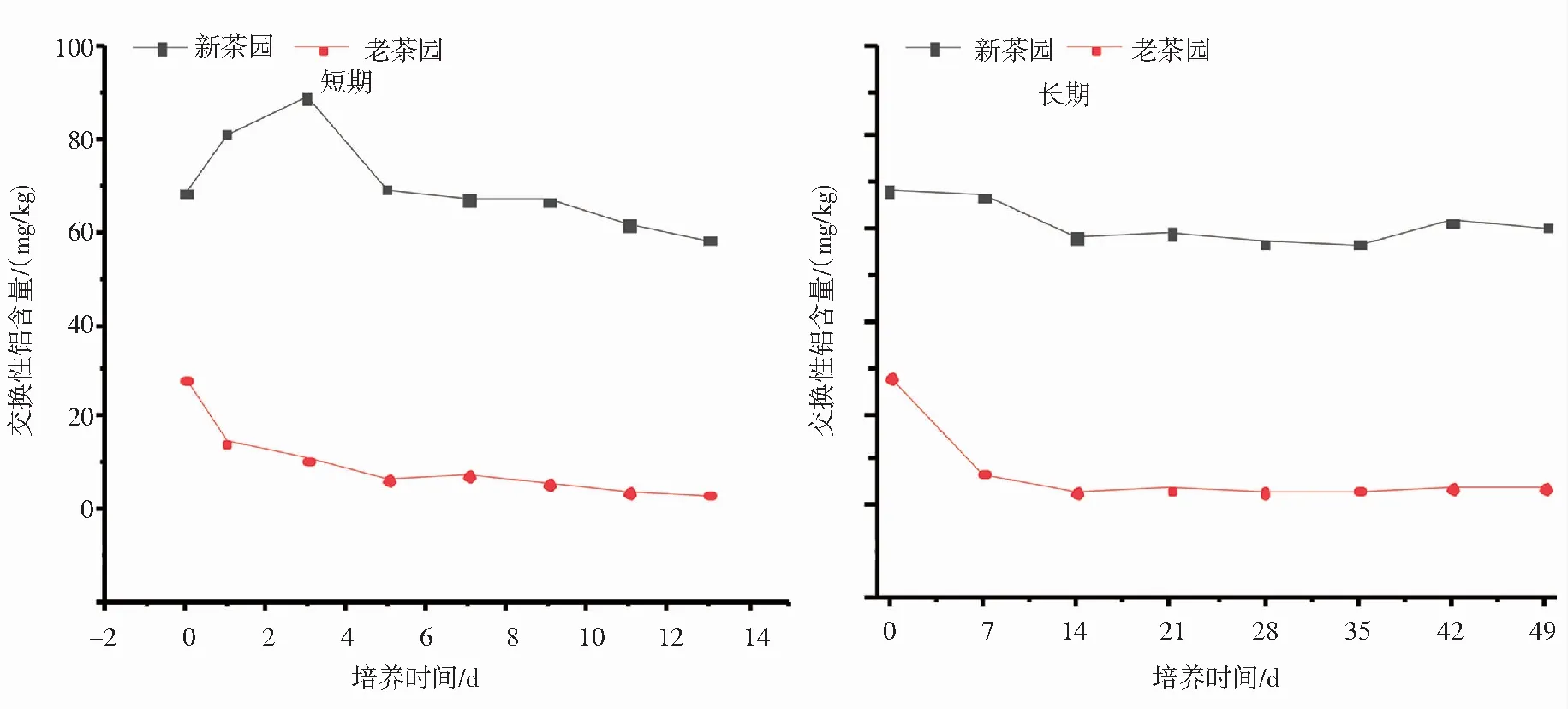
图6 施用硫酸铵后长期和短期时间内2种土壤交换性铝含量的动态变化
2.3.2 施加硫酸铵后土壤中Mn、Cu、Zn、Ca、Mg、Pb、Fe含量的动态变化 土壤中重金属的存在形态直接影响其毒性、迁移及其在自然界中的循环[21]。施入硫酸铵后两种茶园土壤Mn、Cu、Pb、Se、Ca、Mg、Fe等重金属元素含量的动态变化如表3所示。从表3可看出,经49 d培养处理,两种土壤中交换性Cu、Se、Ca、Mg和Pb含量的变化趋势相同,均随着时间延长先降低后逐渐上升,且与pH值呈正相关(表2)。其中Ca、Mg离子含量比其它金属离子更早上升,在第35天后趋于稳定;而Cu、Se含量在第49天还在上升。在新茶园土壤中,Fe的含量随时间延长变化不明显,而老茶园土壤中的Fe含量先缓慢降低到最小值,但在第14天后随时间延长而迅速升高。
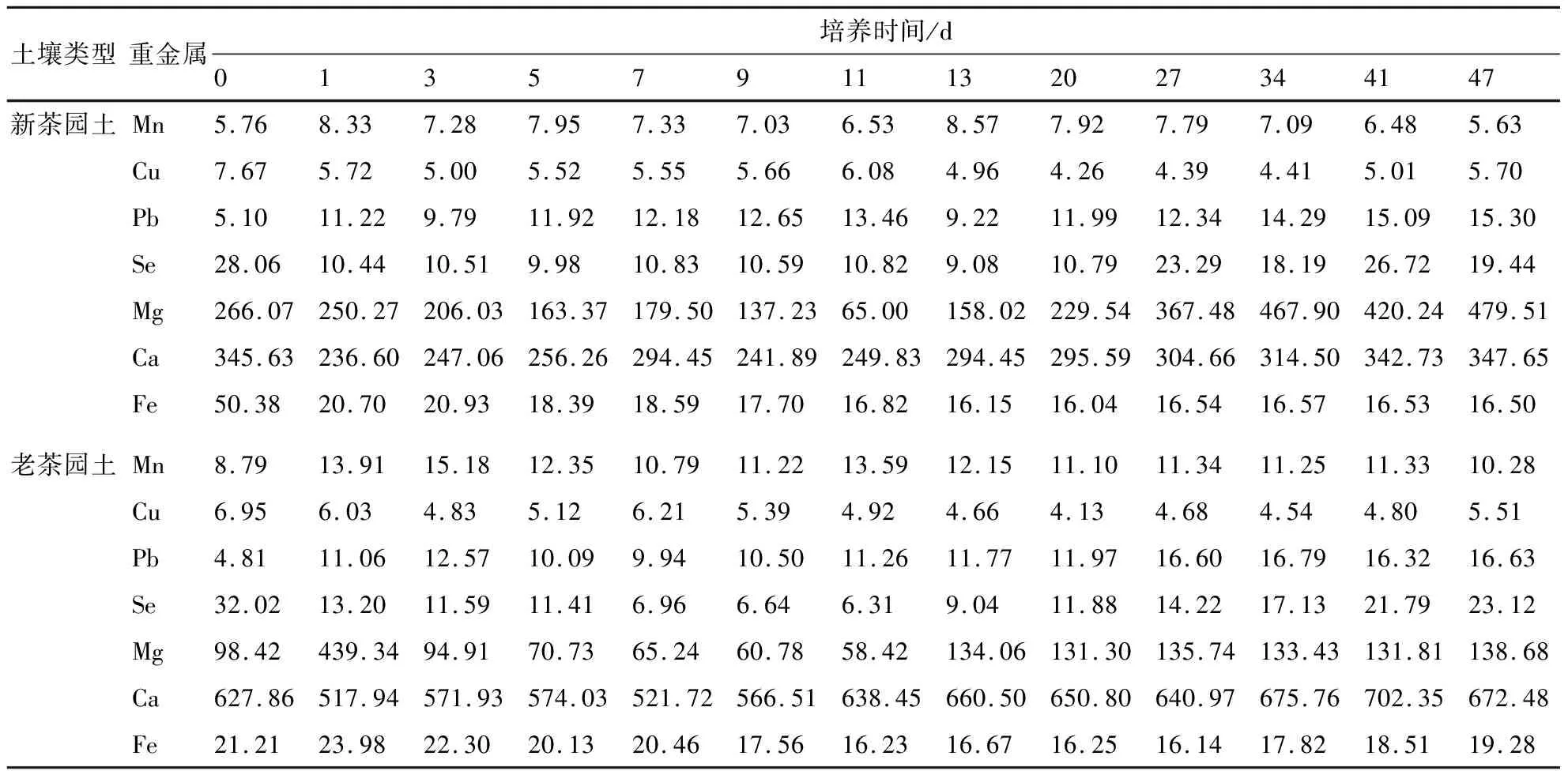
表3 施入硫酸铵后2种茶园土壤Mn、Cu、Pb、Se、Ca、Mg、Fe离子含量的动态变化 mg/kg
3 讨论与结论
本研究静态和动态试验结果表明:在短期内,施加硫酸铵会导致土壤pH值迅速下降,但很快会恢复到原有水平,说明硫酸铵对茶园土pH值的短期影响较大,长期影响很小;土壤pH值随着施用硫酸铵浓度的增加而显著升高;结合两种土壤看,施入硫酸铵经短期处理会降低茶园土壤pH值,经49 d处理施入硫酸铵对土壤pH值的影响不明显,这与傅成诚等[13]的研究结果不同,但与钟宁等[16]的研究结果相同,究其原因,可能是施入硫酸铵后,其被水解成NH4+-N,而NH4+-N在有氧条件下发生硝化作用形成NO3--N,促使土壤pH值下降,之后部分NO3--N又转化为分子态氮或氮氧化合物挥发至空气中,从而使土壤pH值有所回升。施入硫酸铵处理新茶园土壤pH值的变化幅度稍微大于老茶园土壤,也可说明新茶园土壤的酸碱缓冲能力比老茶园土壤弱。
短期动态中NH4+-N含量随着培养时间延长先呈现下降趋势,后迅速上升,最后趋于平稳;随着培养时间延长,土壤中NH4+-N含量先升高后下降,之后趋于平稳,与皮荷杰等[22]的研究结果相同;硝态氮含量则呈现上升的趋势,与沈灵凤等[23]的研究结果相似。短期和长期处理土壤中NH4+-N含量与NO3--N含量总体上呈负相关。在整个培养阶段土壤中NH4+-N含量先升高后下降,后期之所以下降,可能是因为NH4+-N在有氧条件下会发生硝化作用,形成NO3--N,以及部分NH4+会被微生物固定吸收[24]。
从长期培养看,新茶园土壤交换性铝含量与pH值呈负相关,而对老茶园土来说两者间的相关性不大。这可能是老茶园土壤受土壤中阳离子交换量、有机质含量、微生物种群数量、土壤酸度等影响所致,具体原因有待进一步研究。从短期培养看,新茶园土壤交换性铝含量与土壤pH值呈负相关,这一结果与钟宁等[25]的研究结果相同。
本研究还发现,土壤中交换性Cu、Se、Ca、Mg和Pb含量的变化趋势相同,且均与pH值呈正相关,其中Cu含量与pH值的相关性结果与郭朝晖等[26]的研究结果相同,而Ca、Mg含量与pH值的相关性结果与杨艳等[27]的研究结果不同。Mn的含量与pH值呈负相关,此结果与钟宁等[16]的研究结果一致。土壤中Mn的形态有Mn氧化态和Mn2+,Mn2+主要被植物吸收利用,Mn化合物的浓度随pH值升高而下降,且较高pH值有利于微生物促使低价Mn氧化成高价Mn,从而降低活性Mn含量。
