抗PD-1/PD-L1治疗在胃癌或胃食管结合部腺癌中的疗效荟萃分析Δ
2021-12-09魏雨涵曹邦伟
张 颖,魏雨涵,李 莉,曹邦伟#
(1.首都医科大学附属北京友谊医院肿瘤中心,北京 100050; 2.首都医科大学附属北京地坛医院肿瘤诊治中心,北京 100015)
胃癌是全球第三大致死性恶性肿瘤,而我国胃癌的发病率和死亡率在所有恶性肿瘤中均居第二位[1-3]。近年来,虽然早期胃癌患者可通过早期筛查使预后得到极大改善,但对于胃癌晚期确诊患者的治疗却仍然没有有效的手段[4]。对于晚期胃癌患者,传统化疗的总生存期(overall survival,OS)<1年,且患者的生活质量也因相关不良反应而明显降低,因此,积极寻找更多有效的治疗策略是目前亟待解决的重要问题。近年来,以程序性死亡蛋白-1(programmed death-1,PD-1)/程序性死亡蛋白配体-1(programmed death ligand-1,PD-L1)抑制剂为主的肿瘤免疫疗法在多种恶性肿瘤中取得了一系列可喜的成果,使肿瘤治疗发生了革命性的变化。上述免疫检查点抑制剂已被用于黑色素瘤、肺癌、肾细胞癌、头颈癌和尿路上皮癌等多种实体瘤的治疗,成为继手术、化疗、放疗及靶向治疗后的另一个重要的治疗策略[5]。虽然也有研究对PD-1/PD-L1抑制剂用于胃癌的治疗进行了一系列的探索,但疗效并不明确,胃癌患者究竟能否从免疫治疗中获益仍存在争议。因此,本研究收集了目前已发表的关于PD-1/PD-L1抑制剂在晚期胃癌或胃食管结合部腺癌中的临床研究数据,进行荟萃分析(Meta分析),以期对其今后的临床应用提供依据。
1 资料与方法
1.1 纳入与排除标准
1.1.1 纳入标准:(1)前瞻性研究;(2)Ⅱ期及Ⅲ期临床研究;(3)研究对象为经组织学和细胞学确诊的晚期胃癌或胃食管结合部腺癌患者;(4)研究组患者采用抗PD-1/PD-L1药物单药或联合治疗,对照组患者采用化疗或安慰剂。
1.1.2 排除标准:(1)重复发表的文献;(2)综述类及病例报告;(3)回顾性研究;(4)Ⅰ期研究。
1.2 文献检索策略
根据系统综述和Meta分析优先报告条目(preferred reporting items for systematic reviews and Meta-analyses,PRISMA)展开研究。由2名研究人员分别对PubMed、Embase和the Cochrane Library等数据库以及近3年内美国临床肿瘤学会(American society of clinical oncology,ASCO)、2020年欧洲肿瘤内科学会(European society for medical oncology,ESMO)会议摘要进行系统搜索。检索关键词包括“gastric cancer OR gastroesophageal junction cancer OR gastric adenocarcinoma OR gastroesophageal junction adenocarcinoma, pembrolizumab OR nivolumab OR avelumab OR atezolizumab OR durvalumab OR Anti PD-1 OR Anti PD-L1”。检索截止日期为2020年9月26日,语言不限。
1.3 数据提取
由2名研究人员按照预先拟定好的表格,独立提取相关数据并交叉核对,以保证数据的准确性。出现分歧时,由2名研究人员与第3名研究人员讨论达成共识。从文献中提取的信息包括研究名称、第一作者姓名、文献发表年份,治疗线数,患者数量,治疗方案,相应的OS、无进展生存期(progress free survival,PFS)、客观缓解率(objective response rate,ORR)以及3级以上不良反应发生率。
1.4 偏倚风险评估
由2名研究人员利用考克兰手册独立评估每篇纳入文献的偏倚风险,所有分歧通过与第3名研究人员讨论解决。通过RevMan 5.3软件对纳入研究的偏倚风险进行评估,主要包含以下几个主要偏倚来源:随机序列的产生(选择偏倚);分配隐藏(选择偏倚);对受试者和研究人员施盲(实施偏倚);对结局评估人员施盲(测量偏倚);结果数据不完整(随访偏倚);选择性报告(报告偏倚);其他偏倚。
1.5 统计学方法
统计分析以及森林图的绘制通过Stata SE 12软件完成。OS和PFS的Pooled分析结果以风险比(HR)及其95%置信区间(CI)表示;ORR的Pooled分析结果以风险比(RR)及其95%CI表示。I2检验用于评估研究之间的异质性,若P<0.1或者I2>50%,表明研究之间存在异质性,使用随机效应模型;若P>0.1或者I2<50%,表明研究之间不存在异质性,使用固定效应模型。P<0.05时,认为差异有统计学意义。
2 结果
2.1 文献筛选流程与结果
按照拟定的检索方法,初始共检索到422篇文献。通过筛选,排除重复研究及不符合纳入标准的研究,最终共纳入7项临床研究,包括3篇原始文献[6-8]和4篇会议摘要[9-12],见图1。

图1 文献筛选流程与结果Fig 1 Literature screening process and results
2.2 纳入文献的基本特征与质量评价
纳入文献发表于2016—2020年;其中,1篇文献[7]为抗PD-1/PD-L1治疗组与安慰剂组比较;4篇文献[6,8-10]为抗PD-1/PD-L1治疗组与化疗组比较;3篇文献[9,11-12]为抗PD-1/PD-L1治疗+化疗组与化疗组比较。纳入文献的基本特征见表1;3篇原始文献的质量评价见图2。

图2 3篇原始文献的质量评价Fig 2 Quality evaluation of 3 original documents
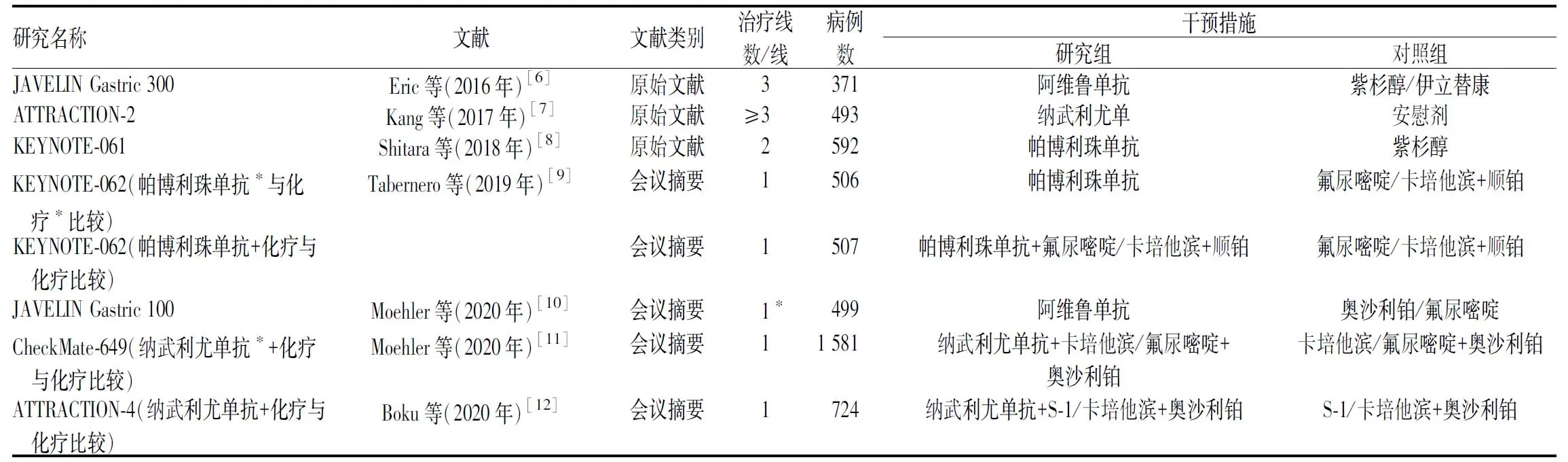
表1 纳入文献的基本特征Tab 1 General characteristics of included literature
2.3 Meta分析结果
各研究之间的异质性较大,因此采用随机效应模型。Meta分析结果显示:(1)单纯抗PD-1/PD-L1治疗组与化疗组患者的OS(HR=0.96,95%CI=0.87~1.07,P=0.451)、ORR(RR=0.65,95%CI=0.39~1.09,P=0.102)的差异均无统计学意义,但两组患者PFS的差异有显著统计学意义(HR=1.45,95%CI=1.17~1.81,P=0.001);(2)ATTRACTION-2研究为抗PD-1/PD-L1治疗组与安慰剂组比较,抗PD-1/PD-L1治疗组与安慰剂组患者的OS(HR=0.63,95%CI=0.51~0.78,P=0.000)、PFS(HR=0.60,95%CI=0.49~0.75,P=0.000)和ORR(RR=29.93,95%CI=1.84~485.72,P=0.017)比较,差异均有显著统计学意义;(3)抗PD-1/PD-L1治疗联合化疗组与化疗组患者的OS(HR=0.84,95%CI=0.76~0.94,P=0.001)、PFS(HR=0.78,95%CI=0.70~0.86,P=0.000)和ORR(RR=1.24,95%CI=1.10~1.39,P=0.000)比较,差异均有显著统计学意义,见表2、图3—5。

图3 研究组与对照组患者OS比较的Meta分析森林图Fig 3 Meta-analysis of comparison of OS between the study group and the control group

表2 纳入研究中研究组与对照组的疗效相关数据比较Tab 2 Comparison of efficacy data between the study group and the control group
3 讨论
肿瘤免疫治疗是继传统治疗方法如手术、化疗、放疗和靶向治疗之后非常有前景的第五大治疗方法。目前,已有多种PD-1/PD-L1抑制剂(纳武利尤单抗、帕博利珠单抗、阿维鲁单抗、阿特珠单抗、卡瑞丽珠单抗和信迪利单抗等)获批国内外适应证。针对上述PD-1/PD-L1抑制剂用于胃癌/胃食管结合部腺癌的治疗也进行了一系列的临床探索,初见疗效。然而,大多数研究结果显示,免疫治疗在胃癌中的缓解率低,疗效并不明确,胃癌患者究竟能否从免疫治疗中获益存在争议。

图4 研究组与对照组患者PFS比较的Meta分析森林图Fig 4 Meta-analysis of comparison of PFS between the study group and the control group
本次Meta分析结果显示,免疫治疗联合化疗与化疗比较、免疫治疗与安慰剂比较,胃癌患者均可以从PD-1/PD-L1抑制剂中获益;然而,免疫治疗与化疗相比,PD-1/PD-L1抑制剂并没有显著降低进展期胃癌或胃食管结合部腺癌患者的死亡风险。甚至有研究结果提示,相比较于化疗,抗PD-1/PD-L1治疗反而增加了30%的疾病进展风险[13]。胃癌患者之所以不能够从免疫治疗中获益,原因可能为,相较于非小细胞肺癌、肾癌及尿路上皮癌等对免疫治疗比较敏感的恶性肿瘤类型,胃癌的免疫原性较弱。因此,寻求联合治疗成为免疫治疗的新思路。免疫治疗联合化疗,化疗药可以破坏免疫抑制性细胞的活性,如调节性T细胞、髓样抑制细胞和肿瘤相关巨噬细胞,还可以通过诱导肿瘤细胞凋亡、主要组织相容性复合体Ⅰ类分子表达调和树突状细胞成熟来促进免疫应答。ATTRACTION-4研究的Ⅱ/Ⅲ期临床研究中,第一部分(Ⅱ期)结果显示,纳武利尤单抗联合SOX方案(S-1+奥沙利铂)、纳武利尤单抗联合CapeOX方案(奥沙利铂+卡培他滨)用于一线治疗手术无法切除的进展期或复发胃/胃食管结合部癌的ORR分别为57.1%、76.5%,显著高于化疗的ORR(约40%)[14]。此外,Ⅲ期临床研究CheckMate-649研究达到主要研究终点时,与化疗相比,纳武利尤单抗联合化疗用于胃癌和食管癌的一线治疗,可显著提升OS、PFS,且在PD-L1 阳性联合分数(combined positive score,CPS)≥5的主要分析人群以及所有随机人群中,均观察到了生存获益[15-16]。上述一系列的阳性结果,使免疫治疗联合化疗的方案有望改变胃癌一线治疗格局,并成为未来新的治疗标准。双免疫联合治疗可增强胃癌/胃食管结合部腺癌患者的抗肿瘤T淋巴细胞反应[17]。CheckMate-032研究中,纳武利尤单抗+伊匹单抗可以较好地退缩N1+N3的靶病灶[18]。此外,免疫治疗联合抗血管靶向治疗,可以通过血管内皮生长因子相关免疫抑制作用、促进T细胞肿瘤浸润以及启动、激活T细胞对肿瘤细胞抗原的应答,从而进一步增强PD-L1抑制剂激活免疫系统杀灭肿瘤细胞的能力。REGONIVO研究数据显示,对于微卫星稳定性(microsatellite stability,MSS)晚期胃癌的治疗,瑞戈非尼联合纳武利尤单抗的ORR达到44%,显示出了显著的疗效改善效果[19]。关于免疫治疗与放疗联合用于胃癌/胃食管结合部腺癌的相关报道少见。以上提示,联合治疗可能是未来进展期胃癌或胃食管结合部腺癌患者更好的选择。
目前尚没有一个优秀的标志物来识别胃癌免疫治疗的获益人群,虽然PD-L1、肿瘤突变负荷(tumor mutation burden,TMB)、微卫星不稳定性(microsatellite instability,MSI)-H/错配修复缺陷(deficient mismatch repair,dMMR)和EB病毒(Epstein-Barr virus,EBV)可能对免疫治疗具有预测作用,但并不十分确切。KEYNOTE-059研究结果显示,PD-L1阳性患者在免疫治疗中获益更加明显[20];但ATTRACTION-2研究结果显示,应用纳武利尤单抗患者的生存益处与PD-L1 肿瘤细胞阳性比例分数(tumor proportion score,TPS)状态无关[7];CheckMate-032研究结果显示,肿瘤PD-L1表达与免疫治疗的疗效并无相关性[18]。因此,PD-L1作为预测生物标志物的意义仍存在争议。MSI和EBV、TMB作为胃癌免疫治疗的疗效预测标志物,目前正在深入探索中。微卫星是散布在人类基因组中的重复的DNA序列,在微卫星中DNA聚合酶更容易出错。由于错配DNA通常由错配修复(mismatch repair,MMR)系统修复,dMMR经常与MSI-H相关。MSI-H/dMMR在肿瘤细胞中发生,并产生高突变,形成免疫细胞能识别的免疫原性新抗原。因此,MSI-H/dMMR的肿瘤表现出密集的免疫细胞浸润,特别是CD8+肿瘤浸润淋巴细胞,被认为对免疫治疗敏感。KEYNOTE-059及KEYNOTE-061研究中,帕博利珠单抗在MSI-H胃癌患者中取得了较好的疗效[8,21]。TMB是肿瘤基因组每个编码区域的总突变数。Samstein等[22]利用1 662例接受免疫治疗的晚期恶性肿瘤患者(包括126例胃癌患者)和5 371例未接受免疫治疗患者的临床和基因组数据,广泛分析了TMB与免疫治疗临床反应之间的关系,观察到高TMB与免疫治疗获益增加之间存在明显的趋势,高TMB表达患者的ORR、PFS获益显著。一项Ⅰb/Ⅱ期临床研究结果显示,高TMB肿瘤患者对抗PD-1抗体特瑞普利单抗的反应更明显,生存期更长[23]。然而,进一步的研究需要更好地评估TMB作为免疫治疗中免疫检查点抑制剂的预测生物标志物。对于EBV阳性的胃癌患者,可增加PD-L1在肿瘤和免疫细胞中的表达,增加γ干扰素基因,同时密集渗透CD8+肿瘤浸润淋巴细胞[24]。可见,免疫治疗在EBV阳性的胃癌患者中可发挥较好疗效。Kim等[21]的研究结果显示,EBV阳性胃癌患者的ORR为100%,高TMB患者的ORR为88.9%,中TMB患者的ORR为20%,低TMB患者的ORR为11.1%。
本次Meta分析的局限:首先,只纳入了7个随机对照研究,纳入的临床研究数目较少,可能会降低检验效能。更多的临床研究仍正在进行中,本研究的结论有待进一步的验证。第二,各研究之间的临床异质性使本研究结论可能存在偏倚。
综上所述,相比于化疗,目前并没有足够的证据支持单纯免疫治疗对晚期胃癌或胃食管结合部腺癌患者存在明显优势,因此临床使用需谨慎。与单纯化疗比较,免疫治疗联合化疗可以显著延长患者的生存期。因此,应进一步发现敏感性及特异性较强的生物标志物以筛选受益人群,以及探索更多的联合治疗策略,从而增强抗胃癌的免疫治疗效应。
