微结构反应器中丙烯酸-3-氯-2-羟丙酯的制备
2021-12-09丰兴坤孟凡琼李怡莹刘建安
丰兴坤,谢 晖,黄 莉,孟凡琼,李怡莹,刘建安
(南京工业大学 化工学院 材料化学工程国家重点实验室,江苏 南京 211800)
丙烯酸-3-氯-2-羟丙酯(3C2HPA)是丙烯酸(AA)与环氧氯丙烷(ECH)开环酯化的主要产物,其结构上含有双键和羟基使其在紫外光固化树脂中有着重要的作用,常作为交联剂或活性稀释剂使用[1-3],也是合成丙烯酸缩水甘油酯的前体原料[4]。而且羟基的α位上有吸电子基氯原子,使得羟基中的氢具有很大的反应活性。在光固化树脂中常作为单官活性稀释剂,具有黏度低、稀释能力强的特点,由于在形成的聚合物中引入氯原子,构成极性较大的碳氯键,使得大分子键间的作用力增强,这使得聚合物具有优良的耐化学性能、力学性能和防腐性能。并且还具有刺激性气味小、成本低、易储存等优点,在光固化树脂、涂料、黏接剂、塑料合金等方面具有很大的应用价值和潜在价值。
丙烯酸和环氧氯丙烷开环产物为3C2HPA和丙烯酸-1-氯-3-羟基-2-丙酯(3C1HiPA)两种异构酯混合物,这是由于环氧氯丙烷在开环反应中会因开环位点不同而产生不同的异构体产物[5]。在光固化领域,这两种异构酯均能作为活性稀释剂,因此,在使用过程中通常不加以区分。在釜式反应器中合成3C2HPA(80~100 ℃反应3~6 h)反应时间长、产物颜色深[6]。由于釜式反应器中传质能力有限,需要长反应时间使反应原料转化完全,导致过程效率低下。然而,反应时间过长会使副产物含量增加,因此,传统工艺中存在的问题仍是该反应在工业化中面临的难题。
微结构反应器是一种利用微加工技术制造,用在化工过程中的结构单元[7]。通常微通道尺寸在微米或毫米范围内,具有体积小、比表面积大的特点,具有极大的传热效率,可实现热量快速移除,从而大大缩短反应时间[8]。在微结构反应器中类似反应有较多的报道,例如Yao等[9]在微通道反应器中研究了均相催化乙酸与甲醇、乙醇、正丙醇和正丁醇的酯化反应,在相同的醇酸摩尔比3∶1、催化剂质量分数均为3%、停留时间为14.7 min时,乙酸酯的收率分别达到74.0%、70.1%、97.2%和92.2%。李明燃[10]研究了微反应器在环状化合物开环反应中的应用,通过微反应器实现环氧氯丙烷与CO2的偶合反应,高效合成环状碳酸酯,结果表明,在温度160 ℃、压力2.0 MPa、n(ECH)∶n(CO2)为1∶2、反应停留时间45.1 s时,ECH的转化率大于99%。因此将微反应技术应用在3C2HPA的合成工艺中,有望解决传统合成面临的问题,达到快速高效合成的目的[11-13]。
1 实验部分
1.1 实验原料和仪器
丙烯酸、丙酮,分析纯,上海凌峰化学试剂有限公司;环氧氯丙烷、三苯基膦,分析纯,阿拉丁试剂有限公司;四丁基溴化铵,分析纯,上海源叶生物科技有限公司;三乙胺、对羟基苯甲醚、KOH,国药集团化学试剂有限公司;无水乙醇,分析纯,无锡亚盛化工有限公司
傅里叶红外光谱仪(FT-IR),美国Nicolet公司;气相色谱仪(GC),安捷伦科技有限公司;Havard注射泵PHD ULTRA,美国哈佛仪器公司;T型不锈钢混合器,北京雄川科技有限公司。微结构反应器材质为聚四氟乙烯(PTFE)盘管,内径为1、2 mm。
1.2 微反应器中丙烯酸-3-氯-2-羟基丙酯的合成
将阻聚剂对羟基苯甲醚MEHQ(质量分数为0.1%)和丙烯酸作为一相,环氧氯丙烷和催化剂作为另一相,使用高压微量注射泵将两相按照一定的体积流速同时推进到延长管中,经过T型微混合器混合后进入微结构反应器中,将微结构反应器置于油浴中加热,另外在反应管后接一段冷却管并置于冰水浴中,最后在出料口处接被压阀(被压0.5 MPa)用来拓宽温度的操作范围,实验装置见图1。

图1 丙烯酸-3-氯-2-羟丙酯的制备工艺Fig.1 Preparation process of 3-chloro-2-hydroxypropyl acrylate
1.3 测试和表征
根据标准GB/T2895—2008测定产物酸值;盐酸-丙酮法测定产物环氧值;采用Nicolet 6700型傅里叶红外光谱仪对产物的结构进行表征,采用KBr压片,测定试样的透光率,扫描范围400~4 000 cm-1;采用Agilent 6890B-5977A型气质连用仪对产物进行表征。色谱条件:毛细管柱HP-5(30 m×0.32 mm×0.25 μm)。分析条件:汽化温度300 ℃,检测器温度300 ℃,采用程序升温,升温速率10 ℃/min,初温40 ℃,终温200 ℃,进样量0.1 μL,检测器:FID,检测器温度240 ℃。
2 结果与讨论
2.1 合成工艺优化
参照文献[6]报道釜式反应器中AA与ECH最佳摩尔比为1∶1.05,ECH的过量保证AA的转化更加充分,这是因为产物3C2HPA作为活性稀释剂使用,酸值高会腐蚀基材,降低附着力,影响交联程度,进而降低涂膜性能。本文中的最佳摩尔比参照文献,不再进行过多的考察。
2.1.1 催化剂种类对反应的影响
国内外对丙烯酸和环氧氯丙烷开环的催化剂研究较多,已见报道的催化剂有铬(Ⅲ)盐、钴(Ⅲ)配合物、胺类、季铵盐、三苯基膦等[14-17]。本文选用三苯基膦、四丁基溴化铵、三乙胺3种实验室常用的催化剂,在反应温度为155 ℃、停留时间为6 min、催化剂质量分数为0.5%、环氧氯丙烷和丙烯酸的总流速为2.4 mL/min、管径2 mm的条件下,探究催化剂种类对反应的影响,结果见表1。
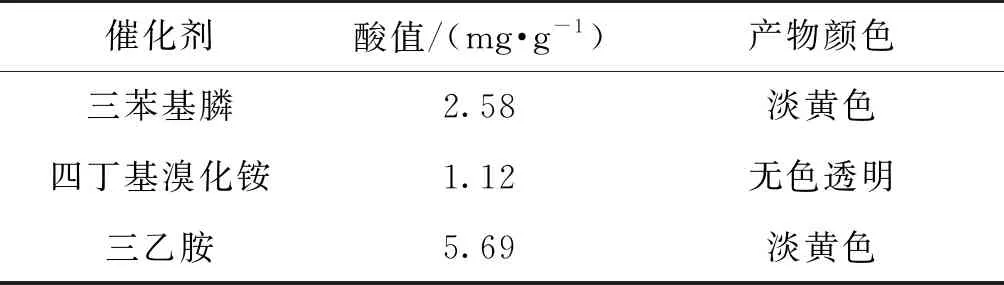
表1 催化剂种类对反应的影响
从表1中可以看出,在相同的条件下,使用四丁基溴化铵作为催化剂,产物酸值最低,产物颜色无色透明。使用三苯基膦和三乙胺会造成产物颜色发黄,而且三乙胺沸点较低,需要提供更高的被压,不利于实验。因此选择四丁基溴化铵作为反应的催化剂。
2.1.2 反应温度和停留时间对反应的影响
在环氧氯丙烷和丙烯酸的总流速为2 mL/min、管径为2 mm、催化剂使用四丁基溴化铵且质量分数为0.5%的条件下,考察停留时间和反应温度对反应的影响。其中通过固定流速改变管长调节停留时间,结果见图2。

图2 反应温度及时间对酸值的影响Fig.2 Effects of the reaction temperature and reaction time on acid value
由图2可知,当反应温度一定时,随着停留时间的增加,产物的酸值逐渐降低,说明延长停留时间有利于反应,反应后期继续延长停留时间,酸值基本不变,而且停留时间过长会造成产物颜色加深。因此最优的停留时间为6 min。
由于AA与ECH的沸点较低,过高的温度会使反应物汽化,导致体系内压力过大,虽然有被压阀提供被压,但过高的压力会导致超出Havard注射泵的工作范围,所以将反应温度范围设定在140~160 ℃。由图2可知,当停留时间一定时,随着反应温度的升高,产物的酸值逐渐降低,这是由于温度升高,分子运动剧烈,碰撞反应的概率更大,活化分子数增加,反应速率得到很大提升。当温度从155 ℃升温到160 ℃时,酸值变化不明显,而且温度高会易引发碳碳双键的聚合堵塞管路。综合考虑实验最优的反应温度为155 ℃。
2.1.3 总流速对反应的影响
在反应温度为155 ℃、停留时间为6 min、催化剂使用四丁基溴化铵且质量分数为0.5%、管径2 mm的条件下,考察总流速对反应的影响。其中通过固定停留时间,改变管长调节流速,结果见图3。

图3 总流速对酸值的影响Fig.3 Effects of the total flow on acid value
从图3中可以看出,随着总流速的增大,酸值逐渐下降。这是因为在微反应体系中,提高流速可以增大流体的总动能,使得原料的混合得更均匀,有利于传质,所以酸值下降明显。继续增大流速,酸值下降不明显,这可能因为达到了层流边界层的极限,传质效果不再提高[18],而且提高流速就需要延长反应管,管路的压降更大,不利于体系的稳定。所以最优的总流速为2.4 mL/min。
2.1.4 不同管径下停留时间对反应的影响
对于微结构反应器而言,反应器管径的大小直接影响反应器的单位比表面积,单位比表面积又直接决定反应的传质传热效率[19]。在反应温度155 ℃、总流速2.4 mL/min、催化剂使用四丁基溴化铵且质量分数为0.5%、停留时间6 min时,考察不同管径下停留时间对反应的影响,管径分别选用1和2 mm,结果见图4。
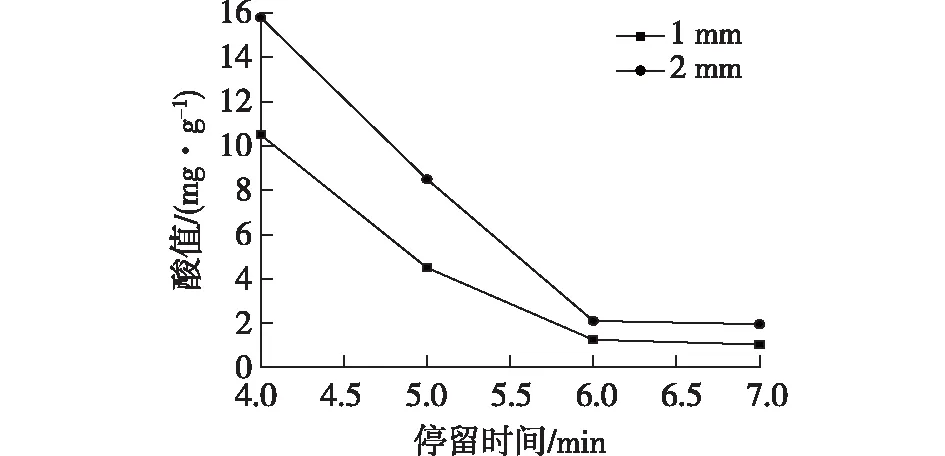
图4 不同管径下停留时间对酸值的影响Fig.4 Effects of residence time on acid value with different diameters of tube
从图4中可以看出,不同管径下产物酸值均随着停留时间的延长,先降低后基本保持不变,使用管径2 mm的反应管在6 min时,酸值为2.1 mg/g,而使用管径1 mm的反应管在6 min时,酸值为1.25 mg/g,说明减小管径有利于反应。在其他条件一定时,流体线速度与管径流量的关系见式(1)。
(1)
式中:u为流体的线速度,m/s;Vs为AA和ECH的总流速,mL/min;d为管径,mm。
从式(1)中可以看出,流体的线速度与管径的平方成反比,上文中得出酸值随着总流速Vs增大而下降,因为Vs与线速度u成正比,说明增加流速和改变管径都是通过影响流体的线速度来增强传质。
2.1.5 催化剂加入量对反应的影响
以四丁基溴化铵为催化剂、在反应温度155 ℃、管径2 mm、停留时间6 min、总流速2.4 mL/min的条件下,考察催化剂加入量对反应的影响,结果见图5。
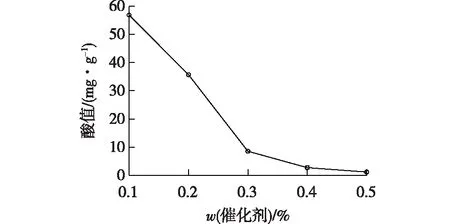
图5 催化剂质量分数对酸值的影响Fig.5 Effects of the catalyst mass fraction on acid value
从图5中可以看出,当催化剂质量分数从0.1%增大到0.4%时,酸值从56.9 mg/g下降到2.69 mg/g,继续增大催化剂质量分数到0.5%,酸值降到1.12 mg/g,这说明在一定范围内增大催化剂用量,有利于反应的进行。到达一定量时,继续增大用量,对反应的影响不大,所以最优催化剂质量分数为0.4%。
2.2 微结构反应器与釜式反应器工艺对比
对比微结构反应器在最优条件下与釜式反应器在n(AA)∶n(ECH)为1∶1.05、催化剂四丁基溴化铵质量分数为0.4%时合成3C2HPA,产物经减压蒸馏,除去未反应的AA和ECH后,经GC检测3C2HPA收率,结果见表2。
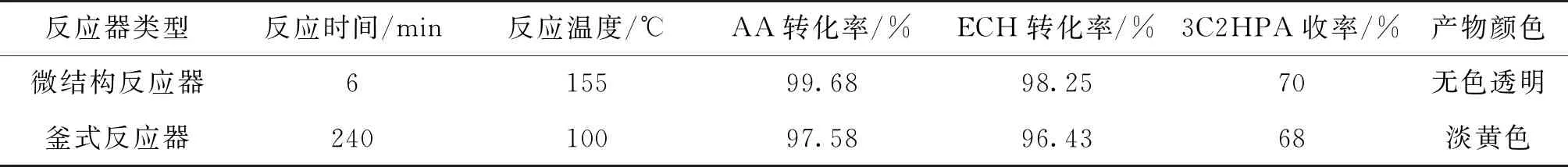
表2 最优条件下产物酸值和环氧值对比
从表2中可以看出,与常规釜式反应器相比,使用微结构反应器合成能够明显缩短反应时间,同样以四丁基溴化铵为催化剂,在三口烧瓶中合成时,反应温度100 ℃,需要4 h,而在微结构反应器仅需6 min而且产物颜色较好,两种合成工艺中丙烯酸和环氧氯丙烷的转化都比较完全,AA的转化率比ECH的转化率高,可能是由于部分AA发生了副反应造成的。
2.3 红外光谱分析
产物的红外光谱图见图6,从图6中可以看出:3 447 cm-1处为羟基的伸缩振动峰;1 728 cm-1处为酯羰基的吸收峰;1 637、810 cm-1处为碳碳双键伸缩振动峰;748 cm-1处为碳氯键伸缩振动吸收峰;1 409 cm-1处为亚甲基弯曲振动吸收峰;1 064 cm-1为碳氧键的伸缩振动吸收峰;同时在915 cm-1附近未出现环氧基的特征吸收峰,1 750~1 820 cm-1未出现羧基的特征吸收峰。综上说明,成功合成出丙烯酸-3-氯-2-羟丙酯。

图6 丙烯酸-3-氯-2-羟基丙酯的红外光谱Fig.6 Infrared spectroscopy spectra of 3-chloro-2-hydroxypropyl acrylate
2.4 MS结果分析
产物的质谱图见图7,从图7中可以看出,m/z165为3C2HPA的分子离子峰(M+),m/z147、m/z98为失去羟基的离子峰,m/z115、m/z49为亚甲基氯处断裂产生的离子峰,m/z86是羟基发生α裂解产生的离子峰,m/z55、m/z43是酯羰基发生α裂解产生的碎片离子峰,碎片离子峰归属表见表3,综上说明成功合成出目标产物。

图7 丙烯酸-3-氯-2-羟丙酯的质谱Fig.7 Mass spectrum (MS) of 3-chloro-2-hydroxypropyl acrylate

表3 质谱图中碎片离子峰归属表
3 结论
1)利用微结构反应器合成丙烯酸-3-氯-2-羟丙酯,确定最佳制备工艺为:反应温度155 ℃、停留时间6 min、总流速2.4 mL/min、催化剂使用四丁基溴化铵且质量分数为0.4%、管径为1 mm的PTFE管。在此条件下丙烯酸和环氧氯丙烷的转化率达到99.82%和98.25%,3C2HPA收率为70%。
2)通过傅里叶红外光谱(FT-IR)、质谱(MS)对产物进行表征,结果表明成功合成出丙烯酸-3-氯-2-羟丙酯。
3)与传统釜式反应器相比,使用微反应器合成可以使反应时间从4 h缩短至6 min,而且产物颜色较好。
