大剂量甲氨蝶呤治疗儿童难治性朗格汉斯细胞组织细胞增生症的临床效果分析
2021-12-08谢瑶赵卫红华瑛孙青吴鹏辉
谢瑶,赵卫红,华瑛,孙青,吴鹏辉
朗格汉斯细胞组织细胞增生症(Langerhans cell histiocytosis,LCH)一般累及单个系统或多个系统,皮肤、骨骼和淋巴结为最常受累部位,血液系统、肝和脾浸润属于危险器官受累(Risk organ+,RO+),部分多系统伴有RO+和/或小年龄患儿(诊断时年龄≤2岁)且对目前常规化疗反应不佳,成为难治性或复发性病例[1-2]。部分轻型患儿不需要治疗即可自愈,但是难治性或复发性LCH患儿若不及时治疗则病情进展快、预后差、死亡率高。由于难治性或复发性LCH患儿的治疗反应及预后不佳,新的治疗方案仍然在探索中。目前国内外常用治疗方案的常规治疗或维持治疗阶段均涉及到甲氨蝶呤(Methotrexate,MTX)的持续静脉滴注治疗,但是最大使用剂量为0.5 g/m2。国际公认将≥1 g/m2的MTX治疗量称为大剂量 MTX(high-dose Methotrexate,HDMTX)[3],在儿童患者中,HDMTX因其具有良好的血-脑脊液屏障透过能力,能够有效预防中枢神经系统白血病,且有稳定的药物浓度维持特性,被广泛应用于白血病及淋巴瘤的治疗。本课题组在既往的研究中发现HDMTX的药物浓度是可控的,在合理调整药物浓度的情况下能够充分保证用药的安全性,因此在可选择的药物范围内,提高MTX剂量具有可行性,且可能对颅内病变的治疗更有针对性。北京大学第一医院儿科血液肿瘤专业组近年来收治的难治性或复发性LCH患儿中,有5例患儿因为治疗过程困难、多次复发或者垂体受累而接受了HDMTX治疗,本研究通过分析该5例患儿的临床特点及预后,探讨HDMTX治疗的可行性及有效性,尤其是在垂体受累患儿中的治疗效果,以提高LCH缓解率并改善其预后。
本文价值:
难治性朗格汉斯细胞组织细胞增生症(LCH)目前被认为属于恶行增殖性疾病,常累及垂体,但是治疗该疾病的方案中所应用的药物较难透过血-脑脊液屏障,而大剂量甲氨蝶呤(HDMTX)广泛应用于儿童白血病治疗,可以有效透过血-脑脊液屏障,且对颅内病变具有治疗和预防作用。本文中LCH患儿多数有垂体受累或者其他特殊原因,因此在充分沟通后采用HDMTX进行治疗。结果提示治疗后疗效评估反应率在70%以上,并且均未观察到严重毒副作用发生,证实在保证用药安全的情况下,可以调整常规化疗药物,将HDMTX用于危险器官受累(RO+)的难治性或复发性LCH患儿的化疗当中,尤其是垂体受累患儿,疗效较好。既往文献中的甲氨蝶呤用药剂量一般在0.5 g/m2,通过本研究,提示针对RO+的难治性或复发性LCH患儿,尤其是垂体受累的患儿,可以试用HDMTX治疗。
1 对象与方法
1.1 研究对象 选取2005—2019年就诊于北京大学第一医院儿科确诊为LCH,存在多系统受累,同时合并RO+或者多次复发的患儿5例作为研究对象,且患儿家属均同意采用HDMTX治疗并签署知情同意书。
1.2 LCH诊断标准 根据《血液病诊断及疗效标准(第3版)》[4]LCH诊断相关内容,患儿具有LCH临床表现,病理学检查示:显微镜下可见分化较好的组织细胞增生、泡沫样细胞、嗜酸粒细胞、淋巴细胞、浆细胞和多核巨细胞,以及组织破坏但没有分化较差的恶性组织细胞;慢性病变过程中可见嗜酸细胞肉芽肿,增生中心出现出血和坏死;并且至少具有下述一项[4]:(1)CD207阳性;(2)CD1a阳性;(3)电镜下伯贝克颗粒阳性。
1.3 治疗方案 常规治疗采取国际组织细胞协会的LCH临床试验方案[5]、德国 DAL-HX 83/90方案[6]、日本 LCH 研究 学 组(Japan LCH Study Group,JLSG)96/02 方 案[7-8]。HDMTX 治疗方案为采用 1~2 g/m2MTX 持续 24 h静脉输注,联合四氢叶酸解救。
1.4 疗效及药物毒副作用评估 对治疗6周时进行疗效评估,分为3个等级:(1)反应良好(Better):LCH症状及体征部分消失,未出现新发病灶;(2)中度反应(Intermediate):症状和体征持续存在无新发进展,或一个病变部位好转但另一个部位疾病进展;(3)疾病进展(Worse):症状、体征恶化和/或出现新病灶[9]。药物毒副作用评估:根据世界卫生组织(WHO)抗癌药急性及亚急性毒性反应分度标准进行评估,3、4级为严重毒副作用[10]。
1.5 资料收集及随访 回顾性查阅患者病历,收集患者的一般资料:性别、起病年龄、入院时年龄;症状和体征:起病症状,骨骼、耳部、血液系统、肝、脾、皮肤、垂体受累情况,是否发生浅表淋巴结肿大、肺损伤情况;治疗方案:HDMTX应用前的常规治疗方案,HDMTX的具体剂量及疗程;药物毒副作用:按照WHO抗癌药急性及亚急性毒性反应分度标准[10]进行比对;预后情况:6周时疗效,复发情况,HDMTX治疗后的疾病转归;随访情况。患儿出院后每周到门诊复诊,每1~3周进行住院化疗,定期记录患儿症状及毒副作用,并选择性进行血常规、C反应蛋白、肝功能、肾功能、电解质等实验室检查以及影像学检查。
2 结果
2.1 LCH患儿一般资料 5例患儿中男4例,女1例;起病年龄为3~9个月,均<1岁;入院时年龄8个月~4岁8个月(见表1)。
2.2 LCH患儿临床特点 起病症状:5例患儿首发症状均有发热,3例有皮疹,1例右下肢活动减少,1例眼眶及右下肢肿物。疾病进展情况:5例患儿均进展为多系统受累,其中4例存在RO+,该4例患儿中2例为复发病例,另1例因在外院行常规治疗,就诊时不能明确是否存在RO+,但就诊时为第3次复发;3例患儿有垂体受累,临床表现为尿崩症状(见表1)。
2.3 LCH患儿治疗方案 5例患儿均采用国际常规方案进行诱导治疗,其中4例患儿治疗期间首先采用常规方案0.5 g/m2中剂量MTX治疗。例1因起病年龄小且起病时存在RO+,最后1个疗程应用HDMTX(1 g/m2)巩固治疗,之后使用长春花碱〔6 mg·(m2)-1·次-1,静脉推注,每3周1次〕以维持治疗。例3常规治疗6周时疗效评估为反应良好,但在治疗6个月时出现复发,继续采用原方案化疗后皮疹反复未见消退,颅骨出现新发缺损,建议采用克拉屈滨治疗,但家属因经济条件拒绝,遂换用HDMTX(2 g/m2)进行治疗6个疗程。例4常规治疗6周时疗效评估为反应良好,但停药1年2个月后复发,骨质破坏较前增多,并且出现垂体受累,中枢性尿崩症状,考虑HDMTX穿透血-脑脊液屏障效果良好,改用 HDMTX(1 g/m2)联合长春花碱〔6 mg·(m2)-1·次-1,静脉推注,每周1次〕、泼尼松〔40 mg·(m2)-1·d-1,口服,4周后逐渐减停〕治疗2个疗程。例5常规治疗6周时疗效评估为中度反应,考虑该患儿亦合并垂体受累,因此采用2个疗程HDMTX(1 g/m2)联合治疗,HDMTX治疗前应用醋酸去氨加压素(0.2 mg/次,口服,3次/d)难以控制尿崩症状,治疗后尿崩症状在相同剂量的药物维持下可以控制。例2患儿因入院时已复发2次,且垂体受累,因此采用HDMTX(2 g/m2)治疗4个疗程。5例患儿采用HDMTX治疗时间距首次用药时间为2个月至4年(见表1)。
治疗过程中5例患儿均于上午8:00(第0 h)开始静脉滴注MTX,前30 min匀速给予总计算药量的1/6作为冲击量以期快速达到稳态浓度;8:30(第0.5 h)开始将剩余药物匀速静脉滴注23.5 h,冲击量及维持量均使用输液泵控制。在输注第6 h抽取静脉血2 ml检测MTX血药浓度根据血药浓度调整后续用药,其后监测24、48 h血药浓度,并在36 h开始进行四氢叶酸解救,根据血药浓度调整解救药物用量。MTX血药浓度测量采用荧光偏振免疫法,均送至北京大学第一医院血药浓度室进行统一检测。
2.4 LCH患儿预后及随访情况 患儿均在北京大学第一医院儿科血液肿瘤专业组进行了长期规律随访。例1在应用1个疗程HDMTX治疗后使用长春花碱维持治疗,常规治疗6周时疗效评估为反应良好,疾病未再复发或进展,目前已停药13年,无病生存;例2连续应用4个疗程HDMTX治疗后肿块消失、颅骨病变稳定,垂体病变得到控制,尿崩症状消失,6周时疗效评估为中度反应,尽管维持治疗3个月后出现第3次复发,但垂体未再受累,最终采用目前国际推荐的LCH二线用药克拉屈滨进行治疗,5个疗程后停药观察5年,无病生存;例3进行第2个疗程HDMTX治疗后,皮疹得到控制,骨骼病变未再进展,6周时疗效评估为反应良好,其后进入维持治疗,6个疗程后目前停药3年,无病生存;例4进行2个疗程HDMTX治疗后,垂体病灶较前缩小,尿崩症状明显好转,6周时疗效评估为中度反应,但是后续治疗中肩胛骨骨质破坏范围较前稍有增大,额骨出现新发病灶,后改用克拉屈滨治疗,目前停药2年,无病生存;例5进行2个疗程HDMTX治疗后,尿崩症状消失,6周时疗效评估为中度反应,但由于治疗过程中合并肺部感染,未再继续应用HDMTX治疗,目前仍处于维持治疗阶段,还在随访当中(见表1)。
2.5 药物毒副作用 在应用HDMTX治疗后,对患儿进行常规监测血常规、肝功能、肾功能、电解质发现,4例患儿出现骨髓抑制,3例患儿出现谷氨酸氨基转移酶升高,3例患儿出现恶心、呕吐等胃肠道反应,但5例患儿均未出现3级及以上的严重毒副作用(见表1)。
3 讨论
LCH是以树突状组织细胞活化增殖并且异常聚集为主要特征的疾病[11],是一种相对比较罕见的疾病,常发生于儿童,且男性发病率高于女性[2]。由于该病临床表现多样、预后差异较大,治疗方案也并不完全一致,目前全身多药联合化疗是该病的一线治疗方法,但是具体用药种类及用药剂量在不同的医疗机构仍然存在一定差别[5-8],然而从复发率、缓解率来看,并没有某种治疗方案明确优于其他治疗方案。2013年GADNER等[1]报道的采用LCH-Ⅲ方案治疗的临床研究中,71%的RO+的LCH患儿对治疗的反应良好,5年无事件生存率(EFS)为84%,复发率为27%;2002年MINKOV等[12]报道的应用DAL-HX 83/90治疗方案的一项多国多中心研究显示,LCH患儿5年EFS为81%,死亡率为19%。2016年MORIMOTO等[8]报道了采用JLSG-02方案进行治疗的研究显示,治疗6周时RO+的LCH患儿的疗效评估反应率(中度反应或反应良好)为76.2%,5年EFS为46.2%。尽管很多轻型LCH患儿可以自发缓解,但是由于近年来难治性LCH患儿复发率始终居高不下(30%~50%),并且容易出现多次复发以及后遗症,因此世界各医疗研究中心对难治性或复发性LCH患儿仍然在寻找更加有效的治疗方案,并且强调综合考虑各种危险因素,结合临床分级及预后等,制定个体化治疗方案[13-14]。近年来国内相关医疗中心也在试用各种改良方案[15-17],本课题组也一直在治疗过程中不断寻求更加有效的个体化治疗措施。
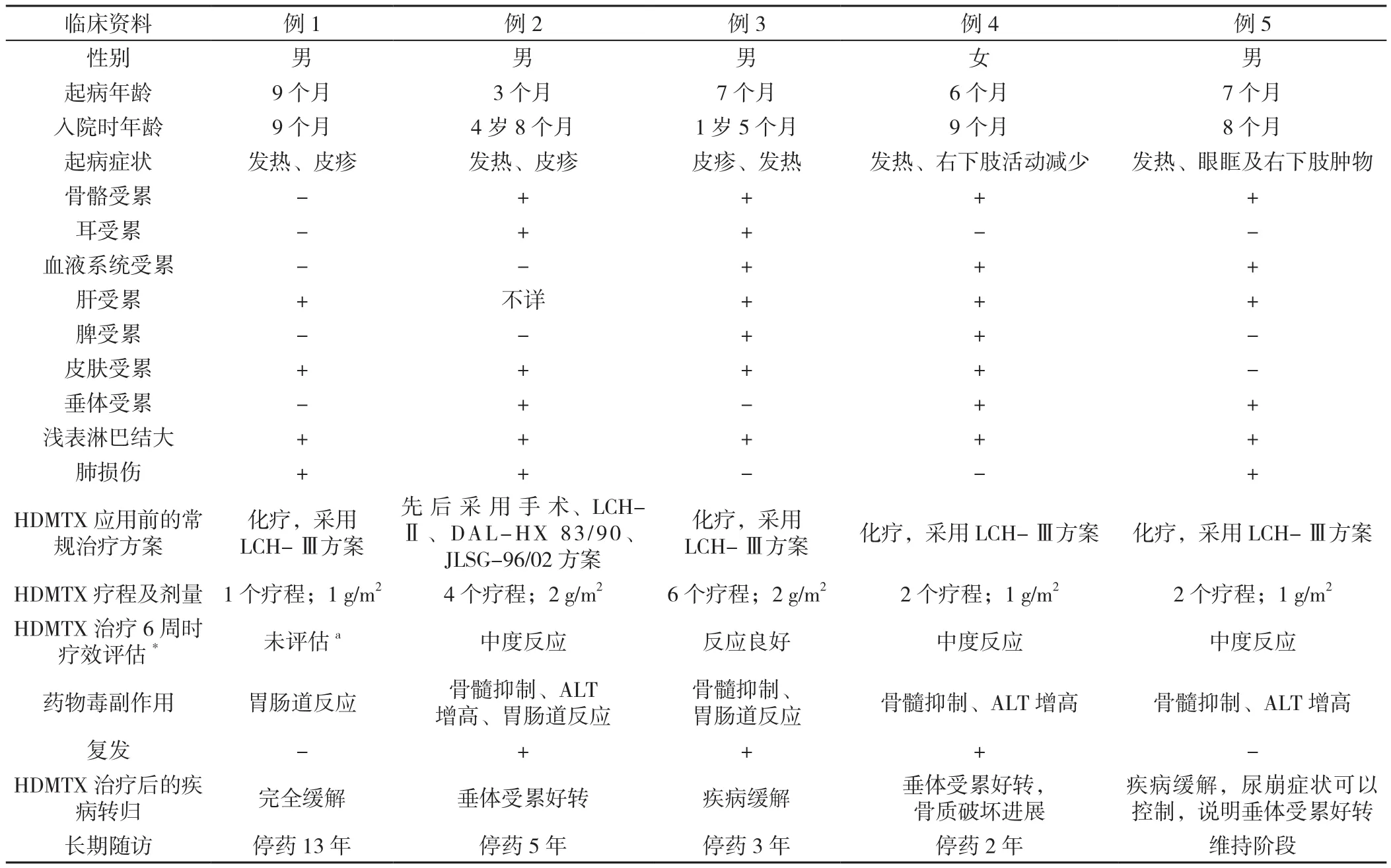
表1 LCH患儿临床资料Table 1 Summary of clinical data of refractory Langerhans cell histiocytosis patients
目前国际组织细胞协会在对既往的LCH-Ⅱ方案进行更新过程中,对部分RO+的LCH患者的治疗方案中加入了中剂量MTX,即LCH-Ⅲ方案,结果显示,LCH-Ⅲ方案的临床疗效优于LCH-Ⅱ方案[1]。尽管该研究还显示加用MTX后与不加MTX相比,出现严重毒副作用的发生率差异有统计学意义,但是笔者认为在MTX浓度可控的情况下,并不会增加应用MTX的风险。目前HDMTX在治疗儿童白血病及淋巴瘤领域的应用最为成熟。近20年,儿童白血病的治愈率快速提高,其中一项重要原因就是HDMTX的应用在极大降低颅脑放疗毒副作用的同时,有效降低了中枢神经系统白血病的发生[18],也就是说,HDMTX充分发挥了该药物能够进入血-脑脊液屏障并稳定维持浓度的药物特性。由此推测,在治疗中枢神经系统受累的LCH患儿(比如垂体受累患儿)时,个体化增加MTX的剂量至HDMTX可能有益。
因此在多种方案治疗效果欠佳,药物选择困难的时候,本课题组试用了HDMTX治疗方案,尤其是对垂体受累的患儿。本文5例LCH患儿中有3例合并垂体受累,主要临床表现为加用去氨加压素仍然难以控制患儿的尿崩症状,并且其他常规化疗药物治疗无疗效。在采用HDMTX治疗之后,2例患儿尿崩症状消失,1例患儿去氨加压素不需加量即可控制尿崩症状,提示HDMTX对垂体病变治疗有效。另外2例非垂体受累的难治性LCH患儿经HDMTX治疗后,病情也得到了缓解,未再复发。由于本课题组在HDMTX应用方面经验丰富,用药过程中严密监测并调整药物浓度,因此在随访过程中所有患儿未出现严重毒副作用。
综上所述,在保证用药安全的情况下,可以调整常规化疗药物,将HDMTX用于RO+的难治性或复发性LCH患儿的化疗当中,尤其是垂体受累患儿,疗效较好。但本研究样本量小,要获得更准确的临床疗效数据需进行大样本研究。此外,对于其他难治性或复发性LCH患儿,可积极尝试克拉屈滨等二线药物治疗。
作者贡献:谢瑶进行文章的构思,收集病例资料,撰写论文并进行中英文修订;赵卫红、华瑛负责研究方案制定;谢瑶、孙青、吴鹏辉进行病例的具体治疗与研究可行性分析;谢瑶、赵卫红负责文章的质量控制及审校;赵卫红对文章整体负责,监督管理。
本文无利益冲突。
