2型糖尿病并发痛性糖尿病神经病变的影响因素研究
2021-12-07吴蓝雪汪四虎黄大祥黄利娟何江章秋
吴蓝雪,汪四虎,黄大祥,黄利娟,何江,章秋
糖尿病是目前临床上最常见的慢性病之一,随着人们生活水平的提高,糖尿病发病率显著提升,并凸显年轻化趋势[1]。糖尿病周围神经病变是糖尿病最常见的慢性并发症之一,而痛性糖尿病神经病变(painful diabetic neuropathy,PDN)约占糖尿病周围神经病变的15%[2],且肢体远端出现对称性疼痛是PDN最常见的临床表现。为此,本研究收集了来自安庆市立医院的273例2型糖尿病(type 2 diabetes,T2DM)患者的相关信息,旨在寻找T2DM并发PDN的影响因素,为今后有效的临床干预和治疗提供参考。
1 资料与方法
1.1 研究标准 纳入标准:符合《中国2型糖尿病防治指南(2017年版)》[3]中T2DM的诊断标准。排除标准:(1)1型糖尿病、妊娠期糖尿病及其他特殊类型糖尿病;(2)存在糖尿病急性并发症、严重肝肾功能不全、手术、创伤等;(3)合并精神疾病;(4)由感染、其他代谢性或中毒性疾病等原因导致的周围神经痛、血管闭塞性疼痛、颈/腰椎病变、脑梗死所致神经痛;(5)病例资料不全或不配合者。
1.2 一般资料 选取2016年1月—2019年12月于安庆市立医院内分泌科住院的符合研究标准的T2DM患者273例,根据其有无PDN分为单纯糖尿病组(NPDN组,n=185)及T2DM并发PDN组(PDN组,n=88)。PDN组纳入标准:(1)四肢表现为痛觉过敏、自发痛或异常性疼痛的神经痛表现;(2)神经病理性疼痛评估量表(Douleur Neuropathique 4 Questions,DN4)评分≥4分;(3)有周围神经病变体征(符合2项及以上):10 g尼龙丝检查为阳性,温度觉异常,振动觉异常,踝反射消失,神经肌电图正常或轻度异常。本研究经安庆市立医院伦理委员会审核批准,患者均对本研究知情同意。
1.3 研究方法
1.3.1 一般资料采集 两组患者的一般资料包括性别、年龄、T2DM病程、吸烟史、饮酒史、体质指数(BMI)、收缩压(SBP)、舒张压(DBP)、胰岛素使用情况、糖尿病视网膜病变(diabetic retinopathy,DR)发生情况、糖尿病肾病(diabetic kidney disease,DKD)发生情况;其中吸烟指吸烟量≥20支/d,饮酒指折合乙醇饮用量男性>140 g/周,女性>70 g/周。
1.3.2 实验室检查指标收集 取患者肘静脉血进行测量,采用葡萄糖生物传感器测量空腹血糖(FPG)、餐后2 h血糖(2 hPG);采用全自动糖化血红蛋白分析仪检测糖化血红蛋白(HbA1c);完善馒头餐耐量试验,采用化学发光免疫分析仪检测空腹C肽(FC-P)、餐后1 hC肽(1 hCP)、餐后2 hC肽(2 hCP);采用全自动生化分析仪检测总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C),采用化学发光法检测血清铁蛋白(SF);采用免疫比浊法检测C反应蛋白(CRP)、尿微量白蛋白。
1.4 观察指标 比较两组患者一般资料及实验室检查指标,探究T2DM并发PDN的影响因素。
1.5 统计学方法 采用SPSS 23.0统计软件进行数据处理。符合正态分布的计量资料以(±s)表示,两组间比较采用成组t检验;非正态分布的计量资料以M(P25,P75)表示,两组间比较采用Mann-whitney秩和检验;计数资料以相对数表示,两组间比较采用χ2检验;T2DM并发PDN的影响因素分析采用多因素非条件Logistic回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者一般资料及实验室检查指标比较 两组患者性别、吸烟史、饮酒史、SBP、DBP、胰岛素使用率、FC-P、TC、TG、HDL-C、LDL-C、SF、CRP、尿微量白蛋白比较,差异无统计学意义(P>0.05);PDN组患者年龄大于NPDN组,T2DM病程长于NPDN组,BMI、DR发生率、DKD发生率、FPG、2 hPG、HbA1c高于NPDN组,1 hCP、2 hCP低于NPDN组,差异有统计学意义(P<0.05,见表1)。
2.2 T2DM并发PDN影响因素的多因素非条件Logistic回归分析 以T2DM并发PDN为因变量,以单因素分析中P<0.05的指标为自变量(赋值见表2),进行多因素非条件Logistic回归分析,结果显示,T2DM病程、DR、DKD、FPG、HbA1c是T2DM并发PDN的影响因素(P<0.05,见表3)。
3 讨论
PDN是临床上常见的糖尿病并发症之一,其主要临床表现为对称性双侧肢体远端疼痛[4],夜间疼痛尤甚,下肢明显,以自发痛、痛觉过敏和异常性疼痛为特征[5],其痛感可表现为针刺样、烧灼样、电击样、撕裂样疼痛等,可导致睡眠障碍、运动异常、情感障碍,影响患者的生活质量和工作能力,严重者甚至会引发抑郁。SMITH[6]研究显示,神经性疼痛包括感觉、运动和自主神经症状,均由周围神经系统或中枢神经系统的原发疾病或功能障碍引起,其病理生理机制复杂;在高血糖的病理基础上,Na+-K+泵受损[7]、受损神经的异位放电、神经生长因子合成的改变、交感神经和感觉神经的可塑性变化、下行性抑制通路功能受损、大脑感觉区域皮质与丘脑间联系功能的丧失均是糖尿病并发PDN的机制[8]。当小纤维神经异常放电时,PDN患者尽管表现为烧灼感疼痛及电击样疼痛,但神经电生理检查可能依旧表现为正常或轻度传导异常,而肌电图及神经传导速度(EMG/NCV)主要反映大神经纤维病变,需要通过皮肤活检对神经纤维密度进行检测才能判定[9],但该检测属于有创性,临床开展率不高,故本研究并
未将神经肌电图及神经传导速度异常列为PDN组纳入标准。

表1 两组患者一般资料及实验室检查指标比较Table 1 Comparison of demographic information and laboratory test results between the two groups
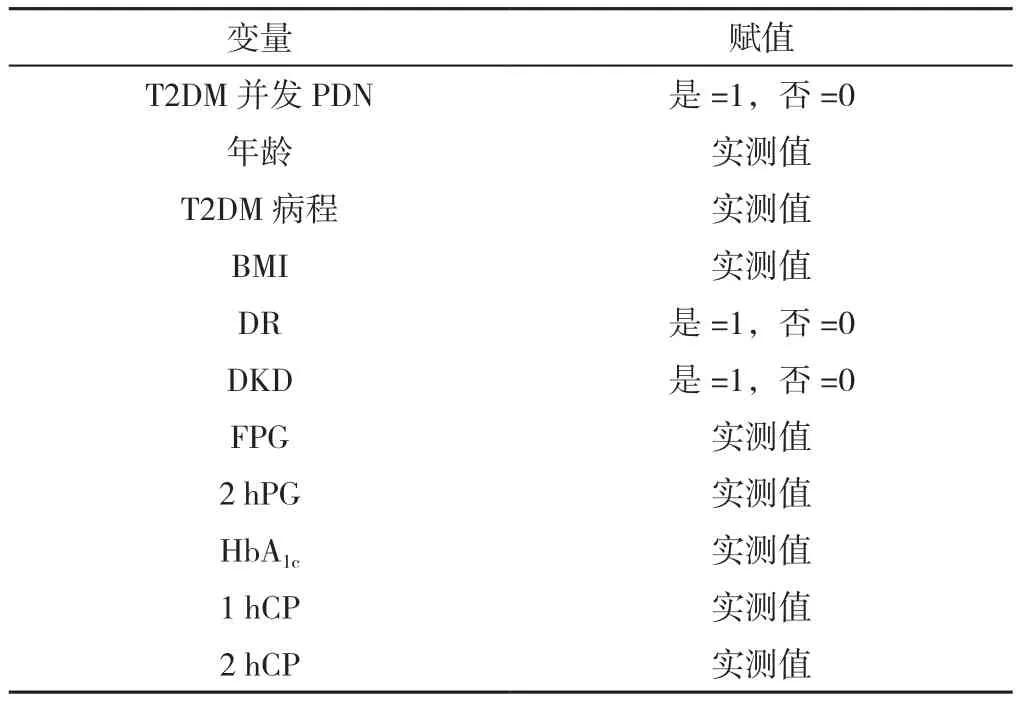
表2 T2DM并发PDN影响因素的多因素非条件Logistic回归分析变量赋值表Table 2 Assignment table for factors associated with painful diabetic neuropathy in T2DM identified with multivariate unconditional Logistic regression analysis

表3 T2DM并发PDN影响因素的多因素非条件Logistic回归分析Table 3 Multivariate unconditional Logistic regression analysis of influencing factors of painful diabetic neuropathy in T2DM
本研究结果显示,FPG、HbA1c是T2DM并发PDN的影响因素。有研究显示高血糖是糖尿病发展过程中发生并发症的重要危险因素[10],机体长期处于高血糖状态会产生大量的氧自由基,影响轴索运输,加重神经元损伤;此外,高血糖影响酶的活性并激活蛋白激酶C途径(PKC途径),使多元醇代谢途径的关键酶醛糖还原酶活性增高,神经元内蓄积大量山梨醇和果糖,无法有效利用,导致细胞内渗透压升高、肿胀,甚至变性坏死[11]。糖代谢紊乱可损伤血管内皮细胞功能并引起神经微循环障碍,如神经内皮细胞肿胀、增生、基膜增厚,内膜毛细血管数目减少等,血液流变学异常使血液呈高凝状态,致血管管腔狭窄,甚至闭塞,从而导致微循环障碍、神经缺血、缺氧性损害;使髓鞘的连续性遭到破坏,导致神经病变,引发神经痛。表观遗传学认为,高血糖所诱导的微血管病变及表观修饰改变在后期血糖控制良好的情况下依然存在,且其损害是不可逆的,而HbA1c是血红蛋白及葡萄糖不可逆的结合,与血糖呈正相关,可反映近12周内的平均血糖,可评估血糖管理程度,因此,早期控制血糖尤其重要[12]。
本研究结果显示,T2DM病程是T2DM并发PDN的影响因素。有研究表明,糖尿病并发症的发生率与糖尿病病程呈正比,糖尿病病程为10年的患者PDN发生率是糖尿病病程为5年患者的2倍以上[13]。本研究结果显示,PDN组患者年龄大于NPDN组;随着年龄增长、T2DM病程延长,PDN发生率升高,这种趋势与国外的报道一致[14]。疼痛根据持续时间的不同可分为急性疼痛和慢性疼痛,前者是在血糖急剧波动的情况下出现,疼痛明显,但持续时间<6个月,常有自限性,临床治疗效果满意,患者预后良好;随着糖尿病病程的延长,胰岛功能衰竭,血糖难以控制,血糖波动加重了微血管损伤、线粒体功能障碍、神经纤维缺血缺氧,因此慢性疼痛持续时间>6个月,此时镇痛效果欠佳,患者预后不良。
糖尿病微血管病变包括DR、DKD,本研究结果显示,DR、DKD是T2DM并发PDN的影响因素,说明各微血管病变的发生、发展同步进行[15]。随着T2DM病程的延长,发生DR、DKD的可能性增大,三者相互影响,因此早期预防尤为重要。
对于T2DM并发PDN的干预,主要处理原则为控制血糖和缓解疼痛[16],稳定的血糖水平是预防糖尿病神经疼痛最有效的措施;应根据患者既往病史、血糖水平及现有实验室检查指标,制定个体化的降糖方案,减少血糖波动;同时采用缓解疼痛的药物治疗,包括三环类抗抑郁药、改善神经微循环药物、抗惊厥药物、营养神经药物、醛糖还原酶抑制剂等。针对糖尿病患者的神经疼痛,美国精神病学会推荐将依帕司他、甲钴胺作为最主要的治疗药物[17],其中依帕司他作为新型醛糖还原酶抑制剂,可减少山梨醇、果糖在体内的蓄积,改善糖尿病多元醇代谢紊乱,恢复细胞Na+-K+三磷腺苷(ATP)酶的活性,减轻神经变性和水肿,加快神经纤维传导速度[18];甲钴胺可为神经组织修复和轴突再生提供良好的前提条件。一项双盲、多中心、临床对照试验表明,抗惊厥药物普瑞巴林可早期、持续改善糖尿病神经痛,且不良反应小,目前已在临床上得到广泛应用[19]。另外,抗氧化剂硫辛酸具有清除氧自由基的作用,可以促进葡萄糖的利用、运输,与依帕司他联合使用效果显著[20]。改善微循环药物如前列地尔及丹参等中药可扩张外周血管、促进神经血流灌注,对于缓解疼痛也有一定的辅助作用。另外严格控制血压、血脂,保持良好的生活方式,遇到疼痛症状及时就诊对缓解疼痛也有帮助。对于顽固性神经痛患者,由于个体化差异较大,非药物治疗作为药物治疗的补充,具有重大意义,其中就包含了中医学的针灸、推拿、敷贴、足浴、锻炼功法等[21],已被临床广泛应用,此外电刺激疗法、红外光治疗、低强度激光治疗也可缓解患者的疼痛[22]。更有研究表明,心理社会干预疗法对PDN也有一定程度的治疗作用[23]。
综上所述,T2DM病程、DR、DKD、FPG、HbA1c是T2DM并发PDN的影响因素,临床对于存在上述影响因素的T2DM患者,需警惕其PDN的发生,早期干预,积极预防,防止严重并发症的出现,减轻患者病痛,提高其生活质量。
本研究局限性:
痛性糖尿病神经病变是糖尿病周围神经病变中一种常见的类型,其中肢体远端的疼痛最多见,其次还有头痛、皮肤神经性疼痛等。本研究主要以肢体远端疼痛为前提收集数据,范围较为局限,且研究对象纳入标准不够严谨,今后拟从肌电图传导速度等方面筛选研究对象。
作者贡献:吴蓝雪进行文章的构思与设计,数据的收集及整理,结果分析及解释,文章撰写、修改;汪四虎、黄大祥、章秋负责研究的实施及可行性分析、文章的质量控制和审校;黄利娟、何江负责数据的整理及统计学处理;章秋对文章整体负责,监督管理。
本文无利益冲突。
